INTRODUCCIÓN
La isquemia aguda de extremidades inferiores se caracteriza por la disminución de la perfusión sanguínea que pone en riesgo la extremidad, con una duración menor o igual a dos semanas. Las causas incluyen el embolismo, la trombosis, las disecciones o la lesión arterial traumática (1-3) y puede abordarse mediante enfoque quirúrgico o endovascular. La amputación y la muerte son los dos desenlaces más temidos (4). La medición preoperatoria de biomarcadores podría servir para evaluar la severidad de la isquemia y predecir qué pacientes no tolerarán los esfuerzos terapéuticos o no tendrán adecuados resultados funcionales después del salvamento de la extremidad. La elevación de la proteína C reactiva (5), la creatina-fosfocinasa (6) y la troponina I (7) se relacionan con peores desenlaces. El índice neutrófilo/linfocito (NLR), un biomarcador inflamatorio, refleja la linfopenia relativa como respuesta al estrés y al desequilibrio inmunológico con predominio de las células efectoras (CD4) sobre las células reguladoras (8-11). Las plaquetas interaccionan con numerosas células inmunológicas en el endotelio y con los leucocitos (12-14) y en la inflamación hay una inhibición de sus propiedades antiadhesivas, lo que condiciona un efecto llamada que perpetúa el estado de “endotelio inflamado” (14). Hay pocos estudios que han valorado el papel del NLR y del índice plaquetas/linfocitos (PLR) en la isquemia aguda.
Este estudio se diseñó para evaluar la relación entre el NLR y el PLR en isquemia aguda, planteando la hipótesis de que su elevación se asocia con la presencia de peores desenlaces: amputación y muerte.
MATERIALES Y MÉTODOS
Realizamos un estudio retrospectivo, analítico y multicéntrico en una cohorte de pacientes en cuatro instituciones de alta complejidad en las ciudades de Medellín y Popayán (Colombia) entre enero del 2017 y diciembre del 2018.
Población del estudio
Se identificaron aquellos pacientes mayores de 18 años que cursaban con isquemia aguda de los miembros inferiores (1) sin otras alteraciones que pudieran interferir en el recuento celular hematológico (enfermedades autoinmunes, cáncer, uso de esteroides o patología de las líneas hematopoyéticas) o con etiologías iatrogénicas o traumáticas. El cálculo del tamaño de la muestra se realizó de acuerdo a la fórmula propuesta por Freeman: 10 * (k + 1). Considerando la inclusión de 10 variables independientes, se necesitaba estudiar como mínimo a 110 pacientes con isquemia aguda de miembros inferiores.
Se estudiaron las variables clínico-demográficas, la clasificación según Rutherford (1) y el tratamiento recibido. Se obtuvieron datos de marcadores bioquímicos, incluidos los NLR y PLR (para efecto del estudio se tomaron los valores al ingreso hospitalario), y se hizo el seguimiento de los desenlaces: amputación, mortalidad intrahospitalaria, supervivencia libre de amputación y supervivencia global a 2 años. La información se obtuvo mediante la revisión de los registros de historias clínicas (las notas de ingreso, la evolución clínica y los resultados de laboratorio), tanto las de hospitalización como las de las consultas de seguimiento. Se contactó por teléfono con los pacientes que no tenían registro de supervivencia a los 2 años después del episodio de isquemia aguda para determinar su supervivencia.
Análisis estadístico
Los datos se analizaron en el paquete estadístico SPSS (versión 24, SPSS Inc. Chicago, II, Estados Unidos). Las variables continuas se presentan como mediana con rangos intercuartiles. Las variables categóricas se presentan como valor absoluto y porcentaje. Las comparaciones se realizaron usando la prueba de χ2 para las variables categóricas y la prueba U de Mann Whitney para las continuas. Calculamos el NLR dividiendo el recuento absoluto de neutrófilos entre los linfocitos y el PLR con el recuento absoluto de plaquetas sobre los linfocitos. Se buscaron los valores de dichos índices que mejor se relacionaban con la amputación y la mortalidad mediante la construcción de curvas ROC y área bajo la curva (AUC). Se realizó un análisis de regresión logística multivariable con el fin de identificar los factores relacionados con la mortalidad intrahospitalaria.
Se analizó la supervivencia con curvas de Kaplan Meier y las diferencias se compararon mediante la prueba de rango logarítmico. Se calcularon los hazard ratio (HR) con sus respectivos IC 95 % por medio de regresión de Cox. Para todos los análisis el nivel de significancia estadística se definió como p < 0,05.
RESULTADOS
Demográficos y clínicos
Se identificaron 140 pacientes con isquemia aguda de los miembros inferiores y con características sociodemográficas homogéneas. De estos, el 56 % correspondió a hombres, con predominio de raza mestiza (95 %). La mediana de edad fue de 76 años (RIQ: 67-84). La comorbilidad más frecuente fue la hipertensión arterial (73 %, n = 102) y se identificó tabaquismo actual en un 26 % (n = 36) o pasado en un 40 % (n = 56). Un 24 % de los casos ya presentaban antecedente de cirugía vascular previa: 17 (50 %) de estos casos eran cirugías derivativas y el 29,4 % (n = 10), amputaciones de la extremidad contralateral. Los pacientes se analizaron en dos grupos: aquellos a los que se les realizó una amputación en el hospital (91 casos, 65 %) y aquellos a los que no se les practicó una amputación (49 casos, 35 %), cuyas características se presentan en la tabla I.
Tabla I. Caracterización sociodemográfica y clínica de la población
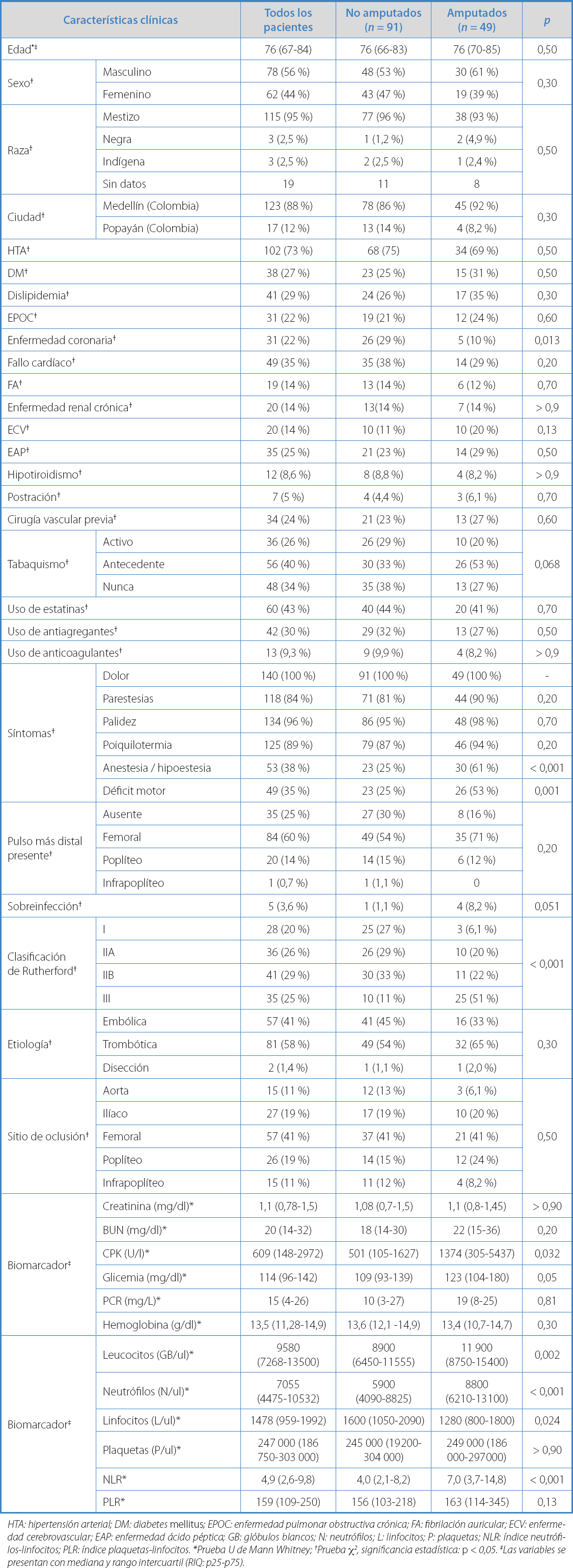
HTA: hipertensión arterial; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; ECV: enfermedad cerebrovascular; EAP: enfermedad ácido péptica; GB: glóbulos blancos; N: neutrófilos; L: linfocitos; P: plaquetas; NLR: índice neutrófilos-linfocitos; PLR: índice plaquetas-linfocitos. *Prueba U de Mann Whitney; †Prueba χ2, significancia estadística: p < 0,05. ‡Las variables se presentan con mediana y rango intercuartil (RIQ: p25-p75).
En el análisis no ajustado, los grupos eran estadísticamente comparables. Como único punto de diferencia se encontró el antecedente de enfermedad coronaria, que fue mayor en los pacientes que no fueron amputados (29 % frente a 10 %; p = 0,013). Los síntomas de dolor, palidez y poiquilotermia fueron los más frecuentes, pero la presencia de anestesia/hipoestesia (61 % frente a 25 %; p < 0,001) y el déficit motor se presentaban con mayor frecuencia en los pacientes amputados (53 % frente a 23 %; p = 0,001). Se encontró como único pulso el femoral (60 %) y se documentaron datos de sobreinfección al ingreso en el 3,6 % de los casos.
La mayoría de los pacientes ingresaron con una clasificación de Rutherford IIB (n = 41, 29 %), seguidos por aquellos que presentaban cambios irreversibles (clasificación Rutherford III), en el 25 % de los casos (n = 35). La etiología más frecuentemente reportada fue la trombosis, en el 58 % (n = 81) de los casos, y la aterotrombosis fue la más prevalente. El sitio de oclusión más frecuente fue la región femoral, en el 41% de los pacientes (n = 57). En el análisis de los biomarcadores, se encontró una relación estadísticamente significativa con el recuento de leucocitos, de linfocitos y de plaquetas entre el grupo de amputados y de no amputados. Al evaluar los NLR, la mediana al ingreso fue de 4,9. El grupo que fue llevado a amputación tenía valores más elevados en (7,0 frente a 4,0; p < 0,001). El PLR fue mayor en los pacientes amputados sin encontrar diferencias estadísticamente significativas (Tabla I).
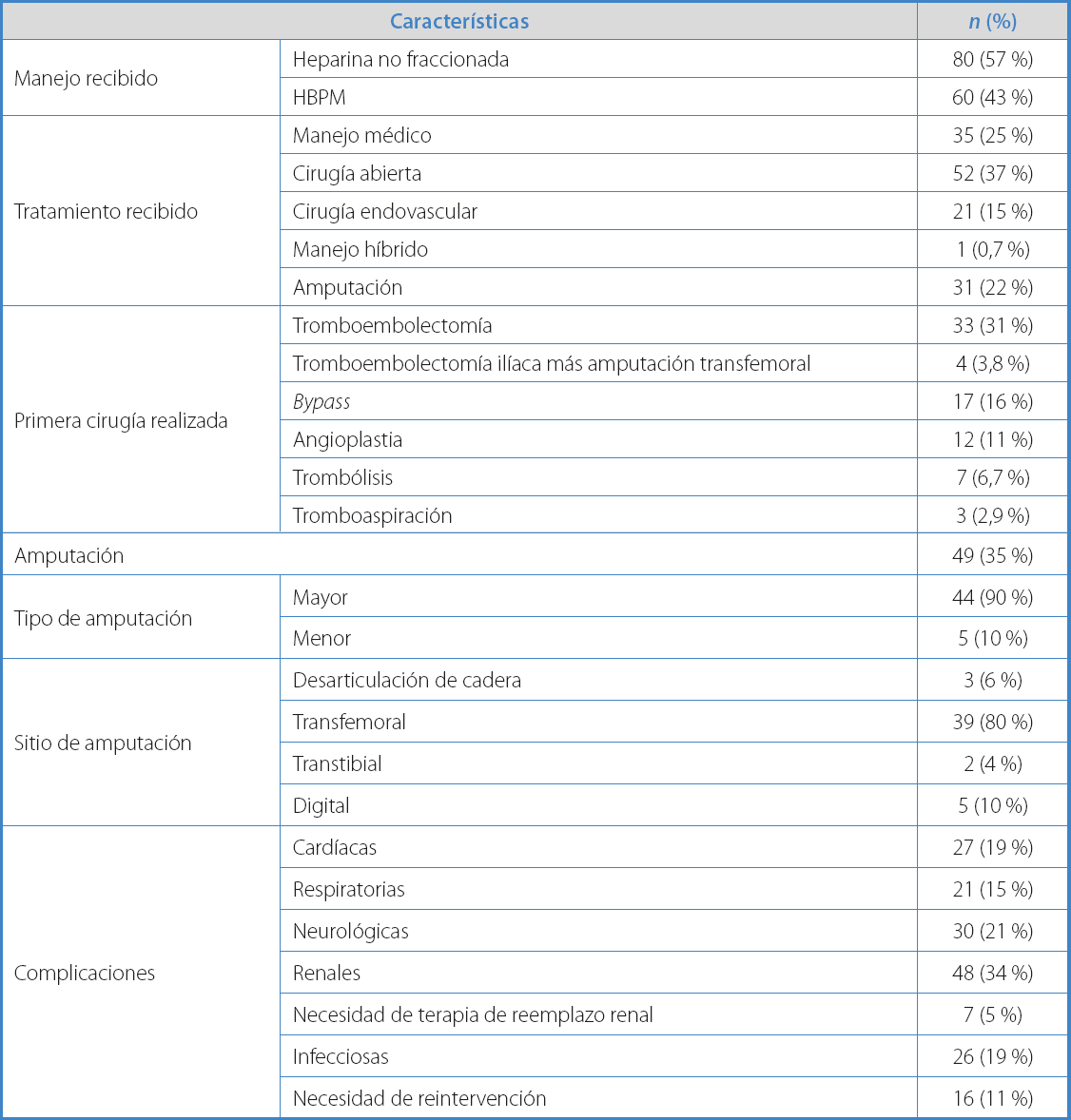
La totalidad de los pacientes recibió anticoagulación formal y la heparina no fraccionada se usó en el 57 % de los casos. Las técnicas quirúrgicas abiertas fueron las más empleadas como terapia de salvamento de la extremidad (37 %). La más frecuente fue la tromboembolectomía, seguida por la amputación primaria en pacientes con cambios irreversibles o postrados en cama 22 % (n = 31) en los que la amputación transfemoral fue la que más se realizó (80 %). En el seguimiento intrahospitalario, el 11 % (n = 16) requirió una segunda intervención. Las complicaciones más encontradas fueron las renales (34 %); sin embargo, solo se requirió hemodiálisis en el 5 % de los pacientes. Las complicaciones neurológicas se presentaron en segundo lugar (21 %), seguidas por las cardiacas (19 %). Se documentó la infección del sitio operatorio en el 19 % (n = 26) de los casos (Tabla II).
En el seguimiento a dos años, solo el 33 % (n = 46) de los pacientes logró tener una supervivencia libre de amputación. El 44 % murió en los siguientes 2 años del diagnóstico y las enfermedades cardiovasculares fueron la principal causa.
ÍNDICES NEUTRÓFILO / LINFOCITOS (NLR)
Se estimó la relación entre el NLR y los dos desenlaces principales (amputación y mortalidad) mediante curvas ROC. Cuando el desenlace estudiado fue la amputación intrahospitalaria, el punto de corte calculado del NLR para nuestra población fue de 5,2, con un área bajo la curva de 0,73 (IC 95 %, 1,55-6,63). Este mismo valor tuvo relación con aquellos pacientes que iban a ser llevados a amputación intrahospitalaria, con una sensibilidad del 63 % y una especificidad del 64 % (Fig. 1) (OR, 3,16; IC 95 %, 2,06-6,81; p = 0,002). Un INL > 5,2 presentó una relación estadísticamente significativa con el tiempo libre de amputación (HR: 3,75; IC 95 %, 2,06-6,81; p < 0,001) (Fig. 2).
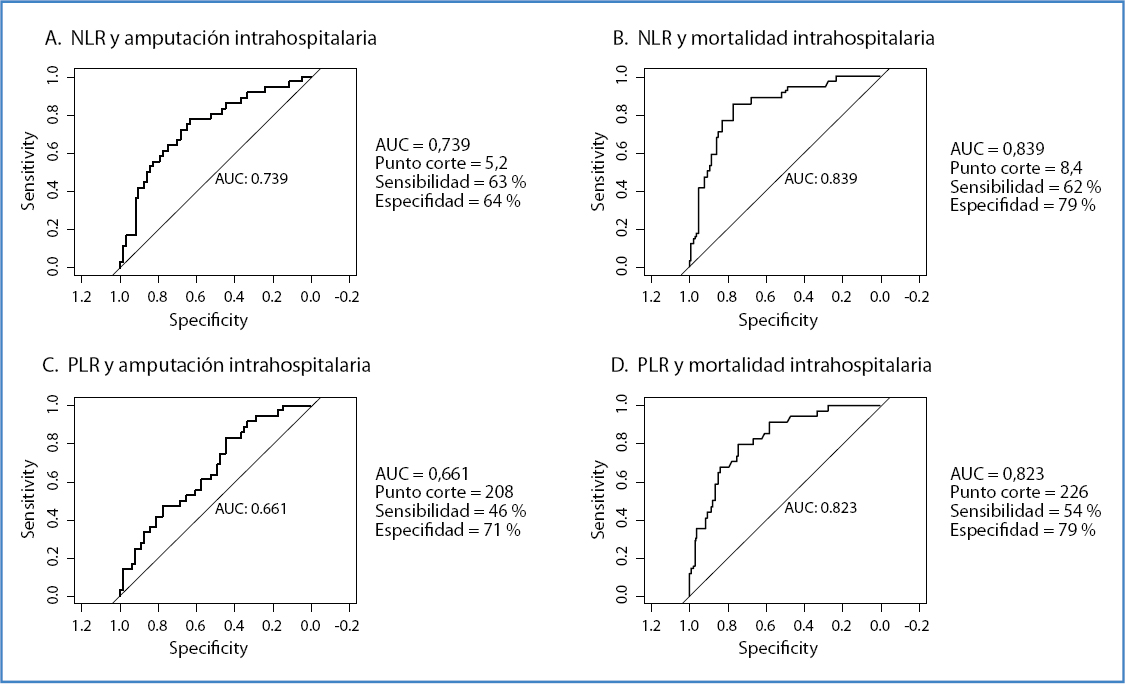
Figura 1. Curvas ROC: A. NLR y amputación intrahospitalaria. B. NLR y mortalidad intrahospitalaria. C. PLR y amputación intrahospitalaria. D. PLR y mortalidad intrahospitalaria. NLR: índice neutrófilos/linfocitos; PLR: índice plaquetas/linfocito; AUC: área bajo la curva.
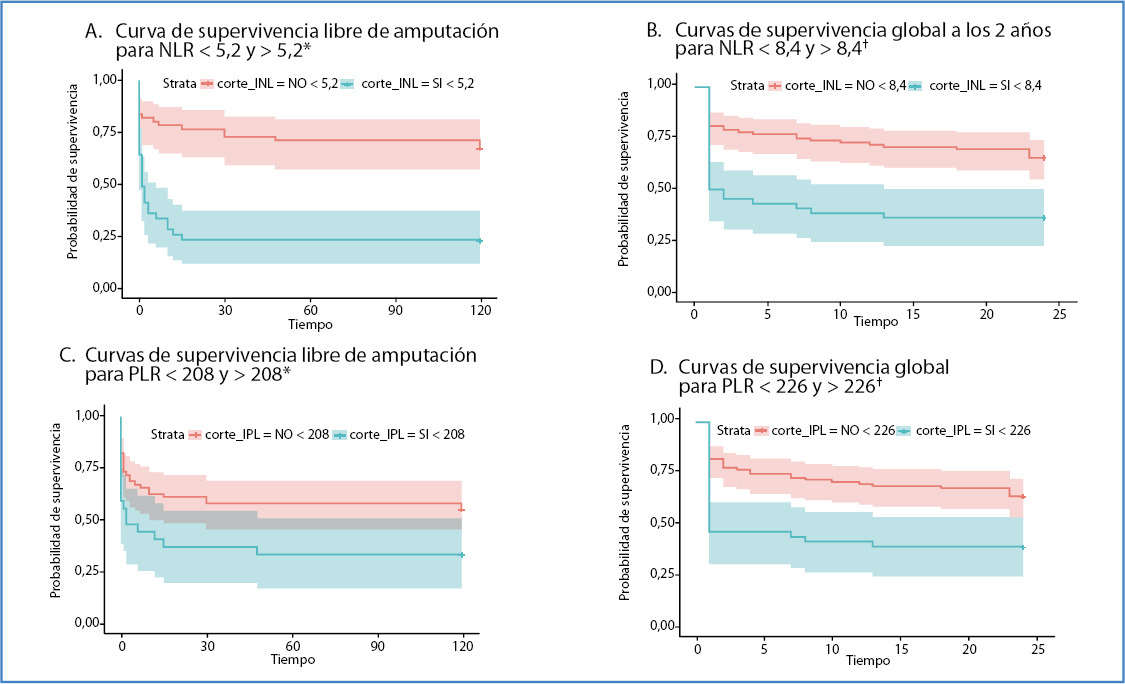
Figura 2. Curvas de Kaplan-Meyer. A. Curvas de supervivencia libre de amputación para NLR < 5,2 y > 5,2; B. Curvas de supervivencia global a los 2 años para NLR < 8,4 y > 8,4; C. Curvas de supervivencia libre de amputación para PLR < 208 y > 208; D. Curvas de supervivencia global para PLR < 226 y > 226. *Tiempo en días. †Tiempo en meses.
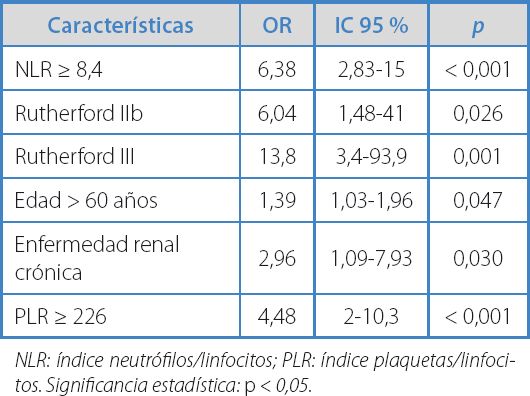
Frente a la mortalidad, el punto de corte por el NLR fue de 8,4, prediciendo con una sensibilidad del 62 % y una especificidad del 79 % la mortalidad intrahospitalaria (AUC: 0,83; OR: 6,38; IC 95 %, 2,83-15) (Fig. 1). Otros factores relacionados con la mortalidad intrahospitalaria fueron: clasificaciones de Rutherford IIB (OR: 6,04; IC 95 %, 1,48-41) y III (OR: 13,8; IC 95 %, 3,4-93,9), edad > 60 años (OR: 1,39; IC 95 %, 1,03-1,96) y la presencia de enfermedad renal crónica (OR: 2,96; IC 95 %, 1,09-7,93) (Tabla III). De igual forma, un NLR > 8,4 se correlaciona con una disminución del doble de la supervivencia global (HR: 2,58; IC 95 %, 1,55-4,28; p < 0,001) (Fig. 2).
ÍNDICE PLAQUETAS / LINFOCITOS (PLR)
Se estimó la relación entre el PLR con amputación y mortalidad mediante curvas ROC. Encontramos que un PLR > 208 no es un predictor de confianza para identificar pacientes con un mayor riesgo de mortalidad intrahospitalaria (sensibilidad: 54 %, especificidad: 79 %, área bajo la curva: 0,82, IC 95 %, 2-10,3; p < 0,001) (Fig. 1). Sin embargo, un PLR > 208 sí se correlaciona con una menor supervivencia libre de amputación (HR: 1,93; IC 95 %, 1,07-3,46; p = 0,02 (Fig. 2). Al valorar la relación del PLR con la mortalidad intrahospitalaria, encontramos que un punto de corte de 226 se relaciona con un mayor riesgo de mortalidad intrahospitalaria: una sensibilidad del 54 %, una especificidad del 79 % y AUC de 0,82 (IC 95 %, 2-10,3; p < 0,001 (Fig. 1). De igual forma, un valor de PLR > 226 se relaciona con un doble de riesgo de mortalidad a 2 años (HR: 2,33; IC 95 %, 1,36-3,89; p = 0,001 (Fig. 2).
DISCUSIÓN
La isquemia aguda de miembros inferiores es una patología vascular grave dada la rapidez de su instauración y la necesidad de un tratamiento oportuno para evitar los desenlaces más temidos: la amputación y la mortalidad. Los índices neutrófilo-linfocito y plaquetas-linfocito son un biomarcador de inflamación sistémica que se han estudiado en patología arterial periférica y, más recientemente, en isquemia aguda.
Nuestra población fue similar a la descrita en la literatura, con una mediana de edad de 76 años y con predominancia del género masculino (15,28-30). El tabaquismo activo se encontró en un porcentaje bajo, similar a lo descrito por Pasqui (29) y menor a lo encontrado por Coelho (30). La HTA fue la comorbilidad más frecuente, al igual que en estudios previos (28-30), y se describió antecedente de EAP en un porcentaje menor que lo evidenciado por otros autores (29,30). Además, encontramos el antecedente de una cirugía vascular previa en un 24 % de los casos, similar a lo descrito por Coelho (30) y menor a lo reportado por Taşoğlu (15). La etiología más frecuente del proceso isquémico fue la aterotrombosis (en un 54 % de las ocasiones), similar a lo descrito en la literatura (29,30), con una distribución simétrica en cuanto al estadio clínico según Rutherford, a diferencia de otros autores, en los que el estadio más frecuentemente encontrado fue el IIB (28-30). Se documenta, según la literatura, que las clasificaciones de Rutherford IIb o III, una edad > 60 años o un antecedente de enfermedad renal crónica se asocian a un mayor riesgo de mortalidad.
Enfocándonos específicamente en los biomarcadores, identificamos que el NLR es un factor predictor independiente para amputación y mortalidad intrahospitalaria en pacientes con isquemia aguda, en concordancia a los hallazgos de Taurino (NLR > 5,0 para amputación y mortalidad) (28), Pasqui (NLR > 5,57 para mortalidad y NLR > 6,66 para amputación) (29) y Coelho (NLR > 5,4 con amputación y mortalidad perioperatoria) (30).
En lo que respecta al uso del PLR, se identificó solo un estudio previo que valora su utilidad en isquemia aguda (29). Nuestro estudio no tuvo poder para mostrar una relación estadísticamente significativa entre el PLR y la amputación diferente a lo reportado por Pasqui, quien encontró que un PLR < 289,9 se correlaciona con un mayor salvamento de la extremidad; sin embargo, en nuestro estudio encontramos que un PLR > 226 es un factor relacionado fuertemente con la mortalidad (OR 4,48, p = < 0,001), lo cual no fue evidenciado por Pasqui.
En el seguimiento en el tiempo, estudios realizados con anterioridad muestran que la tasa de amputación es del 5-35 % (22,23). En nuestro estudio, el porcentaje de amputación fue alto (35 %), lo que podría estar relacionado con la consulta tardía de los pacientes dado el acceso no oportuno a los servicios de salud. Taşoğlu y cols. (15) encontraron que un NLR ≥ 5,2 es un factor de riesgo independiente de amputación en pacientes con isquemia aguda tras embolectomía en un seguimiento a mil días, lo que concuerda con lo observado por nuestra población; sin embargo, más del 50 % de las amputaciones se producen durante los primeros 30 días.
En el seguimiento a 2 años, encontramos una supervivencia libre de amputación solo del 33 %, un valor similar a lo descrito por Coelho (30) en su seguimiento a un año e inferior a lo descrito por Pasqui (29). Al valorar el NLR en el seguimiento temporal, encontramos que un valor > 5,2 se correlaciona con una menor supervivencia libre de amputación, con un HR de 3,75, hallazgos similares a lo descrito por Pasqui (HR: 4,1) (29). La mortalidad temprana está reportada en estudios previos, con valores que oscilan entre el 10 y el 42 % (22-25). En nuestro caso, el porcentaje fue del 25 %, mayor al 16,7 % reportado por Coelho (30). En el seguimiento a 24 meses, la mortalidad se reporta desde el 20-37 % (1,30); en nuestra serie, la mortalidad fue mayor (44 %) y similar a lo descrito por Pasqui (29), con predominancia de las causas cardiovasculares. Si bien nuestro nivel de corte para mortalidad es mayor (NLR > 8,4) que lo descrito por otros autores (28-30), sí estamos de acuerdo en que valores elevados se correlacionan con un incremento en el riesgo de mortalidad en el tiempo. Similar a lo descrito por Pasqui (29), resaltamos que un valor elevado de PLR se correlaciona tanto con una menor supervivencia libre de amputación como con una supervivencia global menor en los pacientes con isquemia aguda en un seguimiento a 24 meses. Por tanto, los hallazgos nos sugieren que un NLR y un PLR obtenidos a partir de una prueba ampliamente disponible y de bajo costo, como un hemograma, proporciona información útil y accesible sobre estos dos desenlaces.
Las limitaciones de nuestro estudio fueron el diseño retrospectivo y la toma de un único valor de NLR y de PLR al ingreso, lo que no permite evaluar la estabilidad de dichos marcadores a lo largo del tiempo.
CONCLUSIONES
La isquemia aguda de miembros inferiores es una patología que requiere una intervención oportuna dada las altas tasas de mortalidad y de morbilidad. En este estudio documentamos que las elevaciones de NLR y de PLR se relacionan con un mayor riesgo de amputación y de mortalidad intrahospitalaria y con una menor supervivencia libre de amputación y de supervivencia global. Al ser obtenidos de un laboratorio ampliamente disponible, pueden usarse como una herramienta más a la hora de estadificar a los pacientes de alto riesgo que ingresan con dicho diagnóstico, los cuales representan un reto para los cirujanos. Se requieren estudios, preferiblemente de carácter prospectivo, que permitan tener una mejor calidad en la evidencia.