INTRODUCCIÓN
Se estima que entre un 18 y un 39 % de los pacientes sometidos a una reparación endovascular de aneurisma aórtico (REVA) presentan arterias ilíacas comunes aneurismáticas o ectásicas. Así, la presencia de zonas no aptas para un adecuado sellado distal aumenta la complejidad y puede comprometer los resultados de este procedimiento (1-4). Una de las opciones disponibles para esta situación consiste en realizar un sellado distal al nivel de las arterias ilíacas externas, ocluyendo las arterias hipogástricas (5). Esta técnica permite aumentar la durabilidad de los procedimientos en comparación con los dispositivos que permiten un sellado distal en ilíacas ectásicas (6-8). Sin embargo, la oclusión de la arteria hipogástrica conlleva la aparición de manifestaciones clínicas derivadas de la isquémica pélvica en el 28-55 % de los casos. Este tipo de complicaciones puede producir una reducción importante de la calidad de vida y, de forma excepcional, tener consecuencias graves que pueden comprometer la vida de los pacientes intervenidos (5,9,10). La utilización de dispositivos ramificados ilíacos (DRI) permite mantener el flujo anterógrado a las arterias hipogástricas, lo que evita este tipo de complicaciones. En la actualidad, se recomienda la preservación de flujo anterógrado de al menos una arteria hipogástrica durante la REVA (11,12). Este tipo de procedimientos supone un aumento de la complejidad en la planificación y en la implantación de los dispositivos e implica la aparición de otras complicaciones (13-19).
El objetivo del estudio es analizar los resultados a medio plazo en la exclusión endovascular de aneurismas aortoilíacos utilizando DRI.
MATERIAL Y MÉTODOS
Diseño de estudio
Se realizó un estudio descriptivo retrospectivo multicéntrico en tres centros de la Comunidad Valenciana: el Hospital Universitario Doctor Peset (Valencia), el Hospital General de Castellón (Castelló de la Plana) y el Hospital de Casa de Salud (Valencia). Se incluyeron los DRI utilizados en el tratamiento endovascular de aneurismas aortoilíacos entre enero de 2008 y julio de 2019.
Se analizaron datos demográficos, anatómicos, intra- y perioperatorios y de seguimiento.
Las indicaciones de tratamiento de los aneurismas en todos los casos fueron una de las siguientes:
1. Aneurisma aórtico con diámetro ≥ 55 mm con aneurisma de arteria ilíaca común o ectasia arteria ilíaca común (AIC) > 20 mm de diámetro.
2. Aneurisma AIC aislado > 30 mm de diámetro.
3. Aneurisma de arteria hipogástrica > 30 mm de diámetro.
Se excluyeron los pacientes de los que no se disponían datos perioperatorios y de seguimiento.
Todos los dispositivos fueron implantados según las instrucciones de uso del fabricante. Hasta diciembre de 2013 el único dispositivo disponible fue Zenith® Branch Iliac Endovascular Graft (Z-BIS, Cook®). Tras dicho periodo, se siguieron los siguientes criterios para elegir el tipo de dispositivo a utilizar en cada caso:
El DRI Excluder® Iliac Branch Endoprosthesis (IBE , Gore®) se implantó cuando:
– Casos en los que existía una importante tortuosidad ilíaca.
– Arterias ilíacas externas con diámetros entre 11-25 mm.
– Situaciones en las que la morfología del aneurisma de aorta infrarrenal favorecía la colocación de una endoprótesis de fijación infrarrenal.
El DRI Cook® Zenith® Branch Endovascular Graft se implantó cuando:
– La distancia entre la arteria renal más baja y la bifurcación aórtica era inferior a 165 mm.
– Cuando las arterias ilíacas comunes presentaban un diámetro proximal entre 12 y 17 mm y longitudes entre 45 y 55 mm.
– Situaciones en las que la morfología del aneurisma de aorta infrarrenal favorecían la colocación de una endoprótesis de fijación suprarrenal.
Se implantaron DRI bilaterales en los casos en los que fue técnicamente factible.
En cuanto a los tipos de stent puente entre la rama del dispositivo y la arteria hipogástrica, se utilizaron los siguientes criterios:
– En los casos en los que se utilizó la endoprótesis Z-BIS (Cook®), hasta el año 2015 se emplearon los stents Advanta (Getinge®); posteriormente, stents Begraft (Bentley®) y Viabahn (Gore®). Se definió el tipo de stent a utilizar según la zona de sellado distal en la arteria hipogástrica. En caso de ser previo a la primera bifurcación, se utilizó un stent balón expandible, mientras que en caso de un sellado mas distal dentro de una rama glútea, se optó por la endoprótesis Viabahn (Gore®).
– Cuando se empleó el dispositivo IBE (Gore®), se utilizó la rama hipogástrica específica de la plataforma Excluder®.
El seguimiento se realizó mediante angio-TAC dentro de los primeros 30 días tras la intervención, y posteriormente de forma anual. En caso de ausencia de endofugas o en pacientes con insuficiencia renal crónica, se consideró el seguimiento mediante radiografía de abdomen y eco-Doppler anual.
Objetivos
Las variables de interés primario a analizar fueron las siguientes:
– Éxito técnico: definido como una adecuada exclusión del aneurisma, manteniendo un flujo directo a la arteria hipogástrica en ausencia de endofugas de tipo I y de tipo III.
– Mortalidad perioperatoria.
– Incidencia de isquemia pélvica: claudicación glútea, colitis isquémica, disfunción sexual e isquemia medular de nueva aparición tras el tratamiento.
– Permeabilidad primaria de la rama hipogástrica y de la rama ilíaca externa evaluada mediante angio-TAC o eco-Doppler.
– Reintervención relacionada con DRI: definido como la realización de procedimientos secundarios a estenosis, oclusión o endofugas relacionadas a una o a ambas ramas ilíacas del DRI.
– Mortalidad relacionada con el aneurisma.
Análisis estadístico
Las variables continuas se presentan como media ± desviación estándar y las variables categóricas como números absolutos y porcentajes.
Se utilizaron modelos univariantes Kaplan-Meier para el análisis de permeabilidad de las ramas ilíaca interna y de la rama ilíaca externa y reintervenciones relacionadas con el DRI. Todos los análisis estadísticos se realizaron utilizando el software IBM SPSS Statistics 24.0.
RESULTADOS
Se incluyeron 80 DRI implantados en 61 pacientes, todos varones, con una media de edad de 72,3 ± 6,4 años. De los dispositivos utilizados, 28 (35 %) fueron Gore® IBE y 52 (65 %), Cook® ZBIS. Dieciocho (29,5 %) procedimientos fueron bilaterales. Las principales características clínicas, comorbilidades y tratamiento de los pacientes se encuentran reflejados en la tabla I.
Tabla I. Características clínicas y tratamiento de pacientes

DM: diabetes mellitus; HTA: hipertensión arterial; ACV: accidente cerebrovascular. EPOC: enfermedad obstructiva; IRC: insuficiencia renal crónica (filtrado glomerular < 60 mL/min/ 1,73 m2); ASA: American Society of Anestesiologyst.
Las características morfológicas de los aneurismas tratados fueron las siguientes:
– AAA > 55 mm asociando ectasia de ilíaca común (> 20 mm): 20 casos (25 %).
-
– Aneurismas de ilíaca común > 30 mm:
Del total de casos, el 5 % (4) asociaba aneurismas de arteria hipogástrica de diámetro > 30 mm.
En todos los casos se implantó una endoprótesis aórtica asociada al DRI. Las características de los procedimientos aórticos, del eje ilíaco contralateral a la implantación del DRI y del tipo de stent puente utilizado se encuentran detalladas en la tabla II.
Tabla II. Características de los procedimientos

AIC: arteria ilíaca común; AIE: arteria ilíaca externa; AII: arteria ilíaca interna.*Porcentaje de stents puentes utilizados según endoprótesis.
La media de tiempo quirúrgico fue de 245,5 ± 58,5 minutos. Los promedios de tiempo de escopia, de dosis de irradiación y de volumen de contraste iodado utilizado fueron de 60,4 ± 29,8 min, 225,4 ± 133,5 Gy/cm2 y 210 ± 119,5 ml, respectivamente.
Se alcanzó el éxito técnico en el 96,3 % (77) de las intervenciones. Las situaciones en las que no se alcanzó fueron: un caso de ateromatosis ostial de la arteria hipogástrica que impidió su cateterización, un caso de disección iatrógena arteria hipogástrica y un caso de cobertura accidental de la rama hipogástrica al colocar el extensor puente entre el DRI y el cuerpo de la endoprótesis aórtica. No existieron casos de mortalidad perioperatoria.
El seguimiento medio fue de 30,1 meses (± 26,3). La incidencia de isquemia pélvica fue del 9,8 % (6). Todos presentaron claudicación glútea, de las que un paciente asoció una colitis isquémica confirmada por sigmoidoscopia y otro caso, disfunción eréctil. En la tabla III se encuentran reflejados las causas y los tiempos de aparición de dichas manifestaciones.
Tabla III. Casos de isquemia pélvica

AII: arteria ilíaca interna; DRI: dispositivo ramifi cado ilíaco; AIC: arteria ilíaca común.
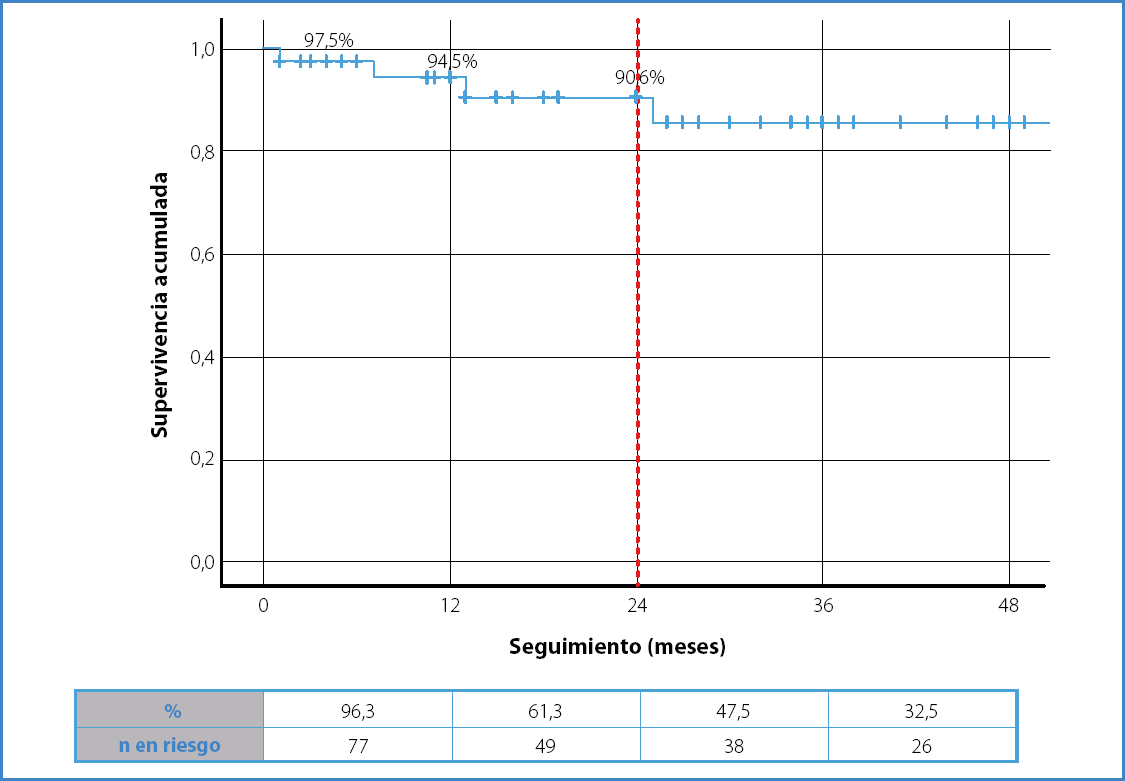
La permeabilidad primaria de las ramas hipogástricas fue del 97,5 %, del 94,5 % y del 90,6 % a los 6, 12 y 24 meses, respectivamente (Fig. 1). Existieron un total de 8 casos de trombosis de rama hipogástrica, de los que 5 (62,5 %) fueron asintomáticos.
La permeabilidad primaria de las ramas ilíacas externas fue del 100 %, del 97,3 % y del 95,5 % a los 6, 12 y 24 meses, respectivamente (Fig. 2). Se presentaron tres casos de trombosis de rama: uno secundario a la trombosis limitada de la rama a ilíaca externa y dos secundarios a la trombosis de DRI completo. Todos fueron tratados mediante bypass extraanatómico fémoro-femoral.
Hubo un 5 % (4) de reintervenciones relacionadas con el DRI durante el seguimiento: dos casos secundarios a las trombosis de la rama ilíaca externa, un caso a la trombosis DRI y un caso relacionado con una endofuga de tipo III por desconexión del stent puente. La endofuga de tipo III se trató mediante un relining del stent hipogástrico. La tasa libre de reintervención secundaria al DRI fue del 100 %, del 96,8 % y del 94,7 % a los 6, 12 y 24 meses, respectivamente (Fig. 3).
Existió un caso (1,6 %) de muerte relacionada con el aneurisma. Fue secundaria a una rotura del aneurisma a los 72 meses por una endofuga de tipo II persistente de arteria mesentérica inferior, a pesar del tratamiento.
DISCUSIÓN
Múltiples series han descrito la utilización de DRI como una técnica efectiva, segura y con una buena permeabilidad a corto y medio plazo. En la literatura, su utilización presenta tasas del 85-100 % de éxito técnico, con un 0-1 % de mortalidad perioperatoria (15-17). Su uso, cada vez está más extendido, ha permitido una mayor compresión de estos dispositivos, lo que ha mejorado su permeabilidad. Se describen escasas complicaciones a corto y medio plazo, con un 5-10 % de isquemia pélvica, un 90-95 % de permeabilidad de la rama a hipogástrica y un 90-94 % de tasa libre de reintervención a los 24 meses (18). En nuestra serie puede observarse que nuestros resultados son comparables con la literatura disponible.
Nuestros resultados en cuanto a las variables operatorias (tiempo quirúrgico, tiempo de escopia, dosis de irradiación y dosis de contraste empleado) son más elevados a los promedios observados en la literatura. Analizando estos resultados, pudo identificarse que presentamos una mayor tasa de endoprótesis complejas asociadas (13,1 %) y DRI bilaterales (29,5 %). Al comparar estos resultados con las series más importantes de DRI, nuestros resultados pueden justificarse por un mayor número de dispositivos bilaterales y endoprótesis complejas asociadas.
Esto lleva a la discusión de la utilización de dispositivos bilaterales. En la actualidad, no existe un consenso claro sobre su utilización. Las actuales guías recomiendan la preservación de al menos una arteria hipogástrica. Sin embargo, la utilización de DRI bilaterales puede llevar a la conclusión de que son innecesarios, dado los incrementos en costes, exposición a contraste yodado y dosis de radiación ionizante; además, preservar una sola arteria hipogástrica puede ser suficiente para prevenir la isquemia pélvica. Rayt y cols. compararon la oclusión bilateral y unilateral de la arteria hipogástrica durante el REVA, donde no encontraron diferencias significativas entre ambas para la aparición de isquemia pélvica y donde la oclusión unilateral presentó una incidencia nada despreciable del 31 % (10).
Por otra parte, al comparar los costes del material necesario para la oclusión de una arteria hipogástrica (coils, microcoils, plugs vasculares, una extensión de rama y fungible) y la colocación DRI (DRI, stent y fungible), la diferencia económica puede ser asumible por el beneficio de preservar una segunda arteria hipogástrica. Marqués y cols. analizaron la implantación de DRI bilaterales y demostraron que es una técnica segura y efectiva, con un éxito técnico y una permeabilidad a medio plazo similares a series con dispositivos unilaterales (18). En nuestra experiencia, consideramos que los DRI bilaterales deben implantarse por equipos con experiencia. Si el implante es técnicamente factible y el paciente presenta criterios para el tratamiento del eje contralateral, debe intentarse la preservación de la arteria hipogástrica, al menos que existan contraindicaciones.
Dado el mayor numero de vasos diana involucrados y consecuentemente la mayor complejidad de los dispositivos, podría existir una mayor incidencia de endofugas o complicaciones relacionadas. Sin embargo, la tasa de endofugas de tipo IB o III relacionadas con el DRI son escasas y concuerdan con las presentadas con nuestra serie. Donas y cols. realizaron un análisis de los procedimientos secundarios en pacientes del registro pELVIS en el que se observó una baja tasa de procedimientos secundarios a endofugas. La principal causa de reintervenciones secundarias al DRI se debieron a la oclusión de la rama a arteria ilíaca externa (19). En nuestra serie, tuvimos un 5 % (4) de reintervenciones relacionadas con el DRI, de los que tres fueron secundarias a la trombosis de la rama a ilíaca externa o del DRI. Adicionalmente, se observó un caso anecdótico de una endofuga de tipo IIIB secundaria a la fractura del stent en el seguimiento.
Por otra parte, una planificación y selección de pacientes adecuadas y el conocimiento de la técnica son fundamentales para lograr una apropiada permeabilidad en estos dispositivos. No debe subestimarse la tortuosidad ilíaca. Consideramos que debe buscarse una zona de sellado distal en la arteria hipogástrica sana, con un diámetro mínimo adecuado, sin una angulación y una carga de trombo excesivas. Parlani y cols. observaron el efecto de seis características adversas potenciales para el riesgo de reintervención. Se consideraron edad, sexo, ilíaco diámetro del aneurisma > 4 cm, aneurisma hipogástrico, asociado reparación aórtica y AAA > 5,5 cm) (20). La presencia de un aneurisma hipogástrico fue el único predictor de reintervención, con una razón de riesgo del 5,8 (95 %; p = ,008). En nuestra experiencia en aneurismas hipogástricos, es importante evitar cuellos distales cortos. Debe tenerse en cuenta que el aterrizaje distal extenso en la arteria glútea asociando embolización de las otras ramas puede tener consecuencias. Cabe destacar que en nuestra serie tuvimos un caso de aneurisma hipogástrico que requirió el sellado en la arteria glútea superior asociando la embolización de colaterales, en el que el paciente posteriormente desarrolló claudicación glútea, a pesar de la permeabilidad del DRI.
Los dos dispositivos utilizados en nuestra serie fueron el Gore® Excluder® Iliac Branch Endoprosthesis y Cook® Zenith® Branch Endovascular Graft. Recientemente un estudio por Masciello y cols. compararon los resultados perioperatorios y a medio plazo de estas dos endoprótesis y presentaron resultados satisfactorios en éxito técnico y permeabilidad a corto y medio plazo, sin encontrar diferencias estadísticamente significativas entre ambas (21). Es fundamental tomar en cuenta las indicaciones de uso de los dispositivos y que ambos dispositivos pueden ser complementarios, lo que permite tratar una mayor cantidad de aneurismas con diferentes anatomías aortoilíacas.
Finalmente, podemos analizar las principales limitaciones de nuestro estudio, que incluyen: la falta de grupo control para comparar la relevancia clínica de nuestros resultados, la falta de aleatorización y su carácter retrospectivo. y la ausencia de resultados a largo plazo, que supone la creación de un adecuado protocolo seguimiento a estos pacientes. Es importante recalcar que este estudio se basó en una experiencia de tres centros y los datos no deben generalizarse.
CONCLUSIÓN
Los dispositivos ramificados ilíacos son una herramienta útil en el tratamiento de aneurismas aortoiliacos, con una alta tasa de éxito técnico, una baja tasa de complicaciones y reintervenciones relacionadas. En nuestra experiencia, los DRI deben considerarse en aneurisma aortoilíacos con una adecuada anatomía vascular, tras realizar una adecuada selección y un estudio preoperatorio de estos pacientes. A pesar de que la aparición de complicaciones tardías y el requerimiento de reintervenciones son bajas, debe realizarse un adecuado seguimiento para mantener el éxito del procedimiento. Pese a los buenos resultados en permeabilidad y tasa libre de reintervenciones a corto y medio plazo, es necesario realizar estudios con seguimiento a largo plazo.