My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actas Urológicas Españolas
Print version ISSN 0210-4806
Actas Urol Esp vol.35 n.7 Jul./Aug. 2011
Guías EAU sobre incontinencia urinaria*
EAU Guidelines on Urinary Incontinence
J.W. Thüroffa, P. Abramsb, K.-E. Anderssonc, W. Artibanid, C.R. Chapplee, M.J. Drakeb, C. Hampela, A. Neisiusa, A. Schrödera y A. Tubarof
aDepartamento de Urología, Johannes Gutenberg University, Mainz, Alemania
bBristol Urological Institute, Southmead Hospital, Bristol, Reino Unido
cWake Forest Institute for Regenerative Medicine, Winston-Salem, NC, Estados Unidos de Norteamérica
dDepartamento de Urología, Azienda Ospedaliera Universitaria Integrata, Verona, Italia
eDepartamento de Urología, Royal Hallamshire Hospital, Sheffield, Reino Unido
fDepartamento de Urología, University of Rome La Sapienza, Roma, Italia
*La traducción de este artículo se ha llevado a cabo con el permiso de la Asociación Europea de Urología.
Dirección para correspondencia
RESUMEN
Contexto: Las primeras directrices sobre incontinencia de la European Association of Urology (EAU) se publicaron en 2001. Dichas directrices se han actualizado con regularidad en los últimos años.
Objetivo: El objetivo de este artículo es ofrecer un resumen de la actualización de las directrices sobre incontinencia urinaria (IU) de la EAU realizada en 2009.
Recogida de evidencias: El comité de trabajo de la EAU formó parte de la IV Consulta Internacional sobre Incontinencia (ICI) y, con permiso de la ICI, llevó a cabo la extracción de la información de relevancia. La metodología de la IV ICI consistió en una amplia revisión de la literatura por parte de expertos internacionales y en la creación de un nivel de consenso. Asimismo, el nivel de evidencia se calificó de acuerdo con un sistema Oxford modificado y los grados de recomendación se atribuyeron en consonancia.
Resumen de evidencias: Está disponible una versión completa de las directrices de la EAU sobre incontinencia urinaria en formato impreso (ampliada y en formato reducido), así como en formato de CD-ROM, pudiendo solicitarse a la oficina de la EAU o en línea en la dirección (http://www.uroweb.org/guidelines/online-guidelines/). La amplitud e invasividad de la evaluación de la IU depende de la gravedad y/o complejidad de los síntomas y signos clínicos, y es diferente para varones, mujeres, personas mayores de salud delicada, niños y pacientes con neuropatías. En el nivel de tratamiento inicial se aplican pruebas básicas de diagnóstico para descartar enfermedades o problemas subyacentes, tales como infecciones del tracto urinario. El tratamiento suele ser conservador (intervenciones en los hábitos de vida, fisioterapia, terapia física, farmacoterapia) y es de naturaleza empírica. En el nivel de tratamiento especializado (cuando haya fracasado la terapia inicial, ante un diagnóstico incierto o si los síntomas y señales son complejos o graves) suele ser necesaria una evaluación más elaborada, incluyendo técnica de imagen, endoscopia y urodinámica. Entre las opciones de tratamiento se incluyen intervenciones invasivas y la cirugía.
Conclusiones: Las opciones de tratamiento de la IU están creciendo en número con rapidez, y estas guías de la EAU proporcionan una gradación de las evidencias (orientada por la medicina basada en la evidencia), así como una escala de recomendaciones para que la valoración sea la adecuada y las opciones de tratamiento estén en consonancia, aplicándose así una perspectiva clínica.
Palabras clave: Incontinencia urinaria. Guías EAU. Revisión. Evaluación. Diagnóstico. Tratamiento.
ABSTRACT
Context: The first European Association of Urology (EAU) guidelines on incontinence were published in 2001. These guidelines were periodically updated in past years.
Objective: The aim of this paper is to present a summary of the 2009 update of the EAU guidelines on urinary incontinence (UI).
Evidence acquisition: The EAU working panel was part of the 4th International Consultation on Incontinence (ICI) and, with permission of the ICI, extracted the relevant data. The methodology of the 4th ICI was a comprehensive literature review by international experts and consensus formation. In addition, level of evidence was rated according to a modified Oxford system and grades of recommendation were given accordingly.
Evidence summary: A full version of the EAU guidelines on urinary incontinence is available as a printed document (extended and short form) and as a CD-ROM from the EAU office or online from the EAU Web site (http://www.uroweb.org/guidelines/online-guidelines/). The extent and invasiveness of assessment of UI depends on severity and/or complexity of symptoms and clinical signs and is different for men, women, frail older persons, children, and patients with neuropathy. At the level of initial management, basic diagnostic tests are applied to exclude an underlying disease or condition such as urinary tract infection. Treatment is mostly conservative (lifestyle interventions, physiotherapy, physical therapy, pharmacotherapy) and is of an empirical nature. At the level of specialised management (when primary therapy failed, diagnosis is unclear, or symptoms and/or signs are complex/severe), more elaborate assessment is generally required, including imaging, endoscopy, and urodynamics. Treatment options include invasive interventions and surgery.
Conclusions: Treatment options for UI are rapidly expanding. These EAU guidelines provide ratings of the evidence (guided by evidence-based medicine) and graded recommendations for the appropriate assessment and according treatment options and put them into clinical perspective.
Key words: Urinary incontinence. EAU guidelines. Review. Assessment. Diagnosis. Treatment.
Introducción
La Primera Consulta Internacional sobre Incontinencia (ICI) de 1998 desarrolló las recomendaciones para la evaluación y el tratamiento de la incontinencia, basándose en el estudio de las evidencias disponibles y en el consenso alcanzado entre expertos internacionales1. Como consecuencia de este proceso se desarrollaron las recomendaciones para la gestión de la incontinencia y se preparó una estructura específica de diagramas de flujo (algoritmos) con recomendaciones para la gestión inicial y especializada en la incontinencia urinaria (IU) en niños, hombres, mujeres, pacientes con vejiga neuropática y pacientes ancianos incapacitados2. Con permiso de la ICI se adoptaron estos algoritmos para las primeras directrices sobre incontinencia de la European Association of Urology (EAU), que se presentaron en 20013, y que han sido actualizadas posteriormente de acuerdo con los resultados de los consensos ICI-2 e ICI-3.
En el caso del ICI-4 se llevó a cabo un amplio análisis de la literatura, incluyendo los resultados de los ICI-1 a ICI-3. Asimismo, se aplicaron los principios de la medicina basada en la evidencia para el análisis y la calificación de los correspondientes artículos publicados en la literatura, para la cual se desarrolló un sistema Oxford modificado4,5. Este enfoque aplica niveles de evidencia al conjunto de artículos analizados, y a partir de ahí se derivan grados de recomendación (tablas 1 y 2).
La actualización de 2009 de las guías de la EAU sobre incontinencia está basada en la ICI-4 realizada en julio de 20086. Las guías de la EAU sobre incontinencia están disponibles en una versión impresa ampliada con una lista completa de referencias, y en una versión resumida7, en CD-ROM y en línea en la página Web de la EAU (http://www.uroweb.org/guidelines/online-guidelines/).
Algoritmos
Los algoritmos (Figura 1, Figura 2, Figura 3, Figura 4, Figura 5) seguirán siendo el esqueleto de las guías y están construidos de forma uniforme para seguir de arriba abajo una vía cronológica que incluya la evaluación del historial y los síntomas del paciente, una evaluación clínica utilizando los correspondientes estudios y ensayos y la definición de la fisiopatología subyacente como base de decisiones de tratamiento racionales. Con el fin de limitar el número de vías diagnósticas en los algoritmos, se han agrupado las presentaciones clínicas por historial y síntomas que requieren una complejidad similar en la evaluación diagnóstica.
Para una mayor simplificación las opciones de tratamiento han sido agrupadas en unos pocos diagnósticos ("trastornos") y en la fisiopatología subyacente de los mismos, para lo cual se ha empleado la terminología estandarizada por la International Continence Society (ICS). Como norma se recomienda en primer lugar la opción de tratamiento menos invasiva, procediendo escalonadamente a opciones de tratamiento cada vez más invasivas cuando la anterior falla.
La extensión y el grado de invasividad de la evaluación diagnóstica se agrupan en dos niveles: tratamiento inicial y tratamiento especializado. El nivel de tratamiento inicial comprende las medidas que generalmente se requieren en el primer contacto del paciente con un profesional de la sanidad. Dependiendo del sistema sanitario y de las restricciones generales o locales de la asistencia, el primer contacto puede ser con personal de enfermería especializado en incontinencia, con un médico de atención primaria o con un médico especialista.
La información primaria sobre la situación del paciente se obtiene mediante el historial médico, un examen físico y pruebas diagnósticas básicas fáciles de realizar para excluir enfermedades o trastornos subyacentes, como pueden ser las infecciones de vías urinarias (IVU). Si se inicia el tratamiento en este nivel de atención, será principalmente de tipo conservador y de naturaleza empírica. El nivel de tratamiento especializado se aplica a pacientes cuyo diagnóstico no pudo realizarse en el nivel de tratamiento inicial, en el cual o ha fallado el tratamiento empírico o el historial, y/ o los síntomas sugieren un trastorno más complejo o grave que requiere una evaluación diagnóstica más detallada u opciones de tratamiento específicas. En este nivel normalmente son necesarios estudios urodinámicos, con el fin de realizar un diagnóstico basado en la patología subyacente, y entre las opciones de tratamiento se encuentran intervenciones invasivas y la cirugía.
Epidemiologíaa
Existe un amplio rango de prevalencias de IU, lo que se explica por las diferencias en la definición de IU, en la metodología epidemiológica y en las características demográficas existentes entre los distintos estudios. Sin embargo, estudios prospectivos recientes han proporcionado datos sobre la incidencia de la IU y su historia natural (progresión, regresión y resolución)8-11.
La bibliografía sobre incidencia y remisión de la IU es aún escasa. Sin embargo, la incidencia anual de IU en mujeres oscila entre el 2 y el 11%, dándose las tasas más elevadas durante el embarazo. Las tasas de remisión completa de la IU oscilan entre el 0 y el 13%. La incidencia anual de la vejiga hiperactiva (VHA) oscila entre el 4 y el 6% con tasas anuales de remisión de VHA entre el 2 y el 3%.
Se ha calculado que la pérdida de orina afecta al 5-69% de las mujeres y al 1-39% de los varones. El amplio rango de prevalencias publicadas refleja las diferencias existentes en la amplitud de la definición de la IU (desde pérdida de orina una vez durante el último año hasta varios episodios de IU diarios o a la semana), en metodología (encuestas telefónicas, cuestionarios por correo, exámenes de pacientes) y en la demografía de la población estudiada. En general, la IU es el doble de frecuente en las mujeres que en los varones. Algunos datos procedentes de estudios efectuados en gemelos indican la existencia de un componente genético notable en la IU, especialmente en la incontinencia urinaria de esfuerzo (IUE)12,13.
Factores de riesgo en las mujeres
El embarazo y el parto vaginal son factores de riesgo importantes, aunque lo son menos con la edad. En contra de la idea popular anterior, no parece que la menopausia sea, en sí misma, un factor de riesgo de IU, y hay datos contradictorios en relación con la histerectomía. La diabetes mellitus es un factor de riesgo en la mayoría de los estudios. La investigación también indica que la restitución estrogénica por vía oral y el índice de masa corporal son factores de riesgo modificables importantes de IU. Aunque un deterioro leve de la función cognitiva no constituye un factor de riesgo de IU, incrementa los efectos de esta. Tabaquismo, dieta, depresión, infecciones de las vías urinarias (IVU) y ejercicio no constituyen factores de riesgo.
Prolapso de órganos pélvicos
Las mujeres que presentan IU como síntoma primario pueden presentar también prolapso de órganos pélvicos (POP), que puede ser sintomático o asintomático. La IUE y el POP muestran patrones de transmisión familiar mediada por factores genéticos o ambientales (NDE: 2). La decisión de si tratar o no el prolapso quirúrgicamente a la vez que la IU está determinada por los síntomas y las molestias que el prolapso le produce a la paciente, y por cómo puede afectar la cirugía de prolapso a los resultados de la cirugía de incontinencia. Por ello la evaluación de la IU deberá incluir una evaluación del POP, y si se confirma este hay que considerar el tratamiento del POP dentro de la estrategia de manejo de la IU, especialmente si es necesaria una intervención quirúrgica. El POP tiene una prevalencia del 5-10% basándose en el hallazgo de una masa que hace prominencia en la vagina. El parto entraña un mayor riesgo de POP en etapas posteriores de la vida, y dicho riesgo aumenta con el número de hijos. No está claro si la cesárea previene la aparición de POP, aunque la mayoría de los estudios indican que la cesárea conlleva un menor riesgo que el parto vaginal de sufrir morbilidad posterior relacionada con el suelo de la pelvis. Algunos estudios señalan que la histerectomía y otras intervenciones pélvicas aumentan el riesgo de POP. Se precisan más estudios.
Factores de riesgo en los varones
Entre los factores de riesgo de IU en los varones figuran la edad avanzada, los síntomas de las vías urinarias inferiores (SVUI), las infecciones, el deterioro funcional y cognitivo, los trastornos neurológicos y la prostatectomía.
Vejiga hiperactiva
La prevalencia de VHA en los varones adultos varía entre el 10 y el 26% y, en las mujeres adultas entre el 8 y el 42%. Aumenta con la edad y, con frecuencia, aparece con otros SVUI. Varias afecciones crónicas comunes, tales como depresión, estreñimiento, trastornos neurológicos y disfunción eréctil se han asociado de manera significativa a VHA, incluso después de ajustar respecto a covariables importantes, como la edad, el sexo y el país14.
Farmacoterapiab
Se han desarrollado muchos fármacos para el tratamiento de la IU (Tabla 3 y Tabla 4). Aunque los fármacos pueden ser eficaces en algunos pacientes, a menudo hay que suspenderlos debido a sus efectos secundarios. Así, los fármacos pueden considerarse como un complemento de la terapia conservadora15.
Fármacos empleados en el tratamiento de la VHA/ incontinencia urinaria de urgencia
La relevancia clínica de la eficacia de los medicamentos antimuscarínicos en comparación con placebo se ha comentado ampliamente16. Sin embargo, en metaanálisis extensos recientes de los antimuscarínicos más utilizados se ha demostrado claramente que estos medicamentos proporcionan beneficios clínicos considerables17-19. Ninguno de los antimuscarínicos de uso habitual (darifenacina, fesoterodina, oxibutinina, propiverina, solifenacina, tolterodina y trospio) constituye un tratamiento de primera línea ideal para todos los pacientes con VHA/ hiperactividad del detrusor (HD). El tratamiento óptimo debe individualizarse, teniendo en cuenta la comorbilidad del paciente, los fármacos concomitantes y los perfiles farmacológicos de los diferentes medicamentos19.
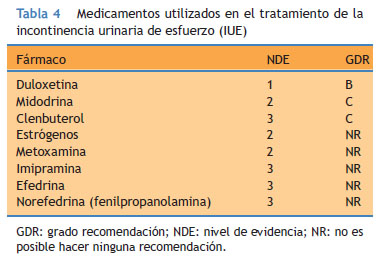
Medicamentos empleados en el tratamiento de la incontinencia urinaria de esfuerzo (IUE)
Entre los factores que pueden contribuir al cierre de la uretra figuran el tono del músculo liso y estriado uretral y las propiedades pasivas de la lámina propia uretral, especialmente su vascularización. La contribución relativa de estos factores a la presión intrauretral sigue siendo objeto de debate. Sin embargo, los datos indican que una parte notable del tono uretral está mediada por una estimulación de los receptores adrenérgicos alfa en el músculo liso uretral por parte de la noradrenalina liberada20,21. Un factor que contribuye a la IUE, principalmente en las mujeres de edad avanzada con falta de estrógenos, puede ser un deterioro de la función de coadaptación de la mucosa. El tratamiento farmacológico de la IUE pretende incrementar la fuerza de cierre intrauretral al aumentar el tono de los músculos liso y estriado uretrales. Hay varios medicamentos que pueden contribuir a este incremento22,23. Su uso clínico se encuentra limitado por una eficacia baja y/o efectos secundarios (Tabla 4).
Tratamiento hormonal de la incontinencia urinaria
Estrógenos
La carencia de estrógenos es un factor etiológico en la patogenia de varios trastornos. Sin embargo, el tratamiento con estrógenos, solos o combinados con un progestágeno, sólo ha logrado malos resultados en la IU. Los datos actuales (NDE: 1) en contra del tratamiento de la IU con estrógenos se basan en estudios diseñados originalmente para evaluar el uso de estrógenos con el fin de prevenir eventos cardiovasculares. De hecho, los datos proceden de análisis secundarios de estos estudios utilizando síntomas subjetivos, comunicados por las pacientes, de pérdidas urinarias. No obstante, estos ensayos aleatorizados y controlados (EAC) extensos revelaron un empeoramiento de la IU preexistente (de esfuerzo y de urgencia) y un aumento de la nueva incidencia de IU con los estrógenos en monoterapia o combinados con un progestágeno. Sin embargo, hay que señalar que la mayoría de las pacientes recibieron estrógenos equinos combinados, lo que quizá no sea representativo de todos los estrógenos y de todas las vías de administración.
En una revisión sistemática de los efectos de los estrógenos sobre los síntomas indicativos de VHA se llegó a la conclusión de que el tratamiento con estrógenos podría resultar eficaz para aliviar los síntomas de VHA y que la administración local puede ser la vía de administración más beneficiosa24. Es posible que el tenesmo vesical, la polaquiuria y la incontinencia de urgencia sean síntomas de atrofia genitourinaria en las mujeres posmenopáusicas de edad avanzada25. Existen evidencias sólidas de que el tratamiento vaginal (local) con estrógenos en dosis bajas puede revertir los síntomas y los cambios citológicos de la atrofia genitourinaria. Sin embargo, los estrógenos (con o sin progesterona) no deben emplearse para tratar la IU, ya que no se ha demostrado que ejerzan un efecto directo sobre las vías urinarias inferiores.
Desmopresina
La desmopresina (DDVAP) fue bien tolerada y conllevó una mejoría significativa de la IU en comparación con placebo en cuanto a reducción de las micciones/ IU nocturnas y aumento de las horas de sueño ininterrumpido. La calidad de vida (CdV) también mejoró. Sin embargo, la hiponatremia es uno de los principales efectos secundarios, clínicamente importantes, de la administración de DDVAP. La hiponatremia puede originar diversos eventos adversos, desde cefalea leve, náuseas, vómitos y anorexia hasta pérdida de conciencia, convulsiones y la muerte. En un metaanálisis se ha comunicado que el riesgo de hiponatremia ronda el 7,6%26, y parece aumentar con la edad, las cardiopatías y un volumen alto de orina en 24 horas27.
Incontinencia en los varonesc
Tratamiento inicial de la incontinencia urinaria en varones (fig. 1)
Evaluación inicial
La evaluación inicial de los varones va dirigida a identificar y excluir a los pacientes con una incontinencia complicada, que han de ser derivados para recibir tratamiento por parte de un especialista. La incontinencia complicada comprende pacientes con incontinencia recurrente tras cirugía previa fallida, con IU total y/o con síntomas asociados como dolor, hematuria, IVU recurrente, síntomas de vaciado deficiente y/o historial de radioterapia pélvica o de cirugía pélvica radical.
El grupo de pacientes con un historial de IU puede estratificarse en cuatro grupos principales de síntomas que son adecuados para el tratamiento inicial: a) goteo postmiccional; b) incontinencia en actividad física; c) incontinencia con síntomas combinados de esfuerzo y urgencia; y d) tenesmo y poliquiuria con o sin incontinencia.
Tratamiento inicial
El tratamiento conservador constituye el abordaje principal de la IU en los varones en el nivel inicial de tratamiento (Tabla 5) y, a menudo, se considera sencillo y de bajo coste. El término "tratamiento conservador" describe cualquier tratamiento que no suponga una intervención farmacológica o quirúrgica. Sin embargo, en procesos tales como la VHA a menudo las estrategias conservadoras se combinan con tratamiento farmacológico.
Muchas intervenciones de tratamiento conservador requieren un cambio de comportamiento que no es fácil de iniciar ni de mantener. La mayoría de los pacientes con síntomas leves o moderados desean probar primero tratamientos menos invasivos. Sin embargo, es posible que los pacientes con síntomas complicados o graves tengan que ser derivados directamente para recibir tratamiento especializado.
En los varones con goteo posmiccional no suele requerirse una evaluación adicional. Sin embargo, el paciente debe ser informado del modo de ejercer una contracción intensa de la musculatura del suelo de la pelvis después de orinar, o de comprimir manualmente la uretra bulbosa directamente después de la micción (GDR: B).
En los varones con IUE, incontinencia de urgencia o incontinencia de esfuerzo/ urgencia mixta, el tratamiento inicial debe incluir un asesoramiento adecuado sobre los hábitos de vida, fisioterapia, pautas miccionales programadas, terapias conductuales y medicación. En general existe poca evidencia de nivel 1 o 2, y la mayoría de las recomendaciones e hipótesis esenciales requieren comprobación adicional mediante ensayos de alta calidad. Si el tratamiento inicial no da resultado después de un tiempo razonable (por ejemplo 8 a 12 semanas), es altamente recomendable acudir a un especialista.
Tratamiento especializado de la incontinencia urinaria en varones (fig. 2)
Evaluación
Es posible que el especialista decida reinstaurar en primer lugar el tratamiento inicial si la terapia previa no ha sido la adecuada. Los pacientes con incontinencia complicada derivadas directamente para recibir tratamiento especializado probablemente necesitarán más pruebas para descartar otras enfermedades subyacentes, por ejemplo citología, cistouretroscopia y estudios de imagen de las vías urinarias. Si los resultados de estas pruebas son normales pueden ser tratados de su incontinencia mediante opciones terapéuticas iniciales o especializadas, según corresponda. Cuando persisten síntomas indicativos de HD o incompetencia esfinteriana se recomienda realizar estudios urodinámicos para confirmar un diagnóstico a tenor de los resultados fisiopatológicos (diagnóstico urodinámico) (Tabla 6).
Tratamiento
Cuando ha fracasado el tratamiento inicial y la incontinencia es molesta para el paciente e influye en su calidad de vida, pueden contemplarse tratamientos invasivos.
Incontinencia después de una prostatectomía radical. El único grupo de varones con IU que se ha investigado suficientemente es el de aquellos que se han sometido a una prostatectomía radical (PR). Sin embargo, las definiciones de continencia tras PR van desde el control total sin pañal ni pérdida, a pérdida de algunas gotas sin pañal (es decir, manchar la ropa interior) hasta entre cero y un pañal por día (es decir, pañal de seguridad).
Los factores de riesgo descritos de incontinencia post-PR comprenden edad en el momento de la cirugía, tamaño de la próstata, comorbilidad, cirugía con conservación nerviosa, estenosis del cuello de la vejiga, estadio del tumor (posiblemente relacionado con la técnica quirúrgica) y disfunción vesical y esfinteriana preoperatoria. El riesgo no guarda relación con la técnica de prostatectomía (radical frente a conservación nerviosa, abierta frente a laparoscópica frente a robótica) de acuerdo con informes de centros de excelencia.
Incompetencia esfinteriana. En el caso de la IUE debida a incompetencia esfinteriana, tras un período de tratamiento conservador de al menos 6-12 meses, el esfínter urinario artificial (EsUA) es el tratamiento de elección para los pacientes con IU moderada o grave. En estudios que muestran los resultados del tratamiento de la IU tras cirugía por obstrucción benigna de la próstata o cáncer de próstata en conjunto, las tasas de éxito del EsUA oscilan entre el 59 y el 90% (0-1 pañal/ día). Las tasas de éxito a largo plazo y la satisfacción elevada de los pacientes parecen compensar la necesidad de revisiones periódicas en algunos sujetos. Hasta que no se observe una experiencia similar con nuevos tratamientos menos invasivos, el EsUA sigue siendo el tratamiento de referencia con el que deben compararse todos los demás tratamientos (NDE: 2) (GDR: B).
La incontinencia recurrente tras la implantación de un EsUA puede ser consecuencia de una alteración de la función vesical, de atrofia uretral o de un fallo mecánico. Se debe retirar quirúrgicamente la totalidad o parte de la prótesis cuando haya infección o erosión de sus componentes. Entre los factores de riesgo se encuentran la cirugía, radioterapia, cateterismo y endoscopia (NDE: 3) (GDR: C). En pacientes con un EsUA implantado el cateterismo o la endoscopia transuretrales requieren la apertura y desactivación previa del esfínter urinario para evitar daños a la uretra.
Incontinencia urinaria de esfuerzo leve a moderada. Las suspensiones para varones son una alternativa en los varones con IUE leve o moderada (la radioterapia es un factor de riesgo adverso). La tasa de éxito mínimo global es del 58% y los mejores resultados se obtienen en los pacientes con pérdidas pequeñas o moderadas de orina que no han recibido radioterapia (NDE: 3) (GDR: C).
Las sustancias de relleno constituyen una opción menos eficaz para algunos varones con IUE leve o moderada. La tasa de fracaso precoz ronda el 50% y los efectos beneficiosos disminuyen con el tiempo (NDE: 3) (GDR: C).
La implantación de globos ajustables compresivos es una nueva opción terapéutica. Parece que se han resuelto las elevadas tasas de complicaciones que se produjeron inicialmente. Sin embargo, se necesitan más datos antes de poder emitir recomendaciones concretas (NDE: 3) (GDR: C).
Incontinencia urinaria de urgencia. En la IU de urgencia (IUU) debida a HD idiopática refractaria, la inyección de toxina botulínica A en el detrusor es un tratamiento mínimamente invasivo, con cierta eficacia, que actualmente se emplea como medicación "no aprobada" en esta indicación. Otras opciones de tratamiento son la neuromodulación y la miectomía del detrusor, que han tenido éxito en algunos pacientes varones. La cistoplastia de refuerzo con segmentos intestinales es potencialmente eficaz para controlar los síntomas, pero puede producir efectos secundarios. La derivación urinaria es una opción final (NDE: 3) (GDR: C).
Vejiga de capacidad reducida. La cistoplastia de refuerzo ha resultado eficaz en caso de vejiga de capacidad reducida por la mayoría de las causas, excepto cistitis por radioterapia (NDE: 3) (GDR: C).
Hipoactividad del detrusor. Si la incontinencia está asociada a un vaciamiento deficiente de la vejiga por hipoactividad del detrusor, debe utilizarse un método eficaz para garantizar el vaciamiento (por ejemplo, el cateterismo intermitente limpio [CIL]) (GDR: B-C).
Obstrucción de salida de la vejiga. Cuando la incontinencia se debe a una obstrucción de salida de la vejiga (OSV), primero debe liberarse la obstrucción (GDR: B-C). Las opciones de tratamiento farmacológico en caso de IU y OSV comprobada son los bloqueadores alfa o inhibidores de la 5-alfa reductasa (GDR: C). Cada vez hay más datos de la seguridad de los antimuscarínicos para tratar los síntomas de VHA en los varones con obstrucción de salida cuando se combinan con un bloqueador alfa (GDR: B).
Incontinencia en las mujeresd
Evaluación inicial de la incontinencia urinaria en las mujeres
La evaluación inicial va dirigida a identificar y excluir a las pacientes con una incontinencia complicada, que han de ser derivadas para recibir tratamiento por parte de un especialista. La incontinencia complicada comprende a pacientes con incontinencia recurrente tras cirugía previa fallida y/o pacientes con síntomas asociados como dolor, hematuria, IVU recurrente, síntomas de vaciado deficiente y/o historial de radioterapia pélvica, de cirugía pélvica radical o sospecha de fístula.
El resto de pacientes con un historial de IU puede estratificarse en tres grupos principales de síntomas que son adecuados para el tratamiento inicial: a) incontinencia en actividad física; b) incontinencia con síntomas combinados de esfuerzo y urgencia; y c) tenesmo y poliquiuria con o sin incontinencia.
La exploración física sistemática incluye una exploración abdominal, pélvica y perineal. Las mujeres deberían realizar una prueba de esfuerzo (toser y tensión) para detectar pérdidas secundarias a incompetencia esfinteriana. Ha de evaluarse si existe POP o atrofia genitourinaria. También es importante evaluar la función voluntaria de los músculos del suelo de la pelvis mediante exploración vaginal o rectal antes de empezar a enseñar ejercicios musculares de suelo pélvico (EMSP). Cuando la IU está asociada a dificultades de vaciamiento y/ o POP debería evaluarse la orina residual posmiccional (ORP).
Tratamiento
En las mujeres con IUE, IUU o IU o mixta el tratamiento inicial consiste en asesoramiento adecuado sobre los hábitos de vida, fisioterapia, una pauta miccional programada, terapia conductual y medicación (Tabla 7, Figura 3). Algunas recomendaciones se basan en un nivel de evidencia sólido y consistente. Sin embargo, muchas otras se basan en evidencias y son básicamente hipótesis que requieren ensayos adicionales en estudios de alta calidad.
Tratamiento especializado de la incontinencia urinaria en mujeres (fig. 4)
Evaluación
Las mujeres con incontinencia complicada derivadas directamente para recibir tratamiento especializado probablemente necesitarán más pruebas diagnósticas (por ejemplo, citología, cistouretroscopia o estudios de imagen de las vías urinarias) para excluir otras enfermedades subyacentes. Si dichas pruebas no revelan ninguna otra patología se debe tratar la IU de las pacientes mediante opciones terapéuticas iniciales o especializadas, según corresponda.
Es probable que las mujeres en que ha fracasado el tratamiento inicial sufran síntomas molestos, o que presenten un deterioro de la CdV y soliciten tratamiento adicional. Si se ha agotado el tratamiento inicial un tratamiento intervencionista puede estar indicado. Se recomienda encarecidamente realizar pruebas urodinámicas para diagnosticar el tipo de IU antes de la intervención, cuando sea probable que los resultados influyan en la elección del tratamiento. También puede ser útil comprobar la función uretral mediante un perfil de presión uretral o la medición de la presión de escape durante las pruebas urodinámicas.
Se recomienda encarecidamente una evaluación sistemática en busca de POP. Se debería emplear el método de Cuantificación del Prolapso de Órganos Pélvicos en los estudios de investigación, y también fuera del entorno de investigación. Se debe tratar cualquier POP sintomático que se presente.
Tratamiento
Incontinencia urinaria de esfuerzo. Cuando se confirma una IUE urodinámica pueden recomendarse las siguientes opciones de tratamiento a las pacientes que presenten alguna movilidad del cuello de la vejiga y la uretra: a) toda la gama de tratamientos no quirúrgicos; b) intervenciones de suspensión retropúbica; y c) operaciones de suspensión del cuello de la vejiga/ suburetrales.
Cuando está indicada la cirugía para IUE hay que tener en cuenta una serie de variables de confusión que determinan el éxito de la cirugía (Tabla 8). Las técnicas quirúrgicas para tratar la IU en las mujeres se recogen en la Tabla 9. La incidencia real de complicaciones asociadas a la cirugía de IU se desconoce, ya que no hay métodos normalizados de notificación ni definiciones. Además, hay discrepancias entre la práctica universitaria y comunitaria. Sin embargo, parece que existe una baja incidencia de la mayor parte de las complicaciones, lo que dificulta la realización de cálculos con poder estadístico en los EAC. Los registros nacionales aportan alguna información sobre el nivel de complicaciones. Las complicaciones son menos probables con una formación quirúrgica adecuada (NDE: 2-3) y las habilidades pueden mantenerse mediante la realización de un mínimo de 20 intervenciones anuales de cada intervención principal de acuerdo con el National Institute of Clinical Excellence (Instituto Nacional de Excelencia Clínica) del Reino Unido. Puede resultar útil corregir un POP sintomático al mismo tiempo. En las pacientes con deficiencia esfinteriana intrínseca ha de contemplarse la utilización de intervenciones de suspensión del cuello de la vejiga, sustancias de relleno inyectables y EsUA.
Hiperactividad idiopática del detrusor. La incontinencia de urgencia (por ejemplo VHA) secundaria a una HD idiopática puede tratarse mediante neuromodulación o refuerzo de la vejiga. La inyección de toxina botulínica puede utilizarse para tratar las HD sintomáticas que no respondan a otros tratamientos (GDR: C). La toxina botulínica se está empleando actualmente para la inyección del detrusor "sin aprobación" para esta indicación.
Vaciamiento deficiente. Las pacientes con disfunción miccional que provoca una ORP pueden padecer OSV o hipoactividad del detrusor. El POP es una causa frecuente de disfunción miccional.
Medición de los resultados. Hasta que no se defina un instrumento universal de valoración, hay que aplicar diversas fórmulas de medición de resultados, entre ellas: a) síntomas y cuestionario de molestias por separado; b) resultados clínicamente importantes (uso de compresa, tasas de reintervención, anticolinérgicos, CAIL e IVU recurrentes); c) complicaciones; d) una herramienta de CdV con mínima diferencia clínicamente importante y un Índice de Impresión Global; y e) resultados en términos de economía sanitaria.
Incontinencia urinaria en personas de edad avanzada de salud delicada
A las personas de edad avanzada sanas se les debe ofrecer una variedad de opciones terapéuticas similar a la de las personas más jóvenes. Sin embargo, las personas mayores de salud delicada requieren un abordaje diferente. La evaluación debe determinar el papel potencial de la comorbilidad, la medicación que toman (con o sin receta y/ o naturopáticos) y el deterioro funcional y/ o cognitivo tanto en la causalidad como en el tratamiento de la IU del paciente. Los estudios y la intervención en personas de edad avanzada y salud delicada deben tener en cuenta el nivel de molestias para el paciente y/ o su cuidador, los objetivos de los cuidados, el grado de cooperación, así como el pronóstico general y la esperanza de vida. En la mayoría de las personas de edad avanzada y salud delicada debería ser posible un tratamiento eficaz que satisfaga los objetivos de la asistencia.
Evaluación
Dado que las personas de edad avanzada y salud delicada presentan una prevalencia muy elevada de IU, habría que realizar una búsqueda y un cribado activos de casos en esta población (GDR: A). En la anamnesis se deben identificar la comorbilidad y la medicación que puedan provocar o empeorar una IU.
La regla nemotécnica en inglés DIAPPERS (delirio, infección, vaginitis atrófica, fármacos, estado psicológico, producción excesiva de orina, movilidad reducida, impactación fecal) incluye algunos trastornos concomitantes y factores a tener en cuenta. Han de destacarse dos alteraciones respecto a la regla nemotécnica original: a) la vaginitis atrófica no causa, por sí sola, IU y no debe tratarse exclusivamente con la finalidad de disminuir la IU aislada (GDR: B); y b) Los criterios de consenso actuales para el diagnóstico de IVU son poco sensibles e inespecíficos en las personas que viven en residencias de ancianos (NDE: 2).
Se debe preguntar directamente al paciente y/o a su cuidador sobre: a) el grado de molestias que causa la IU (GDR: B); b) los objetivos del tratamiento de la IU (sequedad, disminución específica de la intensidad de los síntomas, calidad de vida, reducción de la comorbilidad, disminución de la carga de tratamiento) (GDR: B); y c) El grado probable de cooperación con el tratamiento (GDR: C). También es importante tener en cuenta el pronóstico general y la esperanza de vida del paciente (GDR: C). Todos los pacientes deben someterse a un cribado de hematuria (GDR: C), ya que se desconoce si el tratamiento de la bacteriuria y piuria que no causen otros síntomas resulta beneficioso (ninguna recomendación posible). Este tipo de tratamiento puede ser perjudicial al aumentar el riesgo de resistencia a anticuerpos y provocar efectos adversos graves, como colitis por Clostridium difficile (GDR: C). No hay datos suficientes para recomendar una prueba clínica de esfuerzo en personas mayores de salud delicada.
En las personas de edad y salud delicada con nicturia molesta la evaluación debe centrarse en la identificación de las posibles causas subyacentes, entre ellas (GDR: C) la poliuria nocturna, un problema primario del sueño (como apnea del sueño) y trastornos que puedan originar volúmenes evacuados bajos (por ejemplo, ORPM elevada) (Tabla 10).
Un diario miccional (gráfico de frecuencia-volumen) puede resultar útil en la evaluación de los pacientes con nicturia (GDR: C).
Se pueden realizar los controles de humedad para evaluar la frecuencia de IU en personas que residen en centros de atención de estancia prolongada (GDR: C).
La medición del volumen de orina residual posmiccional (ORPM) puede ser de utilidad en ancianos de salud delicada con diabetes mellitus (sobre todo cuando es de larga evolución), con episodios previos de retención urinaria o antecedentes de ORPM elevada, IVU recurrentes, medicación que altera el vaciamiento de la vejiga (por ejemplo, anticolinérgicos), estreñimiento crónico, IU persistente o que empeora a pesar del tratamiento con antimuscarínicos y estudios urodinámicos previos que revelen una hipoactividad del detrusor u OSV (GDR: C).
El tratamiento de las enfermedades concomitantes (por ejemplo, estreñimiento) y la suspensión de los anticolinérgicos pueden reducir la ORPM. No existe consenso acerca de lo que constituye una ORPM elevada en ninguna población. Puede contemplarse un periodo de cateterismo en pacientes con una ORPM > 200-500ml, en los que la ORPM elevada puede ser un factor importante que contribuye a la IU o la polaquiuria molesta (GDR: C).
Los tipos más frecuentes de IU en las personas mayores de salud delicada son la IUU, la IUE y la IU mixta (en mujeres de edad avanzada de salud delicada). Las personas mayores de salud delicada con IUU de urgencia suelen presentar una hipoactividad del detrusor concomitante con una ORPM elevada en ausencia de obstrucción de salida, un trastorno denominado hiperactividad del detrusor con alteración de la contractilidad durante la micción (HDAC). No hay datos publicados que indiquen que los antimuscarínicos sean menos eficaces o causen retención en las personas con HDAC (ninguna recomendación posible).
Tratamiento inicial de la incontinencia urinaria en las personas mayores de salud delicada (fig. 5)
El tratamiento inicial debe individualizarse y dependerá de los objetivos de la asistencia, las preferencias terapéuticas y la esperanza de vida estimada, así como del diagnóstico clínico más probable (GDR: C).
En algunos pacientes es importante reconocer que la IU contenida (por ejemplo, tratada con pañales) puede ser el único resultado posible para la IU persistente tras el tratamiento de las enfermedades concomitantes y otros factores que contribuyen a la IU. Esto es especialmente cierto en personas de salud delicada con una movilidad nula o mínima (es decir, precisan la ayuda de al menos dos personas para moverse), demencia avanzada (es decir, no pueden decir su nombre) o IU nocturna. Entre los tratamientos conservadores y conductuales para la IU se encuentran cambios de los hábitos de vida (GDR: C), ejercicios vesicales en pacientes en forma y alerta (GDR: B), anticipación de la micción para los pacientes de salud delicada y con deterioro cognitivo (GDR: A). En determinadas personas de salud delicada y con una función cognitiva intacta pueden contemplarse los ejercicios de la musculatura pélvica, aunque no se han estudiado bien en esta población (GDR: C).
Todo tratamiento farmacológico (Tabla 11) debe iniciarse con una dosis baja y ajustarse con revisiones periódicas hasta que se logre la mejoría deseada o aparezcan efectos adversos. La IU puede tratarse normalmente con éxito con una combinación de las estrategias anteriores. Sin embargo, cuando el tratamiento inicial no depara una mejoría suficiente de la IU, el siguiente paso sería reevaluar al paciente para identificar posibles enfermedades concomitantes y/ o un deterioro funcional, contribuir a la IU y tratarlos.
Tratamiento especializado de la incontinencia urinaria en las personas mayores de salud delicada
Debe considerarse la derivación al especialista cuando la evaluación inicial detecte que una persona débil o de edad avanzada con IU tiene: a) otros factores significativos (por ejemplo, dolor o hematuria); b) síntomas de IU que no pueden clasificarse como incontinencia de urgencia, de esfuerzo o mixta, u otra enfermedad coexistente complicada que el médico de atención primaria no pueda abordar (por ejemplo demencia, deterioro funcional); y c) la respuesta al tratamiento inicial sea insuficiente.
El tipo de especialista dependerá de los recursos locales y del motivo de la derivación. Los especialistas quirúrgicos pueden ser urólogos o ginecólogos. A los pacientes con deterioro funcional se les podría derivar a un geriatra o fisioterapeuta. Las enfermeras especializadas en continencia pueden ser útiles en los pacientes que no pueden salir de su domicilio. La decisión de derivar a un paciente ha de tener en cuenta los objetivos de la asistencia, el deseo del paciente o de su cuidador de optar por terapias invasivas y la esperanza de vida estimada.
La edad por sí misma no supone una contraindicación de la cirugía para la incontinencia (GDR: C). Antes de contemplar la cirugía deberá someterse a los pacientes a lo indicado en la Tabla 12.
Contribuciones de autores
JW Thüroff tuvo pleno acceso a todos los datos del estudio y se responsabiliza de la integridad de los datos y de la exactitud del análisis de datos.
Concepto y diseño del estudio: Thüroff, Abrams, Andersson, Artibani, Chapple, Drake, Hampel, Neisius, Schröder, Tubaro.
Adquisición de datos: Thüroff, Abrams, Andersson, Artibani, Chapple, Drake, Hampel, Neisius, Schröder, Tubaro.
Análisis e interpretación de datos: Thüroff, Abrams, Andersson, Artibani, Chapple, Drake, Hampel, Neisius, Schröder, Tubaro.
Redacción del manuscrito: Thüroff.
Revisión crítica del contenido intelectual importante del manuscrito: Thüroff, Abrams, Andersson, Artibani, Chapple, Drake, Hampel, Neisius, Schröder, Tubaro.
Análisis estadístico: Thüroff.
Financiación: ninguna.
Apoyo administrativo, técnico o material: Thüroff.
Supervisión: Thüroff.
Otros: ninguno.
Declaración de financiación
Certifico que todo conflicto de intereses, incluyendo intereses, relaciones y afiliaciones financieras específicas relacionadas con el asunto tratado o con los materiales discutidos en el manuscrito (por ejemplo, el empleo/ la afiliación, subvenciones o financiación, consultorías, honorarios, accionariado u opción de compra de acciones, peritaje, cánones o patentes solicitadas, recibidas o pendientes), son como sigue: El Dr. Thüroff ha participado en ensayos clínicos y ha recibido subvenciones para la investigación de Pfizer.
El Dr. Abrams es consultor para Astellas, Pfizer, Ono y Novartis; ha recibido honorarios como conferenciante de Novartis, Astellas y Pfizer y participa en ensayos para Astellas.
El Dr. Andersson es consultor para Astellas, Novartis, Pfizer, Ono, BioXell y Procter & Gamble y ha recibido honorarios como conferenciante de Procter & Gamble, Novartis y Pfizer.
El Dr. Chapple es consultor para Astellas, Xention, Allergan, Recordati, Ono y Novartis; ha recibido honorarios por su labor como conferenciante de Astellas, Pfizer y Ranbaxy; ha participado en ensayos clínicos para Astellas, Pfizer, Allergan, Recordati y Tanabe y ha recibido subvenciones de Allergan y Pfizer.
El Dr. Drake ha recibido honorarios como conferenciante de Astellas y Pfizer; ha participado en ensayos clínicos de Astellas y ha recibido subvenciones de Astellas y Pfizer.
El Dr. Hampel ha recibido honorarios como conferenciante y ha sido consultor y participa en ensayos clínicos para Bayer y Lilly.
El Dr. Neisius ha recibido honorarios como conferenciante de Siemens Healthcare y Pfizer y ha participado en ensayos clínicos para Bayer y Kendle.
El Dr. Tubaro es consultor para Allergan, GSK, Orion, Novartis, Pfizer y Takeda-Millenium; ha recibido honorarios como conferenciante de Pfizer, Novartis y Sanofi y ha participado en ensayos clínicos para Allergan, Amgen y GSK.
Financiación/ apoyo y papel del patrocinador: ninguno.
aLa presente sección de las guías está basada en las recomendaciones del comité 1 de la ICI presidido por Ian Milson.
bLa presente sección de las guías está basada en las recomendaciones del comité 8 de la ICI presidido Karl-Erik Andersson.
cLa presente sección de las guías está basada en las recomendaciones de los comités 5, 6, 7, 12 y 13 de la ICI presididos por David Staskin, Gordon Hosker, David Vodusek, Andrea Tubaro, Jean Hay-Smith y Sender Herschorn.
dLa presente sección de las guías está basada en las recomendaciones de los comités 5, 6, 7, 12 y 14 de la ICI presididos por David Staskin, Gordon Hosker, David Vodusek, Andrea Tubaro, Jean Hay-Smith y Tony Smith.
Bibliografía
1. Abrams P., Khoury S., Wein A., editors. Incontinen 1st International Consultation on Incontinence. Plymouth, UK: Health Publications; 1999. [ Links ]
2. Thüroff JW, Abrams P, Artibani W, et al. Clinical guidelines for the management of incontinence. En: Abrams P., Khoury S., Wein A., editors. Incontinen 1st International Consultation on Incontinence. Plymouth, UK: Health Publications; 1999. 933-43. [ Links ]
3. Hampel C, Hohenfellner M, Abrams P, et al. EAU guidelines on incontinence. Plymouth UK: Health Publications Ltd; 2001. [ Links ]
4. Phillips B, Ball C, Sackett D, Badenoch D, Straus S, Haynes B, et al. Oxford Centre for Evidence-based Medicine levels of evidence (March 2009). Centre for Evidence Based Medicine Web site. Disponible en: http://www.cebm.net/index.aspx?o=1025. [ Links ]
5. Abrams P, Khoury S, Grant A. Evidence-based medicine overview of the main steps for developing and grading guideline recommendations. En: Abrams P., Cardozo L., Khoury S., Wein A., editors. Incontinen 3rd International Consultation on Incontinence. París: France Health Publications; 2005. 10-1. [ Links ]
6. Abrams P, Cardozo L, Wein A, Khoury S. Incontinen 4th International Consultation on Incontinence. Paris, Fran Health Publications; 2009. [ Links ]
7. Schröder A, Abrams P, Andersson K-E, et al. EAU guidelines on urinary incontinence. European Association of Urology Web site. Disponible en: http://www.uroweb.org/guidelines/online-guidelines/. [ Links ]
8. Offermans MP, Du Moulin MF, Hamers JP, Dassen T, Halfens RJ. Prevalence of urinary incontinence and associated risk factors in nursing home residents: a systematic review. Neurourol Urodyn. 2009; 28:288-94. [ Links ]
9. Botlero R, Davis SR, Urquhart DM, Shortreed S, Bell RJ. Age-specific prevalence of, and factors associated with, different types of urinary incontinence in community-dwelling Australian women assessed with a validated questionnaire. Maturitas. 2009; 20:134-9. [ Links ]
10. Wennberg AL, Molander U, Fall M, Edlund C, Peeker R, Milsom I. A longitudinal population-based survey of urinary incontinence, overactive bladder, and other lower urinary tract symptoms in women. Eur Urol. 2009; 55:783-91. [ Links ]
11. Long RM, Giri SK, Flood HD. Current concepts in female stress urinary incontinence. Surgeon. 2008; 6:366-72. [ Links ]
12. Altman D, Forsman M, Falconer C, Lichtenstein P. Genetic influence on stress urinary incontinence and pelvic organ prolapse. Eur Urol. 2008; 6:918-23. [ Links ]
13. Rohr G, Kragstrup J, Gaist D, Christensen K. Genetic and environmental influences on urinary incontinen a Danish population-based twin study of middle-aged and elderly women. Acta Obstet Gynecol Scand. 2004; 83:978-82. [ Links ]
14. Irwin DE, Milsom I, Reilly K, Badenoch D, Straus S, Haynes B, et al. Overactive bladder is associated with erectile dysfunction and reduced sexual quality of life in men. J Sex Med. 2008; 5:2904-10. [ Links ]
15. Andersson KE, Appell R, Cardozo L, et al. Pharmacological treatment of urinary incontinence. En: Abrams P., Khoury S., Wein A., editors. Incontinen 3rd International Consultation on Incontinence. Paris, Fran Health Publications; 2005. 809-54. [ Links ]
16. Herbison P, Hay-Smith J, Ellis G, Moore K. Effectiveness of anticholinergic drugs compared with placebo in the treatment of overactive bladder: systematic review. Br Med J. 2003; 326:841-4. [ Links ]
17. Chapple C, Khullar V, Gabriel Z, Dooley JA. The effects of antimuscarinic treatments in overactive bladder: a systematic review and meta-analysis. Eur Urol. 2005; 48:5-26. [ Links ]
18. Novara G, Galfano A, Secco S, D'Elia C, Cavalleri S, Ficarra V, et al. Systematic review and meta-analysis of randomized controlled trials with antimuscarinic drugs for overactive bladder. Eur Urol. 2008; 54:740-64. [ Links ]
19. Chapple CR, Khullar V, Gabriel Z, Muston D, Bitoun CE, Weinstein D. The effects of antimuscarinic treatments in overactive bladder: an update of a systematic review and meta-analysis. Eur Urol. 2008; 54:543-62. [ Links ]
20. Andersson KE. Pharmacology of lower urinary tract smooth muscles and penile erectile tissues. Pharmacol Rev. 1993; 45:253-308. [ Links ]
21. Andersson KE, Wein AJ. Pharmacology of the lower urinary tract: basis for current and future treatments of urinary incontinence. Pharmacol Rev. 2004; 56:581-631. [ Links ]
22. Andersson KE. Current concepts in the treatment of disorders of micturition. Drugs. 1988; 35:477-94. [ Links ]
23. Zinner N, Gittelman M, Harris R, Susset J, Kanelos A, Auerbach S, Trospium Study Group. Trospium chloride improves overactive bladder symptoms: a multicenter phase III trial. J Urol. 2004; 171:2311-5. [ Links ]
24. Cardozo L, Lose G, McClish D, Versi E. A systematic review of the effects of estrogens for symptoms suggestive of overactive bladder. Acta Obstet Gynecol Scand. 2004; 83:892-7. [ Links ]
25. Robinson D, Cardozo LD. The role of estrogens in female lower urinary tract dysfunction. Urology. 2003; 62 Suppl 1:45-51. [ Links ]
26. Weatherall M. The risk of hyponatremia in older adults using desmopressin for nocturia: a systematic review and meta-analysis. Neurourol Urodyn. 2004; 23:302-5. [ Links ]
27. Rembratt A, Norgaard JP, Andersson KE. Desmopressin in elderly patients with nocturia: short-term safety and effects on urine output, sleep and voiding patterns. BJU Int. 2003; 91:642-6. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: joachim.thueroff@unimedizin-mainz.de,
irene.keenan@unimedizin-mainz.de
(J.W. Thüroff)
Recibido 29 Marzo 2011
Aceptado 31 Marzo 2011