INTRODUCCIÓN
La asociación entre cáncer y trombosis venosa se conoce desde hace años. Los pacientes diagnosticados de enfermedad tromboembólica venosa (ETV) tienen una incidencia de cáncer del 6 % en el momento del diagnóstico de la ETV y del 10% en el primer año1, de forma que se ha llegado a sugerir que podría suponer un marcador de la existencia de una neoplasia oculta2.
Desde Atención Primaria debemos tener presente esta circunstancia y realizar una exploración completa al paciente sospechoso de padecer ETV y no limitarnos solo al área vascular.
CASO CLÍNICO
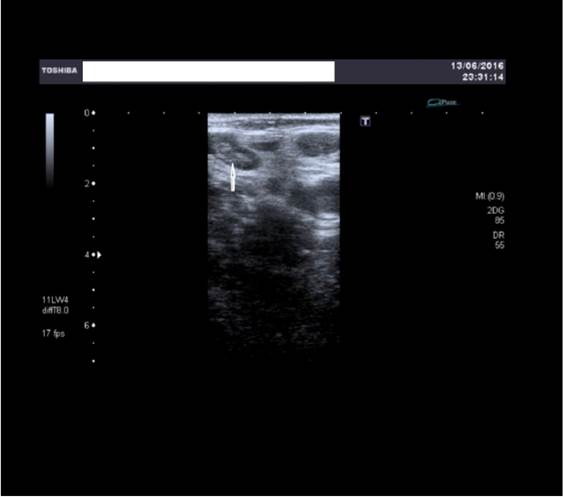
Varón de 46 años sin antecedentes personales de interés. Padre fallecido de cardiopatía isquémica aguda a temprana edad. Refiere que, estando jugando en la playa, notó un fuerte dolor en la pantorrilla izquierda. Hizo reposo relativo con vendaje elástico sin apoyar la pierna. Tomó antiinflamatorios para el dolor. A los 4-5 días comenzó con dolor intenso en el costado izquierdo irradiado al hombro que empeoraba con los movimientos. Mejoró con masajes en su lugar de vacaciones. Tras regresar a su domicilio acudió a nuestra consulta por persistencia del dolor en la pierna izquierda, al que se ha añadido inflamación y tumefacción en las últimas horas. No refería fiebre, pérdida de peso ni otros síntomas generales. Tanto la presión arterial como la auscultación cardiorrespiratoria fueron normales. La pierna izquierda presentaba tumefacción y dolor en la pantorrilla y el muslo; se palpaban varias adenopatías en región inguinal de forma bilateral, de aproximadamente de 1 cm la mayor de ellas. Solicitamos una radiografía de tórax (Figura 1) que mostró una condensación oval sugestiva de infarto pulmonar. Ante este hallazgo derivamos al paciente a urgencias hospitalarias donde, tras constatar elevación del dímero D (resto de la analítica normal), se realizó un eco-doppler objetivándose una extensa trombosis venosa profunda que afectaba a venas gemelares, poplítea y vena femoral superficial izquierda (Figura 2), así como múltiples adenopatías inguinales y poplíteas. El TAC toraco-abdominal confirmó la imagen sospechosa de tromboembolismo pulmonar y puso de manifiesto múltiples adenopatías abdominales y en el área mediastínica. Fue tratado con heparina de bajo peso molecular a dosis terapéuticas y priorizaron nuestra solicitud de punción guiada por ecografía de una de las adenopatías, ante la sospecha de un síndrome paraneoplásico. El resultado de la citología fue positivo para células tumorales malignas: linfoma no Hodgkin B de células del manto.
DISCUSIÓN
El linfoma no Hodgkin de células del manto (LCM) presenta una incidencia de 1-2/100.000 habitantes/año. Representa un 6-9 % de todos los linfomas no Hodgkin3. Se origina en los linfocitos B de la zona interna del manto, frecuentemente en linfocitos naive pre-germinales. Este subtipo de linfoma se presenta por lo general en personas de más de 50 años de edad y su frecuencia es tres veces mayor en los hombres que en las mujeres. Suele tratarse de varones mayores con afectación multiorgánica, ya que en el 70 % se presenta en estadio IV3. Puede haber poliadenopatías periféricas, hepatoesplenomegalia, poliposis linfomatoidea intestinal, síndrome constitucional y presencia de síntomas B, así como expresión leucémica con afectación de médula ósea hasta en un 60-70 % de los casos. El LCM presenta un curso moderadamente agresivo con una mediana de supervivencia global de unos 36 meses, aunque la variante blastoide suele presentar un curso clínico más agresivo con una mediana de supervivencia de 18 meses4. El pronóstico es malo, siendo generalmente una enfermedad incurable con los tratamientos habituales. Sin embargo, hoy se reconoce una mayor heterogeneidad tanto biológica como clínica, con casos de evolución muy agresiva y corta supervivencia y otros de comportamiento indolente y curso crónico5. Nuestro paciente actualmente está en remisión clínica y se ha podido incorporar a su trabajo habitual.
La relación entre la ETV idiopática (tanto el tromboembolismo pulmonar como la trombosis venosa profunda) y el cáncer es un hecho conocido, ya sugerida hace décadas por Trousseau6. Estos episodios trombóticos en ocasiones pueden preceder al diagnóstico de cáncer en meses o años, postulándose como posible marcador de la existencia de una neoplasia oculta2,7. En pacientes con cáncer, la ETV es frecuente y es su segunda causa de muerte8. El cáncer de páncreas, el de cerebro y el de estómago están asociados a una mayor incidencia de ETV. Los pacientes con cáncer diagnosticados de ETV presentan más riesgo de presentar recurrencia de ésta. Asimismo, tienen un riesgo de muerte mayor que los pacientes sin neoplasia asociada9.
La mayoría de las trombosis venosas profundas (TVP) distales suelen ser asintomáticas. Las manifestaciones clínicas, por su baja sensibilidad y especificidad, son de escasa utilidad en el diagnóstico, el cual no debería ser afirmado ni excluido basándose solo en la presentación clínica. Sin embargo, una anamnesis detallada posibilita la identificación de factores de riesgo que, añadidos a determinados hallazgos clínicos, permiten desarrollar modelos de diagnóstico de TVP, como el modelo de Wells10, que considera los antecedentes médicos más fuertemente relacionados con ETV para establecer la probabilidad clínica pretest de presentar TVP: cáncer activo, parálisis o inmovilización reciente de un miembro inferior, cirugía mayor en el último mes, dolor en trayecto venoso profundo, tumefacción en toda la extremidad inferior, aumento del perímetro de la extremidad afectada > 3 cm respecto a la asintomática (medido 10 cm bajo la tuberosidad tibial), edema con fóvea (mayor en la extremidad sintomática), presencia de circulación venosa colateral superficial (no varices preexistentes).
El diagnóstico diferencial de la TVP debe realizarse con: celulitis, tromboflebitis superficial, rotura de quiste de Baker, hematoma muscular, esguince, edema de estasis, síndrome postrombótico, artritis y linfedema. Procesos como la celulitis, miositis, abscesos, tumores benignos y malignos, edema hidrostático de tejidos blandos secundario a insuficiencia cardiaca y renal, y lesiones deportivas deben ser tenidas en cuenta en el diagnóstico diferencial. En la región inguinal las adenopatías pueden confundirse con linfangitis, tumores de tejidos blandos, hematomas, tendinitis y hernias.
Tanto en la anamnesis como en la propia exploración física debemos, como médicos de familia, no olvidar la posibilidad subyacente de neoplasia asociada, ampliando la búsqueda de hallazgos clínicos más allá de los signos clásicos tan poco específicos de TVP. En el caso presentado, la exploración completa del miembro inferior afecto posibilitó el diagnóstico precoz de una patología oncológica habitualmente agresiva y de diagnóstico tardío.