Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista de la Sociedad Española del Dolor
versión impresa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.11 no.4 Madrid may. 2004
REVISIÓN
Bloqueos nerviosos periféricos de la extremidad inferior para analgesia postoperatoria y tratamiento del dolor crónico
V. Domingo1, J. L. Aguilar2 y R. Pelaez3
| Domingo V, Aguilar JL, Pelaez R. Lower limb continuous peripheral nerve blocks for postoperative analgesia and chronic pain. Rev Soc Esp Dolor 2004; 11: 223-237.
| ||
| SUMMARY There is increasing interest in peripheral nerve blocks (PNB) because of potential benefits relative to interactions of anticoagulants and central neuraxial techniques. Among all the regional anesthesia procedures, PNB of the lower limb, and specially sciatic nerve block, are the less known and rarely used. In this paper, we summarize the recent advances in lumbosacral plexus block, with special remark on continuous catheter blocks for postoperative analgesia and chronic pain treatment. The use of long action local anes-thetics combined with a weak motor block, like ropivacaine, permits the combination of a single skin injection technique to achieve an adequate intraoperative analgesia with continuous infusion ones for postoperative analgesia. A detailed knowledge of anatomy as well as cutaneous nerve distribution is needed for the performance of these techniques. The introduction of several image-based techniques, principally ultrasound imaging, may improve the accuracy of nerve localization and needle placement. It also can help to prevent accidental puncture to vessels and other neighbouring structures. Continuous plexus and peripheral nerve blocks offer the potential benefits of prolonged analgesia with fewer side effects, greater patient satisfaction, and faster functional recovery after surgery. © 2004 Sociedad Española del Dolor. Published by Arán Ediciones, S.L. Key words: Peripheral nerve blocks. Sciatic nerve block. Femoral nerve block. Lumbar plexus block. Continuous postoperative analgesia. | RESUMEN Existe un interés creciente por la realización de los bloqueos de nervio periférico (BNP) debido a sus potenciales beneficios como los concernientes a las interacciones de los fármacos anticoagulantes y los bloqueos neuroaxiales. Los BNP de la extremidad inferior, y sobre todo, los bloqueos periféricos del nervio ciático son el pariente pobre de las técnicas de anestesia regional y, en general, son poco conocidos y por tanto poco utilizados. En este artículo se realiza una revisión de los bloqueos del plexo lumbosacro, realizando especial énfasis en los bloqueos continuos mediante catéteres para analgesia postoperatoria y para el tratamiento del dolor crónico. La utilización de anestésicos locales de larga duración de acción, asociada a un escaso bloqueo motor, como es el caso de la ropivacaína, nos permite combinar técnicas de punción única para conseguir una adecuada analgesia intraoperatoria, con las técnicas de perfusión continua para analgesia postoperatoria. Es necesario un conocimiento anatómico preciso, así como de los territorios cutáneos de inervación de las ramas del plexo lumbosacro, para la realización de estas técnicas de bloqueo. La introducción de diferentes técnicas de imagen, fundamentalmente la ultrasonografía, para la localización de las estructuras nerviosas, facilita la realización de estos bloqueos y disminuye el riesgo de lesiones de los órganos adyacentes. La realización de los bloqueos continuos de nervio periférico ofrece el beneficio de una analgesia postoperatoria prolongada, con menores efectos adversos, mayor grado de satisfacción del paciente, y una recuperación funcional más rápida después de la cirugía. © 2004 Sociedad Española del Dolor. Published by Arán Ediciones, S.L. Palabras clave: Bloqueos de nervio periférico. Bloqueo nervio ciático. Bloqueo nervio femoral. Bloqueo plexo lumbar. Analgesia postoperatoria continua.
|
1Facultativo Especialista de Área. Servicio de Anestesiología, Reanimación y Terapéutica del Dolor. DEAA. Hospital Lluís Alcanyis. Xàtiva. Valencia.
2Jefe de Servicio de Anestesiología, Reanimación y Terapéutica del Dolor. DEAA. Clínica Palmaplanas. Palma de Mallorca
3Facultativo Especialista de Área. Servicio de Anestesiología, Reanimación y Terapéutica del Dolor. DEAA. Clínica Palmaplanas. Palma de Mallorca
Recibido: 31-03-04.
Aceptado: 07-04-04.
1. INTRODUCCIÓN
Los bloqueos nerviosos periféricos (BNP) del miembro inferior para cirugía en comparación con los del miembro superior se encuentran infrautilizados, a pesar de que son relativamente sencillos de realizar y tienen un bajo índice de complicaciones. Un estudio realizado en EE.UU. ha demostrado que los BNP, y más concretamente los BNP de miembro inferior, son poco empleados en la práctica anestésica (1). Entre los anestesiólogos en formación se percibe claramente un deseo de realizar más BNP (2). En el pasado, el uso del neuroestimulador en Europa era mínimo comparado con su uso en EE.UU.; sin embargo, con las mejoras de los equipos de estimulación nerviosa se ha producido la situación inversa. En la actualidad, los anestesiólogos franceses en formación realizan un 23% de sus actos anestésicos con anestesia regional. Esto representa un incremento de 14 veces con respecto a los realizados en 1980 y de 16 veces en el uso de los bloqueos de plexo / nervio periféricos (un 21% de todas las anestesias regionales) (3). La gran mayoría de los BNP fuera de los EE.UU. son realizados con neuroestimulador y por tanto, se podría inferir que el método para aumentar la realización de bloqueos de nervio periférico en EE.UU. sería la generalización del uso del neuroestimulador, ya que se considera que el 40% de los anestesiólogos en formación de los EE.UU. presentan una inadecuada formación en la realización de dichos bloqueos (4,5).
A pesar del bajo índice de complicaciones de estos BNP del miembro inferior, estas no se deben infravalorar. La utilización del neuroestimulador parece ser que ha producido una disminución de la percepción del riesgo de lesión neurológica. La incidencia real de lesiones neurológicas tras la utilización del neuroestimulador es desconocida. Numerosos anestesiólogos continúan realizando los BNP con intensidades eléctricas muy bajas (<0,5 mA) (6) para situar la punta de la aguja lo más cerca posible del nervio y mejorar el porcentaje de éxitos de los bloqueos, aunque este punto es en la actualidad controvertido, ya que se puede producir más perjuicio que beneficio (7-10).
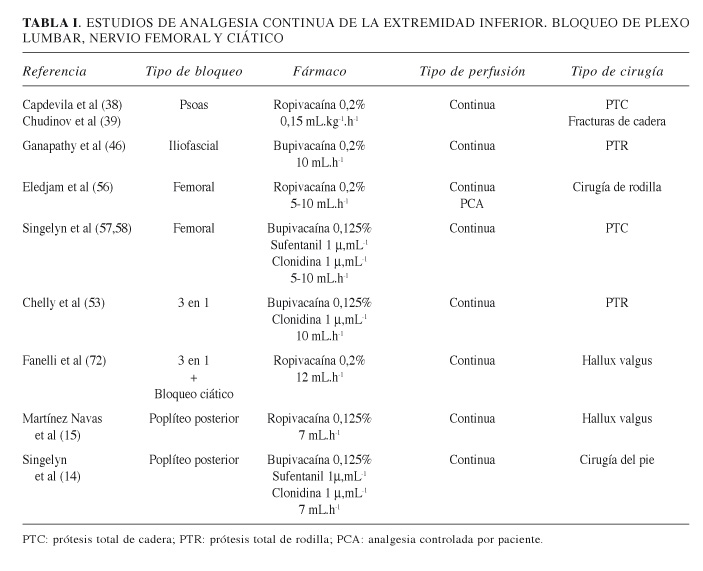
La utilización de BNP para analgesia postoperatoria o para tratamiento del dolor crónico no está tan extendido, a pesar de su utilidad, incluso en el ámbito domiciliario en programas de cirugía mayor ambulatoria (CMA) (11,12). En los últimos tiempos se están publicando un gran número de trabajos con relación a los BNP del miembro inferior para analgesia postoperatoria, muchos de ellos bloqueos continuos mediante catéteres perineurales, fundamentalmente del nervio ciático (13-15) (Tabla I) Un reciente estudio (16) ha demostrado que la mayoría de los pacientes a los que se les practicó un bloqueo periférico continuo para analgesia postoperatoria en su domicilio se encontraban satisfechos con la técnica, siempre que se controlaran diariamente por teléfono, pero sólo un tercio de los pacientes se encontraron satisfechos cuando tuvieron que reprogramar las bombas electrónicas de infusión. La combinación de estas técnicas continuas con la utilización de anestésicos de larga duración, como la ropivacaína, y la adición de clonidina, permiten la realización de cirugías con una intensidad dolorosa media-alta en programa de CMA, con unos postoperatorios relativamente confortables e incluso con la realización de rehabilitación precoz, lo que mejora los resultados de la cirugía. En dolor crónico, la utilización de bloqueos anestésicos mediante catéteres continuos facilita la fisioterapia y es un excelente método analgésico (17-19). Dentro del dolor crónico se debe destacar el importante papel que juegan los bloqueos simpáticos de extremidades en el diagnóstico y tratamiento del síndrome de dolor regional complejo (CRPS) (20-23).
2. RECUERDO ANATÓMICO
La inervación del miembro inferior está asegurada conjuntamente por el plexo lumbar y el plexo sacro.
2.1. Plexo lumbar
El plexo lumbar está formado por la convergencia de las raíces anteriores de los cuatro primeros nervios espinales lumbares. Recibe habitualmente las fibras del 12º nervio torácico y emite hacia el plexo sacro una rama que nace del 4º nervio lumbar. El conjunto del plexo está situado en el interior del músculo psoas mayor en un compartimiento aponeurótico único. En la parte alta del compartimiento se originan directamente ramas terminales: nervio iliohipogástrico e ilioinguinal (L1), nervio genitocrural (L1 y L2), ramas musculares para el cuadrado lumbar (T12-L4), psoas mayor (L2-L4) y psoas menor (L1). Más lateral y distalmente, los nervios espinales L1 a L4 se dividen en ramas anteriores y posteriores. Las fibras de las ramas posteriores se reorganizan y se fusionan para constituir el nervio cutáneo lateral del muslo o femorocutáneo (L1-L2) y el nervio crural (L1 a L3). Las ramas anteriores convergen para formar el nervio obturador (L2-L4) y el inconstante nervio accesorio del obturador (L3-L4).
2.2. Plexo sacro
Está constituido por la unión de las ramas anteriores del último nervio espinal lumbar (L5) con los tres primeros nervios espinales sacros (S1 a S3), a los cuales se agregan dos contingentes de fibras provenientes respectivamente de las raíces anteriores del 4º nervio lumbar y del 4º nervio sacro. El contingente procedente de L4 alcanza la rama anterior de L5 en la proximidad de su salida del conducto espinal, para constituir el tronco lumbosacro. Las ramas anteriores de los otros nervios sacros alcanzan el plexo justo por encima de la gran escotadura ciática, bajo la forma de dos láminas nerviosas. La lámina inferior, plexiforme y delgada, se continúa directamente por el nervio pudendo. La lámina superior se prolonga por el nervio ciático que deja la pelvis a ese nivel.
El nervio ciático es el más grande de los nervios del organismo. En realidad está constituido por dos nervios distintos, el nervio peroneo común y el nervio tibial, rodeados por una vaina común. Estos dos nervios descienden en esta vaina hasta el tercio inferior del muslo, a nivel de la fosa poplítea, donde se dividen en las dos ramas terminales (24-28).
3. TÉCNICAS DE BLOQUEO DEL PLEXO LUMBAR
El bloqueo del plexo lumbar requiere una técnica con la que se sitúa el anestésico en el espacio entre los músculos psoas mayor y cuadrado lumbar y su fascia. Este bloqueo se puede realizar mediante dos tipos de abordaje: el posterior y el anterior. En el abordaje posterior con una única punción se puede bloquear íntegramente el plexo.
3.1. Abordaje posterior
Estudios anatómicos y radiológicos (29) han demostrado que el plexo lumbar se encuentra en el espesor del músculo psoas mayor, en un espacio aponeurótico separado por láminas, que permite separar un plano muscular superficial y un plano profundo. El plano aponeurótico que rodea el plexo deriva de la fascia ilíaca y ha sido llamado compartimiento pléxico del psoas, sin embargo, el nervio obturador presenta una gran variabilidad en su localización, pudiéndose encontrar en el mismo plano que el nervio femoral y el nervio femorocutáneo, o bien fuera del músculo psoas mayor. Esto puede explicar los diferentes resultados en el éxito de este bloqueo encontrados por diferentes autores (30). A pesar de estas variaciones, este abordaje posterior proporciona un bloqueo del nervio obturador en más ocasiones que cuando se realiza por vía anterior (31,32). El bloqueo del plexo lumbar está indicado para cirugía de la extremidad inferior por debajo de L1 y así, para la cirugía de cadera y rodilla es una técnica estándar, tanto para analgesia intra como postoperatoria (2,33,34). En el caso de la cirugía de cadera, se precisa el bloqueo de los dermatomas y osteotomas L1 a L4, por lo que este bloqueo por vía posterior parece el más adecuado. Para analgesia continua postoperatoria, el abordaje posterior parece ser que es el que presenta un menor número de desplazamientos del catéter, comparado con el abordaje anterior, seguramente porque la musculatura paravertebral fija mejor el catéter en un área que presenta una gran movilidad (35). Se han descrito variaciones de las técnicas clásicas de localización de este compartimiento del psoas con la finalidad de mejorar el porcentaje de éxitos del bloqueo, fundamentalmente del nervio obturador, como son la utilización de la neuroestimulación (36), que en la actualidad se considera imprescindible, y técnicas de imagen como la ultrasonografía que nos permite evitar punciones renales accidentales sobre todo en los abordajes muy superiores (L3-L4) (37). El paciente es colocado en decúbito lateral sobre el lado contralateral al que se bloquea, con los muslos y las rodillas flexionados. Con la técnica de Winnie (32) el punto de punción se sitúa en la intersección de la línea que une las crestas ilíacas con la perpendicular pasando por la espina ilíaca posterosuperior. En la técnica de Chayen (31), el punto de punción es más medial y ligeramente más caudal. La aguja se hace avanzar perpendicularmente a la piel progresando a través del cuadrado lumbar y después al plano posterior del psoas mayor hasta su compartimiento pléxico, lo que se traduce en la aparición de contracciones musculares en la extremidad inferior, a nivel del cuádriceps si se utiliza la vía de Winnie, y a nivel de tobillo y pie si se utiliza la vía de Chayen (Fig. 1).
Estudios prospectivos recientes valorando la eficacia del bloqueo continuo del compartimiento del psoas con catéter en prótesis total de cadera (ropivacaína 0,2% a 0,15 mL.kg-1.h-1) han demostrado un éxito del 97% en la colocación del catéter con una excelente analgesia postoperatoria (EVA medio de 10/100 en reposo y de 15-25/100 con la movilización) sin necesidad de opiáceos sistémicos suplementarios. Asimismo, comparando este bloqueo con la analgesia endovenosa con meperidina, se observan unas puntuaciones de EVA (escala visual analógica) menores en los tres primeros días postoperatorios con una satisfacción del paciente mucho mayor (38,39). La técnica para la colocación del catéter es similar a la descrita anteriormente. Se hace avanzar la aguja apareciendo en primer lugar las contracciones de los músculos paravertebrales, que a unos 6-8 cm desaparecen, y aparece entonces la contracción del cuádriceps con una intensidad de neuroestimulación de 0,5 mA, indicando la proximidad del plexo; el catéter es entonces introducido 3-5 cm más allá del orificio de la aguja (40). Un estudio reciente ha considerado que, salvo en caso de duda sobre la localización del catéter, no es necesaria la comprobación radiológica rutinaria del mismo (41) (Fig. 2).
Los volúmenes de anestésico local utilizados son variables y oscilan entre 20 y 40 mL en inyección única, dependiendo de la vía utilizada. Entre las complicaciones que presenta este bloqueo merece destacar el bloqueo peridural, con una incidencia variable según las series (36), el bloqueo subaracnoideo, la punción renal (42), la inyección intravascular y el hematoma del psoas. Se ha descrito incluso la aparición de dolor de miembro fantasma en un paciente amputado de pie tras la realización de un bloqueo de plexo lumbar con la técnica de Winnie. Se consiguió la desaparición del dolor con la realización de un bloqueo del nervio ciático por la vía de Labat (43).
3.2. Bloqueo del plexo lumbar por vía anterior
El nervio crural a nivel del triángulo crural se divide en ramas anteriores y posteriores. Las dos ramas anteriores son el nervio cutáneo lateral del muslo, que asegura la inervación cutánea de la cara anterior del muslo hasta la rodilla, y el nervio cutáneo medial del muslo que asegura la inervación de la cara interna del muslo. Las ramas posteriores son las ramas articulares destinadas a la cadera y a la rodilla, y el nervio safeno, principal rama terminal del nervio crural. Cuando pasa por encima del ligamento inguinal, el nervio crural recorre el surco entre los músculos psoas e ilíaco, por debajo de la aponeurosis común de los dos músculos, la fascia ilíaca. Por debajo del ligamento inguinal se sitúa en el triángulo crural, cuyo suelo está formado por los músculos pectíneo, psoas e ilíaco, y su techo, por la fascia lata.
Bloqueo iliofascial
Esta técnica es una variación del bloqueo del nervio crural o femoral y las indicaciones son similares a las de dicho bloqueo (44,45). En el bloqueo iliofascial, el punto de punción se sitúa 1 cm por debajo de la unión del tercio externo con los dos tercios internos del ligamento inguinal, a fin de no penetrar en el compartimiento específico del nervio crural. La aguja de neuroestimulación de 50 mm es introducida con una inclinación de 75º con respecto a la piel. Se debe notar un primer resalte cuando la aguja atraviesa la fascia lata, seguida de un segundo resalte al atravesar la fascia ilíaca. Al llegar a este punto se angula la aguja 30º y se avanza 1 cm. A este nivel se pueden administrar 25-35 mL de anestésico local. Si queremos colocar un catéter, al llegar a este punto y tras administrar 20 mL de AL para dilatar el compartimiento, se hace avanzar el catéter 15-20 cm cefálicamente y entonces administramos 10 mL más del AL. Un estudio prospectivo, aleatorizado comparando el bloqueo continuo iliofascial con bupivacaína 0,2% a 10 mL.h-1 frente a placebo en cirugía de prótesis total de rodilla (PTR) ha demostrado una disminución del consumo de morfina en el periodo postoperatorio inmediato (46). Estudios recientes muestran unos porcentajes de éxito de colocación del catéter en esta localización de entre el 95-100% (47,48), sin embargo, en el estudio de Ganapathy se demuestra que con un 73% de bloqueo completo del plexo lumbar, la tomografía muestra que sólo el 40% de los catéteres se encuentra situado en la posición ideal (por encima del tercio superior de la articulación sacroilíaca en la vaina del psoas). En cuanto a la toxicidad de los AL en este bloqueo continuo iliofascial, las concentraciones plasmáticas de bupivacaína en niños se mantuvieron dentro de los límites de seguridad, con una buena tolerancia del bloqueo y un alivio satisfactorio del dolor en la mayoría de los casos (49).
Bloqueo del nervio femoral o crural
El principio de la técnica es abordar el nervio crural en el triángulo crural, inmediatamente por debajo del ligamento inguinal. El paciente es colocado en decúbito supino con la extremidad inferior en una abducción moderada (10-20º), la rodilla ligeramente flexionada y el pie en reposo. En general se puede realizar con la extremidad inferior en cualquier posición siempre que se pueda palpar la arteria femoral y localizar el ligamento inguinal. El punto de punción se sitúa 1 cm por debajo del ligamento inguinal y externamente a la arteria femoral (50). Se inserta la aguja perpendicularmente a la piel o con una ligera inclinación proximal hasta que se producen las contracciones del cuádriceps. El paso a través de la fascia lata se percibe claramente, mientras que la expansión de la fascia ilíaca que rodea el nervio suele pasar desapercibida. Una vez en este punto se inyectan 25-30 mL del AL escogido si se realiza una técnica de punción única (Fig. 3). Numerosos estudios clínicos prospectivos confirman el uso de la analgesia continua mediante catéter situado en la vaina femoral en la cirugía de la rodilla (51-53). Esta técnica proporciona mejores resultados en términos de eficacia y tolerancia comparada con la PCA (patient-controlled analgesia) endovenosa, y además proporciona un alivio del dolor similar evitando la retención urinaria, bloqueo motor bilateral e hipotensión si la comparamos con la analgesia epidural. Se han propuesto varios métodos de administración de AL por el catéter femoral para analgesia postoperatoria: bolus intermitentes (PCA), infusión continua, o infusión continua combinada con bolos (54). La utilización de bupivacaína o lidocaína en estas perfusiones se ha asociado con disestesias (51,55) y además la bupivacaína produce bloqueo motor residual. La ropivacaína, que tiene una toxicidad cardiaca y neurológica menor que la bupivacaína, y produce menor grado de bloqueo motor, es una buena elección para los bloqueos nerviosos continuos. Un estudio comparando los tres métodos de administración antes citados para analgesia postoperatoria en cirugía de rodilla, ropivacaína 0,2% en infusión continua a 10 mL.h-1, ropivacaína 0,2% en PCA con bolos de 10 mL con un periodo de cierre de 1 h, y ropivacaína 0,2% en infusión continua a 5 mL.h-1 + PCA con bolos de 5 ml, no ha demostrado la superioridad de ningún método sobre los demás, aunque la PCA mostró un menor consumo de ropivacaína. Durante las primeras 12 h postoperatorias las técnicas con PCA proporcionaron un mayor alivio del dolor tanto en reposo como durante la movilización, aunque posteriormente ya no se encontraron diferencias probablemente debido al efecto acumulativo de los AL durante la infusión continua (56). Asimismo, el bloqueo continuo del nervio femoral puede ser beneficioso en las prótesis totales de cadera (PTC). Un estudio prospectivo comparando la efectividad de la PCA endovenosa, analgesia femoral continua y analgesia epidural continua tras PTC demostró que la analgesia femoral y la epidural necesitaron menos requerimientos de opiáceos que la endovenosa. Además el bloqueo femoral continuo presentó menor incidencia de náuseas, vómitos, prurito y sedación que la PCA endovenosa, y menos incidencia de retención urinaria e hipotensión que la epidural (57,58).
En cuanto a las complicaciones de los catéteres continuos femorales son muy escasas. La colocación de un catéter en las proximidades del nervio y las estructuras vasculares femorales podría ser cuestionada ya que la cateterización venosa femoral presenta un índice de colonización bacteriana bastante elevado (13-34%) (59). La colonización bacteriana del catéter femoral continuo es frecuente, con una incidencia del 57%. En catéteres caudales o epidurales en pediatría, esta incidencia es menor pero también alta (20-35%) (60,61). El sitio de inserción del catéter femoral puede influir en estos resultados del catéter femoral, ya que existe una frecuente contaminación con microorganismos de origen fecal o urinario. La utilización de antibioticoterapia profiláctica, las soluciones de AL (efecto bacteriostático) y el uso de filtros antimicrobianos (0,2 µm) disminuye el riesgo de infección. El germen más frecuentemente aislado es Stafilococo epidermidis en un 72% de los casos, y únicamente en un 1,8% de los casos se produjo bacteriemia con fiebre, que desaparecieron con la retirada del catéter (62). Así pues, la utilización del catéter femoral continuo para analgesia postoperatoria es efectivo, pero induce una colonización bacteriana elevada. No se recomienda el cultivo del catéter de forma sistemática, pero las complicaciones infecciosas requieren la retirada inmediata del catéter, su cultivo, y valorar la realización de una ecografía del psoas para descartar un absceso a ese nivel.
Bloqueo "3 en 1" o paravascular de Winnie
El bloqueo "3 en 1" fue descrito por Winnie en 1973 como una alternativa a las múltiples inyecciones y grandes volúmenes de AL necesarios para conseguir un bloqueo troncular de la extremidad inferior (32,63). Como en el triángulo crural, el nervio crural está envainado por las aponeurosis de los músculos que lo rodean. Propuso inyectar una solución anestésica cerca del nervio crural y favorecer su progresión cefálica en dirección al plexo lumbar a lo largo de los planos constituidos por las expansiones aponeuróticas provenientes de los músculos psoas, ilíaco y transversos, para obtener un bloqueo simultáneo de los nervios crural, femorocutáneo y obturador. Esta hipótesis formulada por Winnie fue confirmada posteriormente (64). Algunos investigadores, sin embargo, han cuestionado la eficacia del bloqueo 3 en 1. El nervio obturador en particular no se bloquea adecuadamente en un porcentaje elevado de casos (65,66). Otros autores utilizando ultrasonografía han conseguido el bloqueo de los tres nervios con una analgesia quirúrgica adecuada y una disminución de los tiempos de latencia del bloqueo (67,68). Con técnicas de resonancia magnética se ha demostrado que la distribución del AL en un bloqueo tres en uno es lateral, caudal y ligeramente medial. De esta manera, el nervio crural se bloquea siempre, el nervio femorocutáneo se bloquea por la distribución lateral del AL, y la rama anterior del nervio obturador se afecta en su punto más distal por la distribución medial; pero la rama posterior del nervio obturador no se bloquea prácticamente nunca (69). Hay que destacar además, que en este estudio, la distribución cefálica del AL se observó únicamente en un 43% de los casos, y que en ningún caso alcanzó las raíces del plexo lumbar. Basándose en los estudios clínicos y radiográficos obtenidos en adultos, Capdevila indica que el AL usado en el bloqueo 3 en 1 difunde por debajo de la fascia ilíaca y en el espesor del psoas mayor, pero muy raramente alcanza el plexo lumbar (44).
En el bloqueo 3 en 1, el punto de punción es el mismo que para el bloqueo del nervio crural, es decir, 1 cm por debajo del ligamento inguinal y por fuera de la arteria femoral. La aguja conectada a un neuroestimulador se introduce con una inclinación de 20-30º con respecto al plano cutáneo hasta obtener las contracciones del cuádriceps. Si queremos utilizar una técnica de inyección única, se administran entonces 30-40 mL del AL seleccionado. En caso de querer realizar un bloqueo continuo con catéter, insertamos el mismo 10-15 cm en la vaina femoral lo más cefálicamente posible para colocarlo en la proximidad del plexo lumbar. A pesar de ello y por lo que hemos comentado anteriormente sólo del 40-90% de los pacientes presentan un bloqueo completo a las 24-48 horas de analgesia continua (54,58,70). La dirección del catéter en un bloqueo continuo 3 en 1 es totalmente impredecible, y sólo el 23% de los catéteres se encuentran en la posición ideal con la punta del mismo cerca del plexo lumbar. Los porcentajes de éxito del bloqueo sensitivo y motor y la calidad de la analgesia postoperatoria van a depender de la posición del catéter debajo de la fascia ilíaca. Cuando la punta del catéter se encuentra en el área del plexo lumbar el bloqueo es completo en un 91% de los casos; si se encuentra en posición medial bajo la fascia este porcentaje se reduce al 52%, fallando básicamente el bloqueo del nervio femorocutáneo; por último cuando el catéter se sitúa lateralmente, el porcentaje de éxito se reduce al 27%, fallando en este caso el bloqueo del nervio obturador (71). Los AL que se pueden utilizar para la realización de este bloqueo son los mismos que para el bloqueo selectivo del nervio crural o para el bloqueo iliofascial. Para analgesia postoperatoria en la cirugía de rodilla, la bupivacaína al 0,125% con clonidina 1 µg.mL-1 a 10 mL.h-1 es una buena elección, aunque ya se han comentado anteriormente las complicaciones de su utilización. El uso de ropivacaína para analgesia continua de plexo proporciona numerosas ventajas como se ha visto anteriormente. La ropivacaína al 0,2% en perfusión continua a 12 mL.h-1, o al 0,75% en bolo único asociada a clonidina (1 µg.kg-1) es una buena elección para analgesia postoperatoria en la cirugía de la extremidad inferior (53,72-74). Las indicaciones de este bloqueo son las mismas que las del bloqueo iliofascial y el bloqueo del nervio crural. Este bloqueo se puede utilizar también para el tratamiento del dolor crónico, como es el caso de la neuralgia postherpética, en la que otros tipos de tratamiento estén contraindicados. En ese caso con 40 mL de bupivacaína 0,25% se consiguió un alivio del dolor de 2 semanas de duración (75).
4. TÉCNICAS DE BLOQUEO DEL PLEXO SACRO
Los bloqueos de las raíces y nervios periféricos del plexo sacro tienen su principal indicación en la cirugía por debajo de la rodilla y fundamentalmente la cirugía del pie y del tobillo. Los bloqueos del nervio ciático son con frecuencia el pariente pobre de la anestesia locorregional, sin embargo, son muy útiles en los traumatismos de pierna y pie, aunque no deben realizarse hasta haber llevado a cabo una cuidadosa exploración sensitivo-motora del territorio del nervio ciático. Si se asocia a un bloqueo del nervio femoral puede permitir la realización de prácticamente cualquier tipo de cirugía de la extremidad inferior. Asimismo, en los últimos tiempos se están utilizando cada vez más, las infusiones perineurales con AL a través de catéteres en el nervio ciático a diferentes niveles.
4.1. Vía para-sacra
El abordaje parasacro del nervio ciático descrito por Mansour (76-78) permite la colocación de catéteres para analgesia continua. Se coloca al paciente en posición de decúbito lateral con el lado a bloquear arriba y flexionada la rodilla y la cadera. Se identifica la espina ilíaca posterosuperior y se dibuja una línea entre ese punto y la tuberosidad isquiática. A unos 6 cm de la espina ilíaca a lo largo de esa línea, se introduce una aguja conectada a un neuroestimulador y se avanza en el plano sagital hasta encontrar la respuesta motora correspondiente al nervio ciático (79) (flexión plantar o dorsal del pie, eversión o inversión del pie).
Se han descrito modificaciones a la técnica parasacra para la colocación de catéteres para analgesia postoperatoria continua. Todas estas modificaciones las podemos agrupar bajo el nombre de técnicas de abordaje subglúteo. Sutherland (80) describió en 1998 el abordaje subglúteo modificado para analgesia continua perineural del nervio ciático. El paciente se coloca en decúbito lateral con el lado a intervenir en la parte superior y el muslo flexionado 45º. Se marcan en la piel el trocánter mayor y la tuberosidad isquiática y se traza una proyección cutánea del nervio ciático, desde el vértice de la fosa poplítea hasta el punto medio de estas dos marcas óseas. En este punto medio se introduce una aguja conectada a un neuroestimulador perpendicularmente a la piel hasta localizar la respuesta motora del nervio ciático. Una segunda aguja de Tuhouy se inserta entonces 5 cm más proximal a la primera aguja y angulada para dirigirse a la punta de la primera aguja. Se conecta entonces el neuroestimulador a esta segunda aguja y se hace avanzar hasta conseguir la respuesta motora del ciático. Una vez localizado se hace avanzar un catéter estimulante 5-10 cm. Este abordaje facilita la colocación del catéter a lo largo del eje del nervio ciático.
Di Benedetto (81) ha descrito un abordaje subglúteo de más sencilla realización y que además permite la colocación con facilidad de catéteres perineurales. El paciente se coloca en posición de Sim (decúbito lateral sobre el costado contralateral, los muslos flexionados a 90º sobre la pelvis y las rodillas dobladas con la extremidad a bloquear en la parte superior). Se traza una línea entre el punto medio del trocánter mayor y la tuberosidad isquiática. Desde el punto medio de esa línea se traza otra línea perpendicular y en dirección caudal de 4 cm. En ese punto se introduce la aguja con un ángulo de 80º con respecto a la piel y se hace avanzar hasta obtener respuesta del nervio ciático. Se administran 20 mL de ropivacaína 0,75% y se introduce un catéter epidural 3-4 cm. Este abordaje ha sido comparado con el abordaje poplíteo posterior, para analgesia postoperatoria continua en cirugía del pie y no se han encontrado diferencias con el mismo (82). Este bloqueo está especialmente indicado en pacientes obesos y además el desplazamiento del catéter es poco frecuente.
Por último, Raj (83) utiliza las mismas referencias anatómicas, pero coloca al paciente en decúbito supino y la extremidad a bloquear en posición de litotomía. En esta posición localiza el nervio a 4-6 cm de profundidad, pero es difícil colocar un catéter.
El anestésico local más utilizado para analgesia postoperatoria es la ropivacaína 0,2%. Se puede administrar en perfusión continua a 5-10 mL.h-1, pero como ya se ha visto anteriormente, se obtiene una mejor calidad de la analgesia mediante una infusión continua a 5 mL.h-1 y PCA en bolos de 10 mL con un período de cierre de 1 hora.
4.2. Abordaje anterior y lateral
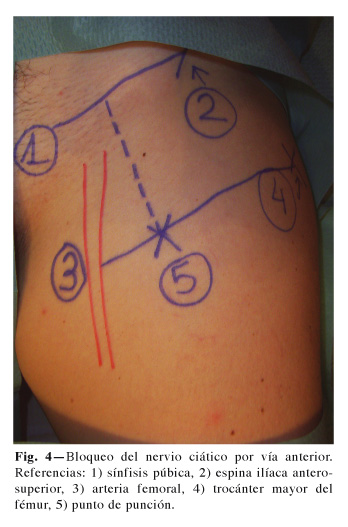
En este abordaje el paciente se encuentra situado en decúbito supino. La vía anterior (84,85) utiliza como referencias la espina ilíaca anterosuperior (EIAS), la espina del pubis y el trocánter mayor del fémur. Se dibujan dos líneas paralelas en la piel: a) la que une la EIAS con la espina del pubis, cruzando el ligamento inguinal; y b) la recta que le es paralela y pasa por el trocánter mayor del fémur. En la unión del tercio medio con el tercio interno del ligamento inguinal, se traza una línea perpendicular a las anteriores; el punto de punción se sitúa en la cara anterior del muslo, en la intersección de esta línea con la línea trocantérea. En ese punto la aguja es introducida casi vertical, con una ligera angulación externa hasta que aparecen las contracciones por estímulo del ciático (Fig. 4). En este abordaje, el trocánter menor del fémur dificulta a menudo el paso de la aguja. En un estudio realizado en cadáveres, Vloka ha demostrado que la rotación interna a 45º de la pierna puede facilitar significativamente el paso de la aguja en el abordaje anterior clásico de Beck; sin embargo, cuando la inserción de la aguja se realiza 2 cm por debajo del trocánter menor, la rotación interna de 45º provoca el efecto contrario y dificulta el paso de la aguja en el 90% de las ocasiones, mientras que la rotación externa facilita el paso de la aguja en el 100% de las ocasiones (86). En la línea de este estudio Van Elstraete (87) propone, basándose en un estudio mediante ultrasonografía, nuevas referencias para la realización del bloqueo ciático por vía anterior. El punto de punción se sitúa 2,5 cm por debajo del ligamento inguinal y 2,5 cm por dentro de la arteria femoral. En ese punto la aguja conectada al neuroestimulador se dirige posterior y lateralmente con un ángulo de 10-15º con respecto al plano vertical hasta encontrar la respuesta motora del ciático. Esta técnica es una alternativa interesante a los abordajes tradicionales, especialmente en pacientes obesos. El problema que presentan estos abordajes por vía anterior es que no se pueden colocar con facilidad catéteres para analgesia postoperatoria. Una alternativa es la utilización de AL de larga duración como la ropivacaína, la bupivacaína o la levobupivacaína.
El abordaje lateral del nervio ciático, se realiza también con el paciente en decúbito supino. Recientemente Pandin ha descrito una modificación de la técnica que permite la colocación de un catéter perineural para analgesia continua postoperatoria (88). Basándose en las descripciones de Guardini y de Raj (83,89), el catéter se inserta caudal con respecto al glúteo mayor, en un punto donde el nervio ciático discurre en un espacio adiposo. En la técnica descrita por Guardini, el punto de punción se localiza 3 cm distal a la prominencia del trocánter mayor del fémur. En el abordaje descrito por Pandin, el punto de punción se localiza 3 cm por debajo y 1 cm caudal al descrito por Guardini. La aguja se dirige 20º hacia arriba y 45º cefálica hasta localizar el nervio junto a la epífisis femoral proximal. La flexión plantar o la flexión dorsal del pie se consideran respuestas adecuadas. Se introduce entonces el catéter 3 cm en el espacio adiposo perineural.
4.3. Abordaje posterior clásico
En la técnica posterior clásica descrita por Labat (90) el paciente se coloca en decúbito lateral sobre el costado contralateral, los muslos flexionados a 90º sobre la pelvis y las rodillas dobladas (posición de Sim). Se traza una línea desde la espina ilíaca posterosuperior hasta el trocánter mayor. En el punto medio de esa línea se traza una segunda línea perpendicular a la primera y en dirección caudal a 3-5 cm se encuentra el punto de punción (Figs. 5 y 6). Winnie (32) modificó esta técnica trazando una tercera línea desde el trocánter mayor hasta el cóccix; el punto donde se encuentre con la perpendicular trazada por Labat es el punto de punción. En dicho punto se introduce la aguja conectada al neuroestimulador perpendicular a la piel, y se hace avanzar hacia la tuberosidad isquiática con una orientación a la vez interna y cefálica hasta que aparecen o bien la flexión plantar o bien la flexión dorsal. En este punto se administran 30-35 mL del AL escogido. La ropivacaína 0,5% o 0,75% sola o con clonidina 1 µg.kg-1 es una buena elección para conseguir una analgesia postoperatoria prolongada, ya que a este nivel es difícil la colocación de un catéter perineural.
4.4. Abordaje mediofemoral
El abordaje mediofemoral del nervio ciático ha sido descrito recientemente (91-93). Este bloqueo se realiza con el paciente en decúbito supino y la referencias anatómicas son el borde posterior del trocánter mayor del fémur y el epicóndilo lateral del fémur. Se traza una línea que conecte ambas estructuras y el punto medio es el lugar de punción (Fig. 7). Se introduce la aguja conectada al neuroestimulador perpendicularmente al plano cutáneo y se hace avanzar hasta localizar la respuesta motora, ya sea flexión dorsal o plantar, que se localiza a unos 7-8 cm de profundidad. En este punto se administran 30 mL de ropivacaína 0,5%, con lo que conseguimos analgesia postoperatoria de hasta 31 horas, con una mediana de 16 horas (94). En esta localización también se pueden colocar catéteres perineurales, para ello basta con angular cefálicamente la aguja para facilitar la inserción del catéter. La ventaja de este bloqueo, aparte de que se realiza en decúbito supino, se encuentra en que el riesgo de punción vascular, si lo comparamos con el bloqueo poplíteo por vía lateral, es muy bajo, y además los resultados analgésicos son comparables a los del bloqueo poplíteo lateral (94).
4.5. Abordaje poplíteo por vía posterior
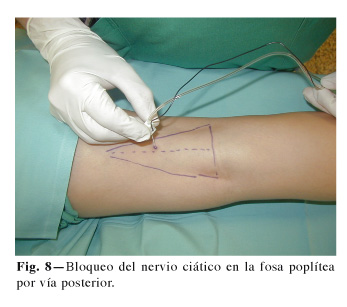
Este bloqueo se realiza con el paciente en decúbito prono, lo que ya supone un problema en pacientes muy ancianos, obesos, etc. El punto de punción se localiza en el vértice superior de la fosa poplítea determinada por el lado interno por los músculos semitendinoso y semimembranoso y por el lado externo por el músculo bíceps femoral (95-98) (Fig. 8). Los estudios anatómicos revelan que el nervio ciático desde su nacimiento en el plexo sacro ya presenta dos troncos separados, el nervio tibial y el nervio peroneo común, envueltos por una vaina perineural (28,99). Ambos troncos se van a separar a nivel del vértice de la fosa poplítea a una distancia media de 60,5 ± 27 mm por encima de la fosa poplítea (100). Este estudio indica que la punción 100 mm por encima de la fosa poplítea asegura el posicionamiento de la aguja en la vecindad o próxima a la división del nervio en el 100% de los cadáveres estudiados. Se han utilizado técnicas de imagen para comprobar la correcta localización del nervio y del catéter como la ultrasonografía (101,102). La aguja conectada al neuroestimulador se introduce con un ángulo de 45-60º con respecto a la piel para facilitar la inserción del catéter. Una vez se localiza la respuesta motora del pie, indistintamente flexión plantar o dorsal, se administran 30-40 mL de ropivacaína 0,5% o mepivacaína 1% si vamos a realizar una técnica de punción única; si colocamos un catéter, este se hace avanzar 3-5 cm más allá de la punta de la aguja. La colocación de un catéter en esta localización plantea el problema de la movilidad de la zona y la posibilidad de rotura o desplazamiento del catéter, lo que puede llegar a ocurrir hasta en un 25% de las ocasiones (14). Un estudio randomizado, doble ciego ha demostrado que el bloqueo ciático continuo con bomba PCRA (patient controlled regional anestesia) en cirugía ambulatoria, disminuye el dolor, el uso de opiáceos y sus efectos adversos, las alteraciones del sueño y se asocia con una elevada satisfacción del paciente (13). Las perfusiones utilizadas para el bloqueo continuo son muy variadas. La ropivacaína 0,2% en perfusión continua a 8 mL.h-1 con bolos PCRA de 2 mL cada 20 minutos es una buena opción. También se han comunicado buenos resultados con la ropivacaína 0,125% en perfusión continua a 7 mL.h-1 (15). Más discutibles parecen las perfusiones continuas de bupivacaína por los posibles problemas de toxicidad asociados y las complicaciones secundarias al bloqueo residual tanto sensitivo como motor (51,55,103). Sin embargo estudios recientes avalan el uso de la bupivacaína 0,25% en perfusión continua a 5 mL.h-1 para analgesia postoperatoria en cirugía ambulatoria de pie y tobillo (12). La bupivacaína 0,125% asociada a sufentanil 0,1 µg.mL-1 y clonidina 1 µg.mL-1 a 7 mL.h-1 proporciona también una adecuada analgesia tras cirugía del pie (14).
4.6. Abordaje poplíteo por vía lateral
Este bloqueo fue descrito por Collum (104) y se realiza con el paciente en decúbito supino. Se coloca la pierna ligeramente elevada con una almohada y se identifica el tendón del músculo bíceps femoral. A continuación se localiza el polo superior de la rótula y se traza una línea vertical desde este punto hasta el tendón del bíceps femoral. El punto de punción queda determinado por la intersección de ambas líneas. La aguja se inserta inmediatamente anterior al tendón del bíceps femoral en el plano horizontal con una ligera angulación cefálica (105). Se identifica el nervio tibial al obtener el movimiento de flexión plantar o inversión del pie, y el nervio peroneo profundo al obtener dorsiflexión o eversión del pie. Parece ser que la respuesta motora que mejor predice el bloqueo sensitivo completo es la flexión plantar (106). Es necesario obtener ambos estímulos para asegurar la calidad analgésica del bloqueo (107). Se han descrito otros abordajes laterales con ligeras modificaciones del punto de punción, en general desplazándolo más proximal para evitar la bifurcación del nervio (108,109). Se ha comparado el bloqueo poplíteo por vía lateral con el posterior y en un primer estudio Hadzic no encontró diferencias entre un tipo de bloqueo y otro (110). Sin embargo, en un reciente estudio (111), nuestro grupo ha observado una mayor duración de la analgesia en el bloqueo poplíteo lateral que en el posterior. Una posible explicación a este hecho es que en el bloqueo realizado por vía posterior se bloquea el nervio ciático antes de que se divida en el nervio tibial y el peroneo común, con lo que el mayor grosor de este nervio puede hacer necesarios mayores volúmenes de AL. Además, en el estudio de Hadzic para la realización del bloqueo lateral únicamente se buscaba un estímulo, mientras que en nuestro estudio se exigían ambos tipos de respuesta. Aunque parece ser que la técnica de inyección múltiple produce mayor disconfort en el paciente (112) en nuestro estudio no se han encontrado diferencias entre un tipo de bloqueo u otro. Cuando se comparó el bloqueo mediofemoral con el bloqueo lateral tampoco se encontraron diferencias en cuanto al confort entre ambos tipos de bloqueo (94).
El abordaje por vía lateral puede ofrecer ventajas para la colocación de un catéter para analgesia continua postoperatoria. En este caso la punción debería realizarse antes de la división del nervio ciático, con una técnica de punción similar a la utilizada para la realización del bloqueo mediofemoral. Una de las ventajas sería una mejor fijación del catéter que en el abordaje posterior, con una menor probabilidad de desplazamiento del mismo. A pesar de las potenciales ventajas de este abordaje para una analgesia continua, no existen estudios clínicos aleatorizados que determinen que este abordaje lateral es adecuado para analgesia continua.
| CORRESPONDENCIA: Vicente Domingo Triadó C/Daniel Balaciart, 4-9-48 46020 Valencia Telef.: 962 289 576 e-mail: vdt5677@mail.ono.es |
BIBLIOGRAFÍA
1. Hadzic A, Vloka JD, Kuroda MM, Koorn R, Birnbach DJ. The practice of peripheral nerve blocks in the United States: A national survey. Reg Anesth Pain Med 1998; 23: 241-6. [ Links ]
2. Horlocker T. Peripheral nerve blocks- Regional anestesia for the new millenium. Reg Anesth Pain Med 1998; 23: 237-40. [ Links ]
3. Clergue F, Auroy Y, Pequignot F, Jougla E, Lienhart A, Laxenaire M. French survey of anestesia in 1996. Anesthesiology 1999; 91: 1509-20. [ Links ]
4. Kopacz DJ, Neal JM. Regional Anestesia and Pain Medicine: Residency Training- The year 2000. Reg Anesth Pain Med 2002; 27 (1): 9-14. [ Links ]
5. Bouaziz H, Mercier F, Narchi P, Poupard M, Auroy Y, Benhamou D. Survey of regional anesthetic practice among French residents at time of certification. Reg Anesth 1997; 22: 218-22. [ Links ]
6. Karaca P, Hadzic A, Yufa M, et al. Painful paresthesiae are infrequent during brachial plexus localization using low-current peripheral nerve stimulation. Reg Anesth Pain Med 2003; 28 (5): 380-3. [ Links ]
7. Auroy Y, Benhamou D, Bargues L, Ecoffey C, Falissard B, Mercier F, et al. Major complications of regional anesthesia in France. The SOS regional anesthesia hotline service. Anesthesiology 2002; 97 (5): 1274-80. [ Links ]
8. Jochum D, Roedel R, Gleyze P, Balliet JM. Bloc interscalenique et chirurgie de l'épaule. Etude prospective d'une série continue de 167 patients. Ann Fr Anesth Reanim 1997; 16: 114-9. [ Links ]
9. Urmey WF. Interscalene block: the truth about twitches. Reg Anesth Pain Med 2000; 25: 340-2. [ Links ]
10. Riegler FX. Brachial plexus block with the nerve stimulator: motor response characteristics at three sites. Reg Anesth 1992; 17: 295-9. [ Links ]
11. Rawal N, Allvin R, Axelsson K, Ekback G, Ohlsson T, Amilon A. Patient-controlled regional analgesia (PCRA) at home: controlled comparison between bupivacaína and ropivacaine brachial plexus analgesia. Anesthesiology 2002; 96: 1290-6. [ Links ]
12. White PF, Issioui T, Skrivanek GD, Early JS, Wakefield C. The use of a continuous popliteal sciatic nerve block after surgery involving the foot and ankle: does it improve the quality of recovery? Anesth Analg 2003; 97: 1303-9. [ Links ]
13. Ilfeld BM, Morey TE, Wang RD, Enneking FK. Continuous popliteal sciatic nerve block for postoperative pain control at home. Anesthesiology 2002; 97 (4): 959-65. [ Links ]
14. Singelyn FJ, Aye F, Gouverneur JM. Continuous popliteal sciatic nerve block: an original technique to provide postoperative analgesia after foot surgery. Anesth Analg 1997; 84: 383-6. [ Links ]
15. Martinez Navas A, Vázquez Gutierrez T, Echevarria Moreno M. Bloqueo poplíteo continuo con ropivacaína mediante catéter estimulante para analgesia postoperatoria tras cirugía del pie. Rev Esp Anestesiol Reanim 2003; 50: 188-91. [ Links ]
16. Ilfeld BM, Esener DE, Morey TE, Enneking FK. Ambulatory perineural infusión: the patients' perspective. Reg Anesth Pain Med 2003; 28 (5): 418-23. [ Links ]
17. Donner B, Schnell P, Zenz M. Indications and limits of nerve block techniques. Z Arztl Fortbild Qualitatssich 1998; 92 (1): 29-33. [ Links ]
18. Aeschbach A, Mekhail NA. Common nerve blocks in chronic pain management. Anesthesiol Clin North America 2000; 18 (2): 429-59, viii. [ Links ]
19. Fischer HB, Peters TM, Fleming IM, Else TA. Peripheral nerve catheterization in the management of terminal cancer pain. Reg Anesth 1996; 21 (5): 482-5. [ Links ]
20. Wechler RJ, Frank ED, Halpern EH, et al. Percutaneous lumbar sympathetic plexus catéter placement for short-and long-term pain relief: CT technique and results. J Comput Assist Tomogr 1998; 22 (4): 518-23. [ Links ]
21. Wu CT, Ho ST, Tsai CS, et al. Repeated lumbar sympathetic blockade for complex regional pain syndromes type I- a case report. Acta Anaesthesiol Sin 1998; 36 (3): 155-8. [ Links ]
22. Chaturvedi A, Dash HH. Sympathetic blockade for the relief of chronic pain. J Indian Med Assoc 2001; 99 (12): 698-703. [ Links ]
23. Aguilar JL, Domingo V, Samper D, et al. Long-term brachial plexus anestesia using a subcutaneous implantable injection system". Reg Anesth 1995; 20 (3): 242-5. [ Links ]
24. Zetlaoui PJ. Anesthésie locorégionale du member inferieur. Encycl Med Chir, Anesthésie-Réanimation Paris-France: Elsevier 1994. p. 36-323-A-10. [ Links ]
25. Dalens B. Anestesia locoregional en niños y adolescentes. Barcelona: Masson-Williams & Wilkins España SA, 1998. p. 327-76. [ Links ]
26. Sobotta J. Atlas Der Anatomie des Menschen. Munich: Urban y Schwarzenberg, 1982. [ Links ]
27. Straja A. Anestesia locoregional P.Gauthier-Lafaye. Barcelona: Masson SA; 1986. p. 109-28. [ Links ]
28. Vloka JD, Hadzic A, Lesser JB et al. A common epineural sheath for the nerves in the popliteal fossa and its possible implications for sciatic nerve block. Anesth Analg 1997; 84: 387-90. [ Links ]
29. Farny J, Drolet P, Girard M. Anatomy of the posterior approach to the lumbar plexus block. Can J Anaesth 1994; 41 (6): 1238-9. [ Links ]
30. Parkinson SK, Mueller JB, Little WL, et al. Extent of blockade with various approaches to the lumbar plexus. Anesth Analg 1989; 68: 243-8. [ Links ]
31. Chayen D, Nathan H, Chayen M. Lumbar plexus: a new posterior approach. Anesthesiology 1973; 45: 95-9. [ Links ]
32. Winnie AP, Ramamurthy S, Durrani Z et al. Plexus blocks for lower extremity surgery. Anesthesiol Rev 1974; 1: 11-6. [ Links ]
33. Enneking FK, Wedel DJ. The art and science of peripheral nerve blocks. Anesth Analg 2000; 90: 1-2. [ Links ]
34. Mitchell ME. Regional anesthesia for hip surgery. Tech Reg Anesth Pain Mgmt 1999; 3: 94-106. [ Links ]
35. Ayers J, Enneking FK. Continuous lower extremity techniques. Tech Reg Anesth Pain Mgmt 1999; 3: 47-57. [ Links ]
36. Pandin PC, Vandesteene A, d'Hollander AA. Lumbar plexus posterior approach: a catheter placement description using electrical nerve stimulation. Anesth Analg 2002; 95: 1428-31. [ Links ]
37. Kirchmair L, Entner T, Kapral S, Mitterschiffthaler G. Ultrasound guidance for the psoas compartment block: an imaging study. Anesth Analg 2002; 94: 706-10. [ Links ]
38. Capdevila X, Macaire P, Dadure C, et al. Continuous psoas compartment block for postoperative analgesia after hip arthroplasty: news landmarks, technical guidelines, and clinical evaluation. Anesth Analg 2002; 94: 1606-13. [ Links ]
39. Chudinov A, Berkenstadt H, Salai M, et al. Continuous psoas compartment block for anesthesia and perioperative analgesia in patients with hip fractures. Reg Anesth Pain Med 1999; 94: 563-8. [ Links ]
40. Liu SS, Salinas FV. Continuous plexus and peripheral nerve blocks for postoperative analgesia. Anesth Analg 2003; 96: 263-72. [ Links ]
41. De Biasi P, Lupescu R, Burgun G, et al. Continuous lumbar plexus block: use of radiography to determine catheter tip location. Reg Anesth Pain Med 2003; 28 (2): 135-9. [ Links ]
42. Aida S, Takahasi H, Shimoji K. Renal subcapsular hematoma after lumbar plexus block. Anesthesiology 1996; 84: 452-5. [ Links ]
43. Martín G, Grant SA, McLeod DB, et al. Severe phantom leg pain in an amputee after lumbar plexus block. Reg Anesth Pain Med 2003; 28 (5): 475-8. [ Links ]
44. Capdevila X, Bibboulet P, Bouregba M, et al. Comparison of the three-in-one and fascia iliaca compartment block in adults: clinical and radiographic analysis. Anesth Analg 1998; 86: 1039-44. [ Links ]
45. Bruelle P, Piffaut V, Cuvillon P, et al. Iliofascial block with a neuroestimulator in adult patients. Reg Anesth 1998; 23: 77. [ Links ]
46. Ganapathy S, Wasserman R, Watson JT, et al. Modified continuous femoral three-in-one block for post-operative pain after total knee arthroplasty. Anesth Analg 1999; 89: 1197-202. [ Links ]
47. Dalens B, Vanneuville G, Tanguy A. Comparison of fascia iliaca compartment block with the 3-in-1 block in children. Anesth Analg 1989; 69: 705-13. [ Links ]
48. Longo SR, Williams DP. Bilateral fascia iliaca catheters for postoperative pain control after bilateral total knee arthroplasty: a case report and description of a catheter technique. Reg Anesth 1997; 22: 372-7. [ Links ]
49. Paut O, Sallabery M, Schreiber-Deturmeny E, et al. Continuous fascia iliaca block in children: a prospective evaluation of plasma bupivacaine concentrations, pain scores, and side effects. Anesth Analg 2001; 92: 1159-63. [ Links ]
50. Khoo ST, Brown TCK. Femoral nerve block- The anatomical basis for a single injection technique. Anaesth Intensive Care 1983; 11: 40-2. [ Links ]
51. Capdevila X, Barthelet Y, Biboulet P, et al. Effects of perioperative analgesic technique on the surgical outcome and duration of rehabilitation after major knee surgery Anesthesiology 1999; 91: 8-15. [ Links ]
52. Dauri M, Polzoni M, Fabri E, et al. Comparison of epidural, continuous femoral block and intrarticular analgesia after anterior cruciate ligament reconstruction. Acta Anaesthesiol Scand 2003; 47: 20-5. [ Links ]
53. Chelly JE, Greger J, Gebhard R, et al. Continuous femoral nerve blocks improve recovery and outcome of patients undergoing total knee arthroplasty. Anesth Analg 1998; 87: 88-92. [ Links ]
54. Singelyn FJ, Gouverneur JM. Extended "three in one" block after total knee arthroplasty: continuous versus patient-controlled techniques. Anesth Analg 2000; 91: 176-80. [ Links ]
55. Borgeat A, Kalberer F, Jacob H, et al. Patient-controlled interscalene analgesia with ropivacaine 0.2% versus bupivacaína 0.15% after major open shoulder surgery: the effects on hand motor function. Anesth Analg 2001; 92: 218-23. [ Links ]
56. Eledjam JJ, Cuvillon P, Capdevila X, et al. Postoperative analgesia by femoral nerve block with ropivacaine 0.2% after major knee surgery: continuous versus patient-controlled techniques. Reg Anesth Pain Med 2002; 27 (6): 604-11. [ Links ]
57. Singelyn F, Gouverneur JM. Postoperative analgesia after total hip arthroplasty: IV PCA with morphine, patient-controlled epidural analgesia, or continuous "3-in-1" block?- a prospective evaluation by our acute pain service in more than 1300 patients. J Clin Anesth 1999; 11: 550-4. [ Links ]
58. Singelyn F, Vanderelst PE, Gouverneur JM. Extended femoral nerve sheath block after total hip arthroplasty: continuous versus patient-controlled techniques. Anesth Analg 2001; 92: 455-9. [ Links ]
59. Durbec O, Viviand X, Potie F, et al. A prospective evaluation of the use of femoral venous catheters in critically ill adults. Care Med 1997; 25: 1986-9. [ Links ]
60. Mc Neely, JK, Trentadue NC, Rusy LM, et al. Culture of bacteria from lumbar and caudal epidural catheters used for postoperative analgesia in children. Reg Anesth 1997; 22: 428-31. [ Links ]
61. Kost-Byerli S, Tobin JR, Greenberg RS, et al. Bacterial colonization and infectious rate of continuous epidural catheters in children. Anesth Analg 1998; 86: 712-6. [ Links ]
62. Cuvillon P, Ripart J, Lalourcey L, et al. The continuous femoral nerve block catheter for postoperative analgesia: bacterial colonization, infectious rate and adverse effects. Anesth Analg 2001; 93: 1045-9. [ Links ]
63. Winnie AP, Ramamurthy S, Durrani Z. The inguinal paravascular technic of lumbar plexus anesthesia: the "3-in-1" block. Anesth Analg 1973; 52: 989-96. [ Links ]
64. Lonsdale M. 3-in-1 block: confirmation of Winnie's anatomical hypothesis. Anesth Analg 1988; 67: 601-2. [ Links ]
65. Lang SA, Yip RW, Chang PC, Gerard MA. The femoral 3-in-1 block revised. J Clin Anesth 1993; 5: 292-6. [ Links ]
66. Atanassoff PG, Weiss BM, Brull SJ, et al. Electro-myography comparison of obturator nerve block to three-in-one block. Anesth Analg 1995; 81: 529-33. [ Links ]
67. Marhofer P, Schrögendorfer K, Koinig H, et al. Ultrasonographic guidance improves sensory block and onset time for three-in-one blocks. Anesth Analg 1997; 85: 854-7. [ Links ]
68. Marhofer P, Schrögendorfer K, Wallner T, et al. Ultrasonographic guidance reduces the amount of local anesthetic for 3-in-1 blocks. Reg Anesth Pain Med 1998; 23: 584-8. [ Links ]
69. Marhofer P, Nasel C, Sitzwolh C, Kapral S. Magnetic resonance imaging of the distribution of local anesthetic during the three-in-one block. Reg Anesth Pain Med 2000; 90: 119-24. [ Links ]
70. Grant SA, Nielsen KC, Greengrass RA, et al. Continuous peripheral nerve block for ambulatory surgery. Reg Anesth Pain Med 2001; 26: 209-14. [ Links ]
71. Capdevila X, Biboulet P, Morau D, et al. Continuous three-in-one block for postoperative pain after lower limb orthopedic surgery: where do the catheters go? Anesth Analg 2002; 94: 1001-6. [ Links ]
72. Fanelli G, Casati A, Beccaria P, et al. A double blind comparison of ropivacaine, bupivacaína, and mepivacaine during sciatic and femoral nerve blockade. Anesth Analg 1998; 87: 597-600. [ Links ]
73. Casati A, Fanelli G, Borghi B, et al. Ropivacaine or 2% mepivacaine for lower limb peripheral nerve blocks. Anesthesiology 1999; 90: 1047-52. [ Links ]
74. Casati A, Magistris L, Fanelli G, et al. Small-dose clonidine prolongs postoperative analgesia after sciatic-femoral nerve block with 0.75% ropivacaine for foot surgery. Anesth Analg 2000; 91: 388-92. [ Links ]
75. Hadzic A, Vloka JD, Saff GN, et al. The "three-in-one block" for treatment of pain in a patient with acute herpes zoster infection. Reg Anesth 1997; 22 (6): 575-8. [ Links ]
76. Mansour NY. Reevaluating the sciatic nerve block: another landmark for consideration. Reg Anesth 1993; 18: 322-3. [ Links ]
77. Morris GF, Lang S, Dust WM. The parasacral sciatic nerve block. Reg Anesth 1997; 22: 223-8. [ Links ]
78. Morris GF, Lang S. Continuous parasacral sciatic nerve block: two case reports. Reg Anesth 1997; 22: 469-72. [ Links ]
79. Taboada M, Rodríguez J, Álvarez J, et al. Bloqueos nerviosos periféricos para anestesia quirúrgica y analgesia postoperatoria de la extremidad inferior. Rev Esp Anestesiol Reanim 2003; 50: 510-20. [ Links ]
80. Sutherland IDB. Continuous sciatic nerve infusions: expanded case report describing a new approach. Reg Anesth Pain Med 1998; 23: 496-51. [ Links ]
81. di Benedetto P, Bertini L, Casati A, et al. A new posterior approach to the sciatic nerve block: a prospective, randomized comparison with the classic posterior approach. Anesth Analg 2001; 93: 1040-4. [ Links ]
82. di Benedetto P, Casati A, Bertini L, et al. Postoperative analgesia with continuous sciatic nerve block after foot surgery: a prospective, randomized comparison between the popliteal and subgluteal approaches. Anesth Analg 2002; 94: 996-1000. [ Links ]
83. Raj PP, Parks RI, Watson TD, Jenkins MT. A new single-position supine approach to sciatic-femoral nerve block. Anesth Analg 1975; 54: 489-94. [ Links ]
84. Beck GP. Anterior approach to the sciatic nerve block. Anesthesiology 1963; 1: 7455-753. [ Links ]
85. Chelly JE, Delauney L. A new anterior approach to the sciatic nerve block. Anesthesiology 1999; 91: 1655-60. [ Links ]
86. Vloka JD, Hadzic A, April E, Thys DM. Anterior approach to the sciatic nerve block: the effects of leg rotation. Anesth Analg 2001; 92: 460-2. [ Links ]
87. Van Elstraete AC, Poey C, Lebrun T, Pastureau F. New landmarks for the anterior approach to the sciatic nerve block: imaging and clinical study. Anesth Analg 2002; 95: 214-8. [ Links ]
88. Pandin P, Vandesteene A, d'Hollander A. Sciatic nerve blockade in the supine position: a novel approach. Can J Anesth 2003; 50 (1): 52-6. [ Links ]
89. Guardini R, Waldrom BA, Wallace WA. Sciatic nerve block: a new lateral approach. Acta Anaesthesiol Scand 1985; 29: 515-9. [ Links ]
90. Labat G. Regional anestesia. Philadelphia: WB Saunders. 1923. p. 289-91. [ Links ]
91. Pham-Dang C. Midfemoral block: a new lateral approach to the sciatic nerve. Anesth Analg 1999; 88: 1426. [ Links ]
92. Morrow MJ. The lateral approach to the sciatic nerve. Anesth Analg 2000; 90: 770. [ Links ]
93. Naux E, Pham-Dang C, Petitfaux F, et al. Bloc du nerf sciatique: une nouvelle voie d'abord latérale mediofemoral. Intérêt de son association à un bloc " 3 en 1" pour la chirurgie du genou. Ann Fr Anesth Reanim 2000; 1: 9-15. [ Links ]
94. Domingo V, Crespo MT, Aguilar JL, et al. A comparison of lateral popliteal versus lateral midfemoral sciatic nerve blockade using ropivacaine 0.5%. Reg Anesth Pain Med 2004; 29 (1): 23-7. [ Links ]
95. Singelyn FJ, Gouverneur JM, Gribomont BF. Popliteal sciatic nerve block by a nerve stimulator. A reliable technique for foot and ankle surgery. Reg Anesth 1991; 16: 278-81. [ Links ]
96. Litchinko M, Diebold P. Block of the sciatic nerve in the popliteal fossa. Ann Fr Anesth Reanim 1993; 12: 601-3. [ Links ]
97. Rorie D, Byer D, Nelson D. Assessment of block of the sciatic nerve in the popliteal fossa. Anesth Analg 1980; 59: 371-6. [ Links ]
98. Monsó A, Santaliestra J, Barbal F, et al. Bloqueo del nervio ciático en la fosa poplítea para cirugía del pie. Rev Esp Anestesiol Reanim 1996;43:27-29. [ Links ]
99. Sunderland S, et al. The sciatic nerve and its tibial and common peroneal divisions: anatomical and physiological features. En: Nerves and nerve injuries. New York: Churchill Livingstone, 1978. p. 925-66. [ Links ]
100. Vloka JD, Hadzic A, April E, Thys DM. The division of the sciatic nerve in the popliteal fossa: anatomical implications for popliteal nerve blockade. Anesth Analg 2001; 92: 215-7. [ Links ]
101. Sinha A, Chan VWS. Ultrasound imaging for popliteal sciatic nerve block. Reg Anesth Pain Med 2004; 29 (2): 130-4. [ Links ]
102. Sites BD, Gallagher J, Sparks M. Ultrasound-guided popliteal block demonstrates an atypical motor response to nerve stimulation in 2 patients with diabetes mellitus. Reg Anesth Pain Med 2003; 28 (5): 479-82. [ Links ]
103. Chelly JE, Greger J, Gebhard R. Ambulatory continuous perineural infusion: are we ready? Anesthesiology 2000; 93: 501-2. [ Links ]
104. Collum CR, Courtney PG. Sciatic nerve blockade by a lateral approach to the popliteal fossa. Anaesth Intensive Care 1993; 21: 236-7. [ Links ]
105. Zetlaoui PJ, Bouaziz H. Lateral approach to the sciatic nerve in the popliteal fossa. Anesth Analg 1998; 87: 79-82. [ Links ]
106. Taboada M, Alvarez J, Cortés J, et al. Lateral approach to the sciatic nerve block in the popliteal fossa: correlation between evoked motor response and sensory block. Reg Anesth Pain Med 2003; 28 (5): 450-5. [ Links ]
107. Paqueron X, Bouaziz H, Macalou D, et al. The lateral approach to the sciatic nerve at the popliteal fossa: one or two injections? Anesth Analg 1999; 89: 1221-5. [ Links ]
108. Vloka JD, Hadzic A, Koorn R, Thys D. Supine approach to the sciatic nerve in the popliteal fossa. Can J Anaesth 1996; 43: 964-7. [ Links ]
109. Dabbas A, Zuzuárregui JC, Arnal MC, et al. Bloqueo poplíteo por vía lateral: una modificación de las referencias anatómicas. Rev Esp Anestesiol Reanim 2003; 50: 126-9. [ Links ]
110. Hadzic A, Vloka JD. A comparison of the posterior versus lateral approaches to the block of the sciatic nerve in the popliteal fossa. Anesthesiology 1998; 88: 1480-6. [ Links ]
111. Domingo V, Cabezudo L, Crespo MT, et al. Estudio comparativo del bloqueo del nervio ciático en el hueco poplíteo por abordaje posterior frente al abordaje lateral con mepivacaína 1% para cirugía del pie. Rev Esp Anestesiol Reanim 2004; 51: 70-4. [ Links ]
112. Fanelli G, Casati A, Garancini P, Torri G. Nerve stimulator and multiple injection technique for upper and lower limb blockade: failure rate, patient acceptance, and neurologic complications. Anesth Analg 1999; 88: 847-52. [ Links ]