INTRODUCCIÓN
El control eficaz del dolor postoperatorio se ha convertido en una parte esencial de los cuidados perioperatorios y su adecuado tratamiento, junto a otros factores como la movilización y la nutrición precoz, se relaciona directamente con la disminución de las complicaciones postoperatorias y de la estancia hospitalaria 1. A pesar de los avances farmacológicos, tecnológicos y de la difusión de protocolos analgésicos, de un 30 a un 75 % de los pacientes sometidos a una intervención quirúrgica experimentan en algún momento dolor de moderado a intenso 2. El dolor agudo postoperatorio (DAP) se asocia a un aumento de la morbilidad y de los costes 3, a una disminución del confort del paciente y a un riesgo más elevado de desarrollar dolor crónico 4.
En la actualidad se presentan diversos retos en el campo del tratamiento del DAP que precisarán de nuevos enfoques y nuevas alternativas terapéuticas.
Prevalencia del DAP por procedimiento quirúrgico.
Guías de actuación basadas en la evidencia.
Controversias en el uso de opioides perioperatorios.
Programas de cirugía fast-track o rehabilitación precoz.
Nuevas vías de administración de opioides.
PREVALENCIA DEL DAP POR PROCEDIMIENTO QUIRÚRGICO
Una encuesta postoperatoria sobre la prevalencia del DAP realizada por Gant y cols. 5 en 300 pacientes mostró resultados similares a las encuestas realizadas hace 10 años por Apfelbaum y cols. 6 y hace 20 años por Warfield and Kahn 7 (Figura 1). A pesar de los avances farmacológicos, organizativos y de protocolización de los tratamientos, los datos muestran que la prevalencia del DAP apenas se ha modificado en los últimos 20 años 8. La prevalencia del dolor moderado se mantiene entre un 45-49 %, y la de dolor intenso y máximo entre un 21-23 % y un 8-18 %, respectivamente.

Fuente: Gan TJ. Current Medical Research and Opinion, 2014.
Fig. 1 Evolución de la prevalencia del DAP.
Por otro lado, la mayoría de los registros del DAP se refieren al dolor en reposo, y existen pocos datos sobre el control del dolor dinámico, que es el que permitirá a los pacientes deambular, iniciar la rehabilitación o la fisioterapia respiratoria, acelerando la recuperación postoperatoria.
Un estudio observacional transversal mediante entrevista y revisión de historia clínica de 234 pacientes postoperados 9) mostró una prevalencia de dolor en reposo (Escala Numérica, EN > 3) del 33 % y en movimiento del 66 %. El porcentaje de dolor intenso (EN > 6) en reposo fue de 1,7 % y en movimiento de 7,3 % (Figura 2). Dos de los factores que se relacionaron con una mayor intensidad de dolor fueron el tipo de abordaje y el procedimiento quirúrgico (p < 0,004).
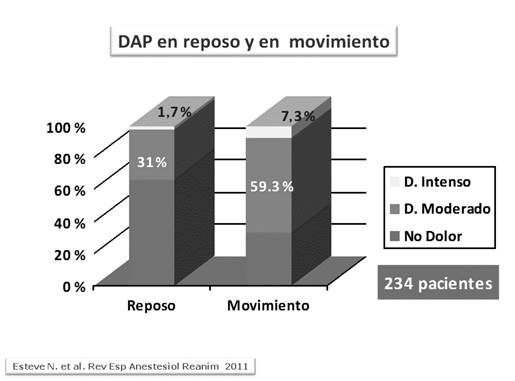
Fuente: Esteve N. et al. Rev. Exp Anestesia1 Reanim, 2011.
Fig. 2 Prevalencia del DAP en reposo y en movimiento.
Los procedimientos y abordajes quirúrgicos en los que un porcentaje superior al 50 % de los pacientes presentó dolor en movimiento se presentan en la Figura 3. Hay que señalar que en el listado aparecen intervenciones en las que se registró dolor controlado en reposo. Coincidiendo con otros estudios 10, los procedimientos más dolorosos al movimiento fueron la cirugía ortopédica (prótesis de rodilla y cadera), la de columna vertebral y la cirugía abierta de traumatología. Otros procedimientos que se asociarían a dolor moderado presentaban sin embargo un alto porcentaje de dolor no controlado en movimiento, como son la mastectomía, la cirugía de ORL abierta, la cirugía laparoscópica, la toracoscopia, la cirugía vascular abierta o la endovascular.
El estudio de Gerbershagen 11 sobre el DAP en 50.523 pacientes de 105 hospitales alemanes, agrupados en 179 intervenciones quirúrgicas, presenta datos muy interesantes. Mostramos en las Tabla I y Tabla II, las intervenciones agrupadas según la media de dolor, leve-moderado (EN 3-5) e intenso (EN 6-7), respectivamente.
Las intervenciones de la Tabla I presentan dolor leve o moderado. Entre ellas destacan los abordajes laparoscópicos, pero también cirugías muy dolorosas como la toracotomía, la hepatectomía o la cirugía de columna vertebral. Hoy en día, en este tipo de cirugías asociadas a dolor intenso se aplican protocolos analgésicos invasivos, como bombas de PCA (analgesia controlada por el paciente) intravenosas y epidurales, que explicarían el adecuado control del dolor.
Sin embargo, en la Tabla II de intervenciones que presentan dolor intenso encontramos, además de la cirugía ortopédica, intervenciones que teóricamente se asocian a dolor leve o moderado. Así vemos que la colecistectomía laparoscópica, la amigdalectomía, la histerectomía o la cesárea presentan medias elevadas de dolor postoperatorio. Tal como plantean los autores del estudio, es probable que la elevada prevalencia del DAP tenga su origen en intervenciones "menores" que no reciben un tratamiento analgésico adecuado.
Conocer la prevalencia del DAP por procedimiento quirúrgico es una buena herramienta para localizar los puntos de mejora en la terapia analgésica postoperatoria de cada hospital. Los protocolos analgésicos específicos para cada tipo de intervención quirúrgica, adaptados al contexto organizativo y de práctica clínica hospitalaria 12, son una garantía para individualizar los tratamientos y responder adecuadamente a las demandas analgésicas de cada paciente.
Otros factores que se han asociado a elevada incidencia de DAP 13 son la edad inferior a 60 años, el dolor crónico preoperatorio y el sexo femenino. Existen resultados contradictorios con respecto a los registros de dolor más elevado en las mujeres. Hay que destacar el gran volumen de intervenciones obstétricas y ginecológicas, con dolor mal controlado, que contribuyen a elevar la incidencia global del DAP.
GUÍAS DE ACTUACIÓN BASADAS EN LA EVIDENCIA
Recientemente se ha publicado la actualización de las Guías del manejo del Dolor Agudo Postoperatorio de la American Pain Society (APS) 14, con el objetivo de promover la aplicación efectiva y segura del tratamiento del DAP, basada en la mejor evidencia disponible. El panel de expertos realiza 32 recomendaciones, agrupadas según la calidad de la evidencia, de las que solo 4 se apoyan en evidencia de alta calidad.
Destacamos, entre todas las recomendaciones, el uso de la analgesia multimodal, la analgesia regional y epidural en procedimientos específicos, las mínimas dosis de opioides, la preferencia de la vía oral frente a la intravenosa, y la modalidad de PCA.
Las recomendaciones con una evidencia débil 15 por la heterogeneidad y baja calidad de los estudios son:
- La educación preoperatoria y la planificación analgésica perioperatoria.
- Las pautas analgésicas adecuadas de transición del hospital al domicilio. Los criterios de derivación al especialista ante la sospecha de dolor postoperatorio persistente.
- La evaluación del dolor y los métodos de monitorización de sedación y depresión respiratoria.
- Las intervenciones no farmacológicas.
- La estructura organizativa óptima de una unidad de DAP.
La dificultad para poder agregar datos en los análisis de toda la abundante literatura sobre el DAP obliga a reflexionar y a establecer consideraciones para mejorar las líneas de investigación futuras (15). Entre ellas destacamos las siguientes:
- Diseño de estudios basado tanto en ensayos clínicos aleatorizados (ECA), como en estudios observacionales sobre datos "reales" de la práctica clínica.
- Grupos de pacientes homogéneos respecto al tipo de intervención quirúrgica, la comorbilidad y los factores de riesgo de incremento del DAP.
- Medidas estandarizadas de resultado: dolor dinámico con maniobras de provocación bien definidas, TOPAR (total pain relief score), SPID (sum of pain intensity differences), interferencia funcional del DAP, efectos adversos, satisfacción del paciente y costes.
- Tiempos de medición adecuados, extendidos a días o semanas del postoperatorio.
CONTROVERSIAS EN EL USO DE OPIOIDES PERIOPERATORIOS
Los opioides están en la primera línea del tratamiento del DAP de moderado a intenso. No obstante, sus efectos adversos limitan en ocasiones las dosis, retrasan la recuperación postoperatoria y pueden poner en peligro la vida del paciente si no se controlan adecuadamente 16. Por otro lado, a pesar de los intensos esfuerzos de investigación, existe una falta de avances reales en el desarrollo de nuevos fármacos analgésicos en los últimos 50 años 17.
Los programas de fast-track o rehabilitación multimodal precoz o intensificada han impulsado el concepto de analgesia libre de opioides (opioid-free analgesia), para evitar los efectos secundarios 18 como las náuseas, vómitos o el íleo postoperatorio, que pueden retrasar el curso postoperatorio. La analgesia multimodal, basada en un concepto amplio de combinación de analgésicos, fármacos coadyuvantes y técnicas analgésicas, se presenta como una alternativa segura y eficaz 19.
No obstante, la evidencia del efecto analgésico de muchos fármacos coadyuvantes es controvertida 16, y también el balance entre la eficacia y los efectos adversos. Por ello, el concepto de ahorro de opioides (opioid-sparing) se ajusta más a la realidad de las opciones analgésicas actuales para el dolor moderado-intenso.
En los últimos años se ha extendido una epidemia en el abuso de opioides en Estados Unidos y Canadá, y también en otros países como los escandinavos 20-22. Entre 1999 y 2010 se ha cuadruplicado la prescripción de opioides, y también el número de muertes y de ingresos hospitalarios asociados al abuso de opioides (Figura 4). Por ello, la Joint Comission, la ASA (American Society of Anesthesiologists) y numerosas agencias gubernamentales han alertado de la necesidad de elaborar recomendaciones específicas y disminuir drásticamente la prescripción de opioides.

Fuente: Kharasch ED, Brunt LM. Perioperative opioids and public healt Anesthesiology 2016;124/(4):960-5.
Fig. 4 Tasas de dispensación de opioides, muertes por sobredosis no intencional e ingresos hospitalarios por adicción de opioides, entre 1999 y 2010.
El uso de opioides perioperatorios es una de las raíces del problema. La necesidad de disminuir el tiempo de ingreso hospitalario, y por ello transferir al domicilio parte del curso postoperatorio, ha incrementado la prescripción de opioides al alta de una intervención quirúrgica. Estos datos se confirman en un estudio realizado en los periodos 2004, 2008 y 2012, en 155.297 pacientes 23, sin uso previo de opioides, intervenidos de síndrome de túnel carpiano, colecistectomía laparoscópica, hernia inguinal y artroscopia de rodilla. Un 70 % de estos pacientes sometidos a procedimientos de bajo riesgo seguían consumiendo opioides a los 7 días del postoperatorio, sobre todo oxicodona-paracetamol. Desde el 2004 se ha incrementado no sólo el número de prescripciones sino también la dosis diaria total de opioide.
El estudio de Al Dabbagh 24 en pacientes operados de fractura de fémur registra un 45 % de uso continuado de opioides a los 6 meses y un 36 % al año.
El estudio de Clarke 25 en 39.140 pacientes, sin opioides previos, mayores de 60 sometidos a cirugía mayor, registra un 3 % (n = 1.229) de pacientes que continúan consumiendo opioides 90 días después de la cirugía.
El problema no es la indicación de los opioides en el dolor moderado-intenso, sino su administración en dolor leve-moderado y las pautas continuadas sin control, más allá de los primeros días del postoperatorio. Por ello, las actuales recomendaciones 26 se basan en minimizar la dosis de opioide, aplicar pautas multimodales y retirar precozmente los opioides cuando puedan ser sustituidos por otros analgésicos. Definir los pacientes con factores de riesgo en el uso prolongado de opioides 26 es un aspecto pendiente que puede contribuir a la prevención del abuso.
PROGRAMAS DE CIRUGÍA FAST-TRACK O REHABILITACIÓN PRECOZ
Los programas de cirugía fast-track o rehabilitación precoz o intensificada han cambiado por completo el curso perioperatorio de los pacientes. Se basan en la aplicación de 10 a 20 medidas perioperatorias, con el objetivo de acelerar la recuperación PO, disminuyendo la respuesta al estrés quirúrgico, las complicaciones, la estancia media y los reingresos.
Los programas de fast-track han evolucionado desde los iniciales 20 elementos planteados por Kehlet 27 en los años 90. El estudio de Feroci 28 sobre 606 pacientes intervenidos de cáncer colorrectal (CCR) registró cinco elementos clave en el análisis multivariante para conseguir buenos resultados: cirugía laparoscópica, retirada precoz de sonda urinaria, uso selectivo de drenajes, nutrición oral sólida y movilización precoz.
Con respecto al DAP, el análisis de la literatura sobre cirugía fast-track no permite elaborar conclusiones. La heterogeneidad de los estudios con respecto a metodología, medidas de dolor, tipos de pacientes y de abordajes quirúrgicos, impide el análisis de resultados. Por ello, actualmente no existe evidencia sobre cuál es la analgesia postoperatoria óptima en los programas de cirugía fast-track.
El primer metanálisis que ha podido realizarse (Chemali ME, 2016 29 ) hace una revisión desde 1966 hasta 2015. Solo 21 ECA cumplen criterios de inclusión, con 1.261 pacientes. No se pueden demostrar diferencias en la intensidad del dolor o en la estancia media según el tipo de analgesia postoperatoria. Tal como indican los autores, se necesitan más estudios y mejor diseñados para extraer conclusiones. Por otro lado, el control del DAP es uno de los muchos factores que intervienen en los resultados clínicos 30, por lo que el análisis aislado de la intensidad del dolor difícilmente registrará un impacto significativo.
Un estudio retrospectivo 31 sobre las bases de datos de 52 hospitales, en 7.221 pacientes intervenidos de CCR, registra una media de dolor en el primer día postoperatorio de 5,1 ± 2,44, es decir, una media elevada que corresponde a dolor moderado-intenso. Agrupan a los hospitales según el alto o bajo volumen de intervenciones y grados de DAP. Los pacientes operados en los hospitales con las puntuaciones más bajas de dolor tienen menos estancia media, (6,5 vs. 7,9 d; p = 0,007) y menos complicaciones postoperatorias (20,3 vs. 26,4 %; p < 0,001) que los hospitales que registraron elevadas puntuaciones en el DAP. En esta evaluación de la práctica real de los hospitales se muestra una gran variabilidad en los resultados, y por primera vez se relaciona el grado de control del DAP con los buenos resultados y las mejores prácticas clínicas.
Se ha puesto en cuestión que el control del DAP se base solo en el objetivo de obtener un EN < 3. De hecho, la realidad muestra que el inicio precoz de la deambulación, de la fisioterapia o de la rehabilitación, son factibles con un nivel moderado de dolor 32. Pretender un dolor con EN < 3 en estos programas de fast-track puede asociarse a inmovilidad del paciente o a efectos secundarios de los analgésicos que retrasen la recuperación.
Se han descrito las siguientes pautas y técnicas analgésicas asociadas a la cirugía fast-track 18:
- Analgesia multimodal: el uso conjunto de distintos fármacos y técnicas analgésicas permite minimizar dosis y efectos secundarios, aumentado la efectividad 33. Se ha demostrado, por ejemplo, que la combinación de paracetamol y un antinflamatorio no esteroideo (AINE) disminuye de un 30 a un 50 % el consumo de opioides 34.
- Analgesia epidural en laparotomía: la analgesia epidural es la más efectiva en el control del dolor dinámico, en el bloqueo del estrés quirúrgico y en la recuperación del tránsito intestinal en la cirugía abdominal mayor por laparotomía 35. Un reciente metanálisis de Pöpping 36) analiza los ensayos publicados sobre morbimortalidad y analgesia epidural, que incluyen a 9.044 pacientes, 4.525 con analgesia epidural. Se registra una disminución de la mortalidad en el grupo epidural frente a la analgesia sistémica de 3,1 vs. 4,9 %, (OR, 0,60; 95 % CI, 0,39-0,93). La analgesia epidural disminuye significativamente la incidencia de arritmias, depresión respiratoria, atelectasias, neumonía, íleo, náuseas y vómitos postoperatorios, acelerando la recuperación del tránsito intestinal. No obstante, se registra mayor incidencia de hipotensión (8,8 vs. 2,3 %), prurito, bloqueo motor y retención urinaria. En esta serie no se detecta ninguna complicación neurológica severa, ni hematoma ni absceso epidural. Se registra un 6,1 % de fallos técnicos.
- Analgesia i.v. controlada por el paciente (PCAIV) en la cirugía mayor laparoscópica: en la actualidad, el abordaje laparoscópico se ha extendido a todos los tipos de cirugía, siendo uno de los factores de peso en la reducción de la estancia media y las complicaciones en la cirugía fast-track. El impacto de la laparoscopia en el dolor postoperatorio es significativo, observándose en cirugía abdominal, por ejemplo, una disminución media de un 34,8 % en el dolor en reposo, de un 33,9 % en el dolor al movimiento 37 y una reducción de un 37 % en el consumo de opioides, comparado con la laparotomía. Esta disminución de los requerimientos analgésicos nos obliga a replantear la indicación de la analgesia epidural en la cirugía laparoscópica, habiéndose demostrado que no aporta ventajas comparada con la analgesia intravenosa. La PCAIV se usa en cirugía mayor laparoscópica 38 sola o en combinación con bloqueos del plano transverso abdominal (TAP) infiltración de la herida quirúrgica. Se ha demostrado que, en este contexto, el uso de opioides no retrasa la recuperación del tránsito intestinal 39, que depende también de otros factores como el abordaje quirúrgico mínimamente invasivo o el inicio precoz de la ingesta oral.
- Lidocaína i.v.: la revisión sistemática de Kranke 40 concluye que existe una evidencia débil sobre el efecto analgésico de la lidocaína i.v. perioperatoria. Los estudios son muy heterogéneos comparados con placebo y con pocos pacientes.
- Pregabalina: la administración perioperatoria de pregabalina está muy controvertida 41. Su efectividad analgésica varía según la intervención quirúrgica, y en algunos estudios no es clínicamente significativa. Hay que tener en cuenta la posibilidad de efectos secundarios, como la sedación o visión borrosa.
- Infusión continua de anestésico local en la herida quirúrgica: el metanálisis de Vnetham 42 concluye que no hay suficiente evidencia que apoye la efectividad analgésica de la infiltración continua de la herida quirúrgica. Se necesitan estudios específicos por procedimiento quirúrgico.
- Bloqueo TAP (plano transverso abdominal): el bloqueo TAP se ha demostrado efectivo en cirugía colorrectal laparoscópica 43, en cesáreas e histerectomías, en cirugía urológica y en el trasplante renal, entre otras. Desde un punto de vista multimodal 44, disminuye el consumo de morfina en un 43 % y el tiempo de inicio de dieta oral.
NUEVAS VÍAS DE ADMINISTRACIÓN DE OPIOIDES
Las principales innovaciones analgésicas se basan en el uso de los viejos fármacos con nuevos dispositivos o nuevas vías de administración 15.
Se han desarrollado nuevos dispositivos de administración de opioides no invasivos o "needel-free", con el fin de eliminar las desventajas de la PCAIV de morfina.
El sufentanilo sublingual (SSTS [Sufentanil Sublingual Tablet System - Zalviso(r)]) está aprobado en la Unión Europea en base a 3 estudios fase III, y pendiente de la aprobación de la FDA (Food and Drug Administration). Es un dispositivo preprogramado 45 que administra nano-tabletas sublinguales de 15 microgramos de sufentanil a demanda del paciente, con un tiempo de seguridad de 20 minutos, durante un periodo de 72 h. El sufentanilo sublingual posee un elevado índice terapéutico, una elevada biodisponibilidad (59 %), así como un rápido tiempo de equilibrio entre el plasma y el sistema nervioso central: 6,2 minutos frente a los 168 minutos de la morfina. Carece de metabolitos activos 46 y su metabolismo no se ve afectado por la edad, el elevado índice de masa corporal (IMC) o la insuficiencia hepática o renal.
El fentanilo transdérmico (Fentanyl Iontophoretic Transdermal System [ITS] - IONSYS(r)), retirado del mercado en 2008, ha sido reintroducido recientemente y aprobado en la Unión Europea y en la FDA 47. Administra en modo PCA 40 microgramos de fentanilo transcutáneo por iontoforesis con un tiempo de seguridad de 10 min. Al igual que el sufentanilo, tiene un rápido inicio de acción (6,6 minutos), y un índice terapéutico mayor que la morfina 48, pero menor que el sufentanilo.
Estos sistemas aportan las siguientes ventajas:
- Evitan la vía intravenosa; por ello incrementan la movilidad y la comodidad del paciente y carecen de la posibilidad de provocar flebitis o bacteriemia.
- Son dispositivos preprogramados, con lo que se evita el error humano en la programación de las bombas de PCA y en la preparación de los fármacos.
- Son opioides de inicio rápido y acción prolongada, sin metabolitos activos, por lo que teóricamente tienen un perfil farmacológico más eficaz y seguro.
- No obstante, presentan también las siguientes desventajas:
- Incremento de costes inicialmente. Están pendientes estudios de coste-efectividad.
- Presentan una incidencia de efectos secundarios similar a la morfina.
- La preprogramación de los dispositivos no permite ajustar las dosis a demandas individuales, como es el caso de los pacientes tolerantes a opioides.
- Su aplicación exclusivamente hospitalaria excluye a los pacientes de cirugía mayor ambulatoria y a los pacientes que precisan continuar el tratamiento opioide en su domicilio.
Estas nuevas alternativas terapéuticas están pendientes de estudios de efectividad por procedimiento, comparando con la analgesia óptima para cada intervención quirúrgica. También se precisan estudios de seguridad en cuanto a la incidencia de efectos adversos en un entorno real de una planta quirúrgica. Se precisan estudios de coste-efectividad y también estudios que comparen entre sí las distintas modalidades no invasivas de administración de opioides.
Estas nuevas alternativas podrían sustituir a la administración de la PCA de morfina a bolos en la cirugía mayor laparoscópica, en la cirugía de columna vertebral o en la cirugía mayor maxilofacial, neurocirugía, ORL o plástica.
Podrían jugar un papel de analgesia de transición en la retirada precoz de los catéteres epidurales o paravertebrales en cirugía torácica o en cirugía vascular.

















