INTRODUCCIÓN
El envejecimiento es un proceso natural y universal, donde interactúan variables como la genética, el medio ambiente, el estilo de vida y las enfermedades crónicas, entre otras, y de cómo lo hagan va a depender en gran medida el modo de envejecer. La vejez está asociada a una pérdida de masa muscular, denominada sarcopenia, que se inicia en la cuarta década de la vida con una disminución de fuerza de alrededor del 1% al año y que se acelera con el transcurso de los años1. La sarcopenia es un síndrome que se caracteriza por una pérdida gradual y generalizada de la masa muscular esquelética y de la fuerza, con riesgo de presentar resultados adversos como discapacidad física, calidad de vida deficiente y mortalidad2. La sarcopenia contribuye a una disminución de la capacidad funcional e independencia en las actividades de la vida diaria, y afecta a la calidad de vida de las personas mayores3. Existe una clara relación entre pérdida de masa y potencia muscular y la pérdida de independencia funcional, que contribuye a las caídas, fracturas y necesidad de internamiento en instituciones sanitarias. La sarcopenia no solo va a tener consecuencias en la movilidad, sino también importantes repercusiones metabólicas, tanto en la regulación de la glucosa como en la masa ósea, el balance de proteínas o el control de la temperatura, entre muchas otras. Todas son, además, características compartidas con el síndrome de fragilidad.
La reducción de la masa y la fuerza muscular se atribuye a la disminución de fibras musculares, sobre todo las de tipo II o rápidas4. La pérdida de masa muscular relativa es más temprana y se sitúa entre los 30 y 40 años, mientras que la masa muscular absoluta no comienza a descender hasta la quinta década de la vida y es mayor en los miembros inferiores que en los superiores y en hombres más que en mujeres5.
La definición actual de sarcopenia incluye la pérdida de masa muscular, de fuerza y cambios cualitativos en el tejido muscular, y se considera que están implicados en dicha pérdida una amplia variedad de procesos como la alteración en la síntesis y degradación de proteínas, la inflamación, las alteraciones hormonales y la disfunción mitocondrial2,6.
La prevalencia del síndrome de sarcopenia va a depender de la definición y de las técnicas utilizadas en su diagnóstico. Según Baumgartner et al.7 esta afecta al 20% de los varones entre 70 y 75 años, al 50% de los de más de 80 años y entre el 25% y el 40% de las mujeres, en las mismas franjas de edad. Por otro lado, el “Informe Mundial sobre el envejecimiento y salud” de la Organización Mundial de la Salud (OMS), publicado en septiembre de 2015, pone de relieve el rápido envejecimiento que está sufriendo la población mundial, indicando que entre los años 2000 y 2050 la proporción de personas mayores de 60 años se duplicará, pasando del 11% al 22%8. En España, los datos son más preocupantes, ya que está sufriendo un crecimiento de envejecimiento demográfico más rápido que el resto de los países de la comunidad europea. Las previsiones futuras señalan que en 2050 habrá 16 millones de personas mayores, que corresponde a un 30% de la población total9. La sarcopenia va a generar discapacidad, enfermedad y dependencia y por tanto debería convertirse en una prioridad para las autoridades sanitarias.
El estilo de vida, los hábitos alimentarios, la actividad física y la presencia de enfermedades son factores que determinan su evolución. De este modo, la sarcopenia se va a ver agravada por el déficit en la ingesta de proteínas, causando una disminución de la función general que conduce a la fragilidad. Hay evidencia de que las intervenciones en actividad física y nutrición son eficaces para disminuir la pérdida de masa magra y mejorar la fuerza muscular. El estilo de vida sedentario, que afecta especialmente a los mayores, hace que la inactividad acelere la pérdida de masa muscular. De este modo, se apuntan como potenciales intervenciones no farmacológicas para el tratamiento de la sarcopenia el ejercicio físico, los suplementos nutricionales o ambas modalidades en conjunción.
OBJETIVO
Conocer los resultados de los últimos estudios sobre el síndrome de sarcopenia y el uso de complementos proteicos para su tratamiento y/o prevención.
METODOLOGÍA
Para la realización de esta revisión sistemática se consultaron publicaciones científicas indizadas en las siguientes bases de datos: MEDLINE a través de su buscador PubMed, Science Direct, SciELO, TRIP database y Dialnet, mediante la combinación de los descriptores del Medical Subjects Headings (MeSH) referentes a “sarcopenia”, “older people”, “aged”, “diet”, “protein supplements”, “dietetic supplements”, “muscle mass” y “muscle strength” y sus equivalentes en español: “sarcopenia”, “persona mayor”, “anciano”, “nutrición”, “alimentación”, “suplemento proteico”, “suplemento dietético”, “masa muscular” y “fuerza muscular”.
Para valorar la calidad metodológica de los ensayos clínicos aleatorizados sometidos a estudio usamos la escala PEDro y solo incluimos aquellos que presentaban una puntuación igual o superior a 6.
La búsqueda se acotó a las publicaciones comprendidas entre los años 2011 y 2016, aunque para la elaboración de los antecedentes y la contextualización del problema no se acotaron las fechas, buscando siempre publicaciones de calidad y de referencia en el síndrome de sarcopenia. Se buscaron ensayos clínicos controlados aleatorizados y revisiones sistemáticas. A través de los ensayos clínicos aleatorizados obtuvimos pautas nutricionales proteicas para el tratamiento y prevención de la sarcopenia en los ancianos, mientras que con las revisiones sistemáticas pudimos obtener una visión amplia del síndrome y poder así contextualizarlo.
Las publicaciones fueron seleccionadas a partir del título y del resumen, y se obtuvo el texto completo para un análisis más detallado. La fecha de la última actualización de la búsqueda se realizó en diciembre de 2016.
Criterios de inclusión
Ensayos clínicos aleatorizados publicados en revistas indizadas de bases de datos internacionales, sujetas a revisión por pares y con acceso al texto completo.
Publicaciones realizadas desde el año 2011 hasta diciembre de 2016.
Las publicaciones deben ser sobre ancianos.
Los artículos deben de haber sido publicados en inglés o español.
Los trabajos originales deben incluir los suplementos proteicos como pauta principal del tratamiento nutricional en el síndrome de la sarcopenia.
La información sobre la intervención debe ser detallada.
Criterios de exclusión
Documentos de interés que no basaran su estudio en personas mayores.
Publicaciones realizadas antes del año 2011.
No se incluyen citas, actas de congresos, cartas al director o editoriales.
Artículos donde los suplementos proteicos no son el componente principal de la pauta nutricional.
Para recoger los datos se ha usado un protocolo personalizado donde se registraron datos generales de la publicación, tipo de publicación, base de datos usada, descriptores del ámbito de estudio, edad de la población, duración del estudio, resumen, metodología utilizada, resultados obtenidos, puntuación PEDro y referencias bibliográficas.
RESULTADOS
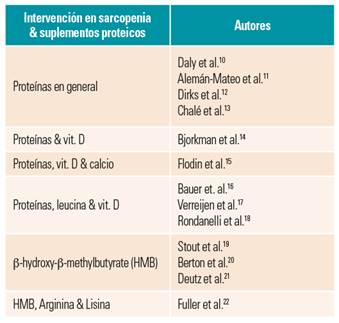
Encontramos 13 artículos sobre suplementos proteicos y el síndrome de sarcopenia en el adulto mayor que cumplían los criterios de inclusión. De estos, 4 hacían referencia a aportes proteicos en general; 1 a suplementos proteicos en combinación con vitamina D; 1 a la suma de proteínas, vitamina D y calcio; 3 a la combinación de proteínas, el aminoácido leucina y vitamina D; 3 al aporte de β-hidroxi-β-metilbutirato (HMB), metabolito de la leucina que influye en el mecanismo de acción de la pérdida de masa muscular reduciendo el catabolismo proteico, y 1 a la combinación de este último junto a los aminoácidos lisina y arginina (tabla 1).
La mayoría de estos autores usan los suplementos proteicos junto a una pauta de ejercicio físico10-14,17-21, generalmente de resistencia progresiva, ya que este tipo de ejercicio es el que presenta los mejores resultados en cuanto a ganancia de masa y fuerza muscular en el tratamiento y prevención de la sarcopenia en el anciano, frente a otro tipo de ejercicios como los aeróbicos, flexibilidad, vibraciones o equilibrio, donde las ganancias no son tan evidentes, aunque se incluyen en diferentes pautas de entrenamiento donde estos ejercicios son combinados entre sí, por los beneficios que reportan al anciano cada uno de ellos.
El modo de aportar las proteínas en los artículos revisados es muy variable. Encontramos trabajos donde las proteínas se dan diariamente, repartidas en 2-3 tomas, y en otros donde solo se aportan tras la pauta de ejercicio físico, que suele tener una frecuencia de 3-5 sesiones semanales. Las proteínas se suelen dar en forma de carne roja, queso, suero de leche o en estado puro, en unas cantidades que oscilan entre 20 y 45 g/día. En cuanto al contenido de aminoácidos esenciales, estos rondan los 9 g/día, y el de leucina en concreto varía entre 4 y 9 g/día. La suplementación con HBM se encuentra entre 1,5 y 3,0 g/día. Estos aportes produjeron en general un aumento de la masa y la fuerza muscular, así como un incremento de la síntesis de proteínas musculoesqueléticas y del tamaño de la fibra muscular en el anciano.
DISCUSIÓN
El estado nutricional es fundamental en el mantenimiento de la fuerza muscular. Los ancianos tienen una tasa de catabolismo proteico mayor, de modo que sus necesidades proteicas son superiores a las del resto de edades. El requerimiento va a ser proporcional al peso y a la composición corporal, pero no a la ingesta de energía, ya que esta se reduce con el envejecimiento. El aporte proteico aumentado no solo va a ser beneficioso para la masa muscular, sino que también lo será para el manejo de otras entidades como la osteoporosis, la obesidad, la diabetes mellitus y el síndrome metabólico. Las necesidades proteicas van a aumentar en un 1% por cada descenso de 100 kcal en la ingesta energética por debajo de 2.000 kcal diarias23. Un estilo de vida sedentario reduce la eficacia de los aminoácidos.
Para lograr una síntesis proteica muscular adecuada es fundamental el aporte de aminoácidos derivados de la dieta. Algunos autores defienden abandonar la concepción de requerimientos proteicos diarios a favor de profundizar en la cantidad de proteínas de alto valor biológico aportadas en cada comida y en el patrón de ingesta a lo largo del día24. Debe asegurarse un aporte proteico suficiente, aunque este dependerá de la situación del anciano y de la edad, ya que esta última va a alterar la función digestiva, así como la biodisponibilidad de algunas proteínas. Los requerimientos mínimos para la síntesis de proteínas estarán entorno a unos 30 g de proteínas diarios o 15 g de aminoácidos esenciales que si están adecuadamente repartidos a lo largo de las diferentes comidas y si son de alto valor biológico favorecerán la síntesis proteica25,26. Son muchos los estudios encontrados sobre aportes proteicos en la sarcopenia10,12-18 y en todos ellos sus autores afirman que una ingesta adecuada de proteínas es parte fundamental del tratamiento de la sarcopenia.
Daly et al.10 dieron durante 24 semanas 240 g de carne roja, repartida en 3 porciones semanales, a mayores de 65 años, y comprobaron que además de mejorar la fuerza y la masa muscular, lo hizo también la función cognitiva. Alemán-Mateo et al11 suplementaron la dieta habitual de 132 ancianos con 210 g de queso ricotta, 3 veces al día, y vieron que tras 12 semanas aumentó la masa muscular y el equilibrio y que atenuó la pérdida de fuerza muscular. La combinación de este aporte proteico y el ejercicio mejora la sensibilización del músculo ante el estímulo nutricional. Incluso se pueden obtener beneficios añadidos optimizando el momento del aporte proteico24.
Diferentes estudios han demostrado que la ingesta de aminoácidos esenciales como la leucina mejora la síntesis proteica cuando se toman al terminar el ejercicio. Estudios como el de Paddon et al.25 consiguieron un aumento del 25% del área transversal del cuádriceps y de un 15% de fuerza extensora tomando un suplemento oral de leucina inmediatamente después del ejercicio, frente a los que lo tomaban 2 horas más tarde. Este efecto igualmente se ha podido comprobar en sujetos encamados. Además, hay que destacar la importancia de ingerir hidratos de carbono de alto índice glucémico junto con los aminoácidos, tras realizar el ejercicio de resistencia, para favorecer la síntesis proteica27.
La leucina tiene una acción fundamental en el inicio de la síntesis proteica. Aumentar la proporción de leucina en una mezcla de aminoácidos esenciales puede mejorar la respuesta anabólica muscular en el anciano, a través de vías intracelulares de síntesis proteica muscular y mecanismos independientes de la insulina, y ser similar a personas jóvenes. La dosis umbral de la leucina para la estimulación de la síntesis de proteína muscular en ancianos parece ser aproximadamente de 3 g, que corresponde a 25-30 g de una proteína de alta calidad. A partir de estos datos, se puede inferir que cualquier comida que contenga menos de la dosis de aminoácidos esenciales como la leucina sería menos anabólica para el músculo esquelético en los adultos mayores. Según Beasley et al.28, los aminoácidos esenciales estimulan el anabolismo proteico muscular en el adulto mayor, pero se desconoce si todos los aminoácidos son necesarios para evitar o reducir la sarcopenia, y afirman que el papel de los suplementos de proteína para reducir o evitar la sarcopenia en el envejecimiento es algo controvertido.
En los estudios hallados para nuestra revisión, Rondanelli et al.18, Bauer et al.16 y Verreijen et al.17 usan la leucina como parte de sus intervenciones nutricionales en pacientes sarcopénicos. Rondanelli et al.18 usaron un suplemento con proteínas de suero de leche que incluían 4 g de leucina, además de otros aminoácidos esenciales (9,4 g) y vitamina D (100 UI), en ancianos con una edad media de 80,3 años durante 12 semanas. Estos autores afirman que la combinación de proteínas, leucina, vitamina D y ejercicio físico no solo mejora la masa y fuerza muscular en los ancianos, sino que además contribuye a aumentar su bienestar. Bauer et al.16 incluían en el preparado nutricional que daban a los ancianos que participaban en su estudio de 13 semanas, 3 g de leucina y conseguían beneficios similares a los de Rondanelli et al. con respecto a la sarcopenia.
El HMB es un metabolito de la leucina que influye en el mecanismo de acción de la pérdida de masa muscular reduciendo el catabolismo proteico29. El HMB es producido de forma natural en humanos y es precursor de la síntesis de colesterol en células musculares. Produce diversos beneficios, como la mejora de la integridad del músculo, ayuda a reducir el daño muscular, protege el músculo del daño relacionado con el estrés, disminuye la degradación proteica en estados de enfermedad, protege la masa muscular e incrementa la síntesis proteica30. Rueda30 demostró con su experimentación en ratas de edad avanzada que la suplementación con HMB tiene efectos positivos en el músculo tras un periodo de inmovilización. Las ratas suplementadas aumentaron la activación de las células satélite, incrementando la formación de nuevo tejido muscular. La suplementación con HMB ayuda a prevenir el daño muscular inducido por el ejercicio. También es una alternativa nutricional mejor que la leucina en el manejo del desgaste muscular asociado a diversas condiciones hipercatabólicas.
En la revisión encontramos diversos ensayos clínicos donde usaban este metabolito19-22. Fuller et al.22 combinaron 2-3 g de HMB con 5-7,5 g de lisina y 1,5-2,25 g de arginina durante 12 meses, en sujetos mayores de 76 años y teniendo en cuenta los niveles séricos de vitamina D. Todos los sujetos suplementados ganaron masa muscular (p < 0,02), pero solo aquellos que tenían niveles sanguíneos de 25-OH-vitamina D ≥ 30 ng/ml obtuvieron ganancias significativas en fuerza (p < 0,02) y por tanto de funcionalidad. Stout et al.19 evaluaron los efectos de 24 semanas de suplementación con HMB (3 g, 2 veces al día) y entrenamiento de resistencia (3 días por semana), y la suplementación de HMB sin entrenamiento alguno en personas mayores de 65 años. Tanto los ancianos que solo fueron suplementados como aquellos que realizaron el ejercicio de resistencia mejoraron la masa total magra, la fuerza, la capacidad funcional y la calidad muscular. De este modo, los autores informaron que el HMB incrementó la fuerza y la calidad muscular sin ejercicio de resistencia progresiva, pero incidieron en que este tipo de entrenamiento es una intervención eficaz para mejorar las medidas de composición y funcionalidad corporales. Berton et al.20 suplementaron con 1,5 g de HMB a un grupo de mujeres sanas de edad avanzada (69,5 años de media) durante un periodo de 8 semanas y posteriormente compararon los resultados obtenidos con otro grupo de mujeres de las mismas características. A esta suplementación se le añadieron 2 días a la semana de ejercicio físico suave. La suplementación no tuvo efectos significativos a corto plazo sobre el rendimiento físico, pero sí que se obtuvieron mejoras sobre la fuerza muscular. Deutz et al.21 dieron un suplemento de 3 g/día de HMB a un grupo de ancianos que mantenían reposo en cama durante 10 días y pudieron comprobar que no se produjeron pérdidas de masa muscular. Los resultados de estos estudios con HMB coinciden con los del metaanálisis de Wu et al.31, en el que llegaron a la conclusión de que el HMB preserva la masa muscular en los adultos mayores y que puede ser útil en la prevención de la atrofia muscular inducida por el reposo en cama y otros factores.
CONCLUSIONES
En el enfoque terapéutico del síndrome de sarcopenia es fundamental la incorporación de proteínas de alto valor biológico a la dieta, que junto al ejercicio de resistencia van a tener un efecto sinérgico sobre el tejido muscular. El suplemento de HMB puede ser de utilidad para preservar la masa muscular y evitar la atrofia muscular en el anciano.
Un estado muscular óptimo en el anciano puede evitar que este se convierta en un anciano frágil y como consecuencia tenga mayor riesgo de caídas, pérdida de la funcionalidad y mayores niveles de dependencia en sus actividades de la vida diaria.