INTRODUCCIÓN
La esquistosomiasis está considerada en la actualidad la segunda parasitosis más importante después de la malaria, y cursa con elevadas tasas de morbilidad y mortalidad, principalmente en países pobres y en vías de desarrollo sin acceso al diagnóstico y tratamiento1,2. Seis especies son los principales agentes de la esquistosomiasis humana, por un lado Schistosoma japonicum, S. mansoni, S. mekongi, S. intercalatum y S. guineansis que causan la esquistosomiasis intestinal en África, Oriente Medio, América del Sur y el Caribe, China, Filipinas, Indonesia, Vietnam y Laos, y por el otro S. haematobium productor de esquistosomiasis urogenital en principalmente en África, en diversas localizaciones en Oriente Medio y recientemente descrito en Francia3.
En 2017 según datos de la OMS, se estima que en África subsahariana unos 436 millones de personas están en riesgo de contraer la infección por S. haematobium, y que anualmente contraen la enfermedad 112 millones de personas4.
La enfermedad por este parásito no es propia del continente europeo. En España los casos son importados por inmigrantes o personas que visitan zonas endémicas, como pueden ser turistas que realizan viajes de aventura y personal del ejército5,6. Sin embargo, recientemente se han descrito y demostrado nuevos casos de infección autóctona por S. haematobium adquirida en Europa7. En 2014 aparecieron los primeros casos de esquistosomiasis urogenital europea en varios miembros de tres familias francesas que no habían viajado a zonas endémicas, y que únicamente referían haber pasado las vacaciones de verano en agosto de 2011 y 2013 en Córcega (Francia), donde se bañaron en el río Cavu8. Desde entonces han ido apareciendo más casos, se llegó a prohibir el baño en el río Cavu9, y el Centro Europeo para la Prevención y Control de Enfermedades (ECDC) publicó ese mismo año un análisis de riesgo en el que se evaluaba la magnitud y riesgo del brote en Europa7, y llevó a cabo una actualización del mismo en 201510.
Los equistosomas son platelmintos de la clase Trematoda con un ciclo de vida complejo. En el caso de S. haematobium, los huevos embrionados llegan al medio externo por la orina de las personas infectadas por el parásito. Cuando los huevos entran en contacto con el agua dulce, tiene lugar la salida del miracidio que penetra en algunas especies de caracoles acuáticos que actúan como primer hospedador intermediario. La relación caracol-parásito es muy específica, sólo ciertas especies de caracoles juegan un papel en la trasmisión, en el caso de S. haematobium se trataría de caracoles del género Bulinus11. En Europa la única especie que encontramos de este género es B. truncatus12. Sin embargo algunos trabajos han demostrado que caracoles de otra especie presente en Europa, Planorbarius metidjensis, hospedador natural de S. bovis, es capaz de actuar también como hospedador intermediario de S. haematobium13. En el caracol se producen dos generaciones de esporocistos y salen de este las formas infectivas, las furcocercarias, que quedan libres en el medio externo donde nadan activamente hasta encontrar al hospedador definitivo humano al que acceden mediante penetración transcutánea. El parásito llega al sistema porta donde madurará a adulto, se empareja y migrarán a los plexos vesicales. La puesta de huevos es en los vasos sanguíneos que irrigan las paredes de la vejiga y salen al exterior por la orina cerrándose el ciclo14.
La clínica de la esquistosomiasis pasa por distintas etapas, coincidiendo con el ciclo del parásito. Cuando se produce la penetración transtegumentaria de la furcocercaria aparece una dermatitis aguda pruriginosa, la “dermatitis del nadador”. En la fase aguda, que equivale a la migración del esquistosómulo y la posterior maduración, los síntomas aparecen varias semanas después de la exposición, entre ellos están diarrea, vómitos, malestar general, hiperreactividad bronquial y fiebre. En la etapa final, el estadio de enfermedad crónica, el organismo reacciona ante los huevos depositados por el helminto en las paredes de la vejiga y uréteres, entre otras localizaciones.
Los síntomas iniciales suelen ser disuria, polaquiuria, proteinuria y hematuria, siendo ésta un signo de gran sospecha. Si persiste la enfermedad, las lesiones pueden evolucionar a fibrosis, calcificación e hidronefrosis. Sin tratamiento que cure la enfermedad, siendo el praziquantel el fármaco de elección15, los esquistosomas parasitan al ser humano entre 3 a 10 años, y en algunos casos pueden llegar a vivir hasta 4016. Además, la infección crónica en muchos pacientes conduce a la aparición de carcinoma de células escamosas (SCC) de la vejiga. Es por ello que S. haematobium fue clasificado en 1994 como carcinógeno del Grupo 1 por la Agencia Internacional para la investigación del Cáncer (IARC)17.
El objetivo de este trabajo fue profundizar en los aspectos más importantes de la epidemiología de este parásito en nuestro medio, realizar una búsqueda de casos publicados de esta enfermedad en Europa en los últimos 20 años. También, investigar sobre estudios publicados que evidenciasen la presencia de B. truncatus y P. metidjensis, potenciales hospedadores intermediarios de este parásito en nuestro país. Y, por último, realizar una evaluación cualitativa de riesgo de que aparezcan casos de esquistosomiasis urogenital en España.
MATERIAL Y MÉTODOS
Se realizó una búsqueda bibliográfica de artículos publicados de casos documentados de infección por S. haematobium en todos los países miembros de la Unión Europea, de forma individualizada para cada uno de ellos. El intervalo de tiempo de la búsqueda se acotó a los últimos 20 años, de 1997 a 2017.
El motor de búsqueda empleado fue PubMed (https://www.ncbi.nlm.nih.gov/pub-med), debido a que en la base de datos Medline están indexadas la mayoría de revistas de literatura médica publicadas. Además, el sistema de búsqueda avanzada de Pubmed permitió sistematizar fácilmente la metodología de trabajo.
Con el objetivo de encontrar el mayor número de casos posibles publicados, se realizaron tres búsquedas diferentes para cada país. En la primera se empleó el nombre del país, en la segunda la nacionalidad de sus habitantes y en la tercera el nombre de la capital de cada uno de los países.
Se utilizó el sistema de búsqueda avanzada de PubMed. Las palabras clave y los campos de búsqueda se detallan en la tabla 1.
Tabla 1 Campos de búsqueda y palaba clave empleada en la búsqueda de casos de S. haematobium en los países de la UE

Realizada la búsqueda, se seleccionaron los artículos según los siguientes criterios de inclusión: el trabajo publicado reportaba uno o más casos de infección demostrada por S. haematobium, bien por la presencia de huevos en orina, y/o resultado de serología positiva; se indicaba el país donde se llevó a cabo el diagnóstico y en el trabajo estaba bien descrito si se trataba de una enfermedad importada o bien era autóctona. Los casos se clasificaron como autóctonos o importados en función de lo publicado por los autores.
Los criterios de exclusión fueron: artículos que no reportasen casos; que se tratase de trabajos que reportaban casos repetidos ya seleccionados (los pacientes que aparecen en varios artículos se contabilizaron de forma individual) y trabajos que tenían como objeto de estudio a alguna especie de parásito distinta a S. haematobium.
Por otro lado se realizó una búsqueda de trabajos que documentasen la presencia en España de potenciales hospedadores intermediarios para S. haematobium, los moluscos gasterópodos (caracoles acuáticos) de las especies Bulinus truncatus y Planorbarius metidjensis11,12,13.
Con el objeto de encontrar la mayor bibliografía posible, la búsqueda se realizó en tres buscadores PubMed, Google Académico, ya que este buscador general abarcaba un amplio espectro dentro de la literatura científica general, y en ResearchGate debido a que en la actualidad, en esta plataforma en expansión por iniciativa de los autores, se puede encontrar una gran cantidad de la literatura científica publicada.
Los motores de búsqueda y las palabras clave empleados para cada una de las especies de caracol se detallan en la tabla 2.
Tabla 2 Palabras claves y buscador empleado para las especies de caracol Planorbarius metidjensis y Bulinus truncatus

De los artículos encontrados se seleccionaron únicamente aquellos en los que se describía la presencia de estos posibles hospedadores intermediarios en nuestro país.
Finalmente, se realizó una aproximación de riesgo cualitativa de contraer la esquistosomiasis urogenital en España siguiendo las directrices del documento guía del Centro Europeo para la Prevención y Control de Enfermedades (ECDC) “Operational guidance on rapid risk assessment methodology” de 201118. Se aplicó la metodología de aproximación combinada, que agrupa en un solo algoritmo preguntas de probabilidad de transmisión junto a cuestiones relacionadas con el impacto de la enfermedad. La opción no combinada fue descartada ya que ésta proporcionaba una evaluación más precisa en situaciones de enfermedad con alta probabilidad y bajo impacto, o bien en enfermedades con baja probabilidad y alto impacto, y ninguno de estos supuestos se daba en este caso. También se evaluó el nivel de confianza del análisis basándose en la consistencia, relevancia y validez externa de la información.
RESULTADOS
Los resultados de la búsqueda de casos de esquistosomiasis urinaria en la Unión Europea fueron los siguientes: Se encontraron un total de 69 artículos. De estos trabajos se seleccionaron 29 que cumplían los criterios de inclusión, mientras que 40 fueron descartados.
En los 29 artículos aceptados se encontraron un total de 481 casos. Se clasificaron 328 como casos importados, los pacientes habían contraído la enfermedad fuera de Europa, y provenían o habían viajado a alguno de los países donde la esquistosomiasis por S. haematobium era endémica. Por otro lado, se identificaron un total de 152 casos autóctonos. En estos trabajos quedaba claramente demostrado por los autores que la enfermedad había sido contraída en Europa.
En la tabla 3 se indican, las palabras claves empleadas en la búsqueda, para cada uno de los países, los artículos encontrados, los trabajos incluidos en los resultados indicando su referencia bibliográfica, y el número de casos indicando en una columna los que eran autóctonos y en otra los importados. Solo se incluyeron aquellos países de la UE en los que aparecían casos publicados.
En la figura 1 se muestran el número de casos de esquistosomiasis urogenital importada que han sido encontrados publicados, y los países de la UE donde sus autores los han reportado.

Fuente: EuroGlobalMap de la web de EuroGeographics
Figura 1 Casos de esquistosomiasis urogenital importada que han sido encontrados publicados, y países de la UE donde sus autores los han reportado.
En la figura 2 se muestra, en un mapa, el número casos encontrados del brote europeo de S. haematobium con origen en Córcega, en función de la nacionalidad de los pacientes que se habían infectado. Hay señalar que tanto los 15 casos descritos en Italia, como los 5 de Alemania, y el caso belga, se correspondían a pacientes que habían viajado a la isla de Córcega dónde contrajeron la enfermedad20,23,34.
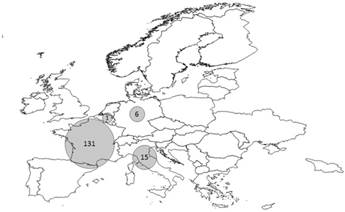
Fuente: EuroGlobalMap de la web de EuroGeographics
Figura 2 Casos publicados del brote autóctono europeo y nacionalidad de las personas a las que afectó.
En cuanto a la presencia de hospedadores intermediarios en España, tras la búsqueda y revisión de la literatura para B. truncatus, se seleccionaron 2 artículos en los que se demostraba la presencia de B. truncatus en El Ejido (Almería)6,47, y en la antigua laguna de Villena (Alicante)47. Además en uno de ellos Dana et al. indicaban y referenciaban otras localizaciones en las que esta especie de caracol se había descrito con anterioridad: Islas Baleares, Gerona, Barcelona, Tarragona, La Coruña, Pontevedra y Huelva6.
Por otro lado, se hallaron 5 artículos que describían la presencia de P. metidjensis en España: uno en Extremadura, concretamente las cuencas de los ríos Guadalquivir, Guadiana y Tajo (Badajoz y Cáceres)48), otro que documentaba la existencia de este caracol en la cuenca baja del río Guadiana, situada entre el embalse de Alqueva (Portugal) y el océano Atlántico49, un artículo donde se describe la presencia de este caracol en varios ríos, arroyos, fuentes y turberas en la Comunidad de Madrid50, y por último dos trabajos en el que habían utilizado caracoles de esta especie para experimentación, en uno de ellos los caracoles se recogieron en la provincia de Málaga51, y en el otro en la provincia de Salamanca52.
En la figura 3 se señalan, con una trama de líneas las provincias de España donde se ha documentado la presencia de ejemplares de B. truncatus, con una trama de puntos las provincias en las que se ha descrito la de P. metidjensis, y en negro donde se han encontrado ambas especies.

Fuente: EuroGlobalMap de la web de EuroGeographics
Figura 3 Provincias de España donde se ha documentado la presencia de ejemplares de Bulinus truncatus y Planorbarius metidjensis.
El resultado del análisis de riesgo cualitativo, siguiendo el algoritmo de aproximación combinado del documento guía del ECDC, fue “Bajo riesgo” de contraer esquistosomiasis urogenital en España. Se consideró: que no hay grupos específicos con mayor riesgo de infección; que el potencial de trasmisión dentro de los Estados miembros de la UE era bajo; que se trataría de casos de una enfermedad inesperada; la capacidad de dispersión dentro de la Unión Europea era baja y que la esquistosomiasis urogenital era una enfermedad con elevada morbilidad pero baja mortalidad para la que existe tratamiento y se pueden aplicar medidas de control.
Según la guía para el análisis de riesgos del ECDC el resultado del nivel de confianza del análisis fue el de satisfactorio ya que se basó principalmente en fuentes fiables. Dentro de la literatura gris se tuvieron en cuenta únicamente aquellos resultados que fueran consistentes.
DISCUSIÓN
Hasta el año 2014, todos los casos de esquitosomiasis que encontramos descritos en Europa habían sido únicamente casos importados de personas inmigrantes y viajeros de países donde esta enfermedad es endémica. Sin embargo, esto cambió ese año cuando se empezaron a reportar los primeros casos de lo que ha sido un brote autóctono europeo localizado en Córcega (Francia). En 2014 Berry et al., describen como a una niña de 4 años y a su padre de nacionalidad francesa, que padecían hematuria macroscópica, se les diagnosticó infección por S. haematobium en el Hospital Universitario de Toulouse. La familia no había viajado a ningún área en la que la esquistosomiasis urinaria fuera endémica, únicamente referían haber pasado las vacaciones de verano en agosto de 2011 y 2013 en Córcega, donde se bañaron en el río Cavu. A raíz de esto se diagnosticó también esquistosomiasis a otras 4 personas de dos familias francesas que pasaron las vacaciones en el mismo lugar8. Holtfreter et al. detallan el mismo año 2014 cinco infecciones en una familia alemana que igualmente se había bañado en el río Cavu en 201334. En 2015, Beltrame et al., publican un estudio realizado en 43 viajeros italianos que habían visitado la isla y se habían bañado en el rio Cavu al menos una vez entre 2011 y 2014, de estos se reportaron 15 infecciones clasificadas en 5 confirmadas, 2 probables y 8 posibles 20. A estos episodios hay que sumar los de Brunet et al., 2015 que presentaron 3 más, miembros de una misma familia francesa, que enfermaron y como en el resto de casos había pasado unos días del mes de agosto de 2013 en Córcega26. En otro estudio publicado en 2015 describen 11 casos más, de los cuales únicamente se confirmaron 2, 6 se clasificaron como probables, y 3 como sospechosos. Se trababa de viajeros de diferentes países que habían visitado Córcega, 9 eran alemanes, 1 canadiense y 1 belga23.
Una vez localizado definitivamente el problema, las autoridades llegaron a prohibir durante un año el baño en el río Cavu9, y en Francia se realizó un cribado nacional que permitió diagnosticar 110 casos más10. En nuestra búsqueda, el número de casos que hemos encontrado documentados es de 152, y se han confirmado casos en personas de cuatro países diferentes de la Unión Europea, Francia, Italia, Alemania y Bélgica.
Los sucesivos trabajos de investigación que se han ido publicando acerca de este singular episodio, han ayudado a esclarecer la complejidad real de este brote. En uno de los primeros trabajos, en el que se secuenció el ADN del parásito de un paciente afectado, se descubrió que en el gen mitocondrial COI aparecía un patrón propio de otra especie de esquistosoma, Schistosoma bovis. En este trabajo Moné et al., demostraron en este caso que el parásito implicado se trataba de un híbrido entre dos especies de esquistosomas, S. haematobium y S. bovis, y por ello los autores plantearon la posibilidad que hubiera sido un híbrido entre S. haematobium y S. bovis el causante de todos los casos del brote de las personas que habían enfermado en la isla francesa41. Sin embargo, en otro trabajo posterior de Boissier et al., realizaron el estudio molecular de huevos y miracidios de 12 pacientes, y demostraron que el brote era aún más complejo, había tres especies de parásitos implicados: S. haematobium, S. bovis y el esquistosoma híbrido S. haematobium-bovis. Encontraron individuos infectados únicamente por S. haematobium, otros que presentaban infección por la especie híbrida S. haematobiumbovis, pacientes que presentaban coinfección con presencia en el mismo individuo de especímenes de S. haematobium y el esquistosoma híbrido S. haematobium-bovis, e incluso demostraron un caso de coinfección en un individuo por S. haematobium y S. bovis53.
Una vez demostrado que había tres especies implicadas en el brote, está aún por esclarecer cuál pudo ser su origen. La hibridación entre ambas especies se podría haber producido en Córcega, y por tanto, el híbrido se trataría de una especie autóctona de la isla. Sin embargo, la hipótesis más probable es que el parásito o los parásitos hubiesen sido importados de algún país del África subsahariana en el que estas especies ya fuesen endémicas, como Senegal54. Además, el análisis molecular de las cepas francesas mostró que existía una estrecha relación filogenética con esquistosomas aislados del norte Senegal, lo que sugiere aún más un origen sud-africano para los parásitos europeos53. Si esto es así los huevos se introdujeron en la isla por algún o algunos individuos provenientes de Senegal u otro país del entorno, que tras orinar en el róo Cavu, hábitat en el que está presente el hospedador intermediario B. truncatus, el ciclo continuó hasta la formación de cercarias. En el caso de las formas infectantes de la especie híbrida de S. haematobium/bovis, además de haber parasitado a seres humanos, podrían haber infectado también al ganado local. Esto explicaría el motivo por el cual el ciclo del parásito ha podido mantenerse activo en la isla. La razón sería que el ganado enfermo ha estado actuando como reservorio de la enfermedad.
El hecho que en el brote esté implicada una especie híbrida es de gran importancia epidemiológica. Se ha demostrado que en algunas ocasiones la hibridación de especies puede ser beneficiosa para las generaciones de descendientes. Entre otras ventajas, puede hacer que aumente el espectro de hospedadores intermediarios a los que infectar, o el de hospedadores definitivos, e incluso ambos. De esta forma puede aumentar su capacidad de diseminación, y/o el número de especies reservorio de la enfermedad55. Los fenómenos de hibridación e introgresión entre parásitos pueden impulsar la aparición y la rápida evolución de nuevas enfermedades zoonóticas. Un ejemplo del aumento de la capacidad de diseminación sería el caso de los híbridos entre dos especies de protozoos, Leishmania infantum con Leishmania major. Cada uno de ellos emplea una especie de vector distinta para trasmitirse, pero se demostró que los híbridos resultantes de estas dos especies eran capaces de trasmitirse utilizando los vectores de ambos56. Como ya se ha mencionado los esquistosomas son altamente específicos en lo que respecta a hospedadores intermediarios, y en Europa es B. truncatus el hospedador intermediario principal de S. haematobium12. Sin embargo otra especie, P. metidjensis que también puede actuar como tal8. Ésta última no se localiza en Córcega, pero sí en otros países de Europa como España. Además, esta especie como dicen Boissier et al., podría ser utilizada también por el híbrido S. haematobium-bovis53. Por todo ello, en el supuesto que el brote de Córcega se tratara realmente de una zoonosis, el problema de salud pública sería mucho mayor, ya que las formas de control y erradicación de estas enfermedades son mucho más complejas que cuando afectan exclusivamente al ser humano.
El análisis de riesgo concluyó que actualmente la probabilidad de contraer la esquistosomiasis urogenital en España es baja para la población en general, además estaría condicionada por múltiples factores. Por un lado los sujetos más expuestos a contraer la enfermedad serían aquellos que llevan a cabo trabajos y/o actividades recreativas que les hagan estar en contacto con aguas dulces que estén contaminadas por furcocercarias, esto a su vez depende de dos cosas: que se introduzcan huevos de esquistosoma en dichas aguas, y que estén presentes hospedadores intermediarios.
Una parte de nuestro trabajo se ha centrado precisamente en la búsqueda de estudios que revelasen la presencia de hospedadores intermediarios en nuestro país y como muestran los resultados, existen poblaciones de B. truncatus y P. metidjensis en diversas localizaciones de nuestra geografía. Por otro lado la introducción de los huevos de esquistosoma, una especie no endémica, solo podría producirse por individuos infectados procedentes de zonas donde sí que está presente la enfermedad, y es importante recordar que en los individuos infectados no tratados, este parásito puede llegar a vivir hasta 40 años. En Europa hemos encontrado documentados 328 casos importados, 3 de ellos en España, de infección por S. haematobium, esta ha sido y será la puerta de entrada para este parásito en Europa. En España residen, según últimos datos procedentes del Instituto Nacional de Estadística (INE) del año 2017, 46.528.966 habitantes de los cuales 4.424.409 constituyen personas nacidas en el extranjero57. Monge-Maillo et al., describen en su trabajo que los extranjeros provenientes de África-subsahariana son principalmente de Guinea Ecuatorial, Nigeria y Senegal, siendo estos dos últimos países endémicos para S. haematobium58. Según últimos datos del INE para el primer semestre de 2016, un total de 633 personas nacidas en Nigeria y 1.973 en Senegal inmigraron a España59. Tampoco hay que olvidar a viajeros internacionales como personal militar, turistas y estudiantes, cada vez más numerosos, que retornan de áreas endémicas donde pueden haber contraído la enfermedad. Citar como ejemplos los casos de 8 viajeros alemanes afectados por esquistosomiasis aguda tras exponerse a las aguas del lago Tanganika35; el de unos estudiantes que contrajeron la enfermedad en un programa de intercambio entre alumnos de escuelas de Escocia y Malawi, donde 13 de ellos se infectaron por esquistosoma60 y casos en personal militar, como el de un grupo de soldados belgas que retornaron de la República Democrática del Congo, y 49 fueron diagnosticados con esquistosomiasis61.
Las principales limitaciones que hemos encontrado en nuestro estudio han sido que, por una parte, nuestra búsqueda, al ser tan amplia, seguramente infravalora el número real de casos documentados en cada país de la UE; a su vez ,que el número de casos publicados, como ocurre en la mayoría de ocasiones, es siempre significativamente inferior al de casos reales. Por otro lado, otra limitación sería la escasez de trabajos publicados acerca de las especies hospedadores intermediarios en España, debido a que consisten en trabajos que tratan un tema muy concreto y altamente especializado.
Las conclusiones principales de nuestro estudio serían que, aunque en España existe bajo riesgo de contraer la enfermedad, el creciente flujo migratorio que se produce en la actualidad, junto al hecho que en nuestro país existen zonas en las que están presentes los hospedadores intermediarios, no se puede descartar la posibilidad que estemos ante un escenario en el que se den las condiciones necesarias para que, en un futuro, pueda aparecer un brote autóctono, bien por S. haematobium o quizás por alguna especie híbrida, similar a lo que ha ocurrido en isla de Córcega. Esto coincide con las conclusiones de otros autores citados en este trabajo53,47,26, y con las de la actualización de la evaluación de riesgo del brote europeo en Córcega llevada a cabo por el ECDC en julio de 2015 donde alerta de un riesgo potencial para otras áreas del sur de Europa10 como es España. Por ello, las Autoridades Sanitarias y de Salud Pública deben estar en alerta ante el riesgo de que esto pueda ocurrir, más aún si se introdujera una especie de esquistosoma híbrida, teniendo en cuenta la dificultad para el control de la enfermedad si aparecen reservorios animales.
Es fundamental hacer especial hincapié en las medidas preventivas como: identificación y formación de grupos de riesgo (militares, cooperantes) e información adecuada a viajeros internacionales (turistas). Recordar que en caso de inmigrantes o personas que han viajado a zonas endémicas la hematuria, aun siendo un síntoma generalmente muy inespecífico, puede ser indicativo de que estamos frente a una infección por este parásito. Sería necesario también aumentar la vigilancia y fomentar los estudios sobre la presencia de los posibles de hospedadores intermediarios en nuestro país. Queremos finalizar citando a Jean-Marie Doby, quien ya en 1966 pronosticó que existía riesgo de que apareciesen casos de esquistosomiasis urinaria en Córcega. Doby se adelantó casi medio siglo a los acontecimientos, e hizo su predicción en base a la abundancia de potenciales hospedadores intermediarios B. truncatus que observó en la isla, y al aumento que se estaba produciendo de mano de obra procedente de África62.















