Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos Españoles de Urología (Ed. impresa)
versión impresa ISSN 0004-0614
Arch. Esp. Urol. vol.60 no.1 ene./feb. 2007
UROLOGÍA ONCOLÓGICA
Terapia endovesical: influencia sobre la progresión en el cáncer vesical superficial
Intravesical therapy: influence on superficial bladder cancer progresion
Jorge García Rodríguez, Jesús María Fernández Gómez, Safwan Escaf Barmadah, Miguel Álvarez Múgica,
Laura Rodríguez Robles, José Luís Martín Benito, Alfonso San Martín Blanco y Javier Regadera Sejas
Servicio de Urología I. Hospital Central de Asturias. Oviedo. Asturias. España.
Dirección para correspondencia
RESUMEN
Objetivo: Revisar la influencia de distintos tratamientos endovesicales sobre la progresión del cáncer vesical superficial.
Métodos: Se revisaron retrospectivamente un total de 473 neoplasias vesicales superficiales. A partir del diagnóstico y la RTU vesical, y en función del resultado anatomopatológico, se plantearon distintos esquemas de seguimiento y tratamiento complementario, se empleó BCG en 139 casos y quimioterapia endovesical en 80 pacientes fundamentalmente Mitomicina C (MMC).
Resultado: Globalmente, el empleo o no de instilaciones vesicales no mostró diferencias estadísticamente significativas en cuanto al tiempo de progresión Resultó factor independiente para explicar un menor tiempo libre hasta la progresión el empleo de terapia endovesical con terapia de mantenimiento frente a inducción.
Conclusiones: La utilización de terapia endovesical de mantenimiento con BCG implicó una progresión más tardía del cáncer vesical superficial, por lo que parece el tratamiento más eficaz, sobretodo en tumores de moderado y alto riesgo.
Palabras clave: Cáncer vesical superficial. Progresión. Tratamiento endovesical.
SUMMARY
Objectives: To review the influence of various intravesical treatments on superficial bladder cancer progression.
Methods: We retrospectively reviewed 473 superficial bladder neoplasias. Based on diagnosis and transurethral resection of bladder tumor (TUR BT), and depending on pathology, we proposed different treatment and follow-up schemes, with BCG in 139 cases and intravesical chemotherapy, mainly Mytomicin C, in 80.
Results: Overall, the use or not of bladder instillations did not show statistically significant differences in time to progression. The use of intravesical therapy and maintenance therapy was an independent risk factor for disease-free time to progression when compared with induction.
Conclusions: The use of maintenance intravesical therapy with BCG resulted in a delayed progression of superficial bladder cancer, so that it seems the most effective treatment, mainly in moderate-high risk tumors.
Key words: Superficial bladder cancer. Progression. Intravesical treatment.
Introducción
El factor pronóstico principal del carcinoma transicional de vejiga es la profundidad de la neoplasia en la pared vesical. Así, la supervivencia de tumores que no invaden el músculo oscila entre un 75 y un 90 % a los 5 años, respecto a un 20 a 50% en los invasores.
Pocos estudios analizan el papel del tratamiento endovesical en el control de la progresión de la enfermedad. Queremos valorar la influencia del tipo de tratamiento, dosis y duración y determinar cual es la mejor opción a la hora de prevenir la progresión en el cáncer vesical superficial.
Material y métodos
Se revisaron retrospectivamente un total de 473 neoplasias vesicales superficiales, de las cuales finalmente 419 fueron útiles para el estudio pues disponían de todos los datos que se querían analizar.
A partir del diagnóstico y la RTU vesical, y en función del resultado anatomopatológico, se plantearon distintos esquemas de seguimiento y tratamiento complementario. En 219 casos (52,3%) se empleó un tratamiento endovesical tras la RTU del tumor vesical. La inmunoterapia con BCG (La cepa de BCG que utilizamos fue la Connaught), representó un 63,5% (n: 139) de todos los tratamientos (empleada en el 33,2% del total de pacientes), utilizando alta dosis (81 mg) en 87 casos y dosis más bajas en 52 casos. Se empleó quimioterapia endovesical en 80 pacientes (19,1% del total), lo cual representa un 36,5% de las terapias endovesicales, siendo fundamentalmente Mitomicina C (MMC) (n: 53). Se emplearon regímenes de mantenimiento (más de 6 instilaciones) en 140 casos, tanto inmuno (65,5% de los tratados con BCG) como quimioterapia (61,3 de los tratados con quimioterapia), lo cual supone globalmente un 63,9% de los pacientes que recibieron tratamiento endovesical postRTU (Tabla I).
Nos basaremos en la clasificación de grupos de riesgo de la Asociación Europea de Urología (EAU), para evaluar los tratamientos (1) (Tabla II).
El análisis estadístico se realizó mediante el programa SPSS, versión 11. Se consideró la existencia de significación estadística cuando la p fue menor de 0,05.
Resultados
Globalmente, el empleo o no de instilaciones vesicales no mostró diferencias estadísticamente significativas (p: 0,0614) en cuanto al tiempo de progresión. Tampoco encontramos diferencias significativas en el tiempo hasta la progresión (p: 0,1614) cuando analizamos las diferentes dosis de BCG y quimioterapia endovesical. Se observó en las curvas de supervivencia que el grupo sin tratamiento presentaba mayor tiempo hasta la progresión. Sin embargo, hay que tener en cuenta que otros factores están influyendo en estas curvas, pues estos pacientes que no reciben tratamiento post RTU tienen mayoritariamente tumores de bajo grado, frente a los que reciben terapia endovesical, que presentan neoplasias de medio o alto grado.
Al estudiar la duración del tratamiento endovesical, se demostró que existían diferencias estadísticamente significativas en el tiempo hasta la progresión (p: 0,046) al comparar tratamientos de inducción (6 lavados semanales) frente a mantenimiento (más de 6 lavados). La terapia de mantenimiento demostró un mayor tiempo hasta la progresión frente al de inducción. La primera mostró un tiempo hasta la progresión similar a la de los pacientes que no habían recibido tratamiento endovesical, que, como se dijo antes, corresponden, en general, a casos de tumores de bajo grado (Figura 1).
Habiendo mostrado diferencias significativas en el estudio univariante de supervivencia (log-rank) y para conocer la influencia de esta variable de forma independiente en el tiempo hasta la progresión, empleamos el modelo de riesgo proporcional de Cox mediante el procedimiento por pasos hacia delante (Wald), incluyendo como covariante de estudio la variable tipo de tratamiento (inducción vs mantenimiento vs nada). Así finalmente, resultó factor independientes para explicar un menor tiempo libre hasta la progresión el empleo de terapia endovesical con terapia de mantenimiento con BCG frente a inducción.
Discusión
La progresión del cáncer vesical superficial, es un factor pronóstico muy importante en cuanto a la supervivencia del paciente. Un claro ejemplo de la actitud agresiva que debemos tomar ante la posibilidad de progresión se refleja en el estudio realizado por Solsona sobre 191 pacientes con cáncer vesical superficial de alto riesgo en los cuales la respuesta clínica al tratamiento endovesical a los tres meses puede ser el factor determinante para tomar una decisión sobre practicar a estos pacientes una cistectomía radical temprana (2).
Los esfuerzos en el tratamiento de esta enfermedad, y sobretodo en los tumores de alto riesgo se han encaminado por tanto hacia buscar la disminución en las tasas de progresión. (3-5). Un estudio del National Bladder Cancer Collaborative Group sobre 249 pacientes Ta y T1 tratados únicamente mediante resección transuretral, nos dice que las tasas de progresión para Ta, T1 y para Grado 1 y 2, y grado 3 son de un 4, 30, 2 ,11 y 45%, respectivamente (6). Mediante la utilización de tratamientos endovesicales adyuvantes intentamos disminuir esta tasa de progresión como se demuestra en el metaanálisis realizado sobre 4.863 pacientes comparando la RTU sola, RTU con tratamiento complementario con BCG y RTU con otros tratamientos distintos de BCG. En este estudio se concluye que la terapia con BCG reduce significativamente el riesgo de progresión después de RTU en pacientes con carcinoma superficial vesical que reciben terapia de mantenimiento, sobre todo en pacientes con riesgo intermedio y alto y aquellos con Cis asociado, traduciéndose en una disminución del 27% en las tasas de progresión (7).
Los tratamientos endovesicales adyuvantes tras la RTU juegan, así un papel fundamental en este sentido reduciendo el riesgo de progresión. (8,9) Shahin y cols sobre 153 pacientes diagnosticados de T1G3 objetivan progresiones en el 33% de pacientes tratados con RTU mas terapia con BCG, frente a un 36% de progresión en pacientes tratados mediante RTU solamente (10). Otro autor, Gunlusoy, publica una tasa de progresión aún mas baja, del 21,7% en T1G3 tratados con BCG. (11) En nuestro estudio no encontramos diferencias estadísticamente significativas en cuanto al tiempo de progresión con el empleo o no de instilaciones vesicales y tampoco cuando analizamos las diferentes dosis de BCG y quimioterapia endovesical, salvo cuando empleamos BCG a largo plazo (mantenimiento), al igual que otro autor, Shelley, que no encuentra diferencias en la progresión de la enfermedad o en la supervivencia utilizando BCG o MMC (12).
Respecto al tipo de terapia, varios estudios comparan la eficacia en cuanto a recidiva y progresión de los tratamientos con BCG frente a MMC (13-16).
Un metaanálisis de Bohle y cols. (17) muestra una superioridad estadísticamente significativa a favor de la BCG con terapia de mantenimiento para la prevención de la progresión frente a la MMC. Estos autores obtienen las mismas conclusiones respecto a recurrencia fundamentalmente, al comparar BCG mantenimiento frente a MMC (18). Lamm evaluando las distintas terapias con BCG y MMC, habla de que la quimioterapia podría ser apropiada para pacientes que tienen muy bajo riesgo de progresión tumoral y para pacientes que no hubieran respondido a la terapia con BCG. (19).
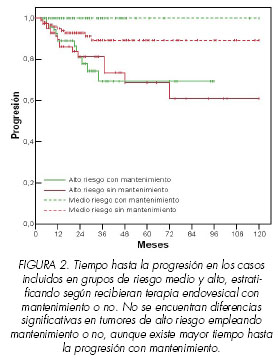
Un estudio de Peyromaure recientemente publicado, analiza 74 pacientes tratados por T1 G3, de estos, 57 son tratados mediante RTU y terapia adyuvante con BCG en régimen de mantenimiento, 10 mediante RTU y MMC y 7 pacientes mediante RTU solamente. Demuestran que en los pacientes del primer grupo la tasa de progresión fue del 23%, significativamente inferior al resto de los grupos (20). Estos resultados coinciden con la mayoría de los trabajos publicados, como la revisión de Lamm donde objetiva una mejoría de la supervivencia a los 4 años del 86% con inducción frente al 92% con mantenimiento (21) o como en el meta-análisis, ya comentado, que se realizó sobre 4863 pacientes comparando la RTU sola, RTU con tratamiento complementario con BCG y RTU con otros tratamientos distintos de BCG. Se concluyó en este estudio, que la terapia con BCG reduce significativamente el riesgo de progresión después de RTU en pacientes con carcinoma superficial vesical que reciben terapia de mantenimiento, sobretodo en pacientes con riesgo intermedio y alto y aquellos con Cis asociado, traduciéndose en una disminución del 27% en las tasas de progresión (7). Nuestros resultados coinciden en estos términos con los publicados, demostrando diferencias estadísticamente significativas en el tiempo hasta la progresión al comparar tratamientos de inducción con BCG (6 lavados semanales) frente a mantenimiento (más de 6 lavados), con un claro beneficio a favor de la terapia de mantenimiento en demostrar un mayor tiempo hasta la progresión, fundamentalmente en grupos de pacientes de moderado y alto riesgo, incluyendo a los pacientes con Cis (Figura 2). En pacientes con bajo riesgo, TaG1, no objetivamos progresión en nuestra serie, por lo que se podría obviar el tratamiento adyuvante. Andius a este respecto determina que la terapia de mantenimiento puede no ser necesaria en estos casos, añadiendo que, con una primera cistoscopia negativa la tasa de progresión es baja, aunque si observa que los pacientes tratados con menos de 6 instilaciones presentan un incremento en el riesgo de progresión (22). Respecto al Tis, se llega a las mismas conclusiones en otro meta-análisis que compara tratamiento con BCG frente a MMC y otros quimioterápicos en 700 pacientes con carcinoma in situ vesical donde la terapia con BCG se considera el tratamiento intravesical de elección en pacientes con Cis. (23).
Conclusiones
1. Globalmente no encontramos diferencias estadísticamente significativas en cuanto al tiempo hasta la progresión con el empleo o no de instilaciones vesicales y tampoco cuando analizamos las diferentes dosis de BCG y quimioterapia endovesical.
2. No obstante la utilización de terapia endovesical de mantenimiento con BCG si implicó una progresión más tardía del cáncer vesical superficial, por lo que parece el tratamiento mas eficaz, sobretodo en tumores de moderado y alto riesgo.
Bibliografía y lecturas recomendadas (*lectura de interés y ** lectura fundamental)
1. OOSTERLINCK, W.; LOBEL, B.; JAKSE, G. y cols.: Guidelines on bladder cancer. Eur. Urol.;41:105. 2002. [ Links ]
2. SOLSONA, E.; IBORRA, I.; DUMONT, R. y cols:. The 3-month clinical response to intravesical therapy as a predictive factor for progression in patients with high risk superficial bladder cancer. J. Urol.;164:685, 2000. [ Links ]
3. HERR, H.W.; BADALAMENT, R.A.; AMATO, D.A. y cols: Superficial bladder cancer treated with bacillus Calmette-Guerin: a multivariate analysis of factors affecting tumor progression. J. Urol. ;141:22,1989. [ Links ]
4. ARRIZABALAGA MORENO, M.; GARCIA GONZALEZ, J.I.; ESTEBAN ARTIAGA, R. y cols:. Progression and prognosis of in situ carcinoma of the bladder treated with BCG. Actas Urol. Esp.;23:670, 1999. [ Links ]
5. PATARD, J.; MOUDOUNI, S.; SAINT, F. y cols. Tumor progression and survival in patients with T1G3 bladder tumors: multicentric retrospective study comparing 94 patients treated during 17 years. Urology.;58:551, 2001. [ Links ]
6. HENEY, N.M.; AHMED, S.; FLANAGAN, M.J. y cols.: Superficial bladder cancer: progression and recurrence. J. Urol.;130:1083, 1983. [ Links ]
**7. SYLVESTER, R.J.; VAN DER MEIJDEN, A.P.; LAMM D.L.: Intravesical bacillus Calmette-Guerin reduces the risk of progression in patients with superficial bladder cancer: a meta-analysis of the published results of randomized clinical trials. J. Urol.; 168:1964, 2002. [ Links ]
*8. DAVIS. J.W.; SHETH, .SI.; DOVIAK, M.J. y cols: Superficial bladder carcinoma treated with bacillus Calmette-Guerin: progression-free and disease specific survival with minimum 10-yearfollowup. J. Urol. ;167:494, 2002. [ Links ]
**9. BOHLE, A.: Intravesical bacillus Calmette-Guerin reduces the risk of progression in patients with superficial bladder cancer: a meta-analysis of the published results of randomized clinical trials. Int. Braz. J. Urol.;28:585, 2002. [ Links ]
10. SHAHIN, O.; THALMANN, G.N.; RENTSCH, C. y cols.: A retrospective analysis of 153 patients treated with or without intravesical bacillus Calmette-Guerin for primary stage T1 grade 3 bladder cancer: recurrence, progression and survival. J. Urol.;169:96, 2003. [ Links ]
11. GUNLUSOY, B.; DEGIRMENCI, T.; ARSLAN, M. Y cols.: Recurrence and progression of T1G3 transitional cell carcinoma of the bladder treated with intravesical bacillus Calmette-Guerin. Urol. Int.;75:107, 2005. [ Links ]
*12. SHELLEY, M.D.; WILT, T.J.; COURT, J. y cols.: Intravesical bacillus Calmette-Guerin is superior to mitomycin C in reducing tumour recurrence in high-risk superficial bladder cancer: a meta-analysis of randomized trials. BJU Int.;93:485, 2004. [ Links ]
13. WITJES, J.A.; MEIJDEN, A.P.; COLLETTE, L. y cols.: Long-term follow-up of an EORTC randomized prospective trial comparing intravesical bacille Calmette-Guerin-RIVM and mitomycin C in superficial bladder cancer. EORTC GU Group and the Dutch South East Cooperative Urological Group. European Organisation for Research and Treatment of Cancer Genito-Urinary Tract Cancer Collaborative Group. Urology.;52:403, 1998. [ Links ]
14. HUNCHAREK, M.; KUPELNICK, B.: The influence of intravesical therapy on progression of superficial transitional cell carcinoma of the bladder: a meta-analytic comparison of chemotherapy versus bacilli Calmette-Guerin immunotherapy. Am. J. Clin. Oncol.;27:522, 2004. [ Links ]
15. MORALES, A.: Results of a randomized phase III trial of sequential intravesical therapy with mitomycin C and bacillus Calmette-Guerin versus mitomycin C alone in patients with superficial bladder cancer. J. Urol.;161:1582,1999. [ Links ]
16. MONTIE, J.E.: The influence of intravesical therapy on progression of superficial transitional cell carcinoma of the bladder. A meta-analytic comparison of chemotherapy versus bacilli Calmette-Guerin immunotherapy. J. Urol.;174:1783, 2005. [ Links ]
*17. BOHLE, A.; BOCK, P.R.: Intravesical bacille Calmette-Guerin versus mitomycin C in superficial bladder cancer: formal meta-analysis of comparative studies on tumor progression. Urology; 63:682, 2004. [ Links ]
**18. BOHLE, A.; JOCHAM, D.; BOCK, P.R.: Intravesical bacillus Calmette-Guerin versus mitomycin C for superficial bladder cancer: a formal meta-analysis of comparative studies on recurrence and toxicity. J. Urol.;169:90. 2003. [ Links ]
19. LAMM, D.L.: Clinical evaluation of immunotherapy: are there differences between papillary and flat in situ bladder cancer. Cancer Surv.;31:99, 1998. [ Links ]
20. PEYROMAURE, M.; ZERBIB, M.: T1G3 transitional cell carcinoma of the bladder: recurrence, progression and survival. BJU Int; 93:60, 2004. [ Links ]
*21. LAMM, D.L.: Preventing progression and improving survival with BCG maintenance. Eur. Urol.;37:9, 2000. [ Links ]
*22. ANDIUS, P.; HOLMANG, S.: Bacillus Calmette-Guerin therapy in stage Ta/T1 bladder cancer: prognostic factors for time to recurrence and progression. BJU Int.;93:980, 2004. [ Links ]
23. SYLVESTER, R.J.; VAN DER MEIJDEN, A.P.; WITJES, J.A. Y cols.: Bacillus calmette-guerin versus chemotherapy for the intravesical treatment of patients with carcinoma in situ of the bladder: a meta-analysis of the published results of randomized clinical trials. J. Urol.;174:86, 2005. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Jorge García Rodríguez
Martínez Vigil, 2 - 2º dcha
33010 Oviedo. (España)
jgrmed@hotmail.com
Trabajo recibido: 18 de junio 2006