Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Actas Urológicas Españolas
versión impresa ISSN 0210-4806
Actas Urol Esp vol.34 no.5 may. 2010
Incidencias y complicaciones en nuestras primeras 250 prostatéctomias radicales robóticas
Complications and incidences in our first 250 robotic radical prostatectomies
J.G. Pereira Arias, M. Gamarra Quintanilla, A. Leibar Tamayo, A. Astobieta Odriozola y G. Ibarluzea González
Servicio de Urología, Urología Clínica, S. L., Bilbao, España
Dirección para correspondencia
RESUMEN
Objetivo: El objetivo del estudio es revisar la incidencia y analizar los factores que puedan contribuir a las complicaciones perioperatorias en los pacientes a los que se realiza una prostatectomía radical robótica basados en nuestra experiencia sobre 250 procedimientos.
Material y métodos: Realizamos un estudio retrospectivo, descriptivo y analítico sobre 250 pacientes consecutivos a los que realizamos prostatectomía radical robótica durante un periodo de 3 años y 2 meses (enero 06-marzo 09). Se registran datos demográficos como: edad, PSA y grado de Gleason preoperatorio y volumen prostático. Todas las intervenciones fueron realizadas por tres cirujanos. Realizamos un abordaje laparoscópico transperitoneal con sistema robótico daVinci de 4 brazos. Empleamos un soporte informático Microsoft Excel. Los parámetros quirúrgicos recogidos son: tiempo de instalación, tiempo de consola, volumen de hemorragia, tasa de transfusión, estancia media y tiempo de sondaje uretral. Revisamos las incidencias y complicaciones intraoperatorias y postoperatorias precoces y tardías en esta serie de pacientes.
Resultados: Los datos demográficos de la serie fueron: edad media de 61,15 años (47-74), PSA medio preoperatorio de 8,18ng/ml (2,6-34ng/ml), Gleason preoperatorio de 6,8 (2-9) y volumen prostático de 34,9cc (12-124cc). Los parámetros quirúrgicos recogidos son: tiempo de instalación: 10,2min (6-47min), tiempo de consola 125min (90-315min), hemorragia media de 150ml (50-1150ml) con una tasa de transfusión del 3,6% (9/250). No se registró mortalidad perioperatoria, ni fue preciso realizar ninguna reconversión a cirugía abierta o laparoscópica en los 250 procedimientos. Un total del 96% pacientes (240/250) tuvieron un curso postoperatorio adecuado sin incidencias reseñables con una estancia media de 4,2 días (3-35 días) y retirada de sonda vesical a los 8 días (5-28días). La tasa global de complicaciones es del 10,4% con solo 3,2% de complicaciones mayores (8/250): 5 complicaciones quirúrgicas y 3 médicas. La tasa de reintervención del 1,6% (4/250): una peritonitis tardía por perforación cecal, 1 hemorragia por lesión de arteria epigástrica, 1 drenaje perineal percutáneo de hematoma retrovescial y una revisión por urinoma tras desalojo accidental de sonda vesical. Un paciente preciso embolización arterial selectiva por hematuria tardía persistente tras fistula de arteria vesical superior. Entre las complicaciones médicas: 1 caso de fracaso renal agudo por púrpura trombótica trombocitopénica resuelto mediante hemodiálisis, y 2 embolias pulmonares tardía resueltas mediante anticoagulación. Se registraron 4 fallos del sistema robótico (1,6%) sin implicación ni necesidad de reconversión quirúrgica. Entre las complicaciones tardías que precisaron alguna maniobra quirúrgica para su resolución destacan: una reparación de hernia umbilical, una meatotomía por estenosis de meato uretral, una incisión endoscópica de esclerosis de anastomosis y una extracción endoscópica de clip vascular metálico y Hem-o-lock tras erosión-migración vesical.
Conclusiones: La prostatectomía radical robótica es una técnica segura y reproducible con óptimos resultados oncológicos y funcionales, con curva de aprendizaje más corta, con excelente ergonomía y visión para el cirujano y con una incidencia de complicaciones comparable e incluso favorable a las series de cirugía abierta y laparoscópica. Las complicaciones se reducen con la curva de aprendizaje sin olvidar que es la experiencia del equipo quirúrgico el factor clave para conseguir mejores resultados.
Palabras clave: Prostatectomía radical robótica. Complicaciones. Incidencia.
ABSTRACT
Objective: To review the incidence of and analyze the factors contributing to perioperative complications in patients undergoing robotic radical prostatectomy in our experience of 250 procedures.
Materials y methods: An analytical, descriptive, retrospective study was conducted of 250 consecutive patients who underwent robotic radical prostatectomy during a period of three years and two months (January 06-March 09). Data recorded included age, preoperative Gleason grade and PSA, and prostate volume. All procedures were performed by three surgeons through a transperitoneal approach using a four-arm daVinci robotic system. Microsoft Excel support was used. Surgical variables recorded included setup time, console operation time, mean bleeding, transfusion rate, hospital stay, and urethral catheterization time. Incidences and intraoperative and postoperative late and early complications in these patients were reviewed.
Results: Demographic data recorded included: mean age, 61.5 years (47-74); mean preoperative PSA, 8.18ng/mL (2.6-34ng/mL); mean Gleason grade, 6.8 (2-9); and mean prostate volume 34.9mL (12-124). Surgical variables recorded included: console setup time, 10.8min (6-47): console operation time, 125min (90-315); mean bleeding, 150mL (50-1150); and a 3.6% (9/250) transfusion rate. There was no peroperative mortality, and no conversion to open or laparoscopic surgery was required. Ninety-six percent of patients (240/250) had an adequate postoperative course, with a mean hospital stay of 4.2 days (3-35) and urinary catheter removal after 8 (5-28) days. Overall complication rate was 10.6%, with major complications occurring in only 3.2% of patients (8/250) and consisting of five surgical and three medical complications. Repeat surgery was required in 1.6% of cases (4/250) due to late peritonitis for cecal perforation, bleeding from epigastric artery, perineal percutaneous drainage of retrovesical hematoma, and pelvic urinoma after bladder catheter dislodgment. One patient required selective arterial embolization for persistent hematuria due to vesical artery fistula. Medical complications included acute renal failure due to thrombotic purpura resolved with hemodialysis in one patient and late pulmonary embolism managed with anticoagulation in two patients. Robot malfunction with no surgical implications or need for surgical conversion occurred in four patients (1.6%). Surgical maneuvers required to resolve late complications included one umbilical hernia repair, one meatotomy for meatal stenosis, one bladder neck endoscopic incision after contracture, and one endoscopic extraction of Hem-o-lok and vascular clip following erosion-migration into the bladder.
Conclusions: Robotic radical prostatectomy is a safe and reproducible procedure with optimal functional and oncological results, a shorter learning curve, greater comfort and vision for surgeons, and a complication rate similar to and even better than reported for open and laparoscopic surgery series. Complications decrease with the learning curve, but surgical team experience continues to be the key factor to achieve better results.
Key words: Robotic radical prostatectomy. Surgical complications. Incidence.
Introducción
Durante las últimas décadas hemos asistido a una evolución en el tratamiento quirúrgico del cáncer prostático organoconfinado. Los principios o pilares sobre los que se han ido produciendo los cambios en esta técnica quirúrgica caminan de la mano de la evolución tecnológica y del mejor conocimiento anatómico. Así, en 1982 Walsh y Donker nos ilustran el camino sobre la preservación nerviosa al identificar las bandeletas neurovasculares responsables de la conservación de la función eréctil. A finales de los 90, grupos europeos nos anuncian un cambio en el abordaje iniciándonos en la laparoscopia. Procedimiento que precisando un aprendizaje laborioso, nos aporta ventajas para el paciente propias de una cirugía mínimamente invasiva1. La introducción de la robótica en el 2001, añade una nueva dimensión a la cirugía mínimamente invasiva dotando al cirujano de unas ventajas en ergonomía, manipulación y visión que permiten acortar la curva de aprendizaje y mejorar los resultados oncológicos y funcionales de la prostatectomía radical2,3.
Nuestra unidad comienza su singladura en cirugía robótica el 26 de enero de 2006, siendo el segundo centro del estado tras la Fundación Puigvert (julio de 2005). El objetivo de este estudio ha sido recoger las incidencias y complicaciones de las primeras 250 prostatectomías radicales robóticas consecutivas realizadas, así como las reflexiones generadas al respecto.
Material y métodos
En un período de 3 años y 2 meses (enero 2006-marzo 2009) se han realizado 250 prostatectomías radicales robóticas (PRR). Las intervenciones han sido realizadas por tres cirujanos, con experiencia laparoscópica previa variable, donde se han añadido sus respectivas curvas de aprendizaje con transito de asistente a consola en los primeros 20 casos respectivamente. El equipo de anestesia y enfermería ha sido el mismo en este trienio. La unidad es abierta habiendo recibido pacientes de diferentes áreas geográficas del estado.
Se realiza un estudio retrospectivo descriptivo y analítico empleando un soporte informático Mirosoft Excel en el periodo referido. Se recogen datos demográficos como: edad, antecedentes quirúrgicos previos, niveles de PSA y grado de Gleason preoperatorio, estadio y volumen prostático. Respecto a la técnica quirúrgica, empleamos un abordaje laparoscópico transperitoneal con sistema robótico daVinci de 4 brazos y 2 trocares accesorios para el ayudante en fosa ilíaca derecha. Realizamos un acceso atérmico anterógrado, interfascial con preservación neurovascular (cuando está indicado) y de fascia endopélvica, sección y posterior sutura individualizada del complejo venoso dorsal, anastomosis continua modificada de Van Velthoven. Suspensión pubovesical anterior en casos seleccionados y linfadenectomía iliobtruratriz en casos indicados (9,54% [21/250] linfadenectomías en nuestra serie). Extracción de la pieza embolsada por la cicatriz umbilical de trocar óptico, drenaje Jaksson-Prat 24-48h por trocar de 12mm de fosa iliaca derecha. Realizamos profilaxis antibiótica y antitrombótica. Se retira la sonda y agrafes de heridas abdominales a los 7-10 días de intervención4.
Recogemos los datos de incidencias y complicaciones intraoperatorias y postoperatorias precoces y tardías. Se define como evolución adecuada el paciente que no precisa maniobra terapéutica alguna en postoperatorio inmediato y no presenta complicaciones relevantes al alta. De igual modo, se reflejan las incidencias tardías (>3 meses) menores. Este último dato, no siempre está disponible (por ej. infecciones urinarias, estenosis uretrales o de meato, ) por tratarse de una unidad abierta con pacientes de áreas geográficas distantes y seguimiento inferior al año en algunos casos. Las complicaciones las definimos de acuerdo a los criterios de Clavien et al con las modificaciones recientes de Dindo et al5,6. De modo y manera que una complicación grado I sería aquella que no amenaza la vida del paciente y que puede requerir cuidados farmacológicos. Grado II complicación menor que puede requerir cuidados médicos (por ej: transfusión de sangre, hiperalimentación, sonda nasogástrica o cateterismo uretral, ) y pudiese suponer amenaza pero sin secuelas. grado III complicación que supone amenaza vital y puede generar secuelas. Precisa actuación quirúrgica abierta, endoscópica o radiointervencionista. Según requiera anestesia general o no sería tipo IIIa (si no precisa anestesia) y tipo IIIb si la precisa. Grado IV complicación que amenaza la vida y precisa cuidados intensivos. Grado V complicaciones que causan fallecimiento.
Resultados
Los datos demográficos recogidos en el estudio son similares a los de otras series de cirugía radical prostática. Son pacientes con edad media de 61,15 años (47-74), con PSA medio preoperatorio de 8,18 ng/ml (2,6-34ng/ml), Gleason preoperatorio medio de 6,8 y volumen prostático de 34,9cc (12-124cc). Estadio clínico T1c 88,4% (221/25o), T2 9,6% (24/250) y T1b 2%(5/250). Entre los antecedentes de tratamientos quirúrgicos y no quirúrgicos prostáticos destacan: 13 resecciones transuretrales prostáticas previas 5,2% (13/250), 2 recidivas locales de crioterapia prostática previa y un fracaso de radioterapia. El 28,4% (71/250) de los pacientes tenía antecedentes de algún tipo de cirugía abdominal previa. Así se registran 23 apendicectomías, 29 herniorrafias inguinales, 6 cirugías sobre hernia hiatal, 10 colecistectomías, 2 nefrectomías radicales y un hemicolectomía izquierda.
Los parámetros quirúrgicos registrados en estas 250 cirugías robóticas son: tiempo de instalación del robot: 10,2min (5-47min), tiempo medio de consola 125min (90-315min), hemorragia media de 125ml (50-1150ml) con una tasa de transfusión postoperatoria del 3,6% (9/250). No se realizaron transfusiones intraoperatorioas. La estancia media hospitalaria fue de 4,2 días (3-35 días) y la retirada de sonda vesical a los 8 días (5-28días).
Las complicaciones se clasifican en intraoperatorios (anestésicas y quirúrgicas), postoperatorias precoces y tardías (médicas y quirúrgicas) y se subclasifican por el tipo y grado de las mismas (intestinales, urológicas, vasculares, neurológicas y grado Clavien I al V). Un total del 96% pacientes (240/250) tuvieron un curso postoperatorio adecuado sin incidencias reseñables. La tasa global de complicaciones es del 10,6% con solo 3,2% de complicaciones mayores (8/250): 5 complicaciones quirúrgicas y 3 médicas. La tasa de reintervención fue del 1,6% (4/250). En la tabla 1 se reflejan las complicaciones, tipo, grado y manejo en nuestra serie de 250 PRR.
Complicaciones intraoperatorias
Se registran 2 complicaciones anestésicas 0,8% (2/250): una dificultad de intubación en paciente con severa espondilitis anquilosante que preciso asistencia de broncoscopio para la misma. Otro paciente presentó una bradicardia y parada cardiaca al finalizar la intervención durante la correción de la posición de Trendelemburg. Se resolvió favorablemente con reanimación y sin secuelas.
Entre las complicaciones quirúrgicas destacan 2 lesiones vesicales 0,8% (2/250) diagnosticadas al finalizar la anastomosis y comprobar la estanqueidad de la misma apreciándose fuga en cara posterolateral izquierda vesical resueltas intraoperatoriamente mediante cistorrafia y sin secuelas posteriores.
Complicaciones postoperatorias
Urinarias: pueden ser precoces o tardías (> 3 meses). Entre las incidencias y complicaciones urinarias precoces tenemos:
• Retención urinaria en 3 casos (3/250) 1,2%: uno de los casos la retención fue secundaria a hematuria con coagulos que precisó sondaje y lavado vesical, en otro paciente se retiró la sonda de manera involuntaria y precoz al 4.o día; y un 3.o tenía como antecedente la reconstrucción de un cuello vesical amplio. Todos fueron resueltos manteniendo sonda vesical 7-10 días adicionales.
• Hematuria importante en 2 casos (2/250) 0,8%: uno de los casos descrito con antelación y que precisó drenaje vesical; y otro paciente con hematuria anemizante severa que merece mención especial. Este segundo caso (n.o189 de la serie) se trata de un paciente hemofílico. Se realizó la intervención sin incidencias bajo tratamiento con factor VIII de coagulación correspondiente. El postoperatorio fue adecuado y en 4 días recibió el alta sin presentar hematuria. En una semana acudió a otro centro hospitalario por hematuria severa obstructiva y anemizante rebelde a drenaje vesical, restauración de factor VIII de coagulación y transfusión de hemoderivados. Se realizó un TAC abdominopélvico que constató la presencia de un tránsito de contraste en pared lateral izquierda vesical desde ramas arteriales a vejiga (figura 1). Ante la sospecha de fistula arteriovesical y sangrado activo se realizó arteriografía objetivándose una fístula de arteria vesical superior izquierda, procediéndose a su embolización exitosa con coils metálicos (figura 2 y figura 3).

Figura 1. TAC abdominopélvico: hemorragia activa de arteria
vesical superior izquierda a vejiga (cortesía Dra.M.E Díez Razquin).

Figura 2. Arteriografía de arteria iliaca izquierda: sangrado activo
de rama vesical superior izquierda (cortesía Dra.M.E Díez Razquin).
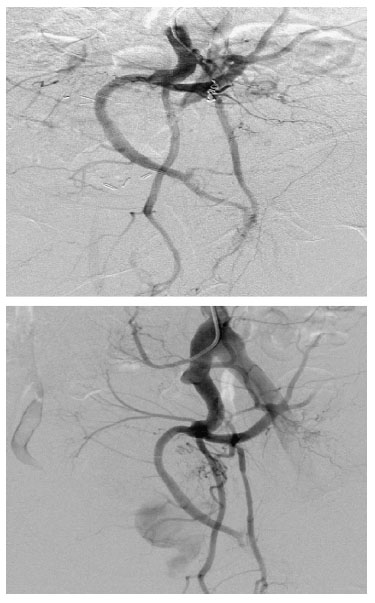
Figura 3. Embolización supraselectiva con coils metálicos de rama
vesical izquierda y control hemorragia (cortesía Dra.M.E Díez Razquin).
• Fístula urinaria (2/250) 0,8%: en uno de los casos se realizó tratamiento conservador manteniendo la sonda uretral y el drenaje durante 18 días y comprobando mediante cistografía la resolución el mismo. En otro paciente (caso n.o 78) la fístula fue secundaria a una tracción y desalojo accidental de la sonda en el postoperaorio precoz lo que ante la imposibilidad de cateterismo condicionó la laparotomía y revisión quirúrgica de la misma con buena evolución posterior.
Entre las complicaciones urinarias tardías destacan las siguientes:
• Estenosis anastomótica: un caso (0,4%) se realizó incisión endoscópica transuretral sin comprometer la continencia y con buena evolución miccional posterior.
• Estenosis de meato: 2 casos (0,8%): manejados conservadoramente mediante dilataciones y meatotomía respectivamente.
• Erosión-migración de clip vascular y Hem-o-lock: un caso (0,4%): se trata de un paciente que a los 9 meses de la PRR, y con adecuada continencia urinaria, refiere un síndrome disúrico terminal, objetivándose en estudio ecográfico vesical, la presencia de una calcificación fija en retrotrígono. Se realizó exploración endoscópica constatando la presencia de un clip metálico y un Hem-o-lok erosionando la superficie vesical a nivel retromeático izquierdo con calcificación grosera en superficie. Se procedió a su resección y extracción sin incidencias posteriores (figura 4).

Figura 4. Cistoscopia: clip metálico de 5mm y Hem-o-lok erosionando
la superficie vesical a nivel retromeático izquierdo con calcificación grosera en superficie.
• Micción espontánea del clip Lapra-Ty: 2 casos (0,8%) sin secuelas relevantes. Clip Lapra-Ty (Ethicon) que empleamos como refuerzo en el extremo de anudado de las 2 suturas de Caprosin 3,0 para la anastomosis uretrovesical.
Complicaciones intestinales
• Peritonitis fecaloidea por perforación cecal en un caso (0,4%): se trata de una complicación grado IIIb de Clavien y la de mayor gravedad de la serie. Se trata de nuestro paciente n.o 23 donde como antecedente destacaba una peritonitis de origen apendicular que precisó liberación de múltiples adherencias intestinales previas al acoplamiento del robot. El postoperatorio precoz transcurrió sin hallazgos relevantes, pero a partir del tercer día comenzó con un cuadro de ligera distensión abdominal, íleo paralítico, incremento de la creatinina y elevación de los leucocitos sin síndrome febril asociado ni signos de peritonismo. El TAC abdominopélvico constató presencia de neumoperitoneo y colección líquida pélvica. Se realizó laparotomía exploradora objetivando una peritonitis fecaloidea por una perforación térmica diferida en ciego. Se realizó cecostomía y drenaje con buena evolución postoperatoria siendo dado de alta a los 28 días de la PRR.
• Ileo paralítico persistente: se registran retrasos en la función intestinal relevantes en 5 pacientes (2%) que condicionaron incremento en la estancia hospitalaria y actuaciones terapéuticas. El manejo inicial fue conservador mediante sonda nasogástrica, y etiológico cuando fue preciso. En un paciente fue suficiente la sonda nasogástrica y la dieta absoluta durante 5 días. En uno de los casos el íleoparalítico derivo de la perforación cecal comentada con antelación, en otros 3 pacientes se debió a la presencia de colecciones líquidas pélvicas: 2 urinomas y un hematoma retrovesical. Los urinomas fueron tratados: uno de ellos de forma conservadora mediante mantenimiento de drenaje y sonda; y otro precisó laparotomía ante el desalojo accidental de la sonda y la imposibilidad de su colocación transuretral, como se ha reflejado con anterioridad. El hematoma retrovescial-prerectal precisó drenaje perineal percutáneo ecoguiado.
• Hernias umbilicales en 3 pacientes (1,2%): se trata de una complicación diferida. En 2 de los casos registrados, la hernia umbilical estaba presente con antelación y fracasó el intento de cierre primario tras la extracción de la pieza. Dos pacientes aceptaron la herniorrafía posterior. No se registraron herniaciones en los puertos laterales del abdomen.
• En nuestra casuística no se presentaron perforaciones rectales (a pesar de 3 cirugías de rescate postfracaso de crioterapia y radioterapia) ni fístulas rectouretrales.
Entre las complicaciones definidas bajo el término «vasculares» agrupamos las de índole hemorrágica, embolígena o trombogénica. Así presentamos:
• Lesión arteria epigástrica en un paciente (0,4%) con trocar robótico de 8mm en pared abdominal lateral izquierda. Fue en los primeros casos, donde abandonábamos 2 drenajes, uno de ellos por ese trocar. El paciente presento un incremento súbito en el débito del drenaje hemático tras la movilización del mismo a las 24h. Ante la sospecha de hemoperitoneo, se realizó laparotomía exploradora infraumbilical, objetivando hemorragia en la arteria epigástrica izquierda y hematoma parietal, resuelto mediante sutura hemostática.
• Hematoma pélvico (retrovesical-prerectal) (0,4%). Se trata de un paciente que tras PRR refiere un intenso tenesmo rectal y dolor en zona perineal sin alteraciones hemodinámicas, ni en el hematocrito ni en el débito del drenaje. Ante la persistencia del cuadro y su rebeldía a la analgesia se comprobó en tacto rectal la protusión en la pared rectal anterior de una masa de consistencia blanda. El estudio de imagen mediante ecografía y TAC pélvico, constató la existencia de una colección líquida densa en espacio retrovesical con impronta en pared anterior del recto. Se realizó punción drenaje perineal ecoguiada con buena evolución posterior.
• Hematomas parietales (4/259) 1,6%. Se presentó en el postoperatorio precoz (48h) y en la pared abdominal lateral derecha, en un grupo de pacientes en un periodo próximo de un mes. Se resolvió mediante actitud expectante y no precisó reposición hemática.
• Púrpura tombótica trombocitopénica en un paciente sin antecedentes conocidos. Presentó insuficiencia renal en postoperatorio inmediato sin datos de pérdida hemática resuelto mediante hemodiálisis. Al parecer el estrés quirúrgico puede poner en evidencia un cuadro de estas características.
• Tromboembolismo pulmonar (2/259) 0,8%. Dos pacientes sin especial riesgo de trombosis venosa: jóvenes, no obesos, corto periodo de intervención quirúrgica, heparinización sistemática, sin pérdidas hemáticas importantes y con alta precoz. Acudieron, a los 5-6 días del alta hospitalaria, por dolor torácico bajo la sospecha de embolia pulmonar resuelto mediante anticoagulación.
• Hematuria secundaria a fístula arteriovesical en un paciente hemofílico, descrito el caso con antelación, y resuelto mediante embolización arterial supraselectiva
Entre otras complicaciones menores se registran: 6 casos de infección urinaria al retirar la sonda (4 orquiepididimitis, 2 cistitis) y una infección de herida umbilical. No se han registrado casos de neuroapraxia, ni lesión del nervio obturador, ni linfoceles sintomáticos.
Entre las malfunciones del sistema robótico se han objetivado 4 casos en nuestra casuística, lo que representan 1,6% del total. En 2 ocasiones el fallo repercutió sobre el 4o brazo robótico, no existiendo impedimento en proseguir la intervención con tres brazos. En otra ocasión, resulto ser el tercer brazo el implicado, pudiéndose concluir la intervención empleando el 4.o brazo en su lugar. En un último caso, el fallo se registró en el guante maestro del brazo robótico izquierdo, bloqueando el sistema al reproducir un movimiento concreto de rotación. Se pudo concluir la intervención sin necesidad de reconversión en ninguno de los episodios.
Discusión
Las complicaciones de la PRR comparten el mismo origen y naturaleza que las complicaciones de la laparoscopia convencional, dado que en procedimiento es de la misma índole y filosofía. Las diferentes series consultadas en la literatura arrojan tasas bajas de complicaciones globales, con baja incidencia de reconversión y reintervención. Los estudios comparativos con cirugía laparoscópica y abierta reflejan datos similares de complicaciones quizás con menor hemorragia, menor incidencia de fístulas y complicaciones intestinales y una menor estancia hospitalaria7. Nuestra revisión sobre 250 PRR refleja que el 96% de los pacientes (240/250) tuvieron un curso postoperatorio inmediato adecuado sin incidencias reseñables. La tasa global de complicaciones fue del 10,4% con solo 3,2% de complicaciones mayores (8/250): 5 complicaciones quirúrgicas y 3 médicas. La tasa de reintervención fue del 1,6% (4/250). La tasa global de complicaciones de la PRR en la literatura es variable, oscilando entre 0,3-19,4%, según se incluyan las complicaciones mayores, menores, precoces y tardías8-13. Si nos centramos en las complicaciones mayores, la incidencia registrada en la literatura varia entre 0,3-6,8% con una media del 3,5% muy similar a nuestro 3,2%8-11. De igual modo, la tasa de reconversión de la cirugía robótica a cirugía abierta o laparoscópica se refleja entorno al 0,8% (entre 0-3%), siendo en nuestra serie de 250 casos del 0%8-12. La tasa de reintervención registrada en la literatura oscila entre el 1-2%. En nuestra casuística se realizaron 4 reintervenciones (1,6%): 3 laparotomías (una por perforación cecal y peritonitis, una por hemorragia de arteria epigástrica y otra por urinoma tras desalojo accidental de catéter uretral y sospecha de dehiscencia anastomótica). Un paciente precisó drenaje percutáneo transperineal ecoguiado de hematoma retrovesical-prerectal. Se realizó un procedimiento de radiología intervencionista en un paciente con fístula arteriovesical resuelto mediante embolización supraselectiva.
A continuación, analizamos de manera pormenorizada el tipo y grado de las complicaciones presentadas en nuestra experiencia y en la literatura. Las complicaciones anestésicas de la PRR pueden derivar del Trendelemburg prolongado y extremo, de la duración de la intervención, las dificultades respiratorias previas y de las compresiones sobre estructuras nerviosas. Así se han documentado dificultades de extubación por edema traqueal persistente y cuadros de neuroapraxia braquial14. La adecuada selección del paciente, el correcto almohadillado de las zonas de decúbito, el manejo oportuno de la fluidoterapia intraoperaoria, la protección ocular y una técnica quirúrgica no prolongada evitaría la mayoría de estas incidencias. En nuestra serie no se han constatado casos de neuroapraxia, no así otros autores que describen 1,6% de incidencia con compresión braquial y ciática con recuperación espontánea8. Un paciente que precisó intubación difícil por severa espondilitis anquilosante requirió mantenimiento de varias horas de intubación en postoperatorio sin más secuelas. El caso de bradicardia y parada cardiaca al finalizar la intervención, debido al desequilibrio hemodinámico en la resolución del trendelemburg, se solventó sin secuelas y sin evidencia posterior de alteraciones cardiacas. Aconsejando un transito del trendelemburg progresivo al finalizar la intervención especialmente si ha sido prolongada o en estado de hipovolemia por hemorragia favorecido por la escasa fluidoterpia aplicada en este tipo de cirugía.
Entre las complicaciones urinarias, la incidencia no difiere de la reflejada en la literatura. Las 2 lesiones vesicales diagnosticadas y resueltas intraoperatoriamente, pueden ser debidas a un intento de ultrapreservación del cuello vesical, y en el afán de separar y conservar las fibras del cuello vesical producir una lesión de las mismas. Así llama la atención que ambas lesiones se dan en la vertiente izdquierda donde un cirujano diestro, empleando la tijera en la mano derecha, presentaría una mayor dificultad en la disección. El problema de la lesión vesical radica en que la misma no pase desapercibida para evitar un fuga urinaria posterior. Su reparación con el sistema daVinci es sencilla, empleando el 4.o brazo para desplazar y rotar la vejiga medialmente. De igual modo, puede que en algunas series no se registre este suceso al ser resuelto in situ. Así mismo, no se registra la necesidad de reconstrucción de cuellos vesicales amplios para facilitar la anastomosis, y por ello su incidencia pueda estar infravalorada. En la literatura se recoge una incidencia baja, entorno al 0,3% de lesiones vesicales, más comunes en próstatas grandes con lóbulos medios voluminosos10,11,15. De igual modo se han descrito lesiones ureterales responsables de urinoma persistente postoperatorio que precisaron ureteroneocistostomia extravescal sobre tutor ureteral11, que no se registraron en nuestra casuística. Nuestra incidencia de retención urinaria es del 1,2% (3/250) y es inferior a la reflejada en distintas series de la literatura donde oscila entre 1,6-4%8,11. Esta escasa incidencia puede ser debido a un tiempo de sonda vesical postoperatorio medio entorno a los 8 días, permitiendo facilitar la cicatrización anastomótica y la reducción del edema tisular. Las series con mayores tasas de retención urinaria se correlacionan con periodos de cateterismo uretral inferiores de 4-5 días11. De igual modo, la necesidad de realizar en ocasiones una reconstrucción mediante puntos laterales o en raqueta del cuello vesical amplio puede condicionar una cicatrización más lenta y mayor riesgo de retención ante retirada precoz de sonda, como ocurrió en uno de nuestros pacientes. De la misma forma, una sutura precisa e impermeable minimizará este riesgo. Algunos autores en la actualidad, preconizan el empleo de talla suprapúbica en lugar de sonda uretral objetivando una reducción del dolor peneano, un mejor confort para el paciente y menor riesgo de retención urinaria20-22.
La hematuria postoperatoria transitoria no es infrecuente después de la PRR, si bien es cierto que llama la atención la rapidez con la que se produce el aclarado de la orina en estos pacientes. Así que hematurias severas no son comunes y se reflejan en la literatura entorno al 0,3%11. En condiciones normales su origen asienta en el cuello vesical y en zona anastomótica. En nuestra serie fueron 2 casos (0,8%). El manejo ha de ser conservador y el drenaje vesical es suficiente para solucionarlo. No obstante, nuestro paciente hemofílico desarrollo una hematuria diferida severa producida por un sangrado activo de la arteria vesical superior izquierda finalmente resuelto mediante embolización arterial selectiva. En la literatura se han descrito hematurias diferidas por seudoaneurisma de ramas pudendas accesorias englobadas en la anastomosis, aunque son casos excepcionales, ante estos hallazgos la oportunidad de un manejo conservador mediante radiología intervencionista es una alternativa eficaz para evitar reintervenciones19.
Las fístulas anastomóticas en PRR son menos frecuentes que en las series de laparoscopia convencional. Así autores reflejan una incidencia del 13,5% en laparoscopia convencional frente a un 7,5% en robótica11. No obstante, la incidencia oscila entre 0,5-7,5% (media de 1,8%)8-11,20. La mayor precisión y facilidad en la realización de anastomosis uretrovesicales impermeables puede justificar esta baja incidencia que en nuestra serie fue del 0,8% (2/250). Su manejo ha de ser conservador de manera inicial, a expensas de prolongar la estancia hospitalaria, mayor riesgo de íleo paralítico y permanencia de sonda uretral y drenaje. Solo ante la imposibilidad de un adecuado drenaje vesical se puede recurrir a reconstrucción anastomótica, recurriendo inicialmente a un abordaje endoscópico y si no es posible el cateterismo, el débito de la fístula es persistente o se produce una dehiscencia severa de la anastomosis, se recurre al abordaje abierto. Uno de nuestros pacientes, tras desalojo accidental de la sonda en postoperatorio precoz, presentó fístula urinaria con débito importante. Ante la sospecha de dehiscencia anastomótica traumática, se realizó laparotomía exploradora. En la intervención se objetivo integridad anastomótica con leve fuga, requiriendo drenaje de la colección y cateterismo uretral. Ante estos hallazgos, es más que probable que un manejo conservador mediante sondaje y mantenimiento del drenaje hubieses sido suficiente, como así realizamos en el otro caso de fístula urinaria.
En la mayoría de series revisadas no se registran las complicaciones urinarias tardías (>3 meses), por ello es difícil conocer su verdadera incidencia. En nuestra casuística se presentó una estenosis anastomótica (0,4%) oscilando en los diferentes trabajos entre (0,6-3%), siendo menos frecuente que en la cirugía abierta (5-32%) y más similar a la laparoscopia convencional (0-3%)10,11. Su presentación clínica como dificultad miccional tiene una demora media de 4,8 meses (3-12 meses)21. La precisión y estanqueidad de la anastomosis que evitaría la fuga urinaria y su potencial efecto deletéreo en la fibrosis anastomótica, pueden ser los argumentos a favor de esta menor incidencia.
El empleo cada vez más común de clips metálicos y Hem-o-lock en la PRR con la finalidad de minimizar el efecto lesivo de la energía térmica en las estructuras neurovasculares puede condicionar la aparición de complicaciones relacionadas con la migración, calcificación o inducción de fibrosis de estos cuerpos extraños. Así, se han descrito casos de esclerosis anastomótica por presencia de Hem-o-lok en la anastomosis en 0,76% de casos. De igual modo se han referido episodios de hematuria tardía por migración vesical e incluso un seudoaneurisma que precisó embolización selectiva, relacionados con la presencia de clips22. En nuestro paciente, es probable que los clips y especialmente el Hem-o-lok con el que ocluíamos el conducto deferente en la línea media, finalizase erosionando el suelo vesical por decúbito. Ante estos hallazgos, se recomienda minimizar el uso de estos clips en la línea media, en conductos deferentes, ni cerca de la anastomosis uretrovesical. De maneara adicional se debe retirar todos aquellos clips que se pierdan para evitar su migración a vejiga y prestar atención a los síntomas miccionales que aparezcan de manera tardía en estos pacientes. De igual modo, empleamos un clip reabsorbible Lapra-Ty (Ethicon) como refuerzo del extremo anudado de la doble sutura para la anastomosis. La micción espontánea del Lapra-Ty íntegro en 2 pacientes, nos ha planteado la idea de abandonar su empleo como refuerzo del anudado sugiriendo su sustitución por un pequeño segmento de conducto deferente obtenido tras su disección.
Las complicaciones intestinales son poco frecuentes pero suelen condicionar actuaciones terapéuticas precoces y pueden revestir gravedad de demorarse su diagnóstico. Las perforaciones ileocolónicas se objetivan en 0,6% de las series consultadas y su forma de presentación es variable. Se pueden producir durante la inserción de los trocares, especialmente con antecedentes de cirugía abdominal previa. Por ello en estos pacientes siempre es aconsejable realizar una técnica abierta de Hasson. De igual modo, se puede producir la lesión durante la adhesiolísis o durante el intercambio de instrumentos durante la cirugía. De ser identificada la lesión intraoperatoriamente, se procederá a su cierre primario o resección intestinal según el alcance de la misma. El empleo de energía monopolar o bipolar durante la adhesiolisis puede producir una lesión térmica, que pase inadvertida y reproduzca una perforación tardía al desprenderse la escara térmica; tal y como ocurrió en nuestro paciente a nivel cecal y tras liberar adherencias de peritonitis apendicular previa. El problema radica en su presentación clínica diferida y abigarrada, de no establecerse su diagnóstico intraoperatorio. Así debemos prestar atención a la presencia de un íleo paralítico primario y distensión abdominal en ausencia de signos de irritación peritoneal23. Nuestro paciente solo reflejaba una ligera distensión abdominal una vez iniciada la tolerancia oral. El estudio radiológico informó de la presencia de un discreto neumoperitoneo que en ocasiones no puede diferenciarse del propio del procedimiento laparoscópico cuando es escaso. La analítica puede no verse alterada hasta que el cuadro este avanzado (leucocitosis con desviación izquierda, incremento de la creatinina). De igual modo; la fiebre, oliguria y otros signos pueden ser de presentación tardía lo que condiciona la necesidad de un estado de alerta diagnóstica. La TAC puede reflejar datos de sufrimiento intestinal, distensión de asas y edema parietal, así como colecciones líquidas con o sin contenido gaseoso. En cualquier caso, ante la sospecha de perforación se impone la laparotomía exploradora para evitar complicaciones sépticas fatales. Se realizará resección intestinal y drenaje apropiado11.
La perforación rectal se ha registrado en la literatura alrededor del 0,9% de las PRR, y oscilan entre el 0,5-9% en las series de cirugía radical abierta24. En nuestras 250 PRR no se ha presentado esta complicación aun realizando cirugía de rescate postcrioterapia en 2 pacientes y un rescate postradioterapia. Los factores de riesgo para la lesión rectal son: fibrosis periprostática, cirugía rectal previa, próstatas pequeñas, antecedente de radioterapia o bloqueo androgénico y tumores localmente avanzados. Los casos descritos tras PRR se producen cerca del ápex en la sección del músculo rectouretralis12. Si se identifica intraoperatoriamente se procede a la sutura en 2 planos, interposición de colgajo epiplóico, dilatación anal, dieta baja en fibra, cateterismo uretral 15 días y antibioterpia apropiada. Si existen antecedentes de radioterapia, contaminación fecal o sutura a tensión se realizará colostomía de descarga.
El íleo paralítico tras la PRR no queda reflejado con exactitud en todas las series, y así oscila entre 0,7-2,8%11,20. Depende fundamentalmente de los criterios de cada autor para registrar si la demora en la dinámica intestinal es o no relevante, y si precisa de medidas terapéuticas como sonda nasogástrica o hiperalimentación. Se presume que su incidencia es más probable en pacientes con cirugía intestinal previa y que precisen de extensas adhesiolisis. De igual modo, las lesiones intestinales son una etiología obvia en estos casos. La realización de un abordaje transperitoneal durante la PRR, permitiría que cualquier colección pélvica: urinoma, hematoma o linfocele irritase el peritoneo y condicionase la aparición de un íleo persistente, tal y como ocurrió en 3 de nuestros pacientes (2 urinomas y un hematoma). El abordaje extraperitoneal minimizaría esta complicación25.
Entre las complicaciones vasculares destacan las de origen hemorrágico. Así, en todas las series de laparoscopia se presenta una incidencia baja de lesión de la arteria epigástirca (0,8%). La cuidadosa retirada de los trocares bajo inspección y la adecuada sutura transparietal hubiese evitado nuestro caso diferido. Nuestro paciente con hematoma retrovesical y presentación clínica inespecífica (tenesmo rectal y dolor perineal) sin evidencia de sangrado activo en drenaje, pudo ser debido a la técnica atérmica en bandeletas neurovasculares y a la ineficacia operativa del drenaje en posición retropúbica. Por ello pensamos que, aunque es una complicación poco frecuente, las técnicas de reconstrucción anterior ampliadas (puboperineoplastia con cierre completo del espacio retropúbico mediante sutura de vejiga a ligamento ileopectíneo de Cowper y pubovesical) pueden impedir el adecuado drenaje del espacio prerectal y facilitar estas colecciones, salvo por el empelo de doble drenaje. Si bien es cierto que no se describe una mayor incidencia en las series consultadas en la literatura donde los autores practican estas técnicas de reconstrucción anatómica del collar pubouretral y puboperineoplastia26,27.
El volumen medio de hemorragia intraoperatoria registrado en nuestra serie es de 125ml (50-1150ml), con una tasa de transfusiones postoperatoria de 3,6% (9/250). De los datos recogidos en la literatura se refleja un volumen medio de hemorragia entre 75-500ml pos-PRR y una tasa de transfusión postoperatoria baja (0-12%) con media de 1,8%7,9-11,20. Son cifras sensiblemente inferiores a las series de laparoscopia convencional (0,3-8,9%) y cirugía abierta (0,3-14%)28,29. Nuestra serie, refleja tasas ligeramente superiores a la media en probable relación a la técnica atérmica completa desde las vesículas seminales y a la sección sin ligadura previa del complejo venoso dorsal para su posterior sutura individualizada. No obstante, el sangrado es discreto y las ventajas en preservación neurovascular y conservación de la integridad del rabdoesfínter uretral así como los resultados en continencia y potencia, ameritan seguir sin modificaciones técnicas al respecto.
La PRR como cirugía pélvica oncológica puede presentar complicaciones tromboembolígenas. No obstante, la curva de aprendizaje corta, una adecuada compresión de extremidades inferiores, la profilaxis antitrombótica y la movilización precoz minimizan este tipo de complicaciones. En nuestra serie se presentaron 2 casos de embolia pulmonar diferidos tratados con anticoagulación. Una revisión de la literatura sobre 5.591 pacientes sometidos a PRR o laparoscópica convencional arroja incidencias bajas de complicaciones tromboembolígenas. Se objetivan tasas de 0,5% de trombosis venosa (31 pacientes: 22 trombosis venosas y 4 embolias pulmonares). Destacando que solo en el caso de presentar factores de riesgo: antecedentes previos de tromboembolismo, hábito tabaquico, tiempo quirúrgico prolongado, mayores de 60 años y obesidad; estaría justificada una profilaxis sistemática con heparina. De igual modo, algunos autores reflejan la importancia de la curva de aprendizaje con una reducción de eventos tromboembólicos del 7,5% en los primeros 40 casos al 1,1% a partir de 100 casos30.
El empleo de una herramienta como el sistema daVinci y la dependencia de la tecnología, está sujeto a imprevistos en forma de fallos mecánicos. La incidencia de esta complicación registrada en la literatura oscila entre 2-5%, aunque la tasa de reconversiones por este motivo es del 0,4%31. En la mayoría de ocasiones son fallos recuperables, que tras desacoplar el robot y reiniciar el sistema se subsanan sin más relevancia que la demora quirúrgica. En ocasiones, se trata de modificar la ubicación de los brazos robóticos para evitar colisiones entre ellos o con el paciente. Aunque su incidencia es baja y el servicio de asistencia técnica es eficaz, conviene informar al paciente de esta posible eventualidad. De igual modo, se debe registrar en el consentimiento informado la oportunidad de reconvertir la cirugía a procedimiento laparoscópico o abierto de producirse un fallo mecánico. Esta situación, obliga a informar que de no realizarse la intervención con el sistema robótico los potenciales beneficios en la reducción de secuelas se pueden ver perjudicados. De igual modo, las unidades con un solo sistema robótico no pueden emplear el recurso de un sistema de repuesto inmediato. Así mismo, es aconsejable iniciar el sistema daVinci antes de proceder a instaurar la anestesia general al paciente8-12.
En nuestra serie no se han registrado linfoceles sintomáticos en las 21 linfadenectomías iliobturatrices realizadas (9,4%). No obstante, su incidencia es más común de lo sugerido en la literatura (0,9%)11, y si se realizasen pruebas de imagen sistemáticas su incidencia sería más elevada. No obstante, el manejo clínico en caso de presentarse dolor, íleo paralítico, sobreinfección sería inicialmente el drenaje percutáneo.
Los diferentes estudios que comparan las complicaciones entre la cirugía abierta, laparoscópica con la robótica reflejan tasas similares aunque con menor incidencia de complicaciones en el abordaje robot-asistido. Así la incidencia de: fístulas urinarias, ileo paralítico, pérdidas hemáticas y estancia hospitalaria son favorables a la cirugía robótica. La tasa de complicaciones de la PRR oscila entre 1-8,8 vs. 4-34% de la laparoscopia. El volumen de hemorragia es inferior en la robótica (234 vs. 482ml), el tiempo quirúrgico es discretamente superior en la curva de aprendizaje pero se alcanza los 182 (141-250min) vs. 234min (151-453min) de la laparoscopia convencional. En líneas generales no existen diferencias significativas entre las diferentes técnicas y la experiencia del equipo quirúrgico condiciona los resultados32-36.
Limitaciones del estudio
Este estudio retrospectivo descriptivo presenta algunas limitaciones obvias. La primera dificultad en el registro de complicaciones estriba en la definición empleada para las mismas, así algunos autores solo reflejan las complicaciones mayores de importancia vital obviando las menores. Por otro lado, aunque existen sistemas de clasificación definidos como el de Clavien, en ocasiones las fronteras entre los diferentes grados no están bien definidas y adolecen de un cierto carácter subjetivo. De igual modo, es sencillo registra las complicaciones intraoperatorias y postoperatorias inmediatas, pero las complicaciones tardías, habitualmente de menor relevancia clínica, pueden perderse en los registros, en especial en unidades abiertas. Si bien es cierto que se trata de un colectivo menor y con eventos de escaso impacto. De igual modo en nuestra serie, se debe tener en cuenta que se suman las curvas de aprendizaje de tres cirujanos lo que sin duda hace difícil establecer el impacto de la casuística en las complicaciones. Si bien es cierto que la tasa global de complicaciones se reduce con la curva de aprendizaje como se aprecia en la serie, habiendo ocurrido la mayoría en los 50 primeros casos.
¿Influye la curva de aprendizaje en la tasa de complicaciones?
Indudablemente es así, que la experiencia en un procedimiento quirúrgico influye en los resultados es algo de sobra conocido37. No obstante, con la PRR se suman la experiencia en cirugía abierta y laparoscopia previas del equipo implicado, sin tratarse en estos casos de un procedimiento de novo. Si bien se ha reflejado en la literatura que la curva de aprendizaje para la PRR es inferior (20-30 casos) a la de la laparoscopia convencional (50-100 casos) incluso para cirujanos sin experiencia previa laparoscópica3,13,37,38. No es menos cierto que probablemente esta curva (medida en número de casos) sea interminable y que con seguridad se precisen más de 100 casos para adquirir pericia en el procedimiento. Lo que es veraz es que el sistema daVinci permite el paso de la cirugía abierta a un abordaje laparoscópico con mayor sencillez facilitando la labor del cirujano en condiciones óptimas de ergonomía y con una herramienta que permite trabajar con un microscopio de 10 aumentos, visión tridimensional y unos instrumentos con 7o de libertad38.
Iniciarse en la cirugía robótica con el sistema daVinci, requiere igualmente un aprendizaje de la nueva herramienta que vamos a emplear. No se trata de realizar un procedimiento quirúrgico nuevo, sino de ejecutarlo con una nueva herramienta. No se está inventando una técnica de exéresis de la próstata sino una forma diferente de hacerla. Al igual, que para realizar resecciones prostáticas comenzamos por conocer, ensamblar y desmontar las piezas del resector, la robótica precisa habituarse con el carro quirúrgico y la consola. Por ello, antes de iniciarse en otros procedimientos es aconsejable familiarizarse con la instalación, acoplamiento del robot, así como los diferentes «trucos» para evitar problemas técnicos durante el procedimiento. Por tanto, esta fase requiere su propia curva de aprendizaje que se traduce en un acortamiento del tiempo de instalación del robot (set up) y de la cirugía. Y para ello es imprescindible el equipo quirúrgico que incluye anestesista, enfermería, asistente y cirujano.
¿Es importante el equipo quirúrgico implicado?
La cirugía robótica, al igual que la laparoscopia, es un trabajo de equipo. El factor más importante en los resultados oncológicos y funcionales de la PRR es la experiencia del equipo quirúrgico más que el tipo de abordaje quirúrgico37. El papel del ayudante es de suma importancia, la experiencia y formación del asistente son garantía de progreso en la curva de aprendizaje39. Consideramos oportuno y necesario experiencia laparoscópica previa del equipo implicado en la cirugía robótica, o en su defecto del ayudante puesto que en caso de fallo técnico del robot se pueda proceder a completar el procedimiento de manera laparoscópica convencional. Algunos autores, abogan por mantener un equipo inicial de tres urólogos que progresan de asistente a consola, reduciéndose la curva de aprendizaje. De este modo, se ha constatado que las segundas y terceras generaciones de cirujanos de consola adquieren pericia en progresión geométrica y de manera más eficaz integrados en equipos de trabajo establecidos40.
¿Qué lección hemos aprendido en este tiempo?
Después de este trienio realizando cirugía robótica, hemos apreciado una evolución lógica como la acontecida en cualquier otro procedimiento quirúrgico. En primer lugar, es preciso familiarizase con la nueva herramienta de trabajo, es preciso un trabajo en equipo con transición de asistente a consola, y es deseable experiencia previa laparoscópica; tal y como se ha comentado en párrafos anteriores. En cuanto a la técnica de PRR que se va a realizar, será aquella con la que esté familiarizada el equipo por su experiencia previa en cirugía abierta o laparoscópica. A medida que se establezcan y asienten las distintas fases de la intervención, se pueden introducir modificaciones en aras a mejorar los resultados oncológicos y funcionales sin perder de vista el objetivo de este procedimiento que es la extirpación de la próstata tumoral con el menor número de daños colaterales posible.
La experiencia reduce las complicaciones y mejora los resultados funcionales, no obstante nuestra curva de aprendizaje corresponde a tres cirujanos solapándose en el tiempo tras realizar cada uno de ellos 20 casos. Aunque se aprecia que las complicaciones mayores acontecen en los primeros 50-100 casos, no es infrecuente que en ocasiones alguna complicación se presente en casos tardíos, puesto que probablemente el equipo quirúrgico acometa procedimientos más complejos y de mayor riesgo.
¿Qué modificaciones hemos introducido después de este periodo?
Entre las reflexiones y modificaciones sobre nuestra técnica establecidas tras este trienio se reflejan las siguientes:
1) Abordaje: realizamos el acceso supraumbilical directo con trocar de 12mm, salvo en pacientes con antecedentes de cirugía abdominal previa, donde realizamos una técnica de Hasson minimizada sin haber encontrado problemas ni complicaciones derivadas del acceso en esta experiencia de 250PRR.
2) Trocarización: el sistema daVinci Standard tiene los instrumentos de 25cm (5cmts más cortos que el sistema actual daVinci S y Si). Por ello, en pacientes obesos, o de talla elevada (>180) es aconsejable disponer los trocares de los brazos robóticos más cercanos al pubis (respetando los 20cm de la raíz del pene, o 18cm de la sinfisis púbica) para garantizar el acceso al ápex, uretra y posterior anastomosis. Todo ello, respetando un adecuado ángulo de entrada en la pelvis para evitar colisiones inoportunas y acceder con facilidad al ápex y a la uretra. No obstante, se puede ganar longitud funcional de los instrumentos avanzando el brazo y el trocar conjuntamente por parte del ayudante.
3) Realizamos técnica atérmica anterógrada desde la disección de los conductos deferentes hasta aislar las bandeletas neurovasculares y llegar al ápex, empleando clips metálicos de 5mm y Hem-o-lok. Aunque recientemente, hemos minimizado el empleo de clips metálicos y Hem-o-Lok en la línea media para evitar la erosión o migración de los mismos a vejiga y evitar interferir en la cicatrización normal de la anastomosis uretrovesical. De igual modo, preservamos la fascia endopélvica, salvo que este indicada técnica extrafascial o en próstatas voluminosas para facilitar su movilización. La reciente micción espontánea del Lapra-Ty, nos ha planteado la idea de abandonar su empleo como refuerzo del anudado del extremo de la doble sutura de Van-Velthoven, sugiriendo su sustitución por un pequeño segmento de conducto deferente obtenido tras su disección, tal y como preconizan algunos autores.
4) Seguimos evitando la sutura indiscriminada y cualquier forma de energía térmica en el complejo venoso dorsal. Y a pesar de incrementar el volumen de sangrado, preferimos una sección del complejo venoso con elevación de la presión del neumoperitoneo y una sutura individualizada para no incorporar ni deteriorar las fibras del rabdoesfinter evitando su probable impacto en la recuperación de la continencia. De igual modo, hemos iniciado una reconstrucción anterior pubovescial para valorar su impacto en la recuperación precoz de la continencia, reservando la reconstrucción posterior en próstatas voluminosas para reducir tensión anastomótica.
5) Drenajes: se exterioriza por el trocar de 12mm en fosa iliáca derecha del ayudante. En los casos de anastomosis impermeable y ausencia de hemorragia se ha valorado la oportunidad de no dejar un drenaje. No obstante, a día de hoy, no creemos inoportuno dejar un drenaje 24h por precaución.
6) Sonda: la mantenemos 7 días y no realizamos sistemáticamente cistografía de no sospecharse fístula urinaria. Algunos grupos abogan por una retirada precoz (5 días) aunque con un mayor riesgo de retención urinaria. Otros autores apuestan por no emplear la vía uretral sino colocar una cistostomía suprapúbica con buena recuperación de la dinámica miccional y confort para el paciente e incluso una rápida recuperación de la continencia16-18.
Conclusiones
La PRR es un procedimiento seguro, así se refleja en esta revisión, donde el 96% de los pacientes (240/250) tuvieron un curso postoperatorio inmediato adecuado sin incidencias reseñables. La tasa global de complicaciones fue del 10,4% con solo 3,2% de complicaciones mayores (8/250): 5 complicaciones quirúrgicas y 3 médicas. La tasa de reintervención fue del 1,6% (4/250) y no fue precisa ninguna reconversión intraoperatoria a cirugía abierta o laparoscópica.
De modo y manera, podemos afirmar que la PRR es una técnica segura y reproducible con óptimos resultados oncológicos y funcionales, con una curva de aprendizaje más corta, con excelente ergonomía y visión para el cirujano y con una incidencia de complicaciones comparable e incluso favorable a las series de cirugía abierta y laparoscópica. Las complicaciones se reducen con la curva de aprendizaje sin olvidar que es la experiencia del equipo quirúrgico el factor clave para conseguir mejores resultados.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Guillonneau B., Cathelineau X., Barret E. Laparoscopic radical prostatectomy. Preliminary evaluation after 28 interventions. Press Med. 1998; 27:1570-4. [ Links ]
2. Menon M., Shrivastava A., Tewari A. Laparoscopic and robot assisted radical prostatectomy: establishment of a structured program and preliminary analysis of outcomes. J Urol. 2002; 168:945-9. [ Links ]
3. Patel V.R., Tully A.S., Holmes R. Robotic radical prostatectomy in the community setting: learning curve and beyond: initial 200 cases. J Urol. 2005; 174:269-72. [ Links ]
4. Pereira JG, Gamarra M, Ibarluzea G. "Prostatectomía Radical asistida por robot" En Perspectivas históricas, presente y futuro de la cirugía laparoscópica urológica. Capítulo 21, pp. 131-151; Editorial Evidencia médica SL, 2008. [ Links ]
5. Clavien P.A., Sanabria J.R., Strasberg S.M. Proponed classification of complications of surgery with examples of utility in cholecystectomy. Surgery. 1992; 11:518. [ Links ]
6. Dindo D., Demartines N., Clavien P.A. Classification of surgical complications: A new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg. 2004; 240:205. [ Links ]
7. Cáceres F., Sánchez C., Martínez-Piñeiro L. Prostatectomía radical laparoscópica versus robótica. Arch Esp Urol. 2007; 60,4:430-8. [ Links ]
8. Motrie A., Van Migem P., De Naeyer G. Robot-Assisted laparoscopic radical prostatectomy: Oncologic and functional results in 184 cases. Eur Urol. 2007; 52:746-51. [ Links ]
9. Rozet F., Jaffe J., Braud G. A direct comparison of robotic assisted versus pure laparoscopic radical prostatectomy: A single institution experience. J Urol. 2007; 178:478-82. [ Links ]
10. Bhandari A., Mcintire L., Kaul S.A. Perioperative complications of robotic radical prostatectomy after the learning curve. J Urol. 2005; 174:915-8. [ Links ]
11. Hu J.C., Nelson R.A., Wilson T. Perioperative complications of laparoscopic and robotic assisted laparoscopic radical prostatectomy. J Urol. 2006; 175:541-6. [ Links ]
12. Patel V., Thaly R., Shah K. Robotic radical prostatectomy: outcomes of 500 cases. BJU Int. 2007; 99:1109-12. [ Links ]
13. Villavicencio H., Esquena S., Salvador J. Prostatectomía radical robótica: Análisis después de 100 casos en la Fundación Puigvert. Actas Urol Esp. 2009; 33:24-9. [ Links ]
14. Phong S., Koh L.K. Anaesthesia for robotic assisted radical prostatectomy: considerations for laparoscopy in Trendelemburg position. Aneasth intensive care. 2007; 35:281-5. [ Links ]
15. El-Hakim A., Leung R.A., Richstone L. Athermal robotic technique of prostatectomy in patients with large prostate glands(>75 g): technique and intial results. BJU Int. 2006; 98:44-7. [ Links ]
16. Menon M., Shrivastava A., Bhandari M. Vattikuti institute prostatectomy: technical modifications in 2009. Eur Urol. 2009; 6:89-96. [ Links ]
17. Krane L.S., Bhandari M., Peabody J.O. Impact of precutaneous suprapubic tube drainage on patient disconfort after radical prostatectomy. Eur Urol. 2009; 56:325-31. [ Links ]
18. Tewari A., Rao S., Mandhani A. Catheter-less robotic radical prostatectomy using custom-made synchronous anastomotic splint and vesicalurinary diversion devi report of the initial series and perioperative outcomes. BJU Int. 2008; 102:1000-4. [ Links ]
19. Beckley I., Patterson B. Delayed hemorrhage from an accesory internal pudendal artery pseudoaneurysm after robotic radical postatectomy: succesful management with CT angiography and embolization. J Endourol. 2007; 21:923-5. [ Links ]
20. Badani K.K., Kaul S., Menon M. Evolution of robotic radical prostatectomy. Assesment after 2766 procedures. Cancer. 2007; 110:1951-8. [ Links ]
21. Msezane L.P., Reynolds W.S., Gofrit O.N. Bladder neck contracture after robotassisted laparoscopic radical prostatectomy. Evaluation of incidence and risk factors and impact on urinary function. J Endourol. 2008; 22:377-83. [ Links ]
22. Blumenthal K.B., Sutherland D.E., Wagner K.R. Bladder neck contracture related to the use of Hem-O-Lok clips in Robot-assisted laparsocopic radical prostatectomy. Urology. 2008; 72:158-61. [ Links ]
23. Bishoff J.T., Allaf M.E., Kirkels W. Laparoscopic bowel injury: incidence and clinical presentation. J Urol. 1999; 161:88. [ Links ]
24. Yee D., Ornstein D.R. Repair of rectal injury during robot-assisted laparoscopic prostatectomy. Urology. 2008; 72:428-31. [ Links ]
25. Madi R., Daignault S., Wood D.P. Extraperitoneal vs intraperitoneal robotic prostatectomy: analysis of operative outcomes. J Endourol. 2007; 21:1553-7. [ Links ]
26. Tewari A.K., Bigelow K., Rao S., Takenaka A. Anatomic restoration technique of continence mechanism and preservation of puboprostatic collar: a novel modification to achieve early urinary continence in men undergoing robotic prostatectomy. Urology. 2007; 69:726I. [ Links ]
27. Takenaka A., Tewari A.K., Leung R.A. Preservation of the puboprostatic collar and puboperineoplasty for early recovery of urinary contience alter robotic prostatectomy: anatomic basis and preliminary outcomes. Eur Urol. 2007; 51:433-40. [ Links ]
28. Rassweiler J., Hruza M., Teber D. Laparoscopic and robotic assisted radical prostatectomy. Critical analysis of the results. Eur Urol. 2006; 49:612-24. [ Links ]
29. Lepor H., Nieder A.M., Ferrandino M.N. Intraoperative and postoperative complications of radical retropubic prostatectomy in a consecutive series of 1,000 cases. J Urol. 2001; 166:1729. [ Links ]
30. Secin T. Multiinstutional study of symtomatic deep venous trombosis and pulmonary embolism in Pca patients undergoing laparoscopic o robotassited laparoscopic radical prostatectomy. Eur Urol. 2008; 53:134-45. [ Links ]
31. Zorn K.C., Gofrit O.N., Orvietto M.A. Da Vinci robot error and failure rates: single institution experience on a single three robot unit of more than 700 cases consecutive of robotic asssited laparoscopic prostatectomies. J Endourol. 2007; 21:1341-4. [ Links ]
32. Boris R.S., Kaul S.A., Sarle R.C., Stricker H.J. Radical prostatectomy: a single surgeon comparison of retropubic, perineal, and robotic approaches. Can J Urol. 2007; 14:3566-70. [ Links ]
33. Tewari A., Srivasatava A., Menon M. and Members of the VIP Team: A prospective comparison of radical retropubic and robot-assisted prostatectomy: experience in one institution. BJU Int. 2003; 92:205. [ Links ]
34. Menon M., Tewari A., Baize B. Prospective comparison of radical retropubic prostatectomy and robot-assisted anatomic prostatectomy: the Vattikuti Urology Institute experience. Urology. 2002; 60:864-8. [ Links ]
35. Ficarra V., Novara G., Artibani W. Retropubic, laparoscopic, and robot-assisted radical prostatectomy: A systematic review and cumulative analysis of comparative studies. Eur Urol. 2009; 55:1037-63. [ Links ]
36. Caballero J.P., Palacios J., Pereira J.G. Prostatectomía radical: comparación de los resultados obtenidos durante las curvas de aprendizaje de la técnica laparoscópica pura y de la técnica asistida por robot con la prostatectomía radical retropúbica. Actas Urol Esp. 2008; 32:968-75. [ Links ]
37. Herrmann T.R. Oncological and functional results of open, robot-asssited and laparoscopic radical prostatectomy: dose surgical approach and surgical experience matter?. World J Urol. 2007; 25:149-60. [ Links ]
38. Ahlering T.E., Skarecky D., Lee D. Successful transfer of open surgical skills to a laparoscopic enviroment using robot interfa initial experience with laparoscopic radical prostatectomy. J Urol. 2003; 170:1738-41. [ Links ]
39. Mandhani A., Berryhill R., Tewari A.K. Prostatectomía robótica atérmica: perspectiva del ayudante quirúrgico. Arch Esp de Urol. 2007; 60,4:375-82. [ Links ]
40. Sim H.G., Yip S.K., Lau W.K. Team-based reduces learning curve in robot-assisted laparoscopic radical prostatectomy. Int J Urol. 2006; 13:560-4. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
jpereira@urologiaclinica.biz
(J.G. Pereira Arias)
Recibido 27 Octubre 2009
Aceptado 12 Diciembre 2009














