Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nefrología (Madrid)
versión On-line ISSN 1989-2284versión impresa ISSN 0211-6995
Nefrología (Madr.) vol.33 no.5 Cantabria 2013
https://dx.doi.org/10.3265/Nefrologia.pre2013.Apr.11898
Tratamiento multidisciplinar de la disfunción y la trombosis de las fístulas arteriovenosas protésicas para hemodiálisis
Multidisciplinary approach to hemodialysis graft dysfunction and thrombosis
Pedro Jiménez-Almonacid1, Enrique Gruss2, Marta Jiménez-Toscano1, Manuel Lasala1, José A. Rueda1, Laura Vega1, Gil Rodríguez3, Raúl De la Cruz4, Mar Pardo1, Beatriz Fernández1, Paula López2, Jaime Martín-Cavana1, Antonio Quintáns1
1 Unidad de Cirugía General y del Aparato Digestivo. Hospital Universitario Fundación Alcorcón. Alcorcón, Madrid
2 Unidad de Nefrología. Hospital Universitario Fundación Alcorcón. Alcorcón, Madrid
3 Unidad de Epidemiología. Hospital Universitario Fundación Alcorcón. Alcorcón, Madrid
4 Unidad de Radiología Vascular. Hospital Universitario Fundación Alcorcón. Alcorcón, Madrid
Dirección para correspondencia
RESUMEN
Objetivo: Análisis de la aplicación de un protocolo multidisciplinar para el mantenimiento de las fístulas arteriovenosas para hemodiálisis protésicas.
Método: Recogida prospectiva de todas las intervenciones realizadas para el tratamiento de la disfunción de las fístulas arteriovenosas protésicas (FAVP) en el período 1999-2007 siguiendo un protocolo multidisciplinario. Las estenosis se trataron mediante angioplastia, (ATP) excepto en casos de persistencia o recurrencia antes de tres meses. Las trombosis fueron tratadas siempre mediante trombectomía quirúrgica y puente de PTFE si fue necesario. Se analizan el número y el tipo de procedimientos, las complicaciones, la permeabilidad primaria y secundaria de las FAVP.
Resultados: Se completó el seguimiento de 96 FAVP. Todas fueron prótesis de PTFE de 6x40 mm (Gore-Tex®). Treinta y seis se colocaron en el antebrazo con anastomosis humerobasílica en asa y 60 en el brazo con anastomosis humeroaxilar curva. Durante el período de estudio fueron necesarios 131 angioplastias transluminales percutáneas, 15 stents, 109 trombectomías y 52 puentes a vena proximal para el mantenimiento de la permeabilidad de las FAVP. La permeabilidad primaria fue del 73,68 %, 60,21 % y 37,52 % a 1, 2 y 3 años, respectivamente. La permeabilidad secundaria fue del 89,49 %, 84,07 % y 66,84 % a 1, 2 y 3 años, respectivamente. Se consiguió evitar la colocación de un catéter central en el 80 % de las intervenciones por trombosis. No se produjeron muertes relacionadas con los procedimientos. La tasa de ingresos hospitalarios relacionados con la trombosis de las FAVP fue de 0,03 paciente/año.
Conclusiones: La aplicación de un protocolo multidisciplinar en el tratamiento de las disfunciones de las FAVP siguiendo las recomendaciones de las guías internacionales prolonga la permeabilidad de las FAVP y disminuye el uso de catéteres centrales.
Palabras clave: Fístula protésica para hemodiálisis, Disfunción, Multidisciplinar.
ABSTRACT
Purpose: To analize the clinic results of the implantation of a multidisciplinary protocol to maintain ermeability of the arteriovenous hemodialysis grafts (AVG).
Methods: Prospective recording of all interventions (radiological and surgical) on AVG dysfunction in the 1999-2007 period. The AVG stenosis were always treated by percutaneous angioplasty (PA) except stenosis recurrence in less than three months or persistence after PA. The AVG thromboses were always treated by surgical thrombectomy plus PTFE bridge if necessary. Complications, primary and secondary AVG patency were reviewed.
Results: Ninety six dysfunction AVG were collected for study. All of them were 6x40mm standard wall PTFE (Gore-Tex®). Thirty six of them were humero-basilic antebraquial loop and sixty were humero-axillary upper arm curve configuration. During the study, 52 PTFE bridges, 109 surgical thrombectomies, 131 PA, and 15 stents were needed to maintain FAVP permeability. Primay patency was 73.68%, 60.21% and 37.52% at one, two and three years respectively. Secondary patency was 89.49%, 84.07% and 66.84% at one, two and three years respectively. We avoid a central venous catheter (CVC) in the 80% of intervention for thrombosis dysfunction. No surgical or radiological related deaths occurred. Median hospital admission related with AVG thrombosis was 0.03/patient/year.
Conclusion: The application of a combined protocol for the treatment of AVG dysfunction and thrombosis, according to DOQI recomendations obtains good results in AVG patency in our experience.
Key words: Graft arterioevenous fistula, Dysfunction, Multidisciplinary.
Introducción
En España, la incidencia y la prevalencia de pacientes con enfermedad renal crónica que necesitan tratamiento renal sustitutivo han aumentado más del 100% en los últimos 15 años1 (desde 61 y 392 pacientes por millón en 1991 a 132 y 1009, respectivamente, en 2007). El grupo de edad que ha registrado un mayor incremento porcentual es el de pacientes mayores de 75 años (del 8,5% de los pacientes prevalentes en 1992 al 40% en la actualidad). En este grupo, la mayoría de los pacientes son tratados mediante hemodiálisis (94% de los pacientes incidentes) y pocos cambian de técnica a lo largo de su vida. Aproximadamente el 10% de los pacientes en hemodiálisis en nuestro medio lo hacen con una fístula arteriovenosa protésica (FAVP)2-5.
Las FAVP son una buena opción en pacientes con ausencia de un sistema venoso superficial adecuado para realizar una fístula autóloga o tras la pérdida de fístulas previas. Tienen la ventaja de ser fáciles de canular, su tasa de fracaso precoz es baja y tienen un tiempo corto de maduración. Sin embargo, presentan una tasa de complicaciones muy superior a las fístulas arteriovenosas nativas (FAV-n) y su permeabilidad es menor a largo plazo. El tratamiento de las estenosis y las trombosis de las FAVP puede realizarse por métodos radiológicos o quirúrgicos. Cada centro debe realizar protocolos de mantenimiento según sus recursos para conseguir unos indicadores de calidad asistencial acordes con las recomendaciones internacionales6,7.
En nuestro hospital, se encuentra en funcionamiento un equipo de accesos vasculares para hemodiálisis multidisciplinario que se ha interesado especialmente por el desarrollo de protocolos y la definición de indicadores en nuestro medio8,9.
En este trabajo presentamos nuestro protocolo de mantenimiento de las FAVP y la evaluación de sus resultados tras ocho años de seguimiento.
Material y métodos
Estudio prospectivo sobre la aplicación de un protocolo para el tratamiento de las disfunciones (estenosis y trombosis) de las FAVP.
Ámbito
Nuestro hospital atiende el acceso vascular para hemodiálisis de un área de salud en la Comunidad de Madrid con 550000 habitantes y de forma regular también a las unidades de las provincias de Ávila y Segovia (250 000 habitantes). En él la historia clínica está informatizada y existe un protocolo específico para las intervenciones relacionadas con las fístulas arteriovenosas que el cirujano responsable cumplimenta al finalizar la intervención. Las intervenciones las realizaron cuatro cirujanos del servicio interesados en el tema pero sin dedicación exclusiva a él (su actividad es la de cualquier cirujano general) y sin guardias específicas. No existe asistencia urgente para procedimientos radiológicos.
Pacientes
Durante el período 1999-2007 se realizaron 130 FAVP en 115 pacientes (15% del total de fístulas arteriovenosas realizadas). Se han excluido del trabajo 34 FAVP por falta de seguimiento (fracaso precoz o traslado a otros centros). En el resto (96) se aplicó un protocolo multidisciplinar para el diagnóstico y el tratamiento de las disfunciones y trombosis. Para el análisis de los resultados contamos con el apoyo de una historia clínica informatizada y un protocolo quirúrgico específico en el caso de los accesos vasculares para hemodiálisis.
Técnica quirúrgica
Se decidió la realización de una FAVP tras descartar la posibilidad de realización de fístula autóloga por presentar un sistema venoso superficial inadecuado o tras el fracaso de fístulas previas. El material utilizado fue en todos los casos politetrafluoroetileno expandido (ePTFE 6 mm x 40 cm). La configuración anatómica de las FAVP se decide en función del calibre del sistema venoso profundo del paciente, utilizando dos formas:
1. Loop o asa antebraquial (puente entre la arteria humeral y la vena basílica o venas humerales), que denominamos LOOP.
2. Curva en brazo (puente entre arteria humeral y vena axilar), que denominamos HAX.
Seguimiento
Se solicitó fistulografía de control en los casos de disfunción de la FAVP, considerando disfunción una presión venosa dinámica > 200 mm/Hg con flujos de 300 ml/min, Kt/V < 0,8 o recirculación > 25%).
Protocolo
El tratamiento de elección inicial en el caso de las estenosis (figura 1) de las FAVP fue la angioplastia transluminal percutánea (ATP) llevada a cabo por radiólogos intervencionistas, salvo en estenosis múltiple o largas u obstrucción completa de la vena de drenaje. Esta se realizó por punción anterógrada de la fístula protésica. Tras un estudio de eco-Doppler y fistulografía, se abordaron las estenosis con guía hidrofílica Terumo 0,035" colocando un introductor 6 F. La indicación de ATP se basó en el estudio morfológico de las estenosis, midiendo gradientes de presión únicamente en casos dudosos. El calibre del balón fue de 6 mm para las estenosis intraprotésicas, utilizándose diámetros de 7 a 8 mm a nivel de la anastomosis o de venas nativas. En caso de estenosis resistentes o recurrentes se utilizaron catéteres cutting balloon (sobre guía de 0,014") de similar calibre a los convencionales. Se colocó un stent en casos de estenosis centrales cuya reparación quirúrgica obligaría a intervenciones quirúrgicas muy invasivas.

Figura 1. Protocolo de actuación en la disfunción de la fístula arteriovenosa protésica por estenosis
ATP: angioplastia transluminal percutánea.
Las indicaciones para tratamiento quirúrgico de las estenosis se limitan a estenosis persistentes (resultado subóptimo de la dilatación percutánea) o estenosis recurrentes en menos de tres meses, realizándose en estos casos un análisis del lugar estenosado mediante la técnica quirúrgica precisa en cada caso (si existía estenosis en anastomosis venosa, se realizó bypass a vena proximal; si la estenosis era intraprotésica, se sustituyó parcialmente la prótesis; y si la estenosis se encontraba en la anastomosis arterial, se llevaba a cabo una nueva anastomosis proximal siempre y cuando no hubiera estenosis arterial distal [por el riesgo de agravar la isquemia]).
Las trombosis (figura 2) se trataron de forma urgente para evitar la utilización de catéteres innecesarios. Se realizó trombectomía quirúrgica con catéter de Fogarty. Si el cirujano no encontró causa para la trombosis, se realizó fistulografía de control de forma urgente y se trataron las estenosis detectadas mediante ATP. Si el cirujano detectó la causa de esta, se corrigió mediante puente protésico de la zona estenosada.
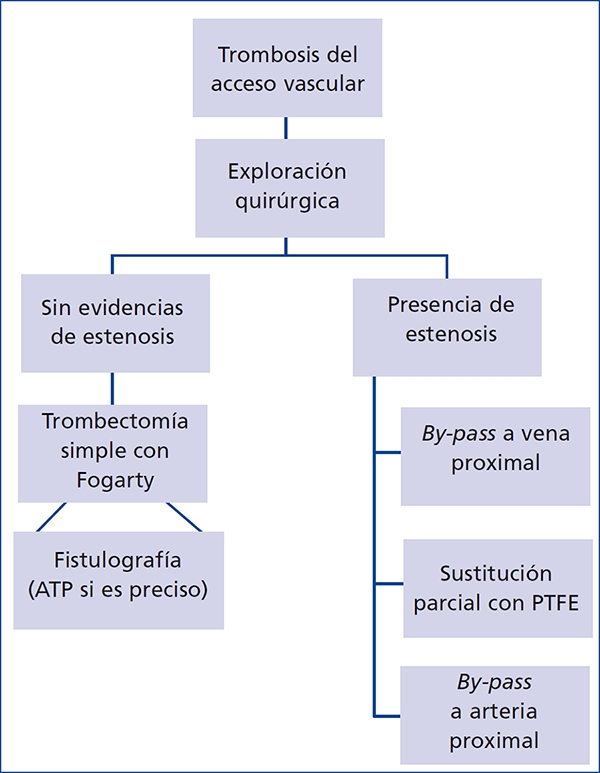
Figura 2. Protocolo de actuación en la trombosis de la fístula arteriovenosa protésica
ATP: angioplastia transluminal percutánea; PTFE: politetrafluoroetileno.
Definiciones y análisis estadístico
Supervivencia primaria: tiempo transcurrido hasta la primera trombosis de la FAVP.
Supervivencia secundaria: tiempo transcurrido hasta la trombosis definitiva.
Tasa de trombosis: episodios de trombosis/FAVP en riesgo/año.
Tasa de ingresos relacionados con la trombosis de la FAVP.
Tras la reparación quirúrgica por trombosis, se consideró permeable la FAVP si se pudo utilizar en la siguiente sesión de diálisis, evitando la colocación de un catéter venoso central (CVC).
El análisis estadístico se realizó con el programa SPSS utilizando curvas de supervivencia de Kaplan-Meier y comparando mediante el test de log-rank.
Ningún paciente recibió tratamiento antiagregante o anticoagulante como indicación de mantenimiento de la permeabilidad del acceso vascular.
Resultados
Se incluyeron un total de 96 FAVP en 88 pacientes para el estudio y seguimiento dentro del protocolo. Treinta y seis de las FAVP fueron LOOP y las restantes 60 fueron HAX.
Durante el período de estudio, siguiendo el protocolo, fueron necesarios 131 ATP, 15 stents, 109 trombectomías y 52 puentes a vena proximal para el mantenimiento de la permeabilidad de las FAVP.
No se produjeron muertes relacionadas con los procedimientos (tanto en la incorporación de la FAVP como en sus reparaciones) y solo se produjo una infección tras la colocación de un stent que precisó su retirada. Tampoco se produjeron embolismos pulmonares ni en la arteria humeral. La tasa de permeabilidad tras el tratamiento quirúrgico de una trombosis fue del 80%, evitándose la colocación de un CVC en el 80% de los episodios de trombosis.
Al finalizar el estudio el 63,5% (n = 61) de las FAVP estaban permeables y el 36,4% (n = 35) de las fístulas estaban trombosadas. El 38,5% (n = 37) de las fístulas seguían permeables cuando el paciente falleció. El 5,1% (n = 5) de los pacientes se trasplantaron con la FAVP permeable. Al finalizar el seguimiento, el 19,7% (n = 19) seguían permeables con el paciente en programa de hemodiálisis.
La tasa anual de ingresos hospitalarios relacionados con la trombosis de las FAVP fue de 0,03 ingresos/paciente/año.
La tasa anual de trombosis de las FAVP durante este período fue de 0,45.
Permeabilidad primaria
La permeabilidad primaria media global (figura 3) fue de 2,55 años, con un intervalo de confianza (IC) al 95% (1,91-3,17). Al año la supervivencia es del 73,68%, a los dos años del 60,21% y a los tres años del 37,52%. Una fístula tipo LOOP tiene una supervivencia media de 2,1 años (0,65-3,55). Al año la supervivencia es del 62,99%, a los dos años del 56,7% y a los tres años del 41,34%. Una fístula tipo húmero-axilar tiene una supervivencia media de 2,6 años (2,02-3,23). Al año la supervivencia es del 79,9%, a los dos años del 61,96% y a los tres años del 41,59% (log-rank 0,33; p-valor 0,57) (figura 4).
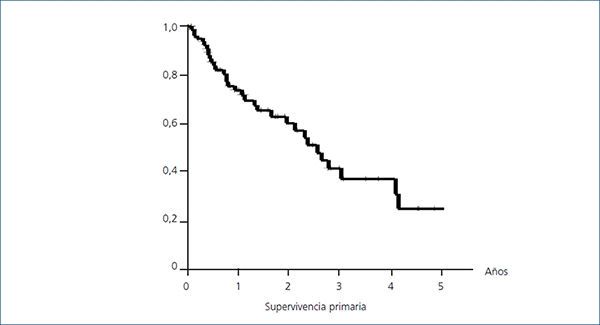
Figura 3. Supervivencia primaria (global)
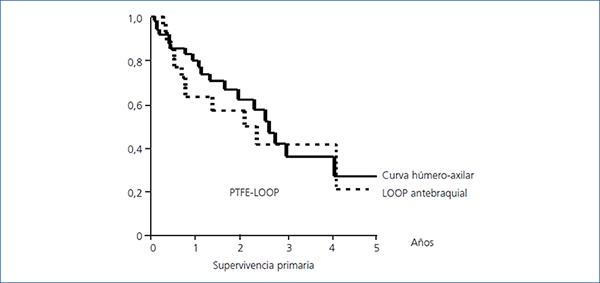
Figura 4. Supervivencia primaria de LOOP antebraquial/húmero-axilar
PTFE: politetrafluoroetileno.
Permeabilidad secundaria
La supervivencia secundaria media fue de 4,65 años, con un IC al 95% (3,96-5,34). Al año sobrevive el 89,49% de las fístulas, a los dos años sobrevive el 84,07% y a los tres años el 66,84% (figura 5). Las fístulas tipo LOOP tienen una supervivencia media de 4,13 años (1,84-6,43). Al año sobreviven el 87,88%, a los dos años el 81,06% y a los tres años el 50,66%. Las fístulas tipo húmero-axilar tienen una supervivencia media de 5,71 años (2,63-8,79). Al año sobreviven el 90,54%, a los dos años el 86,07% y a los tres años el 75,46% (log rank 1,94; p-valor 0,1633) (figura 6). Aunque la permeabilidad de las HAX es superior a la de las LOOP, no existen diferencias estadísticamente significativas.

Figura 5. Supervivencia secundaria (global)

Figura 6. Supervivencia secundaria (loop antebraquial/húmero-axilar)
Discusión
A pesar de presentar una mayor tasa de complicaciones que las FAV-n, las FAVP pueden ser una excelente solución en pacientes con un sistema venoso superficial agotado y, en nuestra experiencia, pueden ser además el acceso definitivo en pacientes ancianos (casi un 40% de nuestros pacientes fallecieron con la FAVP permeable). La intervención quirúrgica no tiene una complejidad técnica muy superior frente a una FAV-n y se puede realizar bajo anestesia local en régimen ambulatorio10. Además, si se aplican protocolos de mantenimiento, es posible rescatar la mayoría de las FAVP, alcanzando tasas de permeabilidad del 90% al año y superiores al 50% a los tres años10-12.
En nuestro centro existe un grupo multidisciplinar de especialistas en accesos vasculares para hemodiálisis desde hace 10 años integrado por nefrólogos, radiólogos y cirujanos. Se han diseñado protocolos de seguimiento e indicadores de calidad asistencial8,9. Además, se ha realizado un reparto del trabajo entre los servicios implicados:
- El seguimiento clínico de las FAVP, así como el diagnóstico de las disfunciones, lo realiza el Servicio de Nefrología y se ha hecho un especial esfuerzo en la detección de las disfunciones de forma precoz.
- El tratamiento de las disfunciones (tanto estenosis como trombosis) de las FAVP puede realizarse por métodos radiológicos o quirúrgicos. En general, la ventaja de las técnicas radiológicas frente a las quirúrgicas es el «ahorro» de territorio vascular proximal, y su desventaja, la necesidad de un mayor número de procedimientos para mantener permeable la FAVP13-21.
El protocolo diseñado en nuestro centro se basa en las recomendaciones DOQI adaptadas a nuestra disponibilidad de medios. Nuestro objetivo nunca ha sido comparar técnicas, sino aplicar en cada caso la más apropiada dependiendo de la disponibilidad de medios y la experiencia del personal.
Se ha considerado el tratamiento de las trombosis como un procedimiento urgente para evitar la colocación de CVC. La disponibilidad de la sala de radiología vascular en nuestro centro tiene un horario limitado, no pudiendo realizarse procedimientos urgentes; por tanto, el tratamiento de las trombosis lo realizó siempre el Servicio de Cirugía, por disponer de una guardia de 24 horas. Por otro lado, el diagnóstico y el tratamiento de las estenosis se realizó en la mayoría de los casos de forma programada por el Servicio de Radiología. Este abordaje tiene la ventaja de realizar el diagnóstico y el tratamiento de la disfunción en el mismo procedimiento, reservando la cirugía para los casos de persistencia o recidiva.
La aplicación rigurosa de este protocolo consigue, en nuestra experiencia, mantener unos indicadores de calidad asistencial acordes con los que exigen las guías nacionales e internacionales6,7 para el tratamiento de las disfunciones y trombosis de las FAVP: porcentaje de permeabilidad a los tres años superior al 50% y tasa de trombosis inferior a 0,5 episodios por paciente y año.
Estos datos tienen repercusión en otros indicadores de calidad asistencial, ya que las FAV son una fuente importante de morbilidad e ingresos hospitalarios. Así, en nuestro centro, las complicaciones del acceso vascular no son la causa fundamental de ingreso, con 0,1 episodios por paciente y año9, es decir, la mitad de lo publicado en otras series3, y en concreto las hospitalizaciones relacionadas con trombosis de las FAVP mínimas.
Creemos firmemente que los mejores resultados en el mantenimiento de las FAVP se obtienen con su abordaje multidisciplinar.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Referencias Bibliográficas
1. Spanish Registry of Renal Patients. Dialysis and renal transplants in Spain. 2006 Report. Nefrologia 2009;29(6):525-33. [ Links ]
2. Rodríguez Hernández JA, López Pedret J, Piera L. Vascular access in Spain: distribution, morbidity and surveillance systems. Nefrologia 2001;21(1):45-51. [ Links ]
3. Ethier J, Mendelssohn DC, Elder SJ, Hasegawa T, Akizawa T, Akiba T, et al. Vascular access use and outcomes: an international perspective from the dialysis outcomes and practice patterns study. Nephrol Dial Transplant 2008;23:3219-26. [ Links ]
4. Roca Tey R. Vascular access for haemodialysis: an unresolved issue. Nefrologia 2010;30(3):280-7. [ Links ]
5. Malek T, Alvarez-Ude F, Gil T, Moledous A, López-Collado M, Núñez C, et al. Changes in vascular access in a dialysis unit in recent years: planning problems, change in preferences, or demographic change? Nefrologia 2008;28(5):531-8. [ Links ]
6. Rodríguez Hernández JA, González Parra E, Julián Gutiérrez JM, Segarra Medrano A, Almirante B, Martínez MT, et al.; Sociedad Española de Nefrología. Vascular access guidelines for hemodialysis. Nefrologia 2005;25 Suppl 1:3-97. [ Links ]
7. Vascular Access 2006 Work Group. Clinical practice guidelines for vascular access. Am J Kidney Dis 2006;48 Suppl 1:S176-247. [ Links ]
8. Jiménez-Almonacid P, Gruss E, Lorenzo S, Lasala M, Hernández T, Portolés J, et al. Definition of processes and indicators for the management of vascular accesses for hemodialysis. Cir Esp 2007;81(5):257-63. [ Links ]
9. Gruss E, Portolés J, Jiménez P, Hernández T, Rueda JA, del Cerro J, et al. Prospective monitoring of vascular access in HD by a multidisciplinary team. Nefrologia 2006;26(6):703-10. [ Links ]
10. Jiménez-Almonacid P, Lasala M, Rueda JA, Gruss E, Hernández P, Pardo M, et al. Outpatient surgery hemodialysis vascular access. Activity integrated into a general surgery department. Nefrologia 2010;30(4):452-7. [ Links ]
11. Jiménez-Almonacid P, Del Río JV, Lasala M, Rueda JA, Vorwald P, Fernández JM, et al. First non-autologous vascular access for hemodialysis: PTFE antebraquial loop. Nefrologia 2004;24(6):559-63. [ Links ]
12. Almonacid PJ, Pallares EC, Rodriguez AQ, Valdes JS, Rueda Orgaz JA, Polo JR. Comparative study of use of diastat versus standard wall PTFE grafts in upper arm hemodialysis access. Ann Vasc Surg 2000;14(6):659-62. [ Links ]
13. Green L, Lee D, Kucey D. A metaanalysis comparing surgical thrombectoy, mechanical thrombectomy, and pharmacomechanical thrombolysis for thrombosed dialysis grafts. J Vasc Surg 2002;36:939-45. [ Links ]
14. Uflacker R, Rajagopalan, Vujic I, Stutley E. Treatment of thrombosed dialysis access grafts: randomized trial of surgical thrombectomy versus mechanical thrombectomy with Amplatz device. J Vasc Interv Radiol 1996;7(2):185-92. [ Links ]
15. Turmel-Rodrigues L, Pengloan J, Baudin S, Testo D, Abaza M, Dahdah G, et al. Treatment of stenosis and thrombosis in haemodialysis fistulas and grafts by interventional radiology. Nephrol Dial Transplant 2000;15(12):2029-36. [ Links ]
16. Gelbfish GA. Surgery versus percutaneus treatment of thrombosed dialysis access grafts: is there a best method? J Vasc Interv Radiol 1998;9(6):875-7. [ Links ]
17. Schwartz C, McBrayer C, Sloan J, Meneses P, Ennis W. Thrombosed dialysis grafts: comparison of treatment with transluminal angioplasty and surgical revision. Radiology 1995;194(2):337-41. [ Links ]
18. Martson W, Criado E, Jaques P, Mauro M, Burnham SJ, Keagy BA. Prospective randomized comparison of surgical versus endovascular management of thrombosed dialysis access grafts. J Vasc Surg 1997;26(3):373-81. [ Links ]
19. Dougherty MJ, Calligaro KD, Schindler N, Raviola CA, Ntoso A. Endovascular versus surgical treatment for thrombosed hemodialysis grafts: a prospective, randomized study. J Vasc Surg 1999;30(6):1016-23. [ Links ]
20. Vega Menéndez D, Polo Melero JR, Flores A, Rueda JA, López Baena JA, García Pajares R, et al. Proximal vein by-pass in the treatment of venous stenosis in expanded polytetrafluoroethylene prosthesis for hemodialysis. Rev Clin Esp 2000;200(2):64-8. [ Links ]
21. Polo JR, Polo J, Vega D, Pacheco D, Gracia-Pajares R. Surgical treatment of stenosis and thrombosis in dialysis grafts. Dialyse-Journal 1999;66:242-5. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Pedro Jiménez-Almonacid,
Unidad de Cirugía General y del Aparato Digestivo,
Hospital Universitario Fundación Alcorcón,
Budapest 1, 28922, Alcorcón, Madrid
pjimenez@fhalcorcon.es
Enviado a Revisar: 2 Ene. 2013
Aceptado el: 10 Abr. 2013














