Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nefrología (Madrid)
versión On-line ISSN 1989-2284versión impresa ISSN 0211-6995
Nefrología (Madr.) vol.34 no.2 Cantabria 2014
https://dx.doi.org/10.3265/Nefrologia.pre2013.Dec.12261
ARTÍCULOS ORIGINALES
Prevalencia de anemia y su manejo clínico en la enfermedad renal crónica estadios 3-5 no en diálisis en Cataluña: estudio MICENAS I
Prevalence of anaemia and its clinical management in patients with stages 3-5 chronic kidney disease not on dialysis in Catalonia: MICENAS I study
Aleix Cases-Amenós1, Alberto Martínez-Castelao2, Joan Fort-Ros3, Jordi Bonal-Bastons4, M. Pilar Ruiz5, Martí Vallés-Prats6, Elisabeth Coll-Piera7, Josep M. Galcerán-Gui8, Investigadores del estudio MICENAS I*
1 Servicio de Nefrología. Hospital Clínic. Barcelona
2 Servicio de Nefrología. Hospital Universitari de Bellvitge. Barcelona
3 Servicio de Nefrología. Hospital Universitari Vall d'Hebron. Barcelona
4 Servicio de Nefrología. Hospital Universitari Germans Trias i Pujol. Barcelona
5Servicio de Nefrología. Hospital Moisés Broggi. Sant Joan Despí. Barcelona
6 Servicio de Nefrología. Hospital Universitari Josep Trueta. Girona
7 Servicio de Nefrología. Fundació Puigvert. Barcelona
8 Servicio de Nefrología. Fundació Althaia Manresa. Barcelona
*Grupo Formado por:
Investigadores del estudio MICENAS I: los siguientes investigadores también participaron en el presente estudio: Arias M. (Hospital Clínic, Barcelona), Perelló M. (Hospital Vall d´Hebron, Barcelona), Samon R. (Hospital Mollet, Barcelona), Agraz I. (Hospital Vall d´Hebron, Barcelona), Bayes B. (Hospital Germans Trias i Pujol, Barcelona), Cañas L. (Hospital Germans Trias i Pujol, Barcelona), Castellote E. (Hospital de Vic, Barcelona), Craver L. (Hospital Arnau de Vilanova, Barcelona), García R. (Hospital Palamós, Girona), Felip A. (Hospital Mataró, Barcelona), Lauzurica R. (Hospital Germans Trias i Pujol, Barcelona), Pou M. (Hospital Terrassa, Barcelona), Ballarín J. (Fundació Puigvert, Barcelona), Puig J.M. (Hospital del Mar, Barcelona), Puig C. (Hospital d'Igualada, Barcelona), Cao H. (Hospital del Mar, Barcelona), Collado S. (Hospital del Mar, Barcelona), Barbosa F. (Hospital del Mar, Barcelona), Martínez-Vea A. (Hospital Universitari Joan XXIII, Tarragona).
El estudio fue patrocinado por la Societat Catalana de Nefrologia con financiación de Roche Pharma en España.
Dirección para correspondencia
RESUMEN
Introducción: La anemia es una complicación frecuente de la enfermedad renal crónica (ERC). El objetivo de este estudio fue conocer la prevalencia de anemia en pacientes con ERC estadios 3-5 no en diálisis atendidos en consultas externas (CCEE) de Nefrología en Cataluña y su manejo clínico.
Metodología: Estudio epidemiológico, de cohorte transversal, multicéntrico, en condiciones de práctica clínica habitual. Recogida de datos mediante un e-CRD que incluía datos de filiación y aquellos relacionados con la anemia (hemoglobina, estatus férrico, tratamiento con agentes estimuladores de la eritropoyesis [AEE] y con otros coadyuvantes). Se definió anemia como unos niveles de hemoglobina < 13,5 g/dl en varones o < 12 g/dl en mujeres o pacientes que recibieran tratamiento con AEE.
Resultados: Se incluyeron 504 pacientes (56,4 % varones, edad media de 67,8 ± 15,5 años): 61,5 % presentaban ERC estadio 3, 30,2 % estadio 4 y 8,3 % estadio 5. Las principales causas de ERC fueron la vascular y la nefropatía diabética. La prevalencia de anemia fue del 58,5 % (n = 295); sin embargo, solo un 14,9 % de los pacientes tenían niveles de hemoglobina < 11 g/dl. Los niveles medios de hemoglobina disminuían y el tratamiento con AEE era más frecuente a medida que progresaba la ERC, pero no se observaron diferencias significativas respecto a la prescripción de hierro, según estadios. Los AEE e intervalos más frecuentemente prescritos fueron darbepoetina alfa con una dosis mediana de 40 μg/bisemanal, seguida por C.E.R.A., con una dosis mediana de 75 μg/mensual y epoetina beta con una dosis mediana de 5000 UI/semanal. De los pacientes con anemia (n = 295), un 36,3 % (n = 107) presentaban ferropenia y de ellos solo un 53,3 % recibía tratamiento con suplementos de hierro.
Conclusiones: Este estudio demuestra la alta prevalencia de anemia, la cual aumenta a medida que progresa la enfermedad, así como el buen control de la misma en la población de pacientes con ERC atendidos en CCEE de Nefrología en Cataluña. Este control se consigue con dosis moderadas de AEE y prescripción de suplementos de hierro en más del 50 % de los pacientes anémicos.
Palabras clave: Anemia, Enfermedad renal crónica, Agentes estimuladores de la eritropoyesis, Ferropenia.
ABSTRACT
Introduction: Anaemia is a common complication of chronic kidney disease (CKD). The aim of this study was to determine the prevalence and clinical management of anaemia in patients with stages 3-5 CKD not on dialysis treated in outpatient Nephrology clinics (OC) in Catalonia.
Methods: Epidemiological, cross-sectional cohort, multicentre study under routine clinical practice conditions. Data collection by electronic data collection log-book (e-DCL) including personal information and data related to anaemia (haemoglobin, iron status, treatment with erythropoiesis-stimulating agents [ESA] and other anaemia treatments). Anaemia was defined as haemoglobin levels <13.5g/dL in males or <12g/dL in females or patients who receive treatment with ESA.
Results: We included 504 patients (56.4% male, mean age of 67.8±15.5 years): 61.5% had stage 3 CKD, 30.2% stage 4 and 8.3% stage 5. The main causes of CKD were vascular and diabetic nephropathy. The prevalence of anaemia was 58.5% (n=295), however, only 14.9% of patients had haemoglobin levels <11g/dL. Mean haemoglobin levels decreased and ESA treatment was more common as CKD progressed, but no significant differences were observed regarding the prescription of iron, according to CKD stages. ESA and intervals most frequently prescribed were darbepoetin alfa with a median dose of 40μg/biweekly, followed by C.E.R.A. with a median dose of 75μg/month and epoetin beta with a median dose of 5,000IU/week. Among the patients with anaemia (n=295), 36.3% (n=107) had iron deficiency and only 53.3% of these patients were treated with iron supplements.
Conclusions: This study demonstrates the high prevalence of anaemia, which increases as the disease progresses and its good control in a CKD patient population treated in Nephrology outpatient clinics in Catalonia. This control is achieved with moderate doses of ESA and iron supplements prescribed in more than 50% of anaemic CKD patients.
Key Words: Anaemia, Chronic kidney disease, Erythropoiesis-stimulating agents, IIron deficiency.
Introducción
La enfermedad renal crónica (ERC) afecta aproximadamente a un 11% de la población adulta en España, según datos del estudio EPIRCE1, y se asocia a una elevada morbimortalidad, sobre todo a expensas de patología cardiovascular2,3. Además, la ERC se relaciona con una serie de complicaciones, entre las cuales se halla la anemia4, la cual se ha vinculado con una mayor morbimortalidad y progresión de la ERC.
La presencia de anemia se observa ya en estadios precoces de la ERC (estadio 3), pero su prevalencia se incrementa a medida que la insuficiencia renal progresa a estadios más avanzados5. La principal causa de la anemia en los pacientes con ERC es el déficit de eritropoyetina, aunque también se han implicado una disminución de la vida media de los hematíes, el déficit de hierro y vitaminas, así como otros factores5.
Desde la introducción de la eritropoyetina recombinante humana, los agentes estimuladores de la eritropoyesis (AEE) se han convertido en la piedra angular del tratamiento de la anemia de la ERC y han permitido reducir los requerimientos transfusionales, mejorar la calidad de vida, y reducir la hipertrofia ventricular izquierda y la morbimortalidad en estos pacientes6-10. Sin embargo, el objetivo de hemoglobina ha sido objeto de debate en los últimos años a raíz de recientes estudios aleatorizados y metaanálisis que han demostrado que la corrección total de la anemia con AEE no se asocia con una mejor supervivencia, una mejoría significativa de la calidad de vida, pero sí con un posible aumento de efectos adversos cardiovasculares11-16.
A raíz de estos resultados, las guías europeas del año 2010 recomendaban una hemoglobina objetivo entre 11 y 12g/dl, sin exceder intencionadamente de 13g/dl17 y la EMA (European Medicines Agency) aconseja no superar unos niveles de hemoglobina por encima de 12g/dl en pacientes tratados con AEE (Ref. EMEA/188068/2007)18.
El objetivo de este estudio fue establecer la prevalencia de anemia en pacientes con ERC en estadios 3, 4 y 5 no en diálisis, atendidos en consultas externas de Nefrología en Cataluña, y conocer su manejo terapéutico (niveles de hemoglobina conseguidos, prescripción de AEE, ferroterapia y otros tratamientos concomitantes) en la práctica clínica.
Material y métodos
Diseño del estudio y recogida de datos
Se trata de un estudio epidemiológico, transversal, multicéntrico, en condiciones de práctica clínica habitual.
Los datos del estudio fueron recogidos durante el año 2010. Se invitó a participar a todos los Servicios de Nefrología en Cataluña y se realizó una encuesta de viabilidad para todos los candidatos. Finalmente se incluyeron 19 centros (90,47% de los invitados), de los cuales 17 reclutaron pacientes (80,95% de los invitados). Dos de los centros invitados finalmente no participaron en el estudio. Los centros participantes aportaron los datos de todos los pacientes visitados consecutivamente en consultas externas de Nefrología que cumplieran los criterios de inclusión y exclusión y dieran su consentimiento a participar en el estudio durante una semana, intentando incluir el máximo de pacientes posible. Los datos se recogieron mediante un cuaderno de recogida de datos electrónico (e-CRD) específicamente desarrollado para el estudio. Se recopilaron datos demográficos de los pacientes (edad, género, peso, talla, estadio de la ERC, tiempo de diagnóstico de la ERC) y datos correspondientes a la anemia (niveles de hemoglobina, niveles de ferritina, índice de saturación de transferrina [IST], tratamiento con AEE, hierro, ácido fólico o vitamina B12). También se estimó el filtrado glomerular (FGe) mediante la fórmula de MDRD-4.
El estudio fue aprobado por los diferentes comités éticos de los hospitales participantes en él y los pacientes debían firmar un consentimiento informado para permitir la recogida de los datos de su historia clínica.
Selección de pacientes
La población objeto del estudio eran pacientes adultos con ERC y FGe inferior a 60ml/min/1,73m2 que no estuvieran en diálisis.
Criterios de inclusión:
- Pacientes con edad igual o superior a 18 años.
- Pacientes con diagnóstico clínico establecido de ERC en estadio 3, 4 y 5 no en diálisis atendidos en consultas externas de Nefrología de Cataluña.
- Pacientes que otorgaran su consentimiento informado por escrito para participar en el estudio.
Criterios de exclusión:
- Pacientes en cuya historia clínica no se disponía de una determinación de hemoglobina reciente (dos meses previos a la inclusión).
- Cualquier situación o estado del paciente que, a juicio del investigador, desaconsejase su participación en el estudio.
Análisis estadístico
Se definió anemia como unos niveles de hemoglobina <13,5g/dl en varones y <12g/dl en mujeres o tratamiento con AEE. Se definió ferropenia como unos niveles de ferritina <100ng/ml y/o IST<20%.
Las variables categóricas se describieron mediante frecuencias absolutas y relativas, incluyendo un intervalo de confianza del 95%. Para la descripción de las variables continuas se utilizó la media, la desviación típica, la mediana, el mínimo y el máximo, incluyendo el número total de valores válidos.
Para las variables cuantitativas se usaron pruebas paramétricas (t de Student o Anova) o no paramétricas (Mann-Whitney o Kruskal-Wallis), según procediera. Para las variables cualitativas se realizó el test de χ2.
Los resultados se consideraron estadísticamente significativos con una P inferior a 0,05.
Los análisis estadísticos se realizaron con el paquete estadístico SAS versión 9.1.3.
Resultados
Población de estudio
Se reclutaron un total de 531 pacientes, de los cuales 27 fueron excluidos por no cumplir los criterios de selección o no disponer de los datos necesarios para evaluar la variable principal, siendo valorables para el análisis 504 finalmente.
Las características de los pacientes incluidos en el estudio están expuestas en la tabla 1. El 61,5% de ellos presentaban ERC estadio 3, el 30,2% se hallaban en estadio 4 y el 8,3% restante en estadio 5. Las causas de la ERC están expuestas en la tabla 1, donde se observa que las etiologías principales son la nefropatía vascular y la diabética, aunque un alto porcentaje de pacientes estaban filiados como de causa desconocida.
Tabla 1. Características de los pacientes incluidos en el estudio. 
IMC: índice de masa corporal.
Datos analíticos sobre anemia y estatus del hierro
Los datos sobre la hemoglobina y el estatus del hierro están expuestos en la tabla 2, donde se recogen los niveles de hemoglobina, sideremia, ferritina e IST en función del estadio de la ERC. La prevalencia de anemia en la población objeto del estudio era del 58,5%, aunque solo el 14,9% de los pacientes presentaba niveles de hemoglobina <11g/dl. La media de hemoglobina de toda la cohorte fue de 12,6±1,6 g/dl, aunque se observa una tendencia a disminuir los niveles de hemoglobina a medida que avanza la ERC. Se observó una correlacion inversa entre FGe y niveles de hemoglobina (figura 1). La media de ferritina de todo el grupo estudiado fue de 158,4±135,8ng/ml, y la media del IST fue de 24,2±11,7%, sin diferencias significativas para la ferritina o el IST en función del estadio de la enfermedad. De los pacientes con anemia (n=295), un 36,3% (n=107) presentaban ferropenia (ferritina <100ng/ml y/o de IST<20%).
Tabla 2. Datos analíticos referentes a la anemia (según los distintos estadios de la enfermedad renal crónica). 
IST: índice de saturación de transferrina.

Figura 1. Correlación entre el nivel de hemoglobina y el filtrado glomerular.
Coef.: coeficiente de correlación Pearson (bivariante); FG: filtrado glomerular; Hb: hemoglobina;
n: número de pacientes; Sig: nivel de significación del test de correlación de Pearson.
Prevalencia de anemia en función de los datos demográficos
El perfil del paciente en función de la presencia o no de anemia está descrito en la tabla 3, sin encontrarse diferencias según el sexo, pero hallándose diferencias significativas en función de la edad (individuos de mayor edad presentan más anemia), de la etiología de la ERC (diabéticos y causa no filiada son las etiologías que presentan mayor prevalencia de anemia), del estadio de la ERC (a medida que progresa la ERC se observa una mayor presencia de anemia) y del FGe (menor FGe entre los pacientes con anemia).
Tabla 3. Perfil del paciente en función de la presencia de anemia. 
ERC: enfermedad renal crónica; FGe: filtrado glomerular estimado; IMC: índice de masa corporal; ns: no significativo.
Tratamientos prescritos para la anemia
El 40,5% de todos los pacientes estaba recibiendo algún tratamiento para la anemia en el momento de la visita. Los datos referentes al tratamiento para la anemia se exponen en la tabla 4, la tabla 5, la tabla 6, la tabla 7 y la tabla 8.
Tabla 4. Tratamiento de la anemia según el estadio de la enfermedad renal crónica. 
AEE: agentes estimuladores de la eritropoyesis; ns: no significativo.
Tabla 5. Tratamiento de la anemia según el estadio de la enfermedad renal crónica en pacientes con anemia. 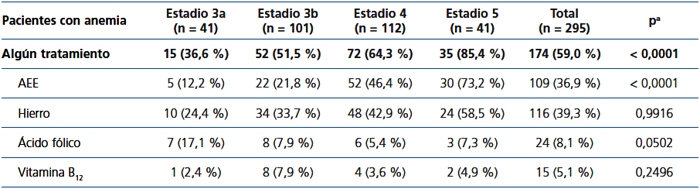
AEE: agentes estimuladores de la eritropoyesis.
aPrueba de χ2.
Tabla 6. Tratamiento con suplementos de hierro en pacientes anémicos y
con ferropenia según el estadio de la enfermedad renal crónica. 
aPrueba de χ2.
Tabla 7. Tratamiento para la anemia según niveles de hemoglobina. 
AEE: agentes estimuladores de la eritropoyesis; Hb: hemoglobina.
Tabla 8. Pacientes en tratamiento con hierro oral y hierro endovenoso según el estadio de la enfermedad renal crónica. 
aPorcentajes calculados sobre el total de pacientes con tratamiento para la anemia.
bPrueba de χ2/test de Fisher.
Nota: para un mismo paciente en tratamiento con hierro, podría indicarse más de un tipo de vía.
En la tabla 4 se describen los tratamientos para la anemia en función del estadio de la ERC. De los pacientes tratados, un 68,0% (n=136) estaba recibiendo un AEE, un 14,5% ácido fólico y un 10,0% vitamina B12. Un 66,0% del total de pacientes con insuficiencia renal crónica y anemia estaba recibiendo suplementos de hierro en el momento de la visita (61% por vía oral y 5% por vía intravenosa). Puede comprobarse como el porcentaje de pacientes tratados aumenta a medida que lo hace el estadio de la ERC (tabla 8). El tratamiento con AEE era más frecuente a medida que progresaba la ERC, mientras que el folato y la vitamina B12 se prescribieron más habitualmente en estadios más precoces, pero no se observaron diferencias significativas respecto a la prescripción de suplementos de hierro según los estadios. No se hallaron diferencias estadísticamente significativas respecto a la prescripción de hierro oral y endovenoso según el estadio de la ERC. Entre el subgrupo de pacientes anémicos se observaron resultados similares a los de la población global, aunque no alcanzaron significación para la vitamina B12 y el ácido fólico (tabla 5). Los AEE y los intervalos más frecuentemente prescritos en nuestra población fueron darbepoetina alfa con una dosis mediana de 40 μg/bisemanal, seguida por C.E.R.A (Continuous Erythropoietin Receptor Activator). con una dosis mediana de 75 μg/mensual, seguida por epoetina beta con una dosis mediana de 5000 UI/semanal. La prescripción de epoetina alfa en la población estudiada fue testimonial.
En la tabla 6 se muestra el tratamiento con suplementos de hierro en el subgrupo de pacientes anémicos con ferropenia, según el estadio de la ERC. De los pacientes con anemia y ferropenia, un 53,3% recibía tratamiento con hierro, el 12,1% no recibía suplementos con hierro y en el resto de los pacientes no estaba especificado en el e-CRD. La prescripción de hierro en pacientes anémicos y ferropénicos fue más frecuente en pacientes con ERC estadio 5 que en estadios más precoces.
En la tabla 7 se muestra el tratamiento para la anemia en función de los niveles de hemoglobina, observándose que un 67,9% de los pacientes con niveles de hemoglobina <11g/dl recibían AEE y/o ferroterapia y un 33,3% ambos. Asimismo, entre los pacientes con hemoglobina >12g/dl el 18% recibían AEE, así como en el 8,2% de aquellos con hemoglobina >13g/dl. De los tratados con AEE, un 43,4% tenían niveles de hemoglobina >12g/dl y un 12,5% niveles de hemoglobina >13 g/dl.
Discusión
Este estudio demuestra una alta prevalencia de anemia en la ERC estadios 3-5 no en diálisis y un adecuado control de esta en pacientes atendidos en 17 consultas externas de Servicios de Nefrología en Cataluña.
La prevalencia de anemia en esta población de pacientes con ERC estadios 3-5 no en diálisis fue del 58,5%, aunque solamente un 14,9% tenían cifras de hemoglobina inferiores a 11g/dl, es decir, que el 85,1% de los pacientes superarían el margen inferior de hemoglobina establecido por las guías europeas17. En el estudio multicéntrico observacional MERENA, realizado en 1129 pacientes con ERC estadios 3 y 4 controlados en consultas externas de Nefrología de España, la prevalencia de anemia fue algo inferior a la del estudio actual (51,3% frente a 58,5%), aunque hay que tener en cuenta que en dicho estudio no se incluyeron pacientes con ERC estadio 5 y que es posible que los criterios de derivación recientemente publicados hayan hecho que los pacientes actualmente atendidos en consultas externas de Nefrología tengan mayores comorbilidades, incluida la anemia, que en estudios anteriores, como el MERENA19. La prevalencia de anemia en 1058 pacientes con ERC no en diálisis de Italia fue del 16%, del 32% y del 51% en estadios 3, 4 o 5, respectivamente, aunque la definición de anemia en este estudio requería niveles menores de hemoglobina (hemoglobina <12g/dl en varones y <11g/dl en mujeres)20. En un reciente estudio prospectivo español de 439 pacientes con ERC no anémicos seguidos durante tres años, un 35% desarrollaron anemia, y estos tuvieron una progresión más rápida de su ERC, y mayor riesgo de hospitalizaciones, de eventos cardiovasculares y de mortalidad21.
Entre los factores demográficos que influyen en la presencia de anemia en la población estudiada se halla el estadio de la ERC (mayor prevalencia de anemia al disminuir el filtrado glomerular), la edad (mayor prevalencia de anemia en pacientes de mayor edad, probablemente relacionado con un menor FGe) y la etiología de la ERC (mayor prevalencia de anemia en nefropatía diabética y menor prevalencia en nefritis intersticial). Estos resultados coinciden con estudios previos que demuestran que la anemia es más frecuente y severa a cualquier nivel de FGe en pacientes diabéticos, comparados con los no diabéticos22,23.
La hemoglobina media de los pacientes con ERC fue relativamente elevada (12,6g/dl), teniendo en cuenta que el 40,5% de los pacientes estaba recibiendo algún tratamiento para la anemia. De los 187 pacientes tratados para la anemia, un 72,7% (136 pacientes) lo estaban siendo con AEE en el momento del estudio.
En estadios más precoces de la ERC, solo un 16,7% de los pacientes en estadio 3a y un 31,3% en 3b recibían algún tratamiento para la anemia, observándose unos niveles medios de hemoglobina de 13,6g/dl y 12,9g/dl, respectivamente. A medida que progresa la ERC se incrementa el porcentaje de pacientes que reciben algún tratamiento para la anemia, llegando a ser de hasta el 85,7% en el estadio 5 y alcanzándose una hemoglobina media de 11,4g/dl.
En los estadios más avanzados de la ERC (4 y 5), el control de la anemia se consigue con el uso más frecuente de los AEE, destacando la prescripción de AEE con una vida media más prolongada, que permiten un intervalo de administración bisemanal o mensual, lo que facilita el cumplimiento, es más cómodo para el paciente y mejora la estabilidad de la hemoglobina. Además, las dosis mensuales de los agentes de vida media más larga (darbepoetina o C.E.R.A.) fueron inferiores a las dosis equivalentes de eritropoyetina, aunque dado el carácter transversal del estudio estos datos deben interpretarse con cautela. Cabe destacar también de dicho estudio que el control de la anemia se consigue con dosis relativamente bajas de AEE (darbepoetina 80 μg/mes, C.E.R.A. 75 μg/mes) respecto a otros estudios con darbepoetina o C.E.R.A.13,24-26. Ello es importante porque las dosis elevadas de AEE se han asociado con una mayor mortalidad27 y las guías aconsejan considerar las dosis de AEE necesarias para conseguir los niveles de hemoglobina17.
En nuestro estudio, un 43,4% de los pacientes anémicos que recibían AEE tenían hemoglobina >12g/dl y un 12,5% hemoglobina >13g/dl, sugiriendo un sobretratamiento con AEE en un porcentaje significativo de ellos. Adicionalmente, en nuestro estudio se observó que 24 pacientes (32,0% de los que tenían hemoglobina <11g/dl) no recibían ningún tratamiento para la anemia.
Aunque los niveles medios de ferritina e IST de todo el grupo estaban por encima de los valores mínimos aconsejados en guías, un 36,3% de los pacientes anémicos presentaba ferropenia. Respecto a la ferroterapia, un 53,3% de los pacientes ferropénicos recibía tratamiento con suplementos de hierro (la mayoría en forma de suplementos de hierro oral), un 12% no recibía hierro y en un 34,5% no se aportó dicho dato. Asumiendo que en el caso en que no se aportaron datos los pacientes no recibían hierro, sugiere un aspecto de mejora en el tratamiento de la anemia en estos pacientes, como indican recomendaciones de expertos y las nuevas guías KDIGO (Kidney Disease Improving Global Outcomes), que promueven la ferroterapia para optimizar la eritropoyesis y la respuesta del tratamiento con AEE28,29.
La principal limitación de este estudio para la interpretación de sus resultados es su naturaleza transversal y que las conclusiones se obtienen a partir de unos niveles de hemoglobina y parámetros férricos en una sola determinación analítica, y a partir de la dosificación de un tratamiento en un momento puntual. Otra limitación proviene de la diferencia entre la definición de anemia válid a para todas las poblaciones (hemoglobina <13,5g/dl en varones y <12g/dl en mujeres) y los niveles de hemoglobina objetivo aceptados para un buen control de la anemia en los pacientes con ERC, definidos a raíz de los últimos estudios multicéntricos prospectivos realizados11-13, que se hallarían entre 10 y 12g/dl, tanto en varones como en mujeres. Además, en este estudio no se valoraron otros parámetros que influyen en el nivel de hemoglobina y la dosis de AEE, tales como presencia de inflamación, parámetros nutricionales, tratamiento con inhibidores de la enzima convertidora de angiotensina o antagonistas de los receptores de la angiotensina II, o niveles de hormona paratiroidea intacta. Además, este estudio no es extrapolable a la población global de pacientes con ERC, ya que muchos son atendidos en Atención Primaria, sino al subgrupo de pacientes atendidos en consultas externas de Nefrología, que presumiblemente tienen más comorbilidades, incluida la anemia.
La principal conclusión de este estudio es que los pacientes afectos de ERC estadios 3, 4 y 5 no en diálisis seguidos en consultas hospitalarias de Cataluña presentan una alta prevalencia de anemia, pero un adecuado control de ella en general. Dicho buen control se consigue con la combinación de dosis moderadas de AEE (sobre todo en fases avanzadas de la ERC) y la prescripción de hierro en más del 50% de aquellos que lo precisan. Sin embargo, se observa un porcentaje significativo de pacientes tratados con AEE y con niveles de hemoglobina >12g/dl y un cierto infratratamiento de la ferropenia, lo que sugiere oportunidades de mejora en el tratamiento de la anemia en nuestros pacientes.
Agradecimientos
Investigadores del estudio MICENAS I. Los siguientes investigadores también participaron en el presente estudio: Arias M. (Hospital Clínic, Barcelona), Perelló M. (Hospital Vall d´Hebron, Barcelona), Samon R. (Hospital Mollet, Barcelona), Agraz I. (Hospital Vall d´Hebron, Barcelona), Bayes B. (Hospital Germans Trias i Pujol, Barcelona), Cañas L. (Hospital Germans Trias i Pujol, Barcelona), Castellote E. (Hospital de Vic, Barcelona), Craver L. (Hospital Arnau de Vilanova, Barcelona), García R. (Hospital Palamós, Girona), Felip A. (Hospital Mataró, Barcelona), Lauzurica R. (Hospital Germans Trias i Pujol, Barcelona), Pou M. (Hospital Terrassa, Barcelona), Ballarín J. (Fundació Puigvert, Barcelona), Puig J.M. (Hospital del Mar, Barcelona), Puig C. (Hospital d'Igualada, Barcelona), Cao H. (Hospital del Mar, Barcelona), Collado S. (Hospital del Mar, Barcelona), Barbosa F. (Hospital del Mar, Barcelona), Martínez-Vea A. (Hospital Universitari Joan XXIII, Tarragona).
Referencias Bibliográficas
1. Otero A, Gayoso P, Garcia F, de Francisco AL; EPIRCE study group. Epidemiology of chronic renal disease in the Galician Population: results of the pilot Spanish Epirce study. Kidney Int Suppl 2005;(99):S16-9. [ Links ]
2. US Renal Data System: USRDS 2009 Annual Data Report. Bethesda, MD: National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases. [ Links ]
3. Rucker D, Tonelli M. Cardiovascular risk and management in chronic kidney disease. Nat Rev Nephrol 2009;5:287-96. [ Links ]
4. Kazmi WH, Kausz AT, Khan S, Abichandani R, Ruthazer R, Obrador GT, et al. Anemia: an early complication of chronic renal insufficiency. Am J Kidney Dis 2001;38:803-12. [ Links ]
5. Astor BC, Muntner P, Levin A, Eustace JA, Coresh J. Association of kidney function with anemia. The Third National Health and Nutrition Examination Survey (1988-1994). Arch Intern Med 2002;162:1401-8. [ Links ]
6. Obrador GT, Roberts T, St Peter WL, Frazier E, Pereira BJG, Collins AJ. Trends in anemia at initiation of dialysis in the United States. Kidney Int 2001;60:1875-84. [ Links ]
7. Foley RN, Parfrey PS, Harnett JD, Kent GM, Murray DC, Barre PE. The impact of anemia on cardiomiopathy, morbidity, and mortality in end-stage renal disease. Am J Kidney Dis 1996;28:53-61. [ Links ]
8. Moreno F, Sanz-Guajardo D, Lopez-Gomez JM, Jofre R, Valderrabano F. Increasing the hematocrit has beneficial effect on quality of life and is safe in selected haemodialysis patients. Spanish Cooperative Renal Patients Quality of life Study Group of the Spanish Society of Nephrology. J Am Soc Nephrol 2000;11:335-42. [ Links ]
9. Cody J, Daly C, Campbell M, Donaldson C, Khan I, Rabindranath K, et al. Recombinant human erythropoietin for chronic renal failure anemia in pre-dialysis patients. Cochrane Database Syst Rev 2005;(3):CD003266. [ Links ]
10. De Nicola L, Chiodini P, Zoccali C, Borrelli S, Cianciaruso B, Di Iorio B, et al.; SIN-TABLE CKD Study Group. Prognosis of CKD patients receiving outpatient nephrology care in Italy. Clin J Am Soc Nephrol 2011;6:2421-8. [ Links ]
11. Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, et al.; CHOIR Investigators. Correction of anemia with epoetin alfa in chronic kidney disease. N Engl J Med 2006;355:2085-98. [ Links ]
12. Drüeke TB, Locatelli F, Clyne N, Eckardt KU, Macdougall IC, Tsakiris D, et al.; CREATE investigators. Normalization of hemoglobin level in patients with chronic kidney disease and anemia. N Engl J Med 2006;355:2071-84. [ Links ]
13. Pfeffer MA, Burdmann EA, Chen CY, Cooper ME, de Zeeuw D, Eckardt KU, et al.; TREAT investigators. A trial of darbepoetin alfa in type 2 diabetes and chronic kidney disease. N Engl J Med 2009;361:2019-32. [ Links ]
14. Palmer SC, Navaneethan SD, Craig JC, Johnson DW, Tonelli M, Garg AX, et al. Meta-analysis: erythropoiesis-stimulating agents in patients with chronic kidney disease. Ann Intern Med 2010;153:23-33. [ Links ]
15. Clement FM, Klarenbach S, Tonelli M, Johnson JA, Manns BJ. The impact of selecting a high hemoglobin target level on health-related quality of life for patients with chronic kidney disease: a systematic review and meta-analysis. Arch Intern Med 2009;169:1104-12. [ Links ]
16. Parfrey PS, Lauve M, Latremouille-Viau D, Lefebvre P. Erythropoietin therapy and left ventricular mass index in CKD and ESRD patients: a meta-analysis. Clin J Am Soc Nephrol 2009;4:755-62. [ Links ]
17. Locatelli F, Aljama P, Canaud B, Covic A, De Francisco, Macdougall IC, et al.; Anemia Working group of European Best Practice (ERBP). Target haemoglobin to aim for with erythropoiesis-stimulating agents: a position statement by ERBP following publication of the Trial to Reduce Cardiovascular Events with Aranesp Therapy (TREAT) study. Nephrol Dial Transplant 2010;25:2846-50. [ Links ]
18. Ref.EMEA/188068/2007 European Medicines Agency starts review of the safety of epoetins. Available at: http://www.halmed.hr/upl/novosti/18806807en.pdf. [ Links ]
19. Martínez-Castelao A, Górriz JL, Portolés JM, De Alvaro F, Cases A, Luño J, et al. Baseline characteristics of patients with chronic kidney disease stage 3 and stage 4 in Spain: the MERENA observational cohort study. BMC Nephrol 2011;12:53. [ Links ]
20. De Nicola L, Minutolo R, Chiodini P, Zoccali C, Castellino P, Donadio C, et al.; Target Blood Pressure LEvels in Chronic Kidney Disease (TABLE in CKD) Study Group. Global approach to cardiovascular risk in chronic kidney disease: reality and opportunities for intervention. Kidney Int 2006;69:538-45. [ Links ]
21. Portolés J, Gorriz JL, Rubio E, de Alvaro F, García F, Alvarez-Chivas V, et al.; NADIR-3 Study Group. The development of anemia is associated to poor prognosis in NKF/KDOQI stage 3 chronic kidney disease. BMC Nephrol 2013;14:2. [ Links ]
22. Dikow R, Schwenger V, Schomig M, Ritz E. How should we manage anemia in patients with diabetes? Nephrol Dial Transplant 2001;17:67-72. [ Links ]
23. Bosman DR, Winker AS, Marseden JT, MacDougall IC, Watkins PJ. Anaemia with erythropoietin deficiency occurs early in diabetic nephropaty. Diabetes Care 2001;24:495-9. [ Links ]
24. Agarwal AK, Silver MR, Reed JE, Dhingra RK, Liu W, Varma N, et al. An open-label study of darbepoetin alfa administered once monthly for the maintenance of haemoglobin concentrations in patients with chronic kidney disease not receiving dialysis. J Intern Med 2006;260:577-85. [ Links ]
25. Minutolo R, Zamboli P, Chiodini P, Mascia S, Vitiello S, Stanzione G, et al. Conversion of darbepoetin to low doses of CERA maintains hemoglobin levels in non-dialysis chronic kidney disease patients. Blood Purif 2010;30:186-94. [ Links ]
26. Frimat L, Mariat C, Landais P, Koné S, Commenges B, Choukroun G. Anaemia management with C.E.R.A. in routine clinical practice: OCEANE (Cohorte Mircera patients non-dialyses), a national, multicenter, longitudinal, observational prospective study, in patients with chronic kidney disease not on dialysis. BMJ Open 2013;3(3):e001888. pii: e001888. doi: 10.1136/bmjopen-2012-001888. [ Links ]
27. Cuevas X, García F, Martín-Malo A, Fort J, Lladós F, Lozano J, et al. Risk factors associated with cardiovascular morbidity and mortality in Spanish incident hemodialysis patients: two-year results from the ANSWER Study. Blood Purif 2011;33(1-3):21-9. [ Links ]
28. Besarab A, Coyne DW. Iron supplementation to treat anemia in patients with chronic kidney disease. Nat Rev Nephrol 2010;6:699-710. [ Links ]
29. KDIGO. Clinical Practice Guideline for Anemia in Chronic Kidney Disease. Kidney Int Suppl 2012;2:279-335. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Aleix Cases-Amenós,
Servicio de Nefrología,
Hospital Clínic,
Villarroel 170, 08036 , Barcelona
E-mail: acases@clinic.ub.es
Enviado a Revisar: 6 Sep. 2013
Aceptado el: 11 Dic. 2013














