Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO  Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.20 no.3 Madrid may./jun. 2005
Original
Niveles plasmáticos y eritrocitarios de zinc y cobre en pacientes críticos con nutrición parenteral y su relación con el contenido de las fórmulas: estudio preliminar
A. M.ª Menéndez*,**, H. Montemerlo*,**, A. R. Weisstaub***, S. Alloatti***, F. Rusi**, M.ª E. Guidoni*,**, C. Casávola****, A. Piñeiro***
y M.ª L. Pita Martín de Portela***
| Resumen Objetivo: Estudiar, en pacientes graves que requirieron nutrición parenteral, la relación entre las cantidades de Zn y Cu presentes en las fórmulas, la evolución clínica y los cambios en algunos parámetros bioquímicos (niveles plasmáticos y eritrocitarios de Zn y Cu) durante terapéutica nutricional parenteral. (Nutr Hosp 2005, 20:189-196) Palabras clave: Zinc. Cobre. Nutrición Parenteral. Paciente crítico. | PLASMATIC AND ERYTHROCYTIC ZINC AND COPPER LEVELS IN CRITICALLY ILL PATIENTS ON PARENTERAL NUTRITION AND THEIR RELATIONSHIP WITH FORMULAS CONTENT: PRELIMINARY STUDY Abstract Objectives: To study in severe patients that required parenteral nutrition the relationship between Zn and Cu amounts present in formulas, the clinical course and changes in some biochemical parameters (plasmatic and erythrocytic Zn and Cu levels) during the parenteral nutrition therapy. (Nutr Hosp 2005, 20:189-196) Key words: Zinc. Copper. Parenteral nutrition. Critically ill patient. |
Correspondencia: Dra. M.ª Luisa Pita Martín de Portela
Cátedra e Nutrición
Facultad de Farmacia y Bioquímica. UBA
Junín 956, 2p
1113 Buenos Aires (Argentina)
E-mail: mportela@ffyb.uba.ar
Recibido: 26-V-2004.
Aceptado: 18-VI-2004.
Financiado por UBA. Subsidio B 103.
Introducción
El zinc (Zn) y el cobre (Cu) son micronutrientes minerales esenciales que regulan numerosos procesos metabólicos y cuya deficiencia produce anormalidades fisiológicas y estructurales1,2.
La deficiencia de Zn ha sido descrita en casi todas las especies animales, presentando como síntomas generales: hiperqueratosis y paraqueratosis de la piel, esófago y estómago, dermatosis, alopecia, lesiones oculares, atrofia testicular, retardo del crecimiento y anorexia. En el caso de deficiencias marginales se ha descrito disminución de la cicatrización de las heridas y alteraciones de la función inmunitaria3,4. Las necesidades diarias para el adulto son discutidas y los estudios basados en la técnica de balance han evidenciado que el adulto normal necesita absorber, en promedio, 2,2 mg/día5,6.
La deficiencia de Cu, en ratas y en el hombre, produce leucopenia con neutropenia, anemia micro-cítica hipocrómica (ferropénica), alteraciones de tejido conectivo, acromotipia, desmielinización y pancitopenia7. Las necesidades diarias de Cu son más discutidas que las de Zn y las cifras sugeridas se basan en algunos estudios basados en la técnica de balance5,6.
Sin embargo, las cantidades de estos minerales que deben ser aportadas por vía parenteral presentan diferencias sustanciales con las de la alimentación oral, donde se debe tener en cuenta la absorción intestinal y la biodisponibilidad6. En la nutrición parenteral total (NPT) los nutrientes llegan directamente al torrente sanguíneo y los requerimientos de Zn y Cu en pacientes graves son motivo de discusión8,9. Además, los mecanismos de homeostasis de estos micronutrientes tanto en individuos sanos como en el paciente grave están interrelacionados de modo no claro. En el pasado, los pacientes que recibieron NPT sin agregado de estos micronutrientes han manifestado alteraciones en los niveles plasmáticos y síntomas clínicos, indicativos de deficiencia aguda de Zn y/o de Cu10.
Por otra parte, tanto el exceso de Zn como el de Cu pueden producir efectos adversos asociados con el deterioro del estado nutricional y alteraciones en la respuesta inmune6. En función de las evidencias clínicas se sugiere precaución en su administración en las fórmulas parenterales puesto que podrían administrarse, en algunos casos, cantidades insuficientes para lograr la recuperación del paciente grave o, en otras situaciones, cantidades que pueden producir manifestaciones de toxicidad10,11.
Sin embargo, la falta de conocimientos hace que se agreguen en las formulaciones parenterales empíricamente12. Además, los componentes que se utilizan para preparar las mezclas de NPT suelen estar contaminados con elementos traza no declarados en sus rótulos y en concentraciones variables según el tipo de fabricantes, componentes, lotes, etc., resultando una subestimación de las cantidades de Cu y Zn realmente administradas en relación a las prescriptas11. Por lo tanto, se debe conocer el contenido real de Cu y Zn en las fórmulas de NPT y efectuar el seguimiento de los pacientes con objeto de modificar los aportes en función de las necesidades. De este modo se podrían evitar tanto las deficiencias como los excesos, que pueden comprometer la evolución del paciente grave.
Objetivos
Ampliar la información acerca de las necesidades de Zn y Cu en pacientes graves, estudiando la relación entre las cantidades presentes en las fórmulas parenterales, la evolución clínica de los pacientes y los cambios en algunos parámetros bioquímicos (niveles plasmáticos y eritrocitarios de Zn y Cu) durante la terapéutica nutricional parenteral.
Material y métodos
El trabajo se realizó de acuerdo a las Normas íticas Internacionales. Los sujetos, o sus familiares a cargo, expresaron su consentimiento, de acuerdo a las Normas de Ética del Comité de Docencia e Investigación de los Centros Asistenciales privados participantes.
Población
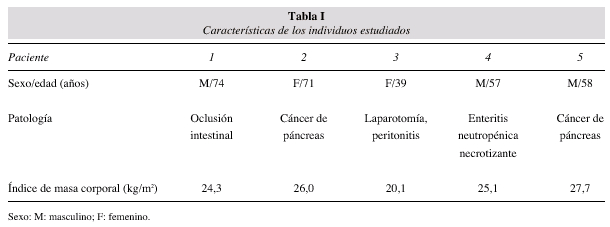
Se estudiaron 5 pacientes críticos, adultos, sometidos a cirugía mayor abdominal, que requirieron NPT, cuyas características figuran en la tabla I.
Fórmulas de nutrición parenteral
Las fórmulas de NPT fueron indicadas por los médicos y se elaboraron con productos farmacéuticos para vía endovenosa, disponibles en el mercado argentino. La elaboración de la NPT se realizó de acuerdo a las siguientes normativas: Normas de Buena Manufactura OMS, 1992/2002; Disposición de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica-ANMAT 2592/2003 de la Autoridad Sanitaria Argentina y el Sistema de Garantía de Calidad Certificado según Normas ISO 9001/2000.
En Argentina, el zinc y cobre se encuentran disponibles en envases con dosis individuales y en multidosis: 1) Dosis individuales: envases de sulfato de zinc con 0,4 mg/ml de Zn (Lab. Rivero) y envases de 1 mg/mL (Lab. FADA y Rivero). En cuanto al cobre son envases de sulfato de cobre de ,4 mg/mL de Cu (Lab. FADA y Rivero). 2) Multidosis: envase multi-dosis de elementos traza que contiene: de Zn 0,327 mg/mL y de Cu 0,076 mg/mL, además de hierro, selenio, cromo, molibdeno, manganeso, fluor, yodo (Tracuti®, Lab. Braun y Ritraz®, Laboratorio Rivero).
Determinaciones de laboratorio
En las fórmulas parenterales administradas se deter-minó el contenido de Zn y Cu al comienzo (To) y al final (Tf) del tratamiento. Las muestras de la NPT fueron previamente mineralizadas por vía seca, durante 12 horas en mufla a 550 °C, hasta cenizas blancas, disueltas en HNO3 p.a. y diluidas adecuadamente con agua ultrapura13.
Los indicadores bioquímicos determinados en los pacientes al comienzo (To) y al final (Tf) del tratamiento fueron: 1) en sangre entera, extraída en ayunas: hemoglobina (Hb) (método de la cianometahemoglobina); 2) en eritrocitos (GR) (previamente lavados con solución isotónica y hemolizados con agua ultrapura): Zn y Cu; 3) en plasma: Zn (ZnPl); 4) en suero: Cu (CuS).
Zn y Cu se determinaron por espectrofotometría de absorción atómica utilizando un espectrofotómetro Varian, modelo SpectrAA-20, con llama de aire-acetileno. Para el Zn se utilizó: slit de 1,0 mm y longitud de onda de 213,9 nm; para Cu: slit de 1,0 mm y longitud de onda de 327,4 nm. Todo el material fue previamente lavado con ácido nítrico al 20% y enjuagado con agua desionizada14.
Análisis estadístico: Los datos descriptivos se expresaron como promedio ± desvío estándar (DE). Se aplicó análisis de regresión y correlación simple con un nivel de confianza de 95% cuando fue necesario15.
Resultados
El contenido de Zn y Cu en las fórmulas parenterales administradas a los pacientes de las dos instituciones figura en la tabla II.
Evolución de los pacientes: dos de los 5 pacientes estudiados, que padecían uno cáncer de páncreas y el otro enteritis neutropénica necrotizante, fallecieron a consecuencia de sepsis con compromiso hemodinámico.
Los niveles de Zn en plasma y eritrocitos de los pacientes estudiados figuran en la tabla III.
Discusión
El hombre adulto contiene entre 2 y 3 g de Zn, distribuído, fundamentalmente, en hueso, tejido muscular y eritrocitos, siendo esencial para la actividad de más de 70 enzimas, de las cuales las más conocidas se relacionan con la utilización de la energía, la síntesis de proteínas y la protección oxidativa. El zinc juega, además, un papel fundamental en la estabilización de ciertas macromoléculas (incluyendo ciertos receptores nucleares de hormonas esteroides, tiroideas y retinoides) y de las membranas celulares; regula la transcripción, uniéndose a proteínas nucleares, formando complejos llamados "Zinc fingers". En general todas esas funciones están relacionadas con la capacidad del Zn de unirse a la histidina y cisteína, estabilizando los sitios activos1,4.
El cobre es otro micronutriente mineral esencial presente en el organismo humano adulto entre 50 y 120 mg. El 60% del contenido total del organismo se encuentra en músculo, piel y esqueleto, aunque los órganos con mayor concentración son hígado y cerebro. La sintomatología de su deficiencia, que se puede presentar en individuos con nutrición parenteral o con diarreas crónicas, se ha podido comprender al identificar cupro-proteínas (cupreínas) y enzimas cobre dependientes que intervienen en reacciones oxidativas relacionadas con el metabolismo del hierro, de los aminoácidos precursores de neurotransmisores, del tejido conectivo y con la destrucción de radicales libres2,6, 7.
Gran parte del avance en el conocimiento de las necesidades de Zn y Cu se ha debido a la administración de fórmulas para nutrición parenteral que no tenían incorporados estos micronutrientes o lo tenían en cantidad insuficiente. Las estimaciones de las necesidades de Zn y Cu aplicando el método factorial proporcionaron información para comenzar a administrar estos micronutrientes en las NPT11. Con esa base la AMA desde el año 1979 recomienda valores de 2,5 a 4 mg/día de Zn y 0,5 a 1,5 mg/día de Cu12 como requerimiento intravenoso para los pacientes adultos alimentados por vía parenteral (tabla V)7. Sin embargo, no hubo ni hay acuerdo unánime en las distintas Sociedades Científicas, y la American Society of Parenteral and Enteral Nutrition estableció en el año 2001 una dosis diaria de Zn de 2,5 a 5 mg y de Cu de 0,3 a 0,5 mg16. Para el Cu estas cifras representan casi la tercera parte de las aconsejadas por la AMA y ESPEN para pacientes adultos (tabla V).
En función de estos conocimientos, la práctica habitual es preparar una solución parenteral con 5 mg de Zn y 0,8 a 1,5 mg de Cu, con la que es factible ajustarse a las recomendaciones fijadas para la AMA, para el adulto, sin aparentes efectos adversos. En Argentina, tanto el Cu como el Zn, son usualmente agregados en la Nutrición Parenteral, como una mezcla de elementos traza o en soluciones individuales de sulfato de Cu y sulfato de Zn, que permiten administrar dosis mayores o menores en relación con los requerimientos particulares de cada paciente. Se debe tener en cuenta que las dosis indicadas por los médicos en nuestro país, para el paciente crítico durante la realización del trabajo, fueron mayores a las recomendadas por diferentes autores, especialmente para el Cu (Tabla V).
Por otra parte, se debe tener en cuenta que los nutrientes administrados en exceso implican riesgo de efectos adversos. Está comprobado que el exceso de Zn produce supresión de la respuesta inmune y deterioro del estado nutricional con respecto al Cu y al Fe. En el caso del cobre los efectos adversos comprobados incluyen alteraciones gastrointestinales, daño hepático, interacción con Zn, Fe y Mo, deterioro del estado nutricional con respecto al Zn y al Fe y disminución de la actividad fagocítica de los polimorfonucleares. Además, se deben cuidar particularmente los excesos de Cu en el caso de pacientes con nutrición parenteral que presenten colestasis o compromiso hepático9.
Por todo lo antedicho es de suma importancia en pacientes que reciben NPT evitar tanto la deficiencia como los excesos de Zn y Cu, para lo cual se impone utilizar indicadores bioquímicos que alerten acerca de ambos problemas. Sin embargo, la evaluación del estado nutricional con respecto a estos micronutrientes minerales no es fácil y constituye un campo de la nutrición en pleno desarrollo, ligado al avance en el conocimiento de sus funciones bioquímicas19. La determinación del elemento traza en estudio en la dieta administrada no asegura el conocimiento del estado nutricional debido a la existencia de tejidos que actúan como depósito de estos elementos minerales, y a complejos mecanismos homeostáticos que regulan sus metabolismos tanto en condiciones normales como patológicas20.
Las determinaciones de Zn y Cu en muestras biológicas tradicionales como suero, plasma y glóbulos rojos, son propuestas como los indicadores más comunes, pese a que presentan diversos inconvenientes, no existiendo, hasta la fecha, un indicador bioquímico único para establecer el estado nutricional con respecto al Zn o al Cu. Por ello, en el presente trabajo se decidió realizar las determinaciones de Zn plasmático, Cu sérico y Zn y Cu en eritrocitos, estudiando previamente los valores de referencia en individuos sanos de Buenos Aires. Dichos valores oscilan entre 42 y 111 µg/dL para el Zn plasmático y entre 1.100 y 1.700 µg/dL de GR21.
La concentración plasmática de Zn refleja el tamaño del "pool" de Zn intercambiable, pero puede interpretarse erróneamente, dado que varía como consecuencia de influencias fisiológicas y patológicas que la alteran, como la presencia de infecciones. Su disminución indica alteraciones metabólicas con riesgo de deficiencia clínica, pero también puede ser la consecuencia de redistribución tisular asociada a estrés metabólico22,23. El aumento de la IL1, que se produce en los casos de infección, inflamación y daño tisular produce captación de Zn por el hígado, médula ósea y timo, disminuyendo el Zn en hueso, piel e intestino24,25. La determinación de Zn en sangre entera o en eritrocitos refleja el estado nutricional en el período de vida media del eritrocito, por ser incorporado en el momento de la eritropoyesis26,27.
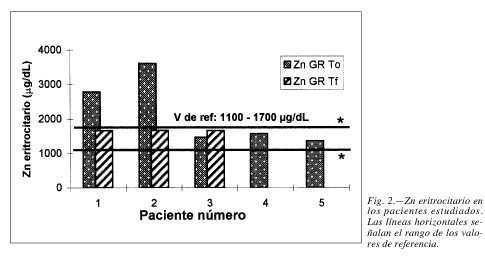
Las figuras 1 y 2 muestran los valores individuales de Zn en plasma y en eritrocitos en los pacientes estudiados a To y Tf, en los casos que se recuperaron. En dichas figuras se han señalado como valores de referencia los obtenidos en individuos normales de Buenos Aires (Argentina), con adecuación nutricional21.
En la figura 1 se puede observar que al inicio de la NPT, los niveles de Zn plasmático fueron sumamente variables, indicando la respuesta individual de redistribución del Zn corporal intercambiable de cada paciente a consecuencia del estrés de su patología y de la cirugía. Los valores a Tf indican la normalización durante el tratamiento. En la figura 2 se visualiza que al inicio de la NPT los niveles de Zn eritrocitario se encontraron dentro de rangos normales en 3 de los 5 pacientes, pero fueron superiores a los de referencia en 2 de ellos, normalizándose durante el tratamiento.
A pesar que los resultados del contenido de Zn en las fórmulas parenterales indican que se administraron cantidades superiores a las aconsejadas, los parámetros bioquímicos no indican en estos pacientes un exceso de Zn. Se debe tener en cuenta que existen diversas situaciones en las cuales está elevado el requerimiento de Zn: el estrés metabólico, que puede aumentar el requerimiento basal de Zn en 2 mg/d; las pérdidas elevadas de Zn en los 20 días posteriores a un trauma, y las pérdidas por los fluídos intestinales por fístulas que pueden representar varias veces los requerimientos normales10. Por ello, se ha considerado que la adición de 4,9 a 5,6 mg/d podría promover mejores niveles de Zn plasmáticos y balance positivo9,11.
La concentración de cobre en suero varía ampliamente, estando influída por la edad, sexo y estado fisiológico, por lo cual no constituye un buen indicador de estado nutricional. Nuestros valores en individuos sanos de Buenos Aires oscilaron entre 45 y 157 µg/dL (datos no publicados), siendo similares a los obtenidos en los estudios epidemiológicos de USA28 que han establecido como rangos de normalidad entre 70-140 µg/dL, para los varones, y 80-155 µg/dL para las mujeres.
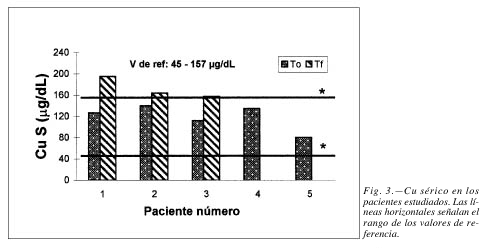
Las figuras 3 y 4 muestran los valores individuales de Cu en suero y eritrocitos en todos los pacientes estudiados a To y a Tf, en los casos que se recuperaron. Estos resultados evidenciaron que: al inicio del tratamiento el Cu sérico se encontró dentro de rangos normales en los 5 pacientes, pero todos los que se recuperaron incrementaron los valores por encima de los de referencia. En cuanto a los valores de Cu eritrocitario a T0, se encontró elevado sólo en uno de los pacientes que fallecieron y se incrementaron en 72% y 71% los valores ya elevados en dos de los tres pacientes que se recuperaron.
Estos resultados reflejarían los elevados valores de Cu hallados en las mezclas de NPT (tabla II), cantidades que no fueron prescriptas por el médico ni tampoco coinciden con los valores teóricos del protocolo de elaboración. El exceso de Cu en las mezclas de NPT podría provenir de la contaminación de las soluciones de nutrientes11 que son provistas por la industria farmacéutica y utilizadas para la preparación.
Por ello, es muy importante conocer la concentración final de Zn y Cu en las mezclas de NPT y la contribución que representa la contaminación con esos oligoelementos presente en cada uno de los componentes provistos por la industria farmacéutica para la preparación de la nutrición parenteral: aminoácidos, vitaminas, agua destilada estéril y sulfato de magnesio11. En este trabajo hemos encontrado que las mezclas de nutrición parenteral total administradas a los pacientes contenían más del doble de Zn y Cu de la cantidad agregada a la preparación (tabla II) según lo declarado en las etiquetas de los componentes.
Estos resultados evidencian que, en los pacientes estudiados, los niveles de Zn en las mezclas de NPT, aunque superiores a los aconsejados para pacientes graves, serían adecuados para evitar la deficiencia y el exceso en los pacientes estudiados en este trabajo. Sin embargo, los niveles de Cu serían elevados en el caso específico de estos pacientes críticos.
Conclusiones
• Las mezclas de NPT deben ser monitoreadas en su contenido de Zn y Cu debido a la variabilidad observada, controlando la contribución de cada uno de los componentes primarios que pueden contener estos micronutrientes como contaminantes no declarados.
• En los pacientes estudiados: 1) los niveles de Zn en las NPT serían adecuados para evitar la deficiencia y el exceso. 2) Los niveles de Cu serían ligeramente elevados. Por ello es importante reducir las dosis de Cu a administrar a los pacientes adultos en estado crítico y controlar las cantidades realmente administradas en las mezclas de NPT.
Referencias
1. Cousins R, Hempe JM: Zinc. En: Present Knowledge in Nutrition, 6a ed., Chap. 28; p. 251-260. ML Brown (ed.). Nutition Foundation, Washington DC, 1990. [ Links ]
2. O'Dell BL: Cooper. En: Present Knowledge in Nutrition, 6a ed., Chap. 29; ML Brown (Ed.) Nutrition Foundation. Washington DC. p. 261-267, 1990. [ Links ]
3. Aggett PJ, Gomerford JG: Zinc and human health. Nutr Rev 1995, 53:S16-S22. [ Links ]
4. King JC, Keen CL: En: Modern Nutrition in health and disease, 8.ª d. Cap. 10. Shils M, Olson J, Shike M, Lea & Febiger. Malvern. USA 1994, 214-230. [ Links ]
5. Food and Nutrition Board Subcommittee of The National Research Council Recommended Dietary Allowances. National Academy Press. Washington, DC, 1989. [ Links ]
6. Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Cooper, Iodine, Iron, Molybdenum, Nickel, Silicon, Vanadium and Zinc. Standing Committee on the Scientific Evaluation of Dietary References Intakes, Food and Nutrition Board & Institute of Medicine. National Academy of Sciences. Washington DC, 2001. [ Links ]
7. Turnlund JR: En: Modern Nutrition in health and disease, 8.º ed. cap. 11. Shils M, Olson J, Shike M Lea & Febiger. Mal-vern, USA, 1994. p. 231-241. [ Links ]
8. Greene HL, Hambidge KM, Schanle R, Tsang RC: Guidelines for the use of vitamins, trace elements, calcium, magnesium and phosphorus in infants and children receiving total parenteral nutrition: report of the Subcommittee on Pediatric Parenteral Nutrient Requirements from the Committee on Clinical Practice Issues of the American Society for Clinical Nutrition. Am J Clin Nutr 1988, 148:1324-42. [ Links ]
9. Okada A, Takagi Y: Trace element metabolism in parenteral and enteral nutrition. Nutrition 1995, 11:106-13. [ Links ]
10. Fleming CR: Trace elements metabolism in adult patients requiring total parenteral nutrition. Am J Clin Nutr 1989, 49:573-9. [ Links ]
11. Pluhator-Murton MM, Fedorak RN, Audette R, Marriage BJ, Yascoff RW, Gramlich R: Trace Element Contamination of TPN. 1. Contribution of component Solutions, JPen 1999, 23:222-7. [ Links ]
12. American Medical Association, Department of Foods and Nutrition: Guidelines for essential trace element preparations for parenteral use: a statement by an expert panel. JAMA 1979, 241(19):2051-2054. [ Links ]
13. Official Methods of Analysis of the AOAC. 13th edition. Washington DC. Association of Official Analytical Chemists, 1980. [ Links ]
14. Perkin Elmer Corp. Analytical method for atomic absorption spectrophotometry. Perkin Elmer corp. Norwalk CT 1971 [ Links ]
15. Sokal RR, Rohi FJ: Biometry: the principles and practice of statistics in biological research. WH Freeman and Company; San Francisco 1969. [ Links ]
16. Shenkin A: Trace elements and vitamins in parenteral and enteral nutrition. En: Basics in Clinical Nutrition. 2.ª ed. Chap. 3.6. p. 66-67. Edited for ESPEN Courses, Czech Republic, 2000. [ Links ]
17. ASPEN Board: Guidelines for the Use of Parenteral and Enteral Nutrition in Adult and Pediatric Patients. JPEN 2002, 25:31SA. [ Links ]
18. Prelack O: Micronutrient supplementation in the criticall III patients: strategies for clinical practice. J Trauma 2001, 51(2):601-20. [ Links ]
19. Solomons NW: On the assessment of zinc and copper nutriture in man. Am J Clin Nutr 1979, 32:856-871. [ Links ]
20. Pita Martín de Portela ML: En Aplicación de la bioquímica a la evaluación del estado nutricional. Cap. IV. Pita Martin de Portela ML, Río ME, Slobodianik NH. López Libreros Editores 1997, 97-120. [ Links ]
21. Weisstaub A, Menéndez AM, Alloatti S, Montemerlo H, Pastene H, De Portela ML: Ingesta de zinc y niveles plasmáticos y eritrocitarios en un grupo de adultos del Gran Buenos Aires. XXVI Reunión Anual del Capítulo Argentino de la Sociedad Latinoamericana de Nutrición (CASLAN). Mendoza, 2-4 octubre 2003. [ Links ]
22. Beisel WR, Pekarek RS, Wannemacher RW: Homeostatic mechanisms affecting plasma zinc levels in acute stress. Trace Elem in Humans Health and Dis 1976, 1:87-106. [ Links ]
23. Jacobs GM, Hambidge KM, Stall C, Pritts J, Nelson D: Daily variations in plasma zinc in normal adult women. Trace Elem in Man and Anim 1988, 6:491-2. [ Links ]
24. Schroeder JJ, Cousins RJ: Interleukin 6 regulates metallothionein gene expression and zinc metabolis in hepatocyte mono-layer cultures. Proc Natl Acad Sci 1990, 87:3137-3141. [ Links ]
25. Braunschweig CL, Sowers M, Kovacevich DS, Gretchen MH, August DA: Parenteral zinc supplementation in adult humans during the acute phase response increases the febrile response. J Nutr 1997, 127: 70-74. [ Links ]
26. Gibson RS: Assessment of zinc status. In: Principles of Nutitional Asessment. Chap 24.5 New York Oxford. Oxford University Press 1990, 542-553. [ Links ]
27. Ruz M, Cavan K, Bettger WJ, Gibson R: Erythrocytes, erythrocytes membranes, neutrophils and platelets as biopsy materials for the assesment of zinc status in humans. Bir J of Nutr 1992, 68:5115-5127. [ Links ]
28. Gibson RS: Assessment of Copper Status. In: Principles of Nutritional Assessment. Chap 24.2. New York Oxford. Oxford University Press 1990, 520-526. [ Links ]