Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.26 no.1 Madrid ene./feb. 2011
Cambios en la composición de la grasa y en la histomorfología hepáticas tras NPT, con y sin intestino ultra-corto
Changes in the fat composition and histomorphology of the liver in TPN, with and without ultra-short bowel
J. M. Morán1, A. Leal2, M.a T. Espín2, E. Maciá Botejara3, J.L. Amaya2, M.a I. Correa2 y J. Saenz Santamaría4
1Departamento de Terapéutica Médico-Quirúrgica. Cirugía Pediátrica. Facultad de Medicina. Universidad de Extremadura. Badajoz.
2Servicio de Cirugía General.
3Servicio de Medicina Interna.
4Servicio de Anatomía Patológica. Complejo Hospitalario Universitario de Badajoz. España.
Agradecemos las aportaciones económicas que, para la realización de este trabajo, provinieron de diversos proyectos de financiación pública y privada:
- Entidad financiadora: JUNTA de EX. Convocatoria de Ayudas Concertadas I+D 97/98.
- Entidad financiadora: F.E.D.E.R. PERÍODO: 2000/2006.
- Entidad financiadora: F.E.D.E.R. PERÍODO: 2000/2006.
Dirección para correspondencia
RESUMEN
Introducción: El síndrome de intestino corto es una insuficiencia grave intestinal cuya etiología más frecuente en adultos son la isquemia intestinal y la enfermedad inflamatoria y en niños las malformaciones congénitas, el vólvulo y la enterocolitis necrotizante, obligando al uso de la NPT. Pero el intestino está íntimamente relacionado con el hígado a través de la circulación entero-hepática y de diferentes sistemas endocrinos entero-hepáticos. La resección intestinal y la Nutrición Parenteral alterarán esta relación, pudiendo variar la composición del tejido hepático y su histomorfología. El objetivo de este trabajo es conocer más concretamente estos posibles cambios.
Materiales y métodos: Utilizamos 3 grupos experimentales: Grupo A (10cobayos), sometidos a una anestesia y laparotomía simple y nutridos durante 10 días con NPT. Grupo B (10cobayos), con resección intestinal yeyuno-ileal total y nutridos durante 10 días con NPT. Grupo Ctr (6 cobayos), sometidos a anestesia y laparotomía simple y nutridos oralmente. Tras este período se estudiaron muestras de sangre y de tejido hepático, tanto para el estudio de la grasa hepática (grasa total, proporciones de lípidos neutros y polares, proporciones de fosfolípidos y de ácidos grasos) como para estudio histológico.
Resultados: Los animales de los grupos A y B, sometidos a NPT, presentan incrementos significativos en la glucemia y en los triglicéridos séricos, y descensos en el coles-terol. Disminuyen el peso y la proporción de grasa por g de hígado, máxime en el GB, así como el cociente LP/LN en los GA y GB. Se modifican las proporciones de fosfolí-pidos, disminuyendo el fosfatidilinositol y aumentando la fosfatidiletanolamina; disminuyendo también el cociente de los AG w6/w3. Histológicamente, aparece una esteato-hepatitis, con disminución marcada de la densidad mito-condrial, siendo mas intensos en el GB.
Conclusión: la NPT altera la composición de la grasa hepática y la histomorfológica del hígado. El SIUC tiene más mecanismos lesionales, potenciándose el daño hepático causado por la NPT.
Palabras clave: Síndrome de intestino corto. Relación hepato-intestinal. Composición hepática. Hepatoesteatosis.
ABSTRACT
Background & Aims: Short Bowel syndrome is a serious intestinal insufficiency. The most common etiology in adults nowadays is intestinal ischemia and inflammatory disease, while in children the most common are congenital anomalies, volvolus and necrotizing entero-colaitis, which makes the TPN obligatory. However the intestine is intimately related to the liver through the entero-hepatic circulation and different endocrinological entero-hepatic systems. Massive intestinal resections and TPN would alter this relationship, and could change the hepatic tissue composition and its histomor-phology. The aim of this work is to know these changes in more detail.
Materials and methods: We used 3 experimental groups: Group A (10 guinea pigs), which was given anesthetic and a simple laparotomy and fed for 10 days with NPT. Group B (10 guinea pigs), underwent total thin intestine resection and were fed for 10 days with NTP. The control group (6 guinea pigs) underwent anesthetic and a simple sham laparotomy and were fed orally. After this period blood and hepatic tissue samples were taken in order to study the liver fat (total fat, proportion of neutral and polar lipids, proportion of phospholipids and fatty acids). Liver biopsies were taken and studied under an optical microscope.
Results: The animals from group A and B, underwent NPT, showed a significant increase in glycemie and serum triglycerides, decreasing the cholesterol in GB. There was a significant decrease in weight and in the proportion of fat per g of the liver tissue, at a maximum level in GB, and an even higher decrease in the LP/LN ratio in GA and GB. There was also a change in the proportion of phospholipids, decreasing the Phosphatidili-nositol and increasing the Phosphatidiletanolamine. There was also a decrease in the AG w6/w3 ratio. Histo-logically appear a steatohepatitys, with a striking decrease in the mitochondrial density, being more intensive in GB.
Conclusions: NPT alters the composition of the hepatic fat and the hystomorphology of the liver. The short bowel syndrome have more lesional mechanisms, favouring the hepatic damage caused by NPT.
Key words: Short bowel syndrome. Hepato-intestinal relationships. Liver composition. Hepato-steatosis.
Abreviaturas
SIC/SIUC: Síndrome de Intestino Corto/Ultracorto.
NPT: Nutrición Parenteral Total.
AB: Ácidos Biliares.
CCF: Cromatografía en Capa Fina.
CG: Cromatografía de Gases.
AG: Ácidos Grasos.
LP: Lípidos Polares.
LN: Lípidos Neutros.
FC: Fosfatidilcolina.
FS: Fosfatidilserina.
FI: Fosfatidilinositol.
FE: Fosafatidiletanolamina.
TBI: Translocación Bacteriana Intestinal.
CEH: Circulación Entero-Hepática.
DHANPT: Daño hepático asociado a la Nutrición Parenteral Total.
GA: grupo A. GB: Grupo B. GCtr: Grupo Control.
Introducción y objetivos
El síndrome de intestino corto y ultracorto (SIC y SIUC) es una forma de fracaso o fallo intestinal en el que se pierden segmentos importantes de superficie absortiva1. Su etiología ha variado a lo largo de los últimos años, de modo que actualmente las causas más frecuentes de intestino corto en adultos serían la isquemia intestinal y la enfermedad inflamatoria, mientras que en niños lo son, con mucho, las malformaciones congénitas y las catástrofes intestinales postnatales: enterocolitis necrotizantes y vólvulos2,3. El SIUC impide un adecuado estado nutricional por vía oral pero, a través de un posterior proceso de adaptación funcional y estructural del intestino, este consigue incrementar su capacidad absortiva, aunque esto puede requerir años. El pronóstico y el manejo del SIC/SIUC están condicionados por la longitud intestinal residual, la edad del paciente, el tipo y el estado del intestino remanente, la presencia de válvula ileocecal, y la enfermedad de base o los trastornos acompañantes3-5. Además, otros fenómenos, como la translocación bacteriana intestinal (TBI) pueden originar sepsis, dificultar la adaptación intestinal e impedir la independencia de la NPT6,7.
El tratamiento fundamental del SIUC, una vez estabilizado el paciente, es el soporte nutricional con nutrición artificial (parenteral y enteral), el aporte de algunos substratos u hormonas estimulantes y/o protectores del crecimiento de la mucosa intestinal, como son la GH y el GLP-2 (glucagon-like peptide-2) y el evitar complicaciones infecciosas, mecánicas y metabólicas, además de prevenir y tratar el daño hepático asociado a la NPT (DHANPT), hasta alcanzar la máxima adaptación posible8-11. La cirugía intestinal puede estar indicada y con diversas técnicas de enlentecimiento y/o aumento de la superficie absortiva, pudiendo verse obligado a llegar al trasplante intestinal, solo o acompañado de otros órganos, como única forma de conseguir la superficie de absorción imprescindible, pero la NPT es el apoyo terapéutico fundamental aunque el DHANPT obligue al trasplante hepato-intestina12-14.
Sabemos que el hígado es un órgano íntimamente relacionado con el intestino, a través de la circulación enterohepática (CEH) de los nutrientes y de los ácidos biliares (AB), del complejo hormonal entero-hepático (CCK, secretina, gastrina, VIP, GIP...) y del cociente portal Insulina/Glucagón15. A estos mecanismos de relación hepato-intestinal se suman los fenómenos de relación hepato-intestinal derivados de la TBI. Pues bien, en condiciones de SIC/SIUC y NPT, estos cambios hepáticos lo son tanto en su composición bioquímica como en sus funciones hepatobiliares15-17. Algunos de estos cambios (bien por las alteraciones en la absorción directa de grasas o, indirectamente a través de los cambios en la circulación de los AB), podrían originar modificaciones en la composición de la grasa hepática (esteatosis simple o cambios en la composición de la grasa estructural), así como modificaciones en la composición de la bilis y en la histomorfología del tejido hepático. Con este trabajo intentamos estudiar esos cambios en la composición de la grasa hepática e histológicos producidos en condiciones de SIUC y NPT, tratando de diferenciar los debidos a una y otra condición.
Material y métodos
Se diseñó un estudio experimental de grupos frente al control, utilizando cobayos de la raza Dunkin Hartley, de entre 575 ± 28 g de peso, procedentes del animalario de la Universidad de Extremadura manteniéndolos en la sala de experimentación en condiciones homologadas de acuerdo a la legislación europea, con ciclos de luz/oscuridad de 12 h, 14 renovaciones de aire/h y a 21oC de temperatura ambiental. Cada animal fue asignado de forma ramdomizada a cada uno de los 3 grupos experimentales:
- Grupo A (n = 10), sometidos a anestesia y laparotomía simple y nutridos durante 10 días con NPT.
- Grupo B (n = 10), sometidos a resección intestinal yeyuno-ileal total y nutridos durante 10 días con NPT
- Grupo Ctr (n = 6), sometidos a anestesia y laparotomía simulada y nutridos oralmente.
Tras 6 horas de ayuno, los animales fueron anestesiados con inyección intraperitoneal de Ketamina (100 mg/kg), Benzodiacepina (20 mg/kg) y Atropina (0,2 mg/kg). También se infiltró la herida con anestesia local. En todos los animales les fue colocado un catéter siliconado subcutáneo (Arrow®) retrocervical, entrando por la yugular. En los animales del GB, la resección intestinal yeyuno-ileal fue seguida del cierre de la unión ileo-cecal y de una anastomosis término-lateral entre la primera asa yeyunal y el colon ascendente (SIUC). Fue pesado el intestino resecado. Todos los animales fueron mantenidos las primeras 24 h con infusión subcutánea de solución glucosalina y acceso libre al agua, seguidas de una mezcla de solución oral con glucosa, aminoácidos y emulsión grasa durante 48 h y, finalmente, de una NPT en los grupos A y B, con la siguiente composición: Energía no protéica: 120 kcal/ kg/día. Volumen: 170 ml/kg/día. Carga osmótica: 800 mOm/kg. Lípidos: MCT/LCT 50/50% a 3,5 g/kg/día. Relación HC/Lípidos: 65/35. Proteínas: 2,5 g/kg/día.). La composición por litro de solución de NPT fue la siguiente:

Cloruro Sódico 10%, 7,5 mi. Fosfato Dipotasico, 11,1 mi. Gluconato Calcico 10%, 11,1 mi. Vitamina C, 15 mi. Oligoelementos, 2,5 mi. Vitaminas, 5 mi. Agua, 453,4 mi. Volumen Total, 1000ml y i 440,8 kcal/L.
La alimentación oral, en el GCtr, se hizo con pienso específico intensivo para cobayo ("Panlab GP intensive"), con la siguiente composición: 88% de materia seca; 4% de grasa, 9% de fibra —celulosa—, 50% de nitrógeno libre, 7% de ceniza, 3,4 kcal/kg, 4.000 mg/kg de Vit. C, minerales, otras vitaminas y oligoelementos, de acuerdo con las especificaciones internacionales para cobayo18. Los animales se mantuvieron vigilados durante 21 días, recogiendo los datos de ingesta y el peso de las heces. En el número final de animales se incluyeron solo los que completaron 10 días sin morbimortalidad y con buen estado de salud.
Al final del estudio los animales fueron nuevamente pesados, anestesiados y re-laparotomizados, extrayéndose 10ml de sangre de la vena cava y perfundiéndose el hígado con solución de Ringer hasta la exanguinación. Luego, se extrajo el hígado en su totalidad y se pesó. Dos porciones del lóbulo derecho fueron fijadas en formaldehído 4%. El resto del hígado fue homoge-neizado y mantenido a -70oC, hasta su procesamiento final.
Las variables estudiadas fueron: Morbimortalidad, evolución del peso, bioquímica sérica (glucemia, creatinina, urea, proteínas totales y albúmina, triglicéridos, colesterol total, iones, bilirrubina total y directa, LDH, FA, GOT, GPT y GGT). Todo mediante un sistema enzimático con autoanalizador Hitachi 3450, Japón19.
El estudio de la composición lipídica del tejido hepático homogeneizado y tras su descongelación, se hizo con los siguientes métodos: Para la valoración del peso de la gota grasa/g de tejido, usamos el método de Folch (Cloroformo/metanol 2/1), secado bajo flujo de N y pesaje con balanza de precisión20/ Para la determinación de los lípidos polares (LP) y neutros (LN) y su relación, usamos la cromatografía en capa fina (CCF). El desarrollo se hizo con una fase móvil de éter dietílico y agua. Así, los lípidos polares quedan en el punto de partida o base de la placa y los neutros arriba21/ El estudio de las fracciones lipídicas de los LP (fosfolípidos), también se hizo mediante CCF, con una fase móvil de Cloroformo/Metanol/H2O/Ac. Acético glacial en proporciones de 60/30/6/1. Identificamos la Fosfatidilcolina (FC), Fosfatidilserina (FS), Fosfatidi-linositol (FI) y Fosafatidiletanolamina (FE). La cuantificación de los resultados obtenidos mediante la CCF (fracciones e LP y LN así como la FC, FS, FI y FE) se hizo con ayuda de un Apple Mcintosh tras escanear las placas con un escáner HP y realizando el procesamiento de imágenes con Adobe Photoshop-6. El programa informático empleado para la lectura densitométrica de las manchas de CCF fue el NIH-Image del Nacional Institute of Health (USA), tras teñir las manchas con vapores de yodo.
El análisis de los Ácidos Grasos (AG) del hígado se hizo mediante cromatografía de gases (CG), bajo lasa siguientes condiciones: uso de un estándar interno de C17. Tras la mutilación de la muestra de hígado mediante el método de Lepage22, los ésteres metílicos fueron inyectados en un equipo Hewlett Packard 3396 con autoinyector y equipado con columnas capilares de Dietilenglicol (3% de chromosorb-SP y 2%SP2300). El programa de gradiente del detector de ionización estuvo entre 150 hasta 220oC. Se determinaron los éste-res metílicos de los AG entre el C16 hasta C22-6w3 y todos los intermedios, comparando sus áreas con la del C17.
Se realizó un estudio estadístico inferencial utilizando la técnica del análisis de datos apareados, mediante un test de Mann-Whitney, comparando los datos finales respecto a los iniciales del peso en los grupos experimentales A y B. Para el resto de los parámetros, se compararon el grupo Control (GCtr) frente a los grupos A y B y estos entre sí, con ayuda de un test no-paramétrico de una sola vía —ANOVA—, mediante un programa Estadístico Instat-1.223. Se aceptó como diferencia significativa, una "p" menor de 0,01.
Finalmente, hicimos el estudio histomorfológico del hígado con microscopía óptica utilizando la tinción de Hematoxilina-eosina, Tricrómico de Masson y tinción específica para mitocondrias.
Resultados
Entre los 17 animales previos utilizados para la puesta a punto de la técnica quirúrgica, hubo una mortalidad del 69%, casi todos en el GB y debido a dehiscencias de sutura, un hemoperitoneo y, en tres casos por sepsis y/o sobrecarga accidental de volumen de infusión. Todos ellos se excluyeron. En los 26 animales finales se contabilizaron dos infecciones de herida, dos exteriorizaciones parciales de catéter con subfusiones cervicales, que se recolocaron.
Aunque a los 10 días todos los animales pierden algo de peso, incluidos los del GCtr, los animales de los dos grupos experimentales, A y B pierden significativamente más que el GCtr, especialmente el GB, debido también al peso del intestino resecado (con un peso de entre 65 y 80g, incluido el contenido de heces). Este peso representa alrededor de un 15% del peso total del animal y puede influir en el peso final de un período experimental de 10 días. La pérdidas de peso las expresamos en % (media de peso final-peso inicial), variando entre el 8 y el 20% en los animales de los GA y B (fig. 1).
En la analítica sérica, destacamos los incrementos significativos y frecuentes de los niveles de glucemia y TG en ambos grupos sometidos a NPT, así como de una disminución del colesterol sérico en los animales del GB —con NPT y SIUC—. Sin embargo, las proteínas totales y la albúmina, así como las otras variables y las transaminasas no se modifican (tabla I).
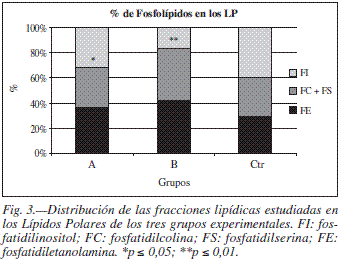
En la grasa hepática se producen cambios importantes. En primer lugar, encontramos una disminución del peso de la gota grasa por gramo de tejido, que no alcanza una diferencia significativa en el GA respecto del control, pero que sí llega a ser significativa en el caso del GB —NPT y SIUC—. Pero este descenso es mucho mayor en la relación o cociente LP/LN, siendo significativo en el GA y muy significativo en el GB respecto del control. Por tanto, además de una disminución cuantitativa de la cantidad de grasa, hay una alteración de la calidad de esta grasa, con disminución del cociente LP/LN, fundamentalmente debido a un incremento en los LN (fig. 2). Si estudiamos las fracciones lipídicas de los fosfolípidos —FE, FC+FS y FI—, también encontramos una alteración en la distribución proporcional de los mismos, con aumento de fosfatidileta-nolamina y disminución de fosfatidilinositol en los dos grupos con NPT, pero más acusada en los animales del GB, con SIUC (fig. 3).
Finalmente y dentro del estudio de la grasa hepática el estudio de los AG del tejido hepático, destacamos la disminución significativa del cociente w6/w3 en los dos grupos con NPT, así como el aumento muy significativo del cociente C18-2 6/C20-4 6 en el GB (tabla II).
Respecto de los hallazgos histomorfológicos con las tinciones de microscopía óptica, las alteraciones son muy importantes en ambos grupos con NPT: se observa una clara microesteatosis en ambos grupos, pero que se convierte en esteatohepatitis en el GB, con SIC, apreciándose infiltrado inflamatorio, seguramente secundario a traslocación bacteriana (fig. 4). Con ayuda del Tricrómico de Masson y de la Hematoxilina-Eosina, observamos que el citoplasma de los animales sometidos a NPT se ha aclarado, llegando a parecer un citoplasma de tipo "célula vegetal" en la mayoría de los animales del GB, con SIUC. Esto debe interpretarse como que el hepatocito de estos animales ha perdido abundantes organelas citoplasmáticas, "aclarándose" su citoplasma (fig. 5). Pero esto queda confirmado con la tinción específica para mitocondrias, comprobándose que, ya en los animales del GA hay una disminución evidente de las mismas respecto del GCtr, llegando a una pérdida muy importante o mayoritaria en los del GB (fig. 6).
Discusión
Desde el inicio de la aplicación de la NP se sabe que, entre las complicaciones principales de la misma está el DHANPT24. Este daño se ha tipificado anatomo-patologicamente en cuatro variantes: esteatosis/estea-tohepatitis, colestasis, colangitis y fibrosis/cirro-sis15,25,26. El primer tipo esta más asociado a la NPT a medio plazo y a adultos mientras que la colestasis a niños y/o a la NPT a más largo plazo. La colangitis podría estar mas en relación con la TBI asociada a las resecciones intestinales y al SIC27-29. Todos estos cambios histomorfológicos son capaces de estimular, mediante los mediadores inflamatorios a las células de Ito e inducir fibrosis hepática que puede acabar en cirrosis irreversible de mal pronostico30. A pesar de la multitud de factores etiopatogénicos que se han asociado al DHANPT, tanto nutricionales -por defecto o por exceso de nutrientes y/o según la composición de la NP y vías de administración31-38 —como relacionados con el paciente, edad, enfermedades, medicación, cirugía etc.—, seguimos desconociendo su etiopatoge-nia39,40. Nos sorprende que habiéndose investigado, clínica y experimentalmente, muchos mecanismos lesionales, y de saberse que el daño hepático es más frecuente y grave en los casos de SIUC, no se hayan analizado pormenorizadamente las alteraciones y cambios de composición que acaecen en el hígado sometido a NP y en pacientes con diferentes tipos de resecciones intestinales, incluyendo el SIUC. Sabemos que tras las resecciones intestinales se altera la CEH de los AB y de otros nutrientes. También sabemos que se altera el complejo hormonal entero-hepático (CCK y somatostatina secretadas en el duodeno/yeyuno, secre-tina, gastrina, VIP, GIP, GLP-2 Cociente portal Insulina/glucagón y otros factores de crecimiento: IGF-I, FGF, EGF, ITF, TGF-α; y β, NT...) y que se modifica la flora intestinal, apareciendo la TBI6-11,15-17,27-28. Además, tras las resecciones intestinales disminuye la absorción de los diferentes principios inmediatos, dependiendo del tramo resecado, y el transporte de los quilomicrones, como consecuencia también de la resección de los linfáticos del mesenterio. Por otro lado, en condiciones de NPT disminuye el flujo portal y la circulación entero-hepática de los AB, tanto por el propio ayuno como porque el flujo de nutrientes llega por vía arterial y no por vía portal, alterándose el eje hormonal entero-hepático antes citado e influyendo negativamente en la flora intestinal. Todo ello puede transformar, además de muchos otros aspectos fisiológicos del hígado, la cantidad y la composición estructural de la grasa hepática. Pero, lo más importante es que, a su vez, estos cambios en la cantidad, proporción y composición estructural de la grasa hepatocelular, podrían ocasionar importantes cambios fisiopatológicos, pues estas modificaciones influyen decisivamente tanto en la movilización y metabolismo de las grasas y de otros nutrientes —lipoproteínas, glucogenogénesis y glucogenolisis etc.— como en el transporte a través de la membrana celular y de las organelas, especialmente en el transporte y metabolismo mitocon-drial15,16,21,41-43. Por lo anterior y porque desconocemos trabajos similares, nos pareció necesario este estudio, para analizar la composición de la grasa hepática y de la histomorfología tisular y mitocondrial del hígado en condiciones de NPT con y sin SIUC.
Desde el punto de vista metodológico, pensamos que el diseño experimental ha sido correcto, tanto en la elección del animal de experimentación, con una anatomía y fisiología hepáticas bastante más similar a la humana que la de otros animales de experimentación utilizados en estos estudios —ej. la rata— como en la configuración de los grupos y en el método utilizado, de datos apareados. Consideramos imprescindible incluir un grupo control para descartar influencias debidas a la anestesia, infusión venosa, restricción de movimiento y estrés etc. Respecto del tiempo experimental, diez días es un tiempo relativamente escaso, pero que muchos estudios también han considerado suficiente para estudios en nutrición artificial, entre los cuales pensamos que pueden incluirse el actual. Nuestro propio grupo de trabajo y otros muchos investigadores, han demostrado que 10 días de experimentación animal en NPT muestra resultados suficientes en múltiples aspectos metabólicos e histomorfológicos21,31,36,37,43-46. Algunos cambios hepáticos posibles de ver en este estudio pudieran deberse a factores propios de un metabolismo de estrés o de tipo inflamatorio, pero nuestro objetivo era valorar si se apreciaban suficientes cambios precoces en la composición y metabolismo graso del hígado, así como en su histomorfología, y los resultados muestran que esto sí se ha conseguido. Así pues, tras valorar el conjunto de resultados, podemos decir que el diseño experimental es adecuado para los objetivos propuestos.
Entrando en la discusión de los resultados, lo primero que destacamos es que, al igual que ocurre en otros animales sometidos a grandes resecciones intestinales, en nuestros animales del GB no se producen diarreas profusas inmediatas y sin estímulo alimentario, que conlleven deshidrataciones y/o dis-electrolitemias graves. Esto puede ser debido a que casi todos los animales, especialmente en los vegetarianos puros, la proporción Intestino Delgado/Intestino Grueso es mucho más equilibrada que en los humanos. Mientras que en los humanos la absorción de agua y electrolitos es muy dependiente solo del colon derecho, en estos animales el gran ciego y la mayoría del colon siguen absorbiendo agua, electrolitos y muchos otros micro y macro-nutrientes. Respecto de la pérdida de peso observada a los 10 días y en los dos grupos sometidos a NPT (GA y GB), pensamos que esta es relativamente escasa. Dado que también el GCtr muestra un pequeño descenso de peso, seguramente debido a la falta de ingesta relacionada con el estado de relativo estrés debido a las condiciones de infusión IV, si ha ello sumamos el mayor estrés quirúrgico y experimental de los animales de los GA y GB, es fácil justificar la mayor pérdida de peso de estos animales. Sobre todo, recordamos que en el GB un 15% del peso ya es retirado tras la resección intestinal, en el acto quirúrgico. Así pues, aunque hay una pérdida significativa de peso a los 10 días, parece que este es cuantitativamente escaso y que se estabiliza al final del período experimental. Para analizar el estado nutricional de nuestros animales, además del peso, hay que valorar los resultados de la analítica sérica, donde los valores de proteínas totales y de albúmina, glucemia y TG se mantienen en límites normales, pareciendo indicar que hemos conseguido un adecuado aporte calórico y proteico. Las variaciones moderadas de glucemia en los animales sometidos a NPT ya han sido descritas en los estudios de NP con animales y se van normalizando a lo largo de la primera semana, sin repercusiones funcionales aparentes21. Los incrementos de los TG séricos también son frecuentes en la NPT y han sido descritos con anterioridad, tanto en humanos como en animales, especialmente con el uso total o parcial de los lípidos habituales derivados de la soja21,36,37,45. En nuestros animales sometidos a NPT estos incrementos fueron moderados y sin que el suero llegara a ser nunca turbio. El descenso significativo del colesterol en el GB, pudiera deberse a dos factores: el primero es que, debido al SIUC el déficit absortito de AB es muy importante, obligando al hígado a un consumo importante del mismo para la síntesis de estos AB. El segundo factor a considerar es que, ante el mayor estrés metabólico que se produce en estos animales, también se utiliza el colesterol tanto con fines energéticos como estructurales (síntesis de cortisol y de hormonas corticoideas, neo-formación de membranas, etc.). Este resultado diferencial con respecto del GA también ha sido descrito en otros estudios nuestros con resecciones intestinales parciales, especialmente tras resección ileal, y a pesar de tener nutrición oral exclusiva47, luego parece estar mas en relación con las resecciones intestinales que con la NPT.
En el estudio de la grasa hepática y en primer lugar, encontramos una disminución leve del peso de la gota grasa por gramo de tejido en los dos grupos experimentales pero que alcanza a ser significativa en el GB. Esto parece contradecir el resultado habitual de esteatosis hepática tras NPT, pues la esteatosis conllevaría un aumento del porcentaje de peso graso en el tejido hepático como consecuencia de la deficiente movilización de la grasa aportada al hígado21,36. Pero hemos de pensar que, a los diez días, medio plazo, el metabolismo de estrés al que están sometidos los cobayas, tras la intervención quirúrgica y las condiciones de habitabilidad estresantes, origina un catabolismo capaz de consumir una alta tasa calórica periférica y hepática, contraria al almacenamiento y/o estancamiento graso y no compensado por el aporte hecho mediante la NPT. Esto explicaría que el cociente gota grasa/g tejido hepático sea mayor en el GA, con menor catabolismo, que en el GB. Si ponemos estos resultados en relación con los hallazgos histomorfológicos estos indican una micro-esteatosis y/o esteato-hepatitis, no una macroesteato-sis. La microestetaosis y esteatohepatitis parecen más debidas a una alteración de la grasa estructural que a un acumulo de la misma. Además vemos que se modifica la calidad de esta grasa, porque disminuye el cociente LP/LN en los grupos sometidos a NPT. Teóricamente, el aporte de lípidos parenterales aumentaría el depósito de grasa —de w6 y fitoesteroles—, pero también aquí hay diferencias entre los dos grupos experimentales, pues es más intenso en los animales del GB, con resección intestinal y NPT. Es decir, en condiciones de SIC/SIUC, se incrementa el porcentaje de LN, probablemente debidos a unas condiciones metabólicas diferentes a las de simple ayuno y NPT21,42,43,48-50. Pero también podemos pensar que es debido a la grave alteración de la CEH y que podría influir en la composición grasa, directamente por alteración de la CEH de los AB y de otros substratos, e indirectamente, a través de mecanismos inflamatorios y hormonales, por aumento de la TBI y por alteración grave de todo el eje hormonal enterohepático y que ya tratamos anteriormente51,52. Si seguimos analizando los resultados de la composición de fosfolípidos de la grasa hepática vemos alteraciones en la distribución de éstos en los animales del grupo A y más aún en los animales del grupo B, con disminución del fosfatidilinositol y aumento de la fosfatidiletanolamina. Cual sería el significado preciso de estos cambios no alcanzamos actualmente a precisarlos, pero el hecho es de que, con la misma NPT pero en condiciones de SIUC, hay diferencias metabolicas y estructurales en la grasa hepática. Y esto también puede ponerse en relación con los hallazgos histomorfológicos, pues también aquí, los animales del GB tienen un patrón de daño tisular diferente, con carácter más inflamatorio (quizá no solo infeccioso o secundario a TBI) y con un daño mitocondrial mayor. En el caso de la mitocondria, recordemos que el metabolismo de los AG poliinsaturados se realiza en su interior, existiendo una relación directa entre la organela y su función y, por tanto, pudiendo verse afectada, lo que pudiera haber acontecido en esta experimentación. De hecho, la disminución significativa de la densidad mitocondrial hepatocitaria se ha demostrado en otras situaciones experimentales, como es en el déficit de Taurina en el hígado de conejo, posiblemente por alteración de la permeabilidad de membrana (53). En cuanto a los AG lo que observamos es una disminución del cociente w6/w3 en los dos grupos con NPT, GA y GB, y un incremento significativo del cociente C18-2w6/C20-4w6 en el GB. Se sabe que el uso de los preparados de lípidos parenterales a base de soja o, como en nuestro caso, con una mezcla de MCT/LCT, aumentan el aporte excesivo de linolénico-w6 y de araquidónico, en vez de los AG Eicosapentaenoico y Docohexaenoico, con consecuencias pro-inflamatorias y oxidativas49-51,54. También es cierto que estos cambios en las proporciones de los AG podrían influir en la síntesis y saturación concreta de los diferentes fosfolípidos y, concretamente, en los fosfolípidos de membrana, influyendo a su vez en la permeabilidad de la membrana celular y también en el estado de hidro o liposolubilidad intracelular, lo que también podría explicar parte de los cambios histomorfológicos que hallamos en estos dos grupos experimentales. Pero el hecho es que, también aquí, hemos de resaltar las diferencias existentes entre los GA y GB, con igual aporte en la NPT pero con diferentes estados de tránsito intestinal. Así que, aparte de los posibles mecanismos lesionales relacionados con la composición de la grasa aportada y que en los años recientes se ha puesto en relación con la aparición de esteatohepatitis y colostasis, hay otros factores lesionales directamente relacionados con la alteración de la CEH, de la TBI y de la alteración del Complejo hormonal entero-hepático, propias del SIUC11,55,56. Y ello explicaría también la mayor aparición de fenómenos inflamatorios (colangitis) que aparecen en los animales del GB, así como de un mayor daño celular, con afectación especialmente de las organelas y descenso importante de la densidad mitocondrial .
No es de extrañar pues, que en los pacientes con DHANPT, los casos de SIUC sean más frecuentes, más graves y con peor pronóstico2-4. Por lo tanto, podemos decir que las resecciones intestinales influyen en la composición de la grasa hepática, con disminución del peso de la gota grasa, alteración en la distribución de los fosfolípidos y de la proporción de los ácidos grasos totales. Estas alteraciones se traducen en cambios histomorfológicos concretos y específicos para cada situación, con afectación intracelular y mitocondrial grave y difíciles de ser compensados por el hígado, al menos a medio plazo.
Referencias
1. Ballesteros Pomar MD, Vidal Casariego A. Síndrome de intestino corto; definición, causas, adaptación intestinal y sobre-crecimiento bacteriano. Nutr Hosp 2007; 22 (Suppl. 2): 74-85. [ Links ]
2. Vanderhoof JA, Langnas AN. Short bowel syndrome in children and adults. Gastroenterology 1997; 113: 1767-1778. [ Links ]
3. Buchmam AL. Etiology and initial management of short bowel syndrome. Gastroenterology 2006; 130: S5-S15. [ Links ]
4. Wales PW, de Silva N, Kim JH, Lecce L, Sandhu A, Moore AM. Neonatal short bowel syndrome: a cohort study. J Pediatr Surg 2005; 40: 755-762. [ Links ]
5. Sigalet DL. Short bowel syndrome in infants and children: an overview. Semin Pediatr Surg 2001; 10: 49-55. [ Links ]
6. García de Lorenzo y Mateos A, Acosta Escribano J, Rodríguez Montes JA. Importancia clínica de la translocación bacteriana. Nutr Hosp 2007; 22 (Suppl. 2): 50-55. [ Links ]
7. O'Keefe SJ. Bacterial overgrowth and liver complications in short bowel intestinal failure patients. Gastroenterology 2006; 130: S67-9. [ Links ]
8. Cunliffe R, Bowling T. Artificial nutrition support in intestinal failure: Principles and Practice of Parenteral feeding. Clin Colon and Rectal Surg 2004; 17: 99-105. [ Links ]
9. Buchman AL. Complications of long-term home total parenteral nutrition: their identification, prevention and treatment. Dig Dis Sci 2001; 46: 1-18. [ Links ]
10. Scolapio JS, Camilleri M, Fleming CR. Effect of growth hormone, glutamine, and diet on adaptation in short-bowel syndrome, a randomized controlled study. Gastroenterology 1997; 113: 1074-81. [ Links ]
11. GR Martin, PL Beck, DL Sigalet: Gut hormones, and short bowel syndrome: The enigmatic role of glucagon-like peptide-2 in the regulation of intestinal adaptation. World J Gastroen-terol 2006; 12: 4117-4129. [ Links ]
12. Vanderhoof JA. Short bowel syndrome in children and small intestinal transplantation. Pediatr Clin North Am 1996; 43:533-550. [ Links ]
13. Muiesan P, Dhawan A, Novelli M, Mieli-Vergani G, Rel M, Heaton ND. Isolated liver transplant and sequential small bowel transplantation for intestinal failure and related liver disease in children. Transplantation 2000; 11: 2323-6. [ Links ]
14. Atalay F, Ozcay N, Gundogdu H, Orug T, Gungor A., Akoglu M. Evaluation of the outcomes of short bowel síndrome and indication for intestinal transplantation. Transpl Proc 2003; 35:3054-6. [ Links ]
15. Moran Penco JM, Salas Martinez J, Maciá Botejara E. What happens in the liver during artificial nutrition? 22nd Espen Congress, Eduational Programme Book. Madrid, 2000; 117-120. [ Links ]
16. Hofmann AF. Defective biliary secretion during total parenteral nutrition: probable mechanisms and possible solutions. JPGN 1995; 20: 376-90. [ Links ]
17. Freund HR. Abnormalities of liver function and hepatic damage associated with total parenteral nutrition. Nutrition 1991; 7: 1-5; discussion 5-6. [ Links ]
18. Hau J, Van Hoosier G, Ritskes-Hoitimga M, Chwalibog A. Nutrient. Requirements, Experimental Design and Feeding Schedules in animal Experimental (chapter 12: pag. 281) En: Handbook of Laboratory Animal Science. Ed CRC Press. 2003. [ Links ]
19. Carpentier YA, Thonnart N.: Parameters for evaluation of lipid metabolism. JPEN 1987; 11(5 Suppl.): 104S-108S. [ Links ]
20. Folch J, Lees M, Sloane Stanley GH. A simple method for the isolation and purification of total lipides from animal tissues. J Biol Chem 1957; 226: 497-505. [ Links ]
21. Espín-Jaime MT, Moran JM, Maciá E, Salas J, Botello F. Composición lipidica hepática tras NPT con LCT vs MCT/LCT como fuente de aporte. Nutr Hosp 1996; (Suppl. 11): 36-39. [ Links ]
22. Lepage G, Roy CC. Direct transesterification of all classes of lipids in a one-step reaction. J Lipid Res 1986; 27: 114-120. [ Links ]
23. Hollander M, Wolfe DA. Nonparametric statistical methods. Jhon Wiley & Sons, Inc. New York, 1973. [ Links ]
24. Peden VH, Witzleben CL, Skelton MA. Total parenteral nutrition. J Pediatr 1971; 78: 180-1. [ Links ]
25. Mullick FG, Moran CA, Ishak KG. Total parenteral nutrition: a histopathologic analysis of the liver changes in 20 children. Mod Pathol 1994; 7: 190-194. [ Links ]
26. Wolfe BM, Walter BK, Shaul DB, Wong L, Ruebner BH.: Effect of total parenteral nutrition on hepatic histology. Arch Surg 1988; 123: 1084-90. [ Links ]
27. Riordan SM, McIver CJ, Willimas R. Liver damage in human small intestinal bacterial overgrowth. Am J Gastroenterol 1998; 93: 234-7. [ Links ]
28. Van Saene HFK, Taylor N, Donnell SC. Gut overgrowth with abnormal flora: the missing link in parenteral nutrition-related sepsis in surgical neonates. Eur J Clin Nutr 2003; 57: 548-53. [ Links ]
29. Nag PC, Lee CH, Wong SPS. High-dose oral erythromycin decreased the incidence of parenteral nutrition-associated cholestasis in preterm infants. Gastroenterology 2007; 132: 1726-39. [ Links ]
30. Craig RM, Neumann T, Jeejeebhoy KN. Severe hepato-cellular reaction resembling alcoholic hepatitis with cirrhosis after massive small bowel resection and prolonged total parenteral nutrition. Gastroenterology 1980; 79: 131-7. [ Links ]
31. Moss RL, Haynes AL, Pastuszyn A, Glew RH.: Methionine infusion reproduces liver injury of parenteral nutrition cholestasis. Pediatr Res 1999; 45: 664-668. [ Links ]
32. Fell JME, Reynolds AP, Meadows N. Manganese toxicity in children receiving long-term parenteral nutrition. Lancet 1996;347: 1218-21. [ Links ]
33. Buchman A. Choline deficiency during parenteral nutrition in human. NCP 2003; 18: 353-8. [ Links ]
34. Spencer AU, Yu S, Tracy TF. Parenteral nutrition-associated cholestasis in neonates: multivariate analysis of the potential protective effect of taurine. J Parent Enteral Nutr 2005; 29: 337-44. [ Links ]
35. Moss RL, Das JB, Ansari G, Raffensperger JG. Hepatobiliary dysfunction during total parenteral nutrition is caused by infusate, not the route of administration. J Pediatr Surg 1993;28: 391-7. [ Links ]
36. Moran JM, Macia E, Salas J, Mahedero G, Climent V. Liver lipid composition and intravenous, intraperitoneal, and enteral administration of intralipid. Nutrition 1994; 10: 26-31. [ Links ]
37. Javid P, Greene AK, Garza J. The route of lipid administration affects parenteral nutrition-induced hepatic steatosis in a mouse model. J Pediatr Surg 2005; 40: 1446-1453. [ Links ]
38. Forchielli ML, Walker WA. Nutritional factors contributing to the development of cholestasis during total parenteral nutrition. Adv Pediatr 2003; 50: 245-67. [ Links ]
39. Kelly DA. Intestinal failure-associated liver disease: What do we know today? Gastroenterology 2006; 130: S70-7. [ Links ]
40. Cavicchi M, Beau P, Crenn P, Degott C, Messing B. Prevalence of liver disease and contributing factors in patients receiving home parenteral nutrition for permanent intestinal failure. Ann Intern Med 2000; 132: 525-32. [ Links ]
41. Colomb V, Jobert-Giraud A, Lacaille F, Goulet O, Fournet JC, Ricour C et al. Role of lipid emulsions in cholestasis associated with long-term parenteral nutrition in children. Transpl Proc 1994; 26: 1467. [ Links ]
42. Degott C, Messing B, Moreau D. Liver phospholipidosis induced by parenteral nutrition: histologic, histochemical, and ultraestructural investigations. Gastroenterology 1988; 95:183-91. [ Links ]
43. Wang H, Khaoustov VI, Krishnan B, Cai W, Stoll B, Burrin DG et al. Total parenteral nutrition induces liver steatosis and apop-tosis in neonatal piglets. J Nutr 2006; 136: 2547-52. [ Links ]
44. Alwayn IP, Gura K, Nose V. Omega-3 fatty acid supplementation prevents hepatic steatosis in a murine model of nonalcoholic fatty liver disease. Pediatr Res 2005; 57: 445-452. [ Links ]
45. Guertin F, Roy CC, Lepage G, Perea A, Giguére R, Yousef I. Effect of Taurine on TPN-associated Cholestasis. JPEN 1991; 15: 247-251. [ Links ]
46. Das JB, Cosentino CM, Levy MF, Ansari GG, Raffensperger JG. Early hepatobiliary dysfunction during total parenteral nutrition: an experimental study. J Pediatr Surg 1993; 28: 14-8. [ Links ]
47. Correa MI, Morán JM, Amaya JL, Leal A, Maciá E, Saenz J. Cambios en la composición de la grasa y en la histomorfologia del hígado tras resecciones intestinales parciales. Nutr Hosp aceptado mayo 2010. [ Links ]
48. Clayton PT, Whitfield P, Iyer K. The role of phytosterols in the pathogenesis of liver complications of pediatric parenteral nutrition. Nutrition 1998; 14: 158-64. [ Links ]
49. Gura KM, Duggan ChP, Collier SB, Jennings RW, Folkman J, Bistrian BR et al. Reversal of parenteral nutrition-associated liver disease in two infants with short bowel syndrome using par-enteral fish oil: implications for future management. Pediatrics 2006; 118: e197-201. [ Links ]
50. Gura KM, Lee S, Valim C, Zhou J, Kim S, Modi BP et al. Safety and Efficacy of a Fish-Oil_Based Fat Emulsion in the Treatment of Parenteral Nutrition_Associated Liver Disease. Pediatrics 2008; 121: e678-e686. [ Links ]
51. Day CP, James OF. Steatohepatitis: a tale of two "hits"? Gastroenterology 1998; 114: 842-845. [ Links ]
52. Van Aerde JE, Duerksen DR, Gramlich L et al. Intravenous fish oil emulsion attenuates total parenteral nutrition-induced cholestasis in newborn piglets. Pediatr Res 1999; 45: 202-208. [ Links ]
53. Moran JM, Salas J, Botello F, Maciá E, Climent V. Taurine and cholestasis associated to TPN. Experimental study in rabbit model. Pediatr Surg Int 2005; 21: 786-792. [ Links ]
54. Wanten GJ, Calder PC. Immune modulation by parenteral lipid emulsions. Am J Clin Nutr 2007; 85 (5): 1171-1184. [ Links ]
55. Liu X, Nelson DW, Holst JJ, Ney DM. Synergistic effect of supplemental enteral nutrients and exogenous glucagon-like peptide 2 on intestinal adaptation in a rat model of short bowel syndrome. Am J Clin Nutr 2006; 84: 1142-50. [ Links ]
56. Forrest EH, Oien KA, Dickson S, Galloway D, Mills PR. Improvement in cholestasis associated with total parenteral nutrition after treatment with an antibody against tumour necrosis factor alpha. Liver 2002; 22: 317-20. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
José M. Morán Penco.
Cátedra de Cirugía. Facultad de Medicina.
Avda. Elvas, s/n.
06071 Badajoz. España.
E-mail: jmmoran@unex.es
Recibido: 23-VII-2010.
Aceptado: 6-IX-2010.