Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.30 no.6 Madrid dic. 2014
https://dx.doi.org/10.3305/nh.2014.30.6.7808
ORIGINAL / Nutrición enteral
Gastrostomía endóscopica percutánea en esclerosis lateral amiotrófica; experiencia en un hospital de tercer nivel
Percutaneous endoscopic gastrostomy in amyotrophic lateral sclerosis. Experience in a district general hospital
Inmaculada Prior-Sánchez, Aura Dulcinea Herrera-Martínez, Carmen Tenorio Jiménez, María José Molina Puerta, Alfonso Calañas Continente, Gregorio Manzano García y María Ángeles Gálvez Moreno
UGC Endocrinología y Nutrición. Hospital Universitario Reina Sofía, Córdoba. España.
Dirección para correspondencia
RESUMEN
Introducción: La Esclerosis Lateral Amiotrófica (ELA) es una enfermedad degenerativa neurológica con afectación de la vía piramidal, produciendo trastornos motores progresivos que evolucionan hasta la parálisis. Estos pacientes pueden asociar disfagia, precisando soporte nutricional a través de de sonda nasogástrica o Gastrostomía Endoscópica Percutánea (PEG). La PEG está asociada con aumento de la supervivencia, sin embargo la evidencia acerca del momento óptimo para su colocación es escasa.
Objetivo: Analizar las características de los pacientes con ELA en el momento de colocación de la PEG y su evolución.
Material y métodos: Estudio descriptivo retrospectivo. Se incluyeron pacientes con diagnóstico de ELA y PEG valorados durante los años 2005-2014 en nuestro hospital. Se analizaron parámetros nutricionales y respiratorios, y evolución de los pacientes. Los resultados se analizaron en el programa SPSS15.
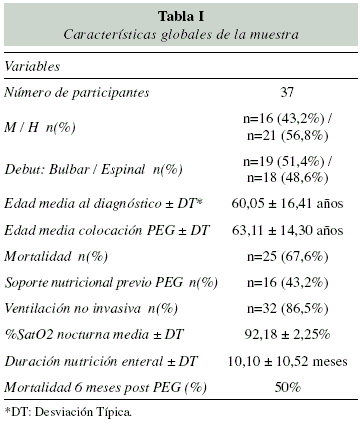
Resultados: 37 pacientes fueron incluidos (56,8% hombres, 43,2% mujeres) con una edad media al diagnóstico 60 años, y edad media de colocación de PEG de 63,1 años, el 48,6% debutó con afectación espinal y el 51,4%, con bulbar. El 43,2% de los pacientes recibieron suplementos previa colocación de PEG durante un promedio de 11,3 meses. La capacidad vital forzada (CVF) media al diagnóstico fue del 65,45±13,67%, evolucionando desfavorablemente hasta un 39,47±14,69% en el momento de colocación de la PEG. El 86,5% de los pacientes precisaron soporte respiratorio con ventilación mecánica no invasiva (VMNI). El 86,5% presentaron disfagia, el 64,9% pérdida de peso > 5-10% de su peso habitual, el 8,1% IMC bajo, el 27% parámetros bioquímicos de desnutrición y el 73% empeoramiento de función respiratoria, por tanto, el 100% cumplían criterios de colocación de PEG según nuestro protocolo. La duración de la nutrición enteral fue de 10,1 meses con una mortalidad del 50% en los primeros 6 meses de la colocación de la PEG.
Conclusiones: Evidenciamos una demora de 3 años entre el diagnóstico y la colocación de la PEG, con una supervivencia del 50% a los 6 meses de la realización de la misma. Más estudios son necesarios para determinar si una colocación más precoz podría aumentar la supervivencia.
Palabras clave: Esclerosis lateral amiotrófica. Nutrición enteral. Gastrostomía.
ABSTRACT
Background: Amyotrophic Lateral Sclerosis (ALS) is a degenerative disorder that affects the pyramidal tract, producing progressive motor dysfunctions leading to paralysis. These patients can present with dysphagia, requiring nutritional support with a nasogastric tube or Percutaneous Endoscopic Gastrostomy (PEG). PEG is associated with increased survival rates. However, the timing of PEG placement remains a significant issue for clinicians.
Objective: To analyse the characteristics of ALS patients at the moment of PEG placement and their progression.
Methods and materials: Descriptive retrospective study including patients diagnosed with ALS and PEG who were assessed during the 2005-2014 period in our hospital. Nutritional parameters and respiratory function were assessed for all patients, as well as their progression. The data was analysed using SPSS15.
Results: 37 patients were included (56.8% men, 43.2% women) with an average age of 60 at diagnosis, and an average age of 63.1 at PEG placement. 48.6% started with spinal affection and 51.4%, with bulbar affection. 43.2% of the patients received oral nutritional supplements prior to PEG placement for a mean period of 11.3 months. The mean forced vital capacity at diagnosis was 65.45±13.67%, with a negative progression up to 39.47±14.69% at the moment of PEG placement. 86.5% of patients required non-invasive positive-pressure ventilation. 86.5% presented with dysphagia, 64.9% with weight loss > 5-10% from their usual weight, 8.1% with low Body Mass Index, 27% with malnutrition and 73% with aworsened breathing function; therefore, 100% met the criteria for PEG placement according to our protocol. The period on enteral feeding was extended for 10.1 months with a mortality of 50% during the first 6 months from PEG placement.
Conclusions: There is evidence of a 3-year delay between diagnosis and PEG placement, with a survival rate of 50% at 6 months from PEG insertion. Further studies are required to establish whether an earlier placement might increase survival rates.
Key words: Amyotrophic lateral sclerosis. Enteral nutrition. Gastrostomy.
Introducción
La Esclerosis Lateral Amiotrófica (ELA) es una enfermedad del sistema nervioso, caracterizada por una degeneración progresiva de las neuronas motoras en la corteza cerebral (motoneuronas superiores), tronco del encéfalo y médula espinal (motoneuronas inferiores). Como consecuencia, se produce una debilidad y atrofia muscular que avanza hasta la parálisis, afectando a la autonomía motora, la comunicación oral, la deglución y la respiración y ocasionando una insuficiencia respiratoria en un plazo de 2 a 5 años de media1. Se estima una prevalencia de 5-10 casos por 100.000 habitantes y una incidencia de 1,2-2,5 casos por 100.000 habitantes y año2.
Existen distintas formas clínicas de presentación: ELA clásica (85%, con afectación cortical y espinal); síndrome de motoneurona inferior puro (10%, o Atrofia muscular progresiva); síndrome de motoneurona superior puro (1%, o Esclerosis lateral primaria, progresión simétrica a tetraparesia espástica con parálisis pseudobulbar).
Es difícil establecer de forma precoz el diagnóstico de ELA debido a su variabilidad clínica y ausencia de marcadores biológicos. Por este motivo, la Federación Mundial de Neurología elaboró un documento de consenso en el que se establecen los criterios diagnósticos de ELA, conocidos como "Criterios de El Escorial" y que se basan en la presencia de signos clínicos compatibles con la enfermedad y exclusión de otras posibles causas3.
Como en otras enfermedades crónicas, la malnutrición es un hallazgo frecuente en los pacientes afectos. Su prevalencia oscila del 16 al 53%, dependiendo de la forma de presentación y estadio de la enfermedad4. Son múltiples los factores que contribuyen a ese deterioro nutricional4-8: disfagia, por afectación de la musculatura bulbar; atrofia y pérdida muscular; alteraciones del estado del ánimo, que conllevan una disminución del apetito y de la ingesta; y un hipercatabolismo8, secundario a un incremento del trabajo respiratorio. Considerando que la desnutrición es un factor pronóstico independiente de supervivencia9-13, el abordaje y valoración nutricional de estos pacientes debe instaurarse de precoz. Se ha visto que una pérdida de peso de >10% en los últimos 6 meses o un IMC menor de 18,5 kg/m2, son factores predictivos de mortalidad.
El soporte nutricional debe instaurarse de forma individualizada dependiendo del estadio de la enfermedad para asegurar un adecuado aporte calórico (tanto en forma de macro como micronutrientes), un buen estado de hidratación y minimizar el catabolismo proteico. Puede ofrecerse en forma de dieta personalizada, empleo de espesantes, suplementos nutricionales, mediante un soporte nutricional enteral (por sonda nasogástrica o gastrostomía), y exclusivamente en casos excepcionales, cuando el tracto digestivo es inviable, en forma de Nutrición parenteral5,6. Sin embargo, la modalidad de elección a largo plazo en la ELA, así como en la mayoría de enfermedades neurológicas degenerativas, es la gastrostomía endoscópica percutánea o PEG (del inglés, Percutaneous Endoscopic Gastrosotomy). Esta técnica está considerada hoy día, como un procedimiento efectivo y seguro que mejora la supervivencia y la calidad de vida de estos pacientes14-16.
A pesar de las ventajas de un soporte nutricional precoz, la mayoría de los pacientes y familiares son reacios a su instauración de forma precoz. Además, no existen criterios consistentes, basados en la evidencia, sobre el momento de su colocación; según la Academia Americana de Neurología15, se debe monitorizar el peso y la presencia de disfagia cada 3 meses, de forma que si se constata alguno de estos síntomas, el soporte nutricional enteral por gastrostomía estaría indicado. No obstante su colocación, está condicionada por la función respiratoria, considerando el momento idóneo cuando la Capacidad Vital Forzada (CVF) se sitúa por encima del 50%, ya que un porcentaje menor, indicaría un mayor deterioro de la de la función pulmonar y por tanto, un mayor riesgo de complicaciones durante el procedimiento.
El objetivo de nuestro estudio consiste en analizar las características y el estado nutricional de los pacientes afectos de ELA en el momento de la colación de la PEG y su evolución posterior.
Material y métodos
Estudio retrospectivo en el que se incluyeron la totalidad de pacientes con diagnóstico de ELA valorados por el Servicio de Endocrinología y Nutrición y sometidos a gastrostomía, durante el periodo Dic-2005/ Dic-2013. Se excluyeron aquellos pacientes con ELA, que rechazaron soporte nutricional con PEG.
Se analizaron variables demográficas (edad, sexo, existencia de otras comorbilidades médicas), parámetros nutricionales (peso, talla, IMC, nivel de prealbúmina, albúmina y proteínas totales), parámetros respiratorios (fundamentalmente Capacidad vital Forzada -CVF- y % Saturación media de 02 nocturna). Las variables nutricionales se midieron tanto de forma basal (antes de la instauración del soporte nutricional enteral) como a los 3-6 meses de la colocación de la PEG.
Se comprobó el cumplimiento de los criterios protocolizados en el Hospital Reina Sofía para indicación de PEG y que se basan en las recomendaciones de la guía asistencial de Esclerosis Lateral Amiotrófica del Sistema Sanitario Público de Andalucía1. Estos son: presencia de disfagia, pérdida de peso de >5-10 % desde el diagnóstico, IMC <18,5 kg/m2 o <20 kg/m2 en personas >65 años, parámetros bioquímicos de desnutrición o deterioro de la función respiratoria.
Igualmente, se recogió la aparición de complicaciones en relación con la PEG (gastrointestinales, mecánicas, infecciosas y metabólicas), la duración del soporte nutricional y el porcentaje de éxitus.
Para el análisis estadístico se empleó el programa SPSS Statistics v.15.
Resultados
Se incluyeron en total 37 pacientes con diagnóstico de ELA en los que se instauró durante su evolución, soporte nutricional enteral mediante PEG. Un 56,8% (n=21) eran hombres y un 43,2% (n=16) mujeres. La edad media al diagnóstico de la enfermedad se sitúo en 60,05±16,41 años, mientras que la edad media de colocación de la PEG se demoró hasta los 63,11±14,30 años. El 43,2% de los pacientes recibieron suplementos nutricionales previa colocación de la PEG durante un promedio de 11,38±21,14 meses. La duración global media del soporte nutricional enteral fue de 10,10±10,52 meses. El 86,5% de los pacientes valorados (n=32), necesitaron soporte respiratorio con ventilación mecánica no invasiva (BIPAP). El porcentaje global de éxitus fue del 67,6% (n=25) con una mortalidad del 50% en los primeros 6 meses tras la colocación de la PEG. No se objetivaron diferencias significativas en cuanto al sexo de las distintas variables, salvo un mayor número de mujeres con hipertensión (Tabla I y II). La capacidad vital forzada (CVF) media al diagnóstico fue del 65,45±13,67%, evolucionando desfavorablemente hasta un 39,47±14,69% en el momento de colocación de la PEG (Figs. 1 y 2). Desde el punto de vista nutricional, presentaron al diagnóstico valores medios de albúmina 3,52±0,52 g/dl, prealbúmina 18,08±6,01 mg/dl, proteínas totales de 6,24±0,55 g/dl e IMC 24,21±3,87 kg/m2, evolucionando a 3,65±0,64 g/ dl; 21,66±10,21mg/dl; 6,26±1,61 g/dl y 25,68±4,89 kg/ m2, respectivamente (Tabla III). El 100% cumplían criterios de colocación de PEG, definidos en el apartado anterior (Fig. 3). Se objetivaron complicaciones en 14 pacientes (Fig. 4). Las más frecuentes fueron las gastrointestinales (21,6%), fundamentalmente estreiimiento y distensión abdominal, seguidas de las infecciosas (13,5%), destacando en este subgrupo 2 neumonías por broncoaspiración. Solo se produjeron complicaciones mecánicas (desplazamiento de la sonda y obstrucción) y metabólicas en cuatro pacientes.
Discusión
La esclerosis lateral amiotrófica es una enfermedad neurodegenerativa con un alto riesgo de malnutrición. Factores como la disfagia, pérdida de apetito, depresión, disnea, e hipermetabolismo4-8, contribuyen al deterioro del estado nutricional. En este sentido, la gastrostomía endoscópica percutánea, se ha convertido en un procedimiento de primera línea para el soporte nutricional de los pacientes con ELA y en general, de pacientes afectos de enfermedades neurológicas degenerativas. Su instauración de forma precoz, es un factor predictivo independiente de supervivencia y se asocia con un incremento de la calidad de vida14-16. En nuestra serie, se objetivó una mejora estadísticamente significativa de los parámetros nutricionales tras la instauración de la PEG. Otro aspecto a destacar, es la asistencia de nuestros pacientes por un equipo multidisciplinar, compuesto por neurólogo, endocrinólogo, neumólogo y rehabilitador. Este tipo de asistencia permite implementar con una mayor costo-efectividad todo el tratamiento de soporte y la elaboración de un protocolo de actuación basado en las guías de práctica clínica1,15-16. En el estudio de Chiò et al19, se obtiene como resultado que la atención en hospitales o centros de tercer nivel, es un factor predictivo de supervivencia, independiente de otras variables pronósticas, como la edad, severidad de la afectación bulbar o estado respiratorio en el momento del diagnóstico. De esta forma, un 100% de nuestros pacientes cumplían criterios de colocación de PEG, ya fuera por la presencia de disfagia, datos de desnutrición calórica o proteica o declive de la función respiratoria. No obstante, y a pesar de estas mejoras en la atención y asistencia clínica, constatamos aún, una demora media de 3 años desde el diagnóstico de la enfermedad hasta la colocación de la PEG, con un deterioro evidente de la función respiratoria; más del 70% de nuestros pacientes presentaban un empeoramiento de la función respiratoria en el momento de instaurar el soporte nutricional con sonda de gastrostomía. Este hecho puede guardar relación con la elevada tasa de mortalidad (67,6%; un 50% durante los primeros 6 meses tras la PEG), ya que uno de los principales factores pronósticos, es el estado de la función respiratoria y la tolerancia o no, al soporte ventilatorio mediante Ventilación Mecánica No Invasiva -VMNI- o traqueotomía17,18. Otro factor que puede haber influido es la edad media ligeramente superior a otras publicaciones10,20. La duración media global de la nutrición enteral (303 ± 315,6 días) ha presentado una gran variabilidad al igual que en otros estudios21, dependiendo del grado de afectación bulbar y respiratorio.
Con respecto a las complicaciones, la mayoría de ellas han sido leves, encontrándose el estreñimiento como el síntoma principal, dato recogido igualmente en otras series21,22. Sin embargo, este problema no puede considerarse como una complicación exclusiva de la nutrición, sino que es inherente a la propia evolución de la enfermedad: por la atrofia y atonía muscular, disminución de la motilidad intestinal, reducción de la ingesta a líquidos o por empleo de medicación opiácea. Solo observamos dos complicaciones graves, en forma de neumonía broncoaspirativa, en dos pacientes con disfunción bulbar muy severa.
Una limitación importante de nuestro estudio, así como de la mayoría de los publicados hasta el momento, es que son series de casos retrospectivos, con la consecuente limitación en la interpretación de los resultados.
Conclusiones
La gastrostomía endoscópica percutánea, es un procedimiento seguro y efectivo, idóneo para el soporte nutricional a largo plazo de los pacientes afectos de ELA. Existe aún, un retraso medio de 3 años desde el diagnóstico hasta la instauración del soporte nutricional enteral. La colocación más precoz de la gastrostomía en estos enfermos podría aumentar la supervivencia, necesitándose para ello la realización de estudios de una mayor potencia estadística.
Referencias
1. Guía asistencial de Esclerosis Lateral Amiotrófica en el SSPA, Edición 2012. Plan de atención a personas afectadas por enfermedades raras en Andalucía. [ Links ]
2. Logroscino G, Traynor BJ, Hardiman O, Chio'A, Couratier P, Mitchell JD, et al. Descriptive epidemiology of amyotrophic lateral sclerosis: new evidence and unsolved issues. J. Neurol Neurosurg Psychiatry 2008;79:6-11. [ Links ]
3. Brooks BR. El Escorial World Federation of Neurology criteria for the diagnosis of amyotrophic lateral sclerosis. Subcommittee on neuron diseases/amyotrophic lateral sclerosis of the World Federation of Neurology Research Group on neuromuscular diseases and the El Escorial "clinical limits of amyotrophic lateral sclerosis" workshop contributors. J Neurol Sci 1994; 124: 96-107. [ Links ]
4. Piquet MA, Nutritional approach for patients with amyotrophic lateral sclerosis. Rev Neurol (Paris) 2006;162(Spec No 2):4S177-87. [ Links ]
5. Greenwood DI. Nutrition management of amyotrophic lateral sclerosis. Nutr Clin Pract 2013 Jun;28(3):392-9. doi: 10.1177/0884533613476554. Epub 2013 Mar 6. Review. [ Links ]
6. Salvioni CC, Stanich P, Almeida CS, Oliveira AS. Nutritional care in motor neurone disease/ amyotrophic lateral sclerosis. Arq Neuropsiquiatr 2014 Feb;72(2):157-63. doi: 10.1590/0004-282X20130185. [ Links ]
7. Muscaritoli M, Kushta I, Molfino A, Inghilleri M, Sabatelli M, Rossi Fanelli F. Nutritional and metabolic support in patients with amyotrophic lateral sclerosis. Nutrition 2012 Oct;28(10):959-66. doi: 10.1016/j.nut.2012.01.011. Epub 2012 Jun 5. Review. [ Links ]
8. Bouteloup C, Desport JC, Clavelou P, et al. Hypermetabolism in ALS patients: an early and persistent phenomenon. J Neurol 2009;256:1236-1242. [ Links ]
9. Cameron A, Rosenfeld J. Nutritional issues and supplements in amyotrophic lateral sclerosis and other neurodegenerative disorders. Curr Opin Clin Nutr Metab Care 2002;5:631-43. [ Links ]
10. Marín B. Desport JC, Kajeu P. Alteration of nutritional status at diagnosis is a prognostic factor for survival of amyotropohic sclerosis patients. J Neurol Neurosurg Psychiatry 2011; 82: 628-34. [ Links ]
11. Desport JC, Preux PM, Truong CT, et al. Nutritional assessment and survival in ALS patients. Amyotroph Lateral Scler Other Motor Neuron Disord 2000;1:91-96. [ Links ]
12. Spataro R, Ficano L, Piccoli F, La Bella V. Percutaneous endoscopic gastrostomy in amyotrophic lateral sclerosis: effect on survival. J Neurol Sci 2011; 304(1-2):44-18. [ Links ]
13. López JJ, Ballesteros MD, Vázquez F y cols. Efecto de soporte nutricional sobre la supervivencia en pacientes con esclerosis lateral amiotrófica. Nutr Hosp 2011; 26 (3): 515-21. [ Links ]
14. Köner S, Hendricks M, Kollewe K, et al. Weight loss, dysphagia and supplement intake in patients with amyotrophic lateral sclerosis (ALS): impact on quality of life and a therapeutic options. BMC Neurology 2013, 13:84. [ Links ]
15. Miller RG, Jackson CE, Kasarskis EJ, et al.; Quality Standards Subcommittee of the American Academy of Neurology. Practice parameter update: the care of the patient with amyotrophic lateral sclerosis: drug, nutritional, and respiratory therapies (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2009 Oct 13;73(15):1218-26. doi: 10.1212/WNL.0b013e3181bc0141. Review. Erratum in: Neurology 2010 Mar 2;74(9):781. Neurology 2009 Dec 15;73(24):2134. [ Links ]
16. EFNS Task Force on Diagnosis and Management of Amyotrophic Lateral Sclerosis:, Andersen PM, Abrahams S, Borasio GD, de Carvalho M, Chio A, Van Damme P, Hardiman O, Kollewe K, Morrison KE, Petri S, Pradat PF, Silani V, Tomik B, Wasner M, Weber M. EFNS guidelines on the clinical management of amyotrophic lateral sclerosis (MALS)--revised report of an EFNS task force. Eur J Neurol 2012 Mar;19(3):360-75. doi: 10.1111/j.1468-1331.2011.03501.x. Epub 2011 Sep 14. [ Links ]
17. Lo Coco D, Marchese S, Pesco MC, La Bella V, Piccoli F, Lo Coco A. Noninvasive positive-pressure ventilation in ALS: predictors of tolerance and survival. Neurology 2006 Sep 12;67(5):761-5. Epub 2006 Aug 9. [ Links ]
18. Bourke SC, Tomlinson M, Williams TL, Bullock RE, Shaw PJ, Gibson GJ. Effects of non-invasive ventilation on survival and quality of life in patients with amyotrophic lateral sclerosis: a randomised controlled trial. Lancet Neurol 2006;5(2):140-47. [ Links ]
19. Chiö A, Bottacchi E, Buffa C, Mutani R, Mora G; PARALS. Positive effects of tertiary centres for amyotrophic lateral sclerosis on outcome and use of hospital facilities. J Neurol Neurosurg Psychiatry 2006 Aug;77(8):948-50. Epub 2006 Apr 13. [ Links ]
20. Rodríguez JF, Oreja C, Sanz I. Evolución de pacientes con esclerosis lateral amiotrófica atendidos en una unidad multidisciplinar. Neurología 2011; 26 (8): 450-60. [ Links ]
21. Ramírez Puerta R, Yuste Ossorio E, Narbona Galdó S, et al.; Esclerosis lateral amiotrófica; complicaciones gastrointestinales en nutrición enteral domiciliaria. Nutr Hosp 2013;28(6):2014-2020. [ Links ]
22. Gómez C, Cos A, García PP y cols. Grupo NADYA-SENPE. Complicaciones de la nutrición enteral domiciliaria. Resultado de estudio multicéntrico. Nutr Hosp 2003; 18: 167-173. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Carmen Tenorio Jiménez.
Avenida Menéndez Pidal s/n.
CP 14004 Córdoba (Córdoba).
E-mail: carmentenoriojimenez@hotmail.com
Recibido: 24-VII-2014.
Aceptado: 6-IX-2014.