INTRODUCCIÓN
La nutrición parenteral (NP) consiste en el aporte de nutrientes directamente al torrente circulatorio por vía intravenosa, a través de una vena central o periférica. Está indicada en aquellas situaciones en las que la alimentación oral o enteral es imposible, insuficiente, está contraindicada y el paciente sufre o puede sufrir un estado de desnutrición.
La desnutrición se asocia a un mayor número de complicaciones para el paciente, ocasionando un aumento de la necesidad de recursos médicos y un incremento de la inversión económica 1. Los pacientes desnutridos presentan un peor estado funcional por disminución de la masa muscular, y una disminución de la respuesta inmunitaria, lo que ocasiona un aumento de las complicaciones y una estancia hospitalaria más prolongada 2.
La NP es una terapia no exenta de complicaciones, tales como desequilibrios electrolíticos, hiperglucemia, hipertrigliceridemia, afectación hepatobiliar, complicaciones infecciosas y mecánicas asociadas al catéter venoso 3. Sin embargo, estudios recientes indican que la mayoría de las muertes acontecidas en pacientes con tratamiento de nutrición parenteral domiciliaria (NPD) estuvieron relacionadas con la enfermedad subyacente y no por una complicación en la administración de la NPD 4.
En los últimos años, ha habido un progreso en la industria farmacéutica (desarrollo de formulaciones nutricionales, catéteres) y en los sistemas sanitarios (equipos de soporte nutricionales muy especializados, mayor capacidad de seguimiento de los pacientes en el domicilio y mayor experiencia) que, junto con el desarrollo de nuevos equipos de asistencia domiciliaria (de hospitalización a domicilio y cuidados paliativos, entre otros), han puesto los medios necesarios para que estos pacientes puedan recibir NPD sin necesidad de aislarlos de su ambiente social y de asumir innecesariamente costosas hospitalizaciones 5,6.
La NPD consiste en la administración de soluciones de nutrición parenteral en el propio domicilio del enfermo, lo que permite a los pacientes estar en su entorno con mayor libertad de horarios, rodeados de su familia y de la confortabilidad de su hogar, mejorando su calidad de vida 7. Además, en ocasiones, cuando el estado funcional del paciente lo permite, se consigue incorporar al paciente a su vida social y laboral 8.
El coste de la NPD no está bien establecido en España. Por ello, el principal objetivo de este proyecto estudio fue estimar los costes directos asociados al manejo de los pacientes que requieren NPD en España, basado en los datos de los Registros de NPD, elaborados por el Grupo NADYA-SENPE (Nutrición Artificial Domiciliaria Y Ambulatoria - Sociedad Española de Nutrición Parenteral y Enteral).
MÉTODOS
DISEÑO DEL ANÁLISIS
El presente análisis del coste de la NPD incluyó una descripción previa de la evolución de los diferentes parámetros clínicos relacionados con el manejo de los pacientes que requieren NPD, desde el año 2007 hasta el 2014. Dicha evolución se obtuvo a través de los Registros de NPD en España en esos años, elaborados por el Grupo NADYA-SENPE 7-11.
El registro de pacientes se realiza a través de la página web del grupo NADYA. Cada Unidad de Nutrición Clínica tiene acceso al registro mediante una clave de acceso y contraseña individualizada que le permite introducir nuevos datos y visualizar los datos acumulados de su propio centro.
POBLACIÓN DE REFERENCIA
El análisis consistió en una revisión de los registros de NPD en España, desde el año 2007 hasta el 2014, incluyendo una estimación del consumo de NPD y de su correspondiente coste. La población del análisis se compuso de pacientes registrados con tratamiento de NPD, desde el 1 de enero al 31 de diciembre de cada año evaluado, pertenecientes a los diversos centros españoles que colaboran en el registro.
VARIABLES
Dentro de los parámetros clínicos, se analizó la siguiente información para los años 2007-2014: número de pacientes que requerían NPD en dicho año, número de episodios por paciente por los que se les administró NPD, duración media de dichos episodios al año, las diferentes vías de acceso por las cuales se administró la NPD y la tasa de complicaciones debidas a la administración de la NPD (Tabla I).
COSTES
En este análisis se han incluido los siguientes costes: coste de las bolsas de NP administradas (bolsas elaboradas en el Servicio de Farmacia, bolsas tricamerales listas para usar y bolsas elaboradas por una empresa farmacéutica externa -catering-), coste de las diferentes vías de acceso venoso (catéteres tunelizados, reservorios y otras vías) y coste de las diferentes complicaciones sufridas debido a la NPD (metabólicas, mecánicas y sépticas).
No se ha considerado ningún otro coste sanitario asociado al manejo de los pacientes, como costes de ingreso hospitalario, pruebas o visitas médicas debido a la dificultad para obtener datos homogéneos. Tampoco se han tenido en cuenta los costes indirectos derivados de gastos de personal o instalaciones, ni los debidos a la enfermedad de base.
El coste de la NPD se calculó en función del tipo de enfermedad de base que requería NPD: patología benigna (definida como toda enfermedad no neoplásica activa) y maligna (definida como enfermedad neoplásica activa).
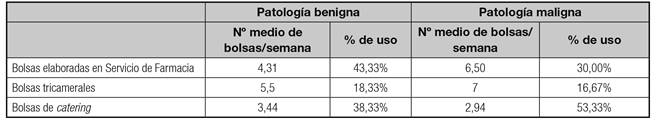
El coste anual promedio se estimó a partir de los datos obtenidos por cada uno de los miembros del panel, evaluando una muestra de los pacientes con NPD. Para ello, se tuvo en cuenta el número de bolsas semanales y la duración media del episodio, así como el tipo de bolsas de NP empleadas (Tabla II).
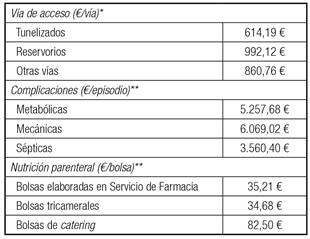
El coste de los diferentes catéteres se obtuvo de la base de datos de costes sanitarios eSalud 12. Para estimar el coste de las complicaciones, se utilizaron costes medios de los grupos relacionados por el diagnóstico (GRD) 13. Los GRD constituyen un sistema de clasificación de pacientes que permite clasificar a los pacientes en grupos clínicamente similares y con consumo similar de recursos sanitarios. Para el coste de las complicaciones metabólicas, se utilizó un promedio de los costes de los GRD 296 (trastornos nutricionales y metabólicos misceláneos, edad mayor de 17 años con complicaciones), GRD 557 (trastornos hepatobiliares y de páncreas con complicación o comorbilidad mayor) y GRD 566 (trastornos endocrinos, nutricionales o metabólicos, excepto trastornos de la ingesta o fibrosis quística con complicación o comorbilidad mayor). Para el coste de las complicaciones sépticas se utilizó el coste del GRD 452 (complicaciones de tratamiento con complicación o comorbilidad). Para el coste de las complicaciones mecánicas se utilizó un promedio de los costes de los GRD 452 (complicaciones de tratamiento con complicación o comorbilidad) y 898 (infecciones y parasitosis con procedimiento quirúrgico).
En la tabla III se especifican los costes unitarios de los recursos incluidos en el análisis. Todos los costes incluidos en el análisis se expresan en euros (€) del año 2015.
ANÁLISIS ESTADÍSTICO
Los análisis estadísticos se desarrollaron con el programa Microsoft Excel 2013. El análisis descriptivo de los parámetros clínicos se realizó mediante gráficos de evolución de los datos del Registro NADYA a lo largo de los años 2007-2014. Las variables continuas se analizaron a partir de datos medios y tasas/año. Para la descripción de variables categóricas se utilizó el número o el porcentaje. Para el análisis de costes se utilizó la media de los diferentes costes unitarios incluidos.
RESULTADOS
VARIABLES CLÍNICAS
Según los datos del Registro NADYA (Tabla I), la población analizada incluyó un total de 133 pacientes que recibieron NPD en el año 2007, dato que ha ido en aumento hasta llegar a los 220 pacientes en el año 2014.
También se analizó la evolución del número medio de episodios que sufrió un paciente promedio al año. El número medio osciló entre 1 y 2 episodios, siendo el 2010, el año en el que hubo más episodios por paciente (1,7 episodios por paciente), y el año 2011, el que menos (1,1 episodios por paciente).
La duración media de los episodios disminuye con los años. En el año 2007, un episodio duraba una media de 323 días, sin embargo, en el año 2014, descendió 120 días (202,8 días por episodio).
El Registro NADYA también obtuvo información acerca de las vías de acceso por las cuales se administraba la NPD. Se observó que en los primeros años, el catéter tunelizado fue la opción más utilizada (en el 60%, 69%, 60% y 69% de los casos para los años 2007, 2008, 2009 y 2010, respectivamente). Sin embargo, a partir del año 2011, dicho porcentaje comienza a descender hasta llegar a un 46% en el año 2014. El porcentaje de pacientes que utilizaban otras vías -entre los que se encuentra el catéter venoso central de inserción periférica (PICC)-, fue incrementándose, desde un 4% en 2007, a un 26% en 2014. El porcentaje de utilización de catéter con reservorio se mantiene constante a lo largo de los años, oscilando entre el 20 y el 30% de pacientes.
La tasa de complicaciones debidas a la NPD también fue registrada por el grupo NADYA. Las complicaciones sépticas fueron las más comunes, seguidas de las metabólicas y, por último, las mecánicas. Sin embargo, la tasa por paciente y año, para los tres tipos de complicaciones, fue baja (0,18, 0,07 y 0,05 para las sépticas, metabólicas y mecánicas, respectivamente).
COSTES DE LA NPD EN FUNCIÓN DEL TIPO DE PATOLOGÍA
El análisis de costes se desarrolló tomando como referencia dos perfiles de pacientes en función del tipo de patología: benigna o maligna.
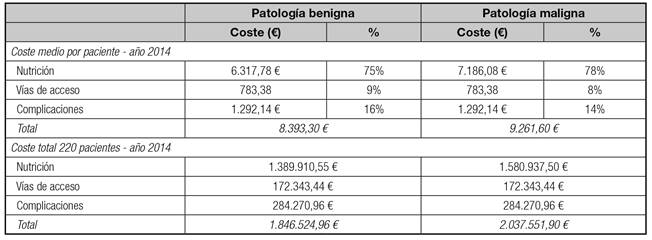
El coste directo anual medio de un paciente con patología benigna que requiere NPD se estimó en 8.393,30 €. Para un paciente con patología maligna, ascendió a 9.261,60 € (Tabla IV).
Considerando que, para el año 2014, un total de 220 pacientes requirieron NPD, se estimó un coste total anual de 1.846.524,96 €, para el caso de pacientes con patologías benignas, incluyendo los 1.389.910,55 € debidos a la fórmula de la NPD. Para el caso de los pacientes con patologías malignas, el coste total anual, para el mismo número de pacientes, ascendería a 2.037.551,90 €, incluyendo 1.580.937,50 € debidos a la fórmula de la NPD.
Tanto en los pacientes con patologías benignas como en los que padecían patologías malignas, la NP fue el recurso que más contribuyó a dicho coste, suponiendo un 75% y un 78% del coste total considerado en este estudio, respectivamente. Por el contrario, los catéteres venosos, fueron las que supusieron un menor coste (un 9% y un 8% sobre el coste total, para patologías benignas y malignas, respectivamente).
DISCUSIÓN
La NPD está indicada en aquellos pacientes, tanto niños como adultos, que no tienen un tracto gastrointestinal funcional o accesible, o bien, en los que son incapaces de mantener un estado nutricional adecuado con alimentación natural y artificial, oral o enteral, y no necesitan estar ingresados en un centro hospitalario para asegurar sus cuidados 14. Las ventajas que esto implica son: una mayor comodidad para el paciente y su reinserción en su entorno familiar y social, la oportunidad de mejora de la gestión de camas hospitalarias para el sistema sanitario y, por consecuencia, una mayor eficiencia económica. Todo ello hace prever que esta modalidad de NP se convierta progresivamente en una práctica consolidada en muchos hospitales de referencia 15.
En España, desde el año 1992, el registro del grupo NADYA de la Sociedad Española de Nutrición Enteral y Parenteral trata de cuantificar la dimensión de la Nutrición Artificial Domiciliaria, tipificar la distribución por patologías, vías y modos de infusión, además de otras variables. A pesar de las ventajas clínicas demostradas para los pacientes, y económicas para el Sistema Nacional de Salud, de sus informes se podría deducir que la NP en España es menos utilizada que en otros países de la Unión Europea 16-19. No obstante, es posible que exista un registro sesgado, ya que no todas las Unidades participan, al tratarse de un registro voluntario.
Sin embargo, tal y como se observa en dichos registros, el empleo de la NPD va en progresivo aumento. Esto es debido a diferentes avances como las bolsas listas para usar, los servicios de catering y la mayor experiencia de los diferentes equipos sanitarios 15. Otra causa de la progresión del uso de la NPD en España es el mayor número de pacientes considerados como candidatos a recibir NPD, sobre todo, pacientes oncológicos, que conforman el grupo patológico más numeroso desde 2003 9.
A pesar de sus múltiples ventajas, es una técnica no exenta de complicaciones, aunque la mayoría de ellas están relacionadas con la enfermedad de base del paciente. Por ello, hay que ser estrictos en sus indicaciones y valorar en todo momento los beneficios y riesgos de su utilización, ya que suponen una elevada carga asistencial y un coste económico considerable 20. La incidencia de las complicaciones relacionadas con la NPD ha ido disminuyendo con el tiempo debido a la existencia de un equipo multidisciplinar experimentado, de protocolos de seguimiento clínico y analíticos y del empleo de técnicas de sellado del catéter con antisépticos o antimicrobianos, convirtiendo la NPD en un tratamiento cada vez más seguro 21-23. La estandarización de las bolsas de nutrición no modifica la calidad de la NP 3, y contribuye a minimizar el número de complicaciones, reduciendo el riesgo de error de cálculo para su formulación, así como el riesgo de infección, ya que se reduce el manejo de los constituyentes de la solución 6,24,25.
Según los resultados obtenidos en este análisis de costes directos, la NPD es un tratamiento que cuesta entre 8.393,30 € y 9.261,60 € por paciente y año, incluyendo los gastos atribuibles a las posibles complicaciones de la NPD. Diversos estudios en diferentes países examinaron diferentes aspectos económicos del tratamiento con NPD 26-34. La mayoría de estos estudios incluye únicamente costes directos sanitarios. Solo en algunos de ellos se incluyen los gastos atribuibles a las complicaciones de la NPD que requieren la hospitalización del paciente. Según sus resultados, el coste anual por paciente es de 75.000-150.000 $ en EE. UU. y 25.000 £ en Reino Unido, costes más altos que los obtenidos para España. Dichos estudios también muestran que la NPD es un 65-80% más barata que el tratamiento con nutrición parenteral en el hospital.
El presente análisis no está exento de una serie de limitaciones que deben tenerse en cuenta a la hora de interpretar los resultados obtenidos. Dado que los registros nacionales se realizan de forma voluntaria al no existir ninguna normativa que obligue a su declaración 35, es posible que las cifras registradas sean datos que infravaloren la realidad. De igual modo, al basarnos en la información reflejada en dichos registros, solo se han podido incluir costes directos sanitarios. Además, los resultados del presente análisis no conllevan la misma calidad metodológica que los que se podrían obtener mediante un estudio prospectivo, diseñado específicamente para recoger los recursos y costes asociados al manejo de los pacientes que requieren NPD. Sin embargo, sí que puede considerarse como una herramienta útil que proporciona información sobre la tendencia de costes para estos pacientes.
A pesar de las limitaciones descritas, conocer la magnitud y características de la NPD en España, puede facilitar la toma de decisiones, tanto clínicas como de gestión.
CONCLUSIONES
La NPD es un tratamiento que en España tiene unos costes directos que oscilan entre 8.393,30 € (patología benigna) y 9.261,60 € (patología maligna) por paciente y año, incluyendo únicamente los gastos atribuibles a las formulaciones de NPD, los catéteres venosos y el manejo de las complicaciones de la NPD.