Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.34 no.4 Madrid jul./ago. 2017
https://dx.doi.org/10.20960/nh.748
TRABAJO ORIGINAL / Nutrición artificial
Estado nutricional y funcional en pacientes con enfermedad pulmonar obstructiva crónica: efectos de la suplementación nutricional oral (estudio OFOS)
Nutritional and functional state of patients with chronic obstructive pulmonary disease: effects of oral nutritional supplementation (OFOS study)
M.a Pilar Benito Martínez1, Jorge E. La Serna Infantes1, Marta Guarro Riba2, Mireia Morera Inglés2, Diego M. Camere Colarossi1 y Marco A. Camere Torrealva1
1Instituto de Enfermedades Respiratorias. Clínica San Gabriel. Complejo Hospitalario San Pablo. Lima, Perú.
2Dirección Médica Laboratorios Ordesa. Sant Boi de Llobregat, Barcelona
Conflicto de intereses: Marta Guarro y Mireia Morera son empleadas de Laboratorios Ordesa S.L.
Registro ClinTrials. Gov: NCT02102009.
Dirección para correspondencia
RESUMEN
Introducción: la pérdida de peso y la desnutrición se asocian a un peor pronóstico de la enfermedad pulmonar obstructiva crónica (EPOC).
Objetivo: el objetivo del estudio OFOS fue valorar la eficacia y tolerabilidad de una nueva fórmula nutricional oral en adultos con EPOC con pérdida de peso o desnutrición.
Métodos: estudio prospectivo, unicéntrico, aleatorizado, abierto y controlado realizado en Lima (Perú). Se incluyeron 99 pacientes ambulatorios de ambos sexos (control [GC]: 49; suplemento [GS]: 50), entre 18 y 80 años con diagnóstico de EPOC y con pérdida involuntaria de peso en los últimos meses o desnutrición. Se evaluaron variables nutricionales, funcionales y de calidad de vida (CV) durante un periodo de intervención de tres meses.
Resultados: a los tres meses, hubo un incremento del índice de masa corporal (IMC) y del índice de masa libre de grasa (IMLG) significativamente superior en el GS: IMC: 5,3% vs. 2,9%, p < 0,001; IMLG: 3,2% vs. 1,9%, p = 0,019. El GS mostró una reducción de casos con IMC < 21 kg/m2 equivalente al 69% vs. 33% en el GC (p = 0,004). Las variables funcionales mostraron una tendencia a la mejoría favorable al GS, siendo significativa para la fuerza de la mano (hand-grip test) en el subgrupo de pacientes con IMLG bajo (p = 0,001). Todas las variables estudiadas de CV mejoraron significativamente en ambos grupos (p < 0,001).
Conclusiones: la suplementación oral durante tres meses con una nueva fórmula completa, polimérica y normocalórica fue bien tolerada y eficaz para el soporte nutricional de pacientes diagnosticados de EPOC con pérdida de peso o desnutrición.
Palabras clave: Soporte nutricional. EPOC. Pérdida de peso. Malnutrición. Fuerza muscular. Calidad de vida.
ABSTRACT
Introduction: Weight loss and malnutrition are associated with a worse prognosis of chronic obstructive pulmonary disease (COPD).
Objective: The main objective of the OFOS study was to assess the efficacy and tolerability of a new nutritional oral formula in adults with COPD with weight loss or malnutrition.
Methods: Prospective, single-centre, randomized, open-label and controlled trial conducted in Lima (Peru). A total of 99 outpatients of both sexes were included (control [GC]: 49; supplement [GS]: 50), aged from 18 to 80 years old, who had been diagnosed with COPD and that suffered from malnutrition or involuntary weight loss during the last months. Nutritional, functional and quality of life (QoL) variables were evaluated during a three-month intervention.
Results: At three months, there was an increase of body mass index (BMI) and fat free mass index (FFMI) significantly higher in the GS: IMC 5.3% vs 2.9%, p < 0.001; FFMI 3.2% vs 1.9%, p = 0.019. The GS showed a reduction of cases with BMI < 21 kg/m2 equivalent to 69% vs 33% in the GC (p = 0.004). Functional variables showed a favourable improvement trend in GS, being significant for the hand-grip test in the subgroup of patients with low FFMI (p = 0.001). All QoL studied variables significantly improved in both groups (p < 0.001).
Conclusions: Oral supplementation with a complete, polymeric and normocaloric new nutritional formula for three months was well tolerated and effective for the nutritional support of patients diagnosed with COPD with weight loss or malnutrition.
Key words: Nutritional support. COPD. Weight loss. Malnutrition. Muscle strength. Quality of life.
Introducción
La afectación del estado nutricional es una de las comorbilidades más comunes del paciente con patologías pulmonares crónicas. Se estima que entre el 10% y el 45% de los pacientes con enfermedad pulmonar obstructiva crónica (EPOC) presentan desnutrición (1), incidencia que puede alcanzar el 63% en pacientes con EPOC moderada-severa que requieren ingresar en un programa de rehabilitación pulmonar (2).
La pérdida de peso y desnutrición están asociadas a un peor pronóstico de la enfermedad, independientemente de la severidad de la afectación de la función pulmonar, y a un mayor riesgo de mortalidad (3). Actualmente se desconocen los mecanismos exactos que conllevan esta marcada pérdida de peso en pacientes con EPOC, por lo que se acepta un probable origen multifactorial derivado de la combinación de distintos factores como el desequilibrio energético (por aumento del gasto energético basal/GEB) (4) y el desequilibrio entre síntesis y catabolismo proteico (2), una ingesta alimentaria reducida (2), la atrofia muscular por baja actividad física (5), el estado de inflamación sistémica y estrés oxidativo (4), así como otros factores más específicos como la susceptibilidad genética (6), la insuficiencia hormonal (4), las exacerbaciones agudas, las complicaciones infecciosas y el efecto térmico de algunos fármacos como los corticoides (7).
Existe una correlación directa entre el índice de masa corporal (IMC) y la supervivencia en EPOC, siendo 21 kg/m2 (2) el punto de corte por debajo del cual se ha observado que la mortalidad aumenta significativamente (2,4). Sin embargo, la determinación del IMC subestima los pacientes en riesgo nutricional y no refleja los cambios en la composición corporal propios de los casos más severos de la enfermedad, por lo que la evaluación de otros parámetros más específicos como la pérdida ponderal en el tiempo (8) y la estimación de la masa libre de grasa (MLG) resultan de especial importancia. Este último, considerado como parámetro indirecto para valorar la reducción de masa muscular, se ha establecido como un factor de riesgo independiente de morbimortalidad (2,9-11). Generalmente, se considera que existe baja masa muscular cuando el índice de masa libre de grasa (IMLG) es menor de 15 kg/m2 en mujeres y de 16 kg/m2 en varones (2).
Resultados de distintos estudios sugieren que incluso pequeñas mejoras en el estado nutricional de los pacientes con EPOC pueden mejorar la fuerza y resistencia de los músculos respiratorios, la respuesta al ejercicio o la calidad de vida (4). Entre los métodos utilizados para mejorar el estado nutricional de estos pacientes, hay evidencia sobre distintas medidas farmacológicas y suplementarias como el uso de estimulantes del apetito y complementos alimenticios (1,9). Dada la relevancia de la composición corporal en la EPOC, guías de referencia internacional como las de la American Thoracic Society (ATS) y la European Respiratory Society (ERS) recomiendan el apoyo nutricional en pacientes en programas de rehabilitación pulmonar mediante el seguimiento de un plan de alimentación y/o suplementación durante al menos 12 semanas.
El uso de otro tipo de medidas, como el empleo de suplementos con omega-3, orientadas al tratamiento de mecanismos subyacentes como la inflamación crónica se propone a partir de la evidencia sobre un posible efecto beneficioso en la reducción de la respuesta inflamatoria en estos pacientes (12,13). Otras intervenciones, como la ingesta de fibra de distintos orígenes, sugieren cierta asociación con una reducción de marcadores específicos de inflamación (14) elevados en la EPOC (15) y una reducción del riesgo de nuevos diagnósticos de esta patología en estudios de población general (16).
Así pues, se plantea un estudio con el objetivo de valorar la eficacia y tolerabilidad de una nueva fórmula nutricional completa polimérica, normocalórica (1,09 kcal/ml) y normoproteica (15% valor calórico total [VCT]), enriquecida con prebióticos (fructooligosacáridos [FOS]) y ácidos grasos omega-3 (α-linolénico y DHA) y administrada diariamente durante tres meses en adultos con EPOC con pérdida involuntaria de peso en los últimos meses o desnutrición.
Métodos
Estudio prospectivo, unicéntrico, aleatorizado, abierto y controlado en el que se incluyeron, de forma consecutiva, pacientes de ambos sexos de entre 18 y 80 años con diagnóstico de EPOC que consultaron de forma ambulatoria en la Clínica San Gabriel (Complejo Hospitalario San Pablo) de Lima, Perú, entre marzo de 2014 y abril de 2015. El diagnóstico de EPOC fue clínico (confirmado por espirometría) e incluyó casos de bronquiectasias, secuelas específicas de tuberculosis, fibrotórax, enfermedad pulmonar intersticial difusa, bronquitis crónica, enfisema y/o asma. La severidad de la EPOC se clasificó según los criterios de la Global Initiative for Chronic Lung Disease (GOLD): leve (volumen espiratorio forzado en el primer segundo (VEF1) ≥ 80%), moderada (50% ≤VEF1< 80%), grave (30% ≤VEF1< 50%) y muy grave (VEF1 < 30%) (17).
Instituto Nacional de Salud de Perú (INS, Ministerio de Salud), el Comité Institucional de Ética en Investigación PRISMA y el Comité de Ética Institucional del Complejo Hospitalario San Pablo. Todos los pacientes fueron informados del desarrollo del estudio y firmaron el consentimiento informado. El estudio se realizó de acuerdo con la Declaración de Helsinki y se registró en el sitio web ClinicalTrials.gov (Ref: NCT02102009).
Los criterios de inclusión exigían el cumplimiento de los valores establecidos para intervención nutricional por desnutrición y/o riesgo nutricional específicos (2): IMC < 21 kg/m2 (o < 23 kg/m2 en pacientes ≥ 65 años); pérdida involuntaria de peso: > 10% en los últimos seis meses o > 5% en el último mes; o IMLG < 15 kg/m2 en mujeres y < 16 kg/m2 en varones. Se excluyeron pacientes clínicamente inestables, con indicación de otros suplementos nutricionales o nutrición parenteral y/o con otras patologías como tuberculosis pulmonar activa, insuficiencia respiratoria aguda y/o inmunodepresión conocida.
INTERVENCIÓN NUTRICIONAL
El producto de estudio es una fórmula de nutrición enteral completa polimérica, normocalórica (1,09 kcal/ml) y normoproteica (15% VCT) en formato polvo y de sabor vainilla (Vitafos® Vainilla (Perú)/ Fontactive® Forte (España) (Laboratorios Ordesa S.L.); cada 100 g de producto contienen 16,5 g de lactoproteínas (100% séricas), 16,5 g de grasas (33% VCT) mezcla de aceites vegetales y de pescado, fuente de ácidos grasos esenciales omega-6, omega-3 y DHA (7,3 mg/100 g), 57,7 g de carbohidratos (maltodextrina y sacarosa), fibra prebiótica FOS (5 g), vitaminas y minerales. Una ración de producto (57 g en 200 ml de agua) aporta 258 kcal, 9,4 g de proteínas, 4,2 g de DHA, 3 g de FOS y alrededor del 25-30% de los valores de referencia de nutrientes (VRN) de la mayoría de vitaminas y minerales.
VARIABLES DE ESTUDIO
Los pacientes se distribuyeron de forma aleatoria en dos grupos: el grupo que recibió el suplemento nutricional (GS) y el grupo control (GC). La aleatorización se realizó mediante una lista generada por ordenador, asignando un código al paciente de forma consecutiva. El investigador comunicaba por teléfono el código del nuevo paciente a Peruvian Clinical Research S.A.C. (Organización de Investigación por Contrato), que a su vez le indicaba a qué grupo debía asignarse según el listado de aleatorización. Ambos grupos recibieron consejos dietéticos y rehabilitación física, según la práctica clínica habitual del centro. Tras el cálculo del gasto energético total (GET) y la valoración del registro de consumo energético de 24 horas, se determinó la cantidad diaria de producto necesaria para cubrir la diferencia entre la ingesta calórica real y el GET en los pacientes del GS.
En la valoración basal se registraron datos sobre el perfil del paciente (edad, sexo, factores de riesgo de desnutrición, actividad física, diagnóstico base/tipo/severidad de EPOC) y aquellos relacionados con su estado nutricional (peso, talla, pliegues cutáneos), la dieta habitual previa a la inclusión en el estudio, la estimación de los requerimientos energéticos diarios (gasto energético total [GET]) (18), porcentaje de cobertura de los mismos y pérdida de peso involuntaria durante los seis meses y un mes previos a la inclusión. La evaluación del IMLG se realizó por antropometría y cálculo según fórmulas de Durnin-Womersley (1974) y Siri (1961) (19). Se clasificó a los pacientes siguiendo los criterios propuestos en Casanova y cols. 2009: "caquexia" (IMC < 21 + IMLG < 17 para los varones y < 14 para las mujeres); "sarcopenia" (IMC ≥ 21 + IMLG < 17 para los varones y < 14 para las mujeres); "semidesnutrición" (IMC < 21 + IMLG ≥ 17 para los varones y ≥ 14 para las mujeres) (4). El GET se calculó mediante la corrección del gasto energético en reposo (GER) según Harris-Benedict (19), un factor de actividad física (FA), uno de estrés (FE) y de temperatura (T): GET = GER x FA x FE x T, siendo FA igual a: reposo en cama = 1; movimiento en la cama = 1,2; deambulación = 1,3; FE se estableció en 1,3 (20) y T igual a: 37o = 1; 38o = 1,2; 39o = 1,3.
Se valoró la función respiratoria mediante espirometría (Spirobank G®) reportada comoVEF1 y la función muscular a partir del hand-grip strength test (prueba de fuerza de la mano medida) y del 6-minutes walking distance/6MWD (prueba de marcha de seis minutos), según las guías de la ATS (2).
Para evaluar el impacto del soporte nutricional en la calidad de vida (CV) se utilizó el Cuestionario Respiratorio de Saint George (CRSG, versión española) (21), un instrumento específico y autoadministrado que, con un rango de puntuación de 0 a 100, cuantifica el grado de afectación de tres dimensiones: síntomas (tipo y frecuencia), actividad (limitación de actividades físicas por la enfermedad respiratoria), e impacto (social, laboral, psicológico y de control de la salud) (21).
SEGUIMIENTO
Los pacientes se controlaron mensualmente hasta los tres meses, valorando cambios en el peso, IMC e IMLG, la incidencia de complicaciones respiratorias e infecciosas, la tolerabilidad del producto y revisión del GET para adecuar el aporte de suplemento nutricional en caso necesario. Además, se evaluó la evolución de las pruebas funcionales de espirometría, hand-grip strenght y 6MWD, y la CV. Los pacientes del GS valoraron mediante un diario personal las características organolépticas del producto y su tolerabilidad digestiva.
ANÁLISIS ESTADÍSTICO
Los resultados del análisis descriptivo se presentan en forma de media ± desviación estándar (DE) y rango (variables cuantitativas), total de casos y porcentajes (variables cualitativas) con intervalos de confianza del 95% (IC 95%). Los cambios en las puntuaciones de variables principales se describen en forma de porcentaje de cambio respecto a la puntuación previa.
Las comparaciones entre proporciones se llevaron a cabo utilizando pruebas Chi-cuadrado de Pearson y las diferencias entre variables numéricas se estudiaron mediante ANOVA de un factor y t de Student. Las diferencias entre las distintas dimensiones de la escala de CV se analizaron con la prueba de Wilcoxon. Todos los análisis estadísticos han sido realizados con el software SPSS (v22.0) para Windows.
Resultados
Se incluyó un total de 99 casos (49 en el GC y 50 en el GS), de los cuales se registraron cuatro abandonos en la primera visita de control y ocho a los tres meses, todos del GS. En todas las discontinuaciones los individuos alegaron motivos personales (trabajo, viaje, etc.), sin reportar efectos adversos relacionados con el tratamiento recibido en el estudio. La población de estudio presentó una media de edad de 42,3 ± 19,2 años y fue principalmente integrada por mujeres (72,6%). La proporción de fumadores, fue del 12,6%. En la mayoría de los casos, la severidad de la EPOC fue moderada (56,3%), con una baja proporción de casos clasificados como graves (10,3%).
La mayoría de características de ambos grupos, tales como la distribución por género, proporción de fumadores y medidas antropométricas, fueron comparables, si bien se observaron diferencias en la edad, significativamente menor en el GC (p < 0,001), y una mayor ingesta calórica en los pacientes de este grupo (p < 0,001). La distribución de cada uno de los tipos de patología pulmonar fue heterogénea, observándose diferencias significativas entre grupos en los porcentajes de pacientes con asma bronquial (67,4% del GC vs. 21,1% del GS), enfisema pulmonar (0% GC vs. 15,8% GS) y bronquitis obstructiva crónica (14,3% GC vs. 34,2% GS). Este desequilibrio se tradujo en diferencias próximas a la significación estadística en cuanto a la distribución de la severidad de la EPOC entre grupos de tratamiento (p = 0,098), donde el GS acumuló el 79% de los pacientes en las categorías moderada-grave vs. 57,2% en el GC (Tabla I).
RESULTADOS NUTRICIONALES
Ambos grupos mostraron valores medios basales similares de IMC, IMLG y de pérdida de peso durante los seis meses y cuatro semanas previos al inicio del estudio (media global de pérdida de peso de 7,1 ± 1,2 kg y 2,3 ± 1,4 kg, respectivamente). Del mismo modo, la distribución entre grupos de los pacientes con IMC < 21 kg/m2 fue homogénea: 73,5% en el GC y 73,9% en el GS. En el GS, la media de raciones de suplemento ingeridas por día fue de 2,76 ± 1,32 al primer mes y de 2,63 ± 1,06 en el segundo y tercer mes de seguimiento, con un valor energético de 712 ± 340 y 678 ± 273 kcal/día, respectivamente. El GS mostró un incremento significativo de la ingesta energética diaria a los tres meses en comparación con el GC, solo con consejos dietéticos (+76,4% vs. +38,7%; p < 0,001), consiguiendo una media de porcentaje de cobertura de los requerimientos energéticos del 100% a diferencia del GC (100,5 ± 12,7 vs. 95,9 ± 6,3; p = 0,028). Los pacientes que recibieron suplementación mostraron una ganancia ponderal de peso del 5,3% frente al 2,9% en el GC, equivalente a 2,9 kg y 1,5 kg, respectivamente (p < 0,001). Se observó un aumento del IMC y del IMLG en ambos grupos del estudio, con porcentajes superiores en el GS (IMC: 5,3% vs. 2,9%, p < 0,001, e IMLG: 3,2% vs. 1,9%, p = 0,019) (Fig. 1).
Al final del estudio, el GS mostró una reducción de los casos con IMC < 21 kg/m2 equivalente al 69% vs. 33% en el GC; p = 0,004 (Fig. 2), reducción que también se observó al utilizar el punto de corte de IMLG de < 15 kg/m2 en mujeres y < 16 kg/m2 en varones (35,5% menos de casos en el GS vs. el 12,9% en el GC [p = 0,038]).
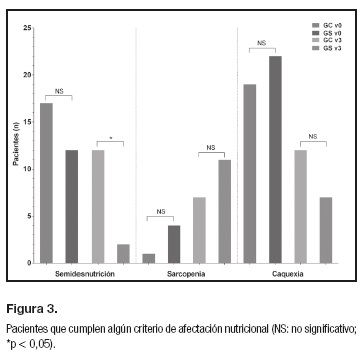
Si bien al inicio del estudio el GC tenía menos casos con afectación nutricional (75,5% vs. 82,6%; OR = 0,65 [0,24-1,78]; p = 0,456), después de recibir el complemento alimenticio durante tres meses el GS era el que presentaba menos de estos casos (63,3% vs. 52,6%; OR = 1,55 [0,65-3,67]; p = 0,382). Se observaron resultados significativos cuando se compararon los pacientes de cada grupo que a los tres meses cumplían criterios de semidesnutrición, siendo casi seis veces más probable encontrar un paciente con tales signos en el GC que en el GS (24,5% vs. 5,3%; OR = 5,84 [1,22-27,94]; p < 0,05). Del mismo modo, se observó una tendencia similar favorable al GS cuando se compararon los pacientes que a los tres meses cumplían criterios de caquexia (24,5% vs. 18,4%; OR = 3,35 [0,87-12,95]; p = 0,086) (Fig. 3).
RESULTADOS FUNCIONALES
A pesar de las diferencias basales, que muestran mejor VEF1 en el GC (p = 0,012), transcurridos los tres meses de suplementación se registraron valores estadísticamente comparables (p = 0,072) entre los pacientes con suplemento (70,1 ± 12,9) y control (76,3 ± 17,8), con una mayor tasa de cambio durante la intervención favorable al GS (4,3% vs. 1,3%, p = 0,490). Por otra parte, el hand-grip strength test o el 6MWT mostraron mejorías desde la inclusión en ambos grupos, con tendencia a observar una mejora más amplia en el GS. Cuando se comparó la evolución de estas variables en el subgrupo de pacientes con IMLG bajo a la inclusión, se observaron diferencias significativas en la mejora del hand-grip test (p = 0,001) y una tendencia a la mejoría en el 6MWD (p = 0,138) favorable al GS (Tabla II).
Calidad de vida
Las comparaciones entre grupos de las puntuaciones basales de CV muestran mayor afectación en el GS, tanto en base a la puntuación global (p = 0,023) como en la del impacto sobre diferentes actividades de la vida diaria (p = 0,039). Si bien esta diferencia se mantuvo a lo largo de los tres meses de estudio, todas las variables estudiadas dentro de esta dimensión mejoraron significativamente en ambos grupos (Tabla III).
VALORACIÓN DEL SUPLEMENTO NUTRICIONAL
En cuanto a la valoración subjetiva del suplemento alimenticio, el 89,1% de los pacientes opinaron que la fórmula les gustó "mucho/bastante", mientras que el resto la calificó como "normal". La tolerabilidad de ambas intervenciones fue buena, observándose cambios mínimos en el número y consistencia de las deposiciones diarias y en la presencia de flatulencias, sin diferencias significativas entre grupos (p = 0,437).
Discusión
En el presente estudio, la suplementación nutricional con una fórmula completa polimérica normocalórica normoproteica con ácidos grasos omega-3 y prebióticos durante tres meses, en pacientes con pérdida de peso o desnutrición diagnosticados de EPOC, demuestra su tolerabilidad y eficacia en la mejoría de los parámetros nutricionales de peso, IMC e IMLG y en variables funcionales como la fuerza de la mano, con resultados significativamente mejores que en el grupo control, que solamente recibió consejos dietéticos y rehabilitación física.
El estudio OFOS es el primer estudio con una muestra tan elevada de pacientes con EPOC desnutridos, formada mayoritariamente por mujeres y por una baja proporción de fumadores/as, difiriendo de lo esperable en estudios con pacientes con EPOC (9). Previamente, otros trabajos habían descrito escenarios parecidos donde la severidad de la EPOC se había relacionado con un mayor grado de desnutrición (22). Además, en Perú, a diferencia de otros países, la EPOC se asocia a la exposición a humo de biocombustibles o al postratamiento de tuberculosis, y no tanto al consumo de tabaco (23). Esta circunstancia podría explicar la baja edad media de la población del estudio, que en países occidentales habitualmente se sitúa por encima de los 60 años (9,24), debido a que la inhalación de humo se produce en los hogares desde edades tempranas, pudiendo provocar una manifestación anticipada de la EPOC en comparación con la que predominantemente se asocia al tabaquismo. Concretamente, Janagath y cols. observaron en áreas rurales de Perú una tasa de prevalencia de EPOC asociada al uso de biocombustibles para cocinar del 2,22%, con un riesgo atribuible poblacional de EPOC debido a la exposición diaria del 55%. La inhalación de humo de biocombustibles se relaciona con las actividades domésticas, dado que en Perú, así como en otros países en vías de desarrollo, es habitual el uso de hornos de leña para cocinar en los hogares (25). Teniendo en cuenta este contexto sociocultural, los más expuestos a esta contaminación doméstica son mujeres y niños, fenómeno que explicaría la elevada proporción de mujeres incluidas en el estudio (25),
Según los resultados nutricionales observados en este estudio, el suplemento utilizado aumentó eficazmente la ingesta energética y ayudó a cubrir los requerimientos energéticos estimados de cada individuo. El aumento de ≥ 2 kg de peso corporal que Schols y cols. relacionaron con la mejora de la supervivencia y que se ha sugerido como objetivo terapéutico en este tipo de pacientes (3,24) fue sobrepasado ampliamente a los tres meses en el grupo estudio. Además, la comparación entre diferencias porcentuales de ganancia de peso sugiere que, si bien ambos grupos mostraron una pérdida similar a las cuatro semanas y seis meses previos a la inclusión, los pacientes que recibieron el suplemento junto con consejos dietéticos y rehabilitación física mostraron una recuperación nutricional superior a la del grupo control. Igualmente, al analizar la evolución de los valores de IMC e IMLG, la tasa de pacientes que consiguieron superar los puntos de corte indicativos de desnutrición y depleción muscular fue significativamente superior en el GS. Curiosamente, esto comportó un aumento de pacientes con sarcopenia en el GS, dato que tiene su explicación en el flujo de pacientes que previamente estaban más graves y cumplían criterios de caquexia, pero consiguieron mejorar su estado nutricional durante el estudio. Estos resultados, junto con la baja edad media y baja proporción de casos con EPOC severa, podrían explicar la baja incidencia de complicaciones durante el estudio.
En cualquier caso, la evolución del número de pacientes con valores de IMC e IMLG indicativos de desnutrición mostró una tendencia a la mejoría en ambos grupos de estudio, si bien en todos los casos los resultados fueron superiores en el GS. Por lo tanto, los resultados de este estudio muestran la importancia de instaurar precozmente en este tipo de pacientes una intervención nutricional que incluya, además de consejos dietéticos y un programa de rehabilitación física, un suplemento nutricional para acelerar la recuperación del estado nutricional.
Las variables funcionales se consideran de suma importancia en la evaluación clínica de la desnutrición; de hecho, se ha sugerido que la fuerza muscular responde más rápidamente a la depleción o recuperación nutricional que las variables antropométricas y, además, se les atribuye cierto valor predictivo, especialmente en el caso del hand-grip test (26). En general, el porcentaje de mejora de la función motora fue siempre superior en el GS, siendo todavía más evidente en los pacientes más desnutridos. Por contra, no se observaron diferencias en la función pulmonar (espirometría), en línea con los resultados mostrados en el metaanálisis de Collins y cols., donde los resultados más significativos se observaron en la función motora (HGT) sin observarse diferencias significativas en la función respiratoria (VEF1), hecho que puede asociarse a la naturaleza irreversible de la patología pulmonar en la EPOC (24).
Si bien en el metaanálisis de Ferreira y cols. se concluyó que la suplementación nutricional puede promover la mejora de la calidad de vida en pacientes con EPOC, en el estudio OFOS solo hemos observado una tendencia a la mejoría difícilmente atribuible al efecto exclusivo del uso del suplemento. Una limitación con la que nos encontramos para estudiar la CV fue la reducción de la muestra disponible para esta variable, dada la especificidad del CRSG para individuos mayores de 40 años.
La principal limitación de nuestro estudio fue que las poblaciones de ambos grupos no eran completamente homogéneas en la visita basal: los pacientes del grupo con suplementación fueron significativamente mayores, siendo la edad uno de los factores más relacionados con la desnutrición (4), y tenían un menor porcentaje de cobertura de requerimientos energéticos a través de la dieta. Además, la distribución del tipo de patología pulmonar tampoco fue homogénea (ningún enfisema en el GC y, sin embargo, dos tercios de los casos con asma en este grupo), hecho que puede explicar las diferencias en los valores de VEF1 y la distancia total obtenida en la prueba 6MWDN, donde el grupo control obtuvo mejores resultados al inicio del estudio. De todos modos, si bien estos factores pueden ocasionar un sesgo en el estudio, debe considerarse que las diferencias basales otorgaban un mejor pronóstico de la enfermedad a los pacientes del grupo control.
El estudio OFOS aporta nuevos datos sobre el impacto de la suplementación nutricional en pacientes EPOC con pérdida involuntaria de peso en los últimos meses o desnutrición, con un producto de composición completa y equilibrada, enriquecido con prebióticos y ácidos grasos omega-3, bien tolerado y aceptado por los pacientes durante los tres meses de intervención. Estos resultados deberían contrastarse en nuevos estudios en poblaciones con grados de desnutrición más severa (IMC < 18,5 kg/m2), así como contemplar periodos de seguimiento más prolongados para poder corroborar si la recuperación nutricional y funcional observada se mantiene en el tiempo.
Bibliografía
1. Hsieh MJ, Yang TM, Tsai YH. Nutritional supplementation in patients with chronic obstructive pulmonary disease. J Formos Med Assoc 2016;15:595-601. [ Links ]
2. American Thoracic Society. Standards for the diagnosis and management of patients with COPD. American Thoracic Society; 2004. [ Links ]
3. Schols AM, Slangen J, Volovics L, Wouters EF. Weight loss is a reversible factor in the prognosis of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998;157:1791-7. [ Links ]
4. Casanova-Macario C, De Torres-Tajes JP, Martín-Palmero MA. EPOC y malnutrición. Arch Bronconeumol 2009;45:31-5. [ Links ]
5. Wagner PD. Possible mechanisms underlying the development of cachexia in COPD. Eur Respir J 2008;31:492-501. [ Links ]
6. Broekhuizen R, Grimble RF, Howell WM, Shale DJ, Creutzberg EC, Wouters EF, et al. Pulmonary cachexia, systemic inflamatory profile, and the interleukin 1-511 single nucleotide polymorphism. Am J Clin Nutr 2005;82:1059-64. [ Links ]
7. Casaburi R, Bhasin S, Cosentino L, Porszasz J, Somfay A, Lewis MI, et al. Effects of testosterone and resistance training in men with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2004;170:870-8. [ Links ]
8. Grupo de trabajo de la guía de práctica clínica sobre Atención Integral al paciente con Enfermedad Pulmonar Obstructiva Crónica (EPOC). Desde la Atención Primaria a la Especializada. Sociedad Española de Medicina de Familia (semFYC) y Sociedad Española de Neumología y Cirugía Torácica (SEPAR); 2010. Disponible en: http://www.guiasalud.es/GPC/GPC_468_EPOC_AP_AE.pdf. [ Links ]
9. Ferreira IM, Brooks D, White J, Goldstein R. Nutritional supplementation for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;12:CD000998. [ Links ]
10. Lou P, Zhu Y, Chen P, Zhang P, Yu J, Zhang N, et al. Prevalence and correlations with depression, anxiety, and other features in outpatients with chronic obstructive pulmonary disease in China: A cross-sectional case control study. BMC Pulm Med 2012;12:53. [ Links ]
11. Sanders KJ, Kneppers AE, Van de Bool C, Langen RC, Schols AM. Cachexia in chronic obstructive pulmonary disease: new insights and therapeutic perspective. J Cachexia Sarcopenia Muscle 2016;7:5-22. [ Links ]
12. Giudetti AM, Cagnazzo R. Beneficial effects of n-3 PUFA on chronic airway inflammatory diseases. Prostaglandins Other Lipid Mediat 2012;99:57e67. [ Links ]
13. De Batlle J, Sauleda J, Balcells E, Gómez FP, Méndez M, Rodríguez E, et al. Association between omega3 and omega6 fatty acid intakes and serum inflammatory markers in COPD. J Nutr Biochem 2012;23:817e21. [ Links ]
14. Ma Y, Griffith JA, Chasan-Taber L, Olendzki BC, Jackson E, Stanek EJ 3rd, et al. Association between dietary fiber and serum C-reactive protein. Am J Clin Nutr 2006;83:760-6. [ Links ]
15. Díaz O, Iglesia R, Ferrer M, Zavala E, Santos C, Wagner PD, et al. Effects of non invasive ventilation on pulmonary gas exchange and hemodynamics during acute hypercapnic exacerbations of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1997;156:1840-5. [ Links ]
16. Varraso R, Willett WC, Camargo CA Jr. Prospective study of dietary fiber and risk of chronic obstructive pulmonary disease among US women and men. Am J Epidemiol 2010;171:776-84. [ Links ]
17. Iniciativa Global para la Enfermedad Pulmonar Obstructiva Crónica. Guía de bolsillo para el diagnóstico y manejo de la EPOC: una guía para profesionales sanitarios. México; 2014. Disponible en: http://goldcopd.org/wp-content/uploads/dlm_uploads/2016/04/GOLD_Pocket_Spanish.pdf [ Links ]
18. Consulta Mixta, O. M. S. FAO de Expertos en Régimen Alimentario, Nutrición y Prevención de Enfermedades Crónicas. Dieta, nutrición y prevención de enfermedades crónicas: informe de una Consulta Mixta de Expertos OMS/FAO. OMS, Serie de Informes Técnicos; 2003. p. 916. Disponible en: http://www.fao.org/wairdocs/who/ac911s/ac911s00.htm. [ Links ]
19. Salas-Salvadó J. Nutrición y dietética clínica. 2a ed. España: Elsevier; 2008. [ Links ]
20. Alvarez Hernández J. Enfoque terapéutico global de la disfunción muscular en la EPOC. Nutr Hosp 2006;3:76-83. [ Links ]
21. Ferrer M, Alonso J, Prieto L, Plaza V, Monsó E, Marrades R, et al. Validity and reliability of the St George's Respiratory Questionnaire after adaptation to a different language and culture: The Spanish example. Eur Respir J 1996;9:1160-6. [ Links ]
22. Vestbo J, Prescott E, Almdal T, Dahl M, Nordestgaard BG, Andersen T, et al. Body mass, fat-free body mass, and prognosis in patients with chronic obstructive pulmonary disease from a random population sample. Am J Respir Crit Care Med 2006;173:79-83. [ Links ]
23. Jaganath D, Miranda JJ, Gilman RH, Wise RA, Diette GB, Miele CH, et al.; CRONICAS Cohort Study Group. Prevalence of chronic obstructive pulmonary disease and variation in risk factors across four geographically diverse resource-limited settings in Peru. Respir Res 2015;16:40. [ Links ]
24. Collins PF, Elia M, Stratton RJ. Nutritional support and functional capacity in chronic obstructive pulmonary disease: A systematic review and meta-analysis. Respirol 2013;18:616-29. [ Links ]
25. López M, Mongilardi N, Checkley W. Enfermedad pulmonar obstructiva crónica por exposición al humo de biomasa. Rev Peru Med Exp Salud Pública 2014;31(1):94-9. [ Links ]
26. Norman K, Stobäus N, González MC, Schulzke JD, Pirlich M, et al. Hand grip strength: Outcome predictor and marker of nutritional status. Clin Nutr 2011;30:135-42. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
M.a Pilar Benito Martínez.
Complejo Hospitalario San Pablo.
Clínica San Gabriel.
Av. La Marina. 2955.
San Miguel, Lima. Perú.
e-mail: nutritionhealth@gmail.com
Recibido: 16/11/2016
Aceptado: 13/03/2017