INTRODUCCIÓN
La enfermedad celiaca (EC) es un desorden autoinmune intestinal crónico que involucra al gluten dietario como gatillante de la enfermedad 1, convirtiéndose en una de las causas más comunes de malabsorción crónica. Esta enfermedad es el resultado de un daño en el intestino delgado con pérdida del área de superficie absortiva, llevando a una falla de la capacidad para absorber una cantidad adecuada de calorías 2. La pobre absorción característica de la enfermedad se manifiesta en bajo peso corporal y, consecuentemente, en un bajo índice de masa corporal (IMC).
El mecanismo exacto por el cual el gluten daña la mucosa intestinal es desconocido. Sin embargo, la reacción de las células T a la gliadina deaminada por la transglutaminasa produce una variedad de citoquinas inflamatorias, las cuales pueden contribuir al daño de la mucosa 3. La subpoblación de linfocitos CD4+ efectores, denominada Th17 4, tiene propiedades que han sido asociadas con la activación de los neutrófilos, la producción de citoquinas y la síntesis de proteasas que causan daño tisular 5. En la EC, las células Th17 específicas para gluten son capaces de producir citoquinas proinflamatorias como IL-17, IL-21, IL-22 y IFNϒ 6,7. Además, se ha observado una mayor expresión de IL-21 8, la cual podría estar relacionada con una sobrerregulación de las metaloproteinasas en cultivo de biopsias de pacientes celiacos no tratados 9. La expresión de la metaloproteinasa de matriz 1 y la metaloproteinasa 3 induce la degradación de la membrana extracelular y la activación de fibroblastos subepiteliales en biopsias de pacientes no tratados 10.
Una pobre absorción en pacientes celiacos produce deterioro del peso corporal y dificultad en la ganancia de peso. Esto puede ser el resultado de un aumento en la expresión de interleuquinas Th17 específica para gluten (IL-Th17), que genera una mayor extensión del daño intestinal. Hasta el momento no existen estudios que relacionen la expresión de interleuquinas del patrón Th17 con el estado nutricional en pacientes celiacos en enfermedad activa.
Totora y cols. demostraron que en pacientes adultos celiacos recién diagnosticados el 12,2% presentaban sobrepeso y el 8,1%, obesidad 11. En el mismo sentido, Kabbani y cols. encontraron que la prevalencia de sobrepeso y obesidad era del 32% en pacientes celiacos adultos 12.
En base a estos antecedentes, se planteó como hipótesis que los pacientes celiacos con sobrepeso/obesidad presentarían una menor expresión de interleuquinas Th17 en comparación con los pacientes con estado nutricional normal. Así, el objetivo de este estudio fue comparar la expresión de interleuquinas Th17 en pacientes celiacos con peso normal y sobrepeso/obesidad.
MÉTODOS
SUJETOS
Se reclutaron pacientes adultos con diagnóstico de EC (confirmados por biopsia), tratados en los centros médicos de la red de salud "UC-Christus" de Santiago de Chile, entre los meses de marzo de 2013 y junio de 2014. Los criterios de inclusión fueron los siguientes: a) diagnóstico de EC por biopsia intestinal; y b) edad de diagnóstico > 18 años. Este estudio fue aprobado por el Comité de Ética de la Escuela de Medicina de la Pontificia Universidad Católica de Chile. Todos los pacientes estuvieron de acuerdo en participar en el estudio y firmaron el consentimiento informado.
El tamaño muestral se estimó en base a la comparación de dos grupos independientes y un tamaño de efecto estimado (Hedges' g) de al menos 1,2 entre el grupo de pacientes normales y el grupo con sobrepeso/obesidad en la expresión de interleuquinas Th17. Utilizando un nivel de significancia estadística de 0,05 y una potencia estadística del 80% se determinó un tamaño muestral de siete pacientes por grupo.
EVALUACIÓN ANTROPOMÉTRICA
El índice de masa corporal (IMC) fue utilizado para definir el estado nutricional de los pacientes. El IMC fue registrado y clasificado de acuerdo al criterio de la Organización Mundial de la Salud en: bajo peso (< 18,5), normal (18,5-24,9), sobrepeso (25-29,9) y obesidad (> 30) 13.
MARCADORES SEROLÓGICOS
La determinación de anticuerpos antitransglutaminasa (TTG) se realizó en suero de los pacientes mediante kit comercial de ELISA (Immco Diagnostics, Buffalo, NY). Los anticuerpos antiendomisio (EMA) se evaluaron mediante inmunofluorescencia indirecta para IgA (Immco Diagnostics, Buffalo, NY). Para EMA se considera un test positivo cuando hay fluorescencia en la reacción, mientras que para TTG se considera un test positivo cuando hay ≥ 25 UI/ml.
GENOTIPIFICACIÓN DE ANTÍGENOS LEUCOCITARIOS HUMANOS (HLA)
Previamente se extrajo el DNA total a partir de linfocitos de sangre periférica con kit de extracción comercial. La tipificación completa de HLA fue con kit comercial (Invitrogen®, Brown Deer, WI). El proceso de tipificación se subdividió en cuatro pasos: amplificación de regiones polimórficas por técnica de PCR, desnaturalización química, hibridización y reacción de detección.
BIOPSIA DE INTESTINO DELGADO
La biopsia de intestino delgado fue obtenida por un procedimiento endoscópico. Se tomaron tres muestras de la porción distal del duodeno de cada paciente. La lesión histológica fue clasificada de acuerdo al criterio de Marsh-Oberhuber 14.
EXPRESIÓN DE IL-TH17 (IL-17F, IL-17A, IL-21 E IL-26)
El RNA total fue aislado desde biopsias de duodeno usando el método de extracción por Trizol (Invitrogen®, Grand Island, NY) y retro-transcrito a cDNA mediante el kit cDNA sintetasa (MBI Fermentas®, Hanover, MD). La PCR cuantitativa (QPCR) fue ejecutada en un sistema de PCR a tiempo real AB 7500, utilizando el método TaqMan(tm) (Applied Biosystems, Foster City, CA). Los datos de expresión génica fueron recolectados a través del Ct (cycle threshold) de cada gen mediante el programa High Resolution Melt (HRM) v2.0 provisto por Applied Biosystem (Perkin Elmer, Foster City, CA). Para la normalización de los datos se empleó un gen constitutivo de referencia (glyceraldehyde 3-phosphate dehydrogenase, GAPDH). Para comparar la expresión relativa de los resultados entre las muestras de estudio (peso normal versus sobrepeso/obesidad), se utilizó el método 2-∆∆Ct implementado por Applied Biosystem (Perkin Elmer, Foster City, CA).
ANÁLISIS ESTADÍSTICO
Para evaluar la significancia estadística entre los grupos se utilizó la prueba U de Mann-Whitney. Para evaluar la diferencia entre proporciones se utilizó el test de proporciones de dos muestras. Se consideró una significancia estadística un valor p de ≤ 0,05. Todos los análisis estadísticos se hicieron utilizando el programa Stata 10.1.
RESULTADOS
Se reclutaron y aceptaron participar en el estudio un total de 22 pacientes con diagnóstico reciente de enfermedad celiaca, 21 mujeres y un hombre. La Tabla 1 muestra las características clínicas de ambos grupos. El grupo de pacientes con sobrepeso/obesidad presentó una alta frecuencia del genotipo HLA DQ2-DQ8 en comparación con el grupo con IMC normal, y esta diferencia fue significativa.
Tabla I. Características de los pacientes de acuerdo al estado nutricional

Los resultados se presentan como mediana y rango.
*p ≤ 0,05, prueba U de Mann-Whitney y test de proporción de dos muestras.
Con respecto a la expresión de los genes evaluados, se encontró una tendencia a una mayor expresión de Th17F e IL-26 en el grupo de pacientes con sobrepeso/obesidad, aunque esta diferencia no alcanzó significancia estadística (Fig. 1).
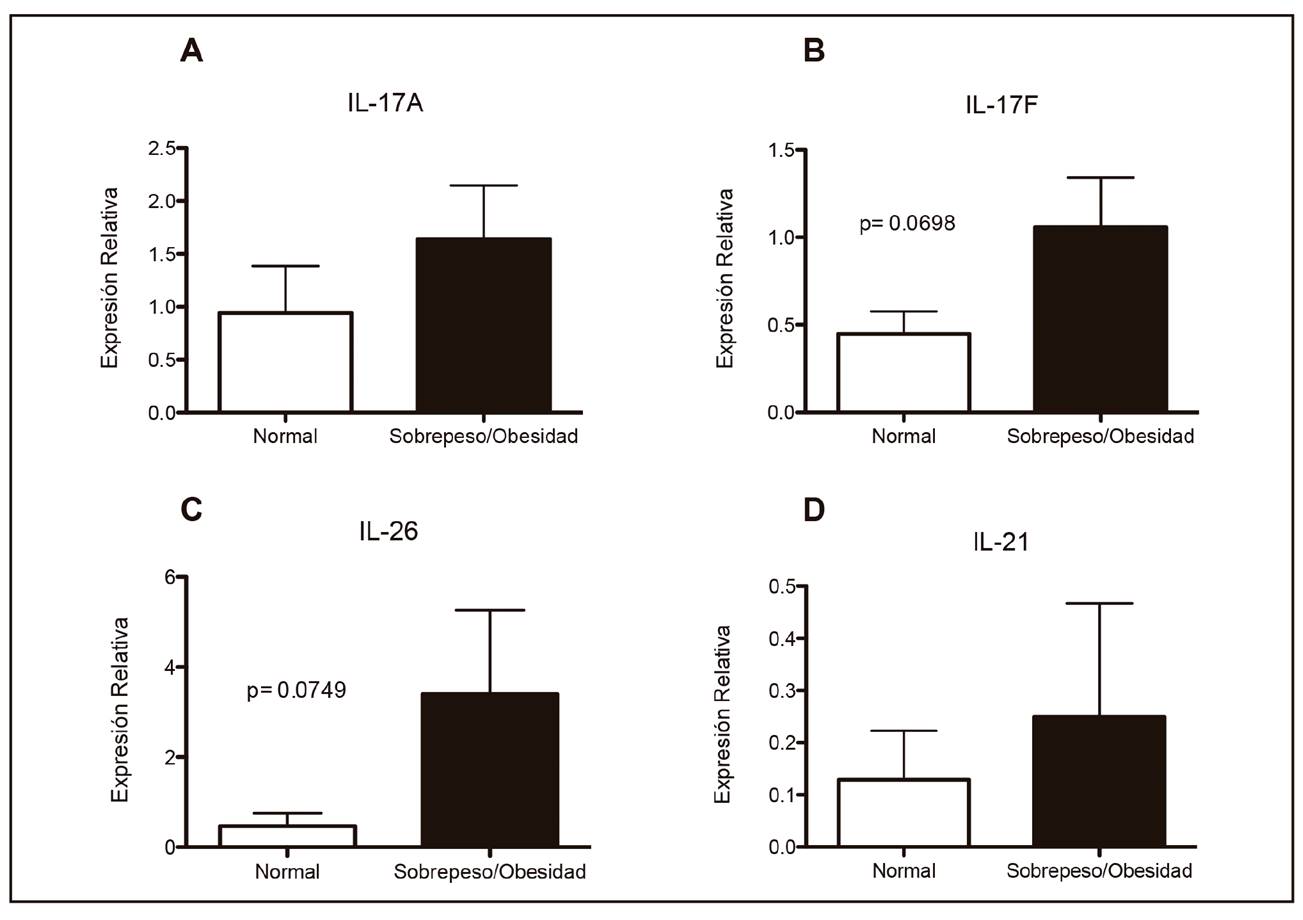
Figura 1. Comparación entre los niveles de expresión relativa del mRNA de IL-17A (A), IL-17F (B), IL-26 (C) y IL-21 (D) en pacientes celiacos con peso normal (IMC 18,5-24,9 kg/m2) versus sobrepeso/obesidad (IMC > 25 kg/m2) usando PCR cuantitativo en tiempo real (QPCR). Los niveles de los transcritos fueron normalizados con GAPDH RNA (prueba U de Mann-Whitney).
DISCUSIÓN
El presente estudio demostró que en pacientes celiacos con la enfermedad activa, la expresión de IL-Th17 no era diferente entre pacientes con estado nutricional normal y pacientes con sobrepeso/obesidad. Los pacientes celiacos con sobrepeso y obesidad fueron el 32% de la muestra total, similar a lo reportado en el estudio de Kabbani 12. La causa del exceso de peso corporal presente en la enfermedad activa o no tratada, a pesar de la malabsorción de la vellosidad intestinal atrofiada, no es clara. Una posible explicación puede estar relacionada con el mecanismo de compensación duodeno-yeyuno a través de un aumento de la absorción en segmentos distales del intestino 15. La hipótesis compensatoria se refiere a la adaptación intestinal que consiste en cambios morfológicos de la mucosa, incluido un aumento de la altura de la vellosidad, de la profundidad de la cripta y del número de células epiteliales 16. Esto podría explicar que no existan diferencias en el patrón de interleuquinas en pacientes con distinto IMC. En este sentido, un peso corporal mayor podría ser consecuencia de la hipótesis compensatoria.
La respuesta Th17 estimula la producción de citoquinas y promueve la síntesis de proteasas que producen daño tisular. También está relacionado a la activación de neutrófilos 17, que favorece la inducción de la respuesta inflamatoria. Sin embargo, nuestro estudio no muestra diferencia entre el patrón de expresión de las interleuquinas Th17 de pacientes con peso normal en comparación a los con sobrepeso/obesidad. Esta respuesta podría ser a nivel local en el duodeno sin generar cambios en áreas más extensas del intestino. Por otro lado, esto podría estar explicado por la condición inflamatoria que acompaña a la adiposidad. En este sentido, un estudio reciente en niños con enfermedades autoinmunes reportó que la obesidad era un factor independiente que se asociaba a una elevada frecuencia de células Th17 circulante 18. Estos últimos antecedentes abren la posibilidad de futuras líneas de investigación en las cuales sea factible estudiar el rol del estado inflamatorio de la obesidad en la patogenia de la enfermedad celiaca.
Una de las limitaciones de este estudio es que no se dispone de antecedentes de la ingesta alimentaria y de la capacidad de absorción de los pacientes. Estas dos variables podrían contribuir a explicar la malnutrición por exceso observada.
CONCLUSIONES
El exceso de peso corporal en pacientes celiacos no está influenciado por los niveles de expresión de interleuquinas Th17. Es necesario realizar estudios que evalúen la masa intestinal y la capacidad absortiva del intestino que nos permitan explicar la alta prevalencia de exceso de peso en estos pacientes.














