INTRODUCCIÓN
La enfermedad renal crónica avanzada (ERCA), definida como descenso grave del filtrado glomerular (FG) por debajo de 30 ml/min/1,73 m2, incluye los estadios 4 y 5 de la clasificación de la enfermedad renal crónica (ERC) 1 .
La malnutrición asociada a la enfermedad renal es un problema clínico creciente que predispone a un peor pronóstico y puede conducir a aumento de la morbimortalidad si no se interviene a tiempo 2.
La mayoría de estudios sobre nutrición y ERC están realizados en pacientes en diálisis con una prevalencia de malnutrición que oscila entre el 35 y el 65% 3,4. Apenas existen estudios sobre pacientes en ERCA no en diálisis y son estudios de pequeño tamaño que han reportado una prevalencia de malnutrición del 12-28% 5,6,7.
El concepto de malnutrición engloba tanto los problemas derivados del déficit como del exceso de ingesta de nutrientes 8,9,10. De hecho, los pacientes renales también han sucumbido a la epidemia de sobrepeso y obesidad que afecta al resto de la población.
Las medidas higiénicas-dietéticas son una parte fundamental del tratamiento del paciente crónico y el consejo nutricional debe ser la primera recomendación junto con la incentivación de la realización de ejercicio físico en la medida de sus posibilidades. En la etapa prediálisis, el asesoramiento dietético se emplea como medida renoprotectora y antiproteinúrica para prevenir tanto el sobrepeso como la desnutrición a lo largo de todos los estadios de la enfermedad renal. La mayoría de estas recomendaciones se basan en restricciones y prohibiciones, habitualmente demasiado estrictas y no individualizadas. Dichas medidas llevan a los pacientes a preguntar en cada consulta: "Doctor, ¿qué puedo comer?". Algunas de las restricciones más extremas no han demostrado ofrecer ventajas significativas en los pacientes ni mejorar su pronóstico, e incluso podrían empeorar la calidad de vida y el bienestar de nuestros pacientes provocando malnutrición 11. La alimentación es el aspecto del tratamiento en el que más pueden participar los pacientes renales y puede crear mucha ansiedad, lo cual afecta negativamente a la calidad de vida.
La calidad de vida relacionada con la salud (CVRS) se ha definido como la evaluación que realiza el individuo respecto a su salud y su grado de funcionamiento para la realización de las actividades cotidianas, que incluye las funciones física, psicológica y social, la percepción general de la salud, la movilidad y el bienestar emocional 12. La ERCA tiene un gran impacto sobre la CVRS desde los estadios iniciales de la enfermedad hasta su fase terminal. Los síntomas urémicos, las restricciones dietéticas y su tratamiento se ven reflejados en la calidad de vida de estos pacientes y esto conduce a un aumento de la mortalidad 13.
Por ello, nos planteamos si interviniendo en la nutrición en forma de intervención nutricional personalizada mejorarían los parámetros de CVRS comparados con el tratamiento estándar.
MATERIAL Y MÉTODOS
PARTICIPANTES Y DISEÑO DEL ESTUDIO
Se trata de un ensayo clínico de intervención educativa, unicéntrico, randomizado, abierto y controlado, cuya población a estudio son los pacientes de la consulta ERCA de Albacete. El estudio fue aprobado por el comité ético y de investigación de nuestro hospital.
Participaron pacientes de 18 a 80 años diagnosticados de ERCA y atendidos en las consultas de Nefrología del Hospital General Universitario de Albacete. Los criterios de inclusión fueron no haber recibido previamente tratamiento renal sustitutivo, no control previo por nutricionista y capacidad para dar un consentimiento informado. Los criterios de exclusión incluyeron cualquier enfermedad infecciosa o tumoral activa.
Los pacientes se aleatorizaron en dos grupos: control e intervención.
En ambos grupos se realizó la valoración nutricional mediante la valoración global subjetiva (VGS) e índice de masa corporal (IMC), medidas ambas en primera visita y a los tres, seis y 12 meses. Para medir la CVRS se emplea la versión española del cuestionario de salud SF-36, realizado a los seis y 12 meses 14. El SF-36 evalúa el impacto de la enfermedad en el funcionamiento adaptativo y proporciona un perfil del estado de salud. Contiene 36 ítems con formato de respuesta tipo Likert de dos, tres, cinco y seis puntos según el ítem, con un rango de 0 a 100: a mayor puntuación, mejor estado de salud. Estos 36 ítems componen ocho dimensiones: función física, rol físico, dolor corporal, salud general, vitalidad, función social, rol emocional y salud mental. Por la agregación de estas dimensiones se calculan dos componentes: el componente de salud física (CSF) y el componente de salud mental (CSM).
En el grupo intervención se realizó la intervención nutricional de forma individual y colectiva con la ayuda de dietistas, endocrinos, nefrólogos y cocineros profesionales, así como recuerdos telefónicos durante el año de seguimiento. Pacientes y familiares aprendieron conceptos básicos de alimentación, métodos de cocinado y preparación de alimentos adaptadas a sus necesidades, sistema de intercambio de alimentos y, de forma individualizada, se dieron los consejos en cuanto a los cambios que debían realizar en su dieta según su historia clínica para las ingestas de macro y micronutrientes. Se realizaron seis sesiones colectivas, ocho recuerdos telefónicos durante el año y talleres de cocina con el fin de aprender conceptos sobre alimentación enfocados a su enfermedad y facilitar el contacto entre pacientes y familiares.
En el grupo control se realizaron las mismas mediciones, aplicándose las instrucciones habituales sobre estilo de vida que se dan en la consulta ERCA.
El objetivo principal del estudio fue determinar si esas restricciones están justificadas y si un programa de intervención nutricional personalizado que las minimice mejoraría los parámetros de CVRS comparados con el tratamiento estándar.
El objetivo secundario, además, fue determinar la situación nutricional y la prevalencia de malnutrición en la consulta ERCA de Albacete.
ANÁLISIS ESTADÍSTICO
Para la descripción de la muestra se han utilizado medidas de tendencia central (media y desviación típica) en el caso de las variables métricas y medidas de frecuencia (frecuencia absoluta y porcentaje) en el caso de las variables cualitativas. Las diferencias entre grupos, cuando se trata de variables cuantitativas, se han evaluado mediante la prueba t de Student (pruebas paramétricas) o mediante la prueba U de Mann-Whitney (pruebas no paramétricas).
Las comparaciones intergrupales de variables cualitativas se han realizado mediante la prueba de Chi-cuadrado, utilizando el estadístico exacto de Fisher en aquellas ocasiones en las que existían casillas con una frecuencia esperada inferior a 5. En el caso de las comparaciones intragrupo, para evaluar la progresión de los participantes a lo largo del estudio, comparando sus resultados en las cuatro visitas en las variables métricas, se han utilizado el modelo lineal general para medidas repetidas (pruebas paramétricas) y el estadístico de Friedman (prueba no paramétrica). Para las comparaciones intragrupo de variables cualitativas a lo largo de las cuatro visitas se ha utilizado la prueba Q de Cochran para muestras relacionadas.
Para analizar las variables asociadas con la calidad de vida, evaluada mediante la escala SF36, se realizaron varias regresiones lineales. Como variables dependientes (una por modelo), se han introducido la puntuación en la dimensión mental y la puntuación en la dimensión física (todas a los seis y a los 12 meses). Como variables independientes se han utilizado el haber recibido el tratamiento, el sexo, el IMC y la VGS. Se ha utilizado el método por pasos hacia atrás.
Los análisis estadísticos del estudio se han realizado con el software SPSS (versión 20).
RESULTADOS
El estudio incluyó un total de 75 pacientes distribuidos de forma aleatoria en un grupo control con 35 pacientes y un grupo intervención con 40. En el grupo control la edad media fue de 56,6 años (DE: 13,24) y en el grupo intervención, de 57,3 años (DE: 13,26). El 60% del grupo control fueron varones y el 52,5% en el grupo intervención.
La causa más frecuente de enfermedad renal fue la etiología glomerular en el grupo control y la nefropatía intersticial crónica en el grupo intervención. Los dos grupos presentan una elevada incidencia de factores de riesgo cardiovascular; más del 70% en ambos grupos presentaba hipertensión arterial (HTA), dislipemia e hiperuricemia. Ambos grupos presentaron, al menos, tres comorbilidades asociadas. En cuanto a edad, sexo, hábitat, causa de la insuficiencia renal y comorbilidad asociada no hubo diferencias significativas entre los dos grupos (Tabla I).
Tabla I. Características de la muestra y por grupos. Comorbilidad asociada

HTA: hipertensión arterial; DL: dislipemia; DM: diabetes mellitus; VP: vasculopatía periférica; ECV: enfermedad cerebrovascular; CI: cardiopatía isquémica.
Mediante la VGS se clasificó a los pacientes en tres categorías: a) paciente bien nutrido; b) paciente moderadamente o con sospecha de estar malnutrido; y c) paciente severamente desnutrido. Encontramos una malnutrición en forma de desnutrición medida por VGS para categoría B del 20% en el grupo control y del 29,3% en el grupo intervención. Para la categoría C no hubo ningún paciente en el grupo control y solo dos (4,9%) en el grupo intervención al inicio del estudio. Ya desde la visita 2, se produjo una mejoría en el grupo intervención respecto a los controles, aunque las diferencias no son significativas (p > 0,05) (Tabla II).
Tabla II. Valoración global subjetiva (VGS) basal, a los 3, 6 y 12 meses del estudio
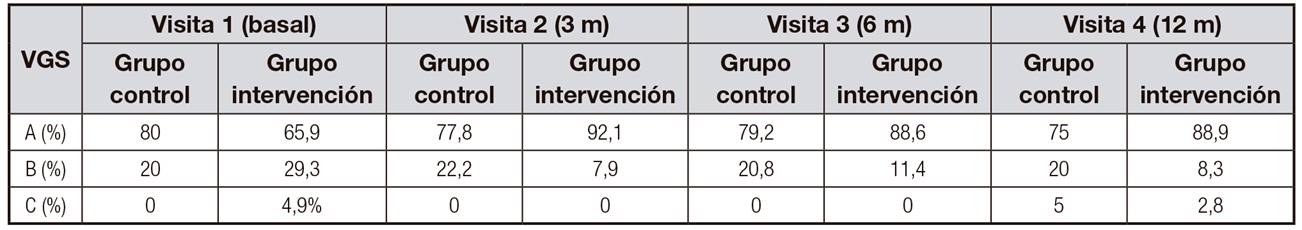
A: bien nutrido; B: desnutrido leve o en riesgo de desnutrición; C: desnutrido grave.
El IMC (kg/m2) mostró inicialmente una situación de sobrepeso en ambos grupos, con una media de 28,83 (DE: 5,4) y 26,96 kg/m2 (DE: 4,09), respectivamente, sin cambios a lo largo del estudio (p > 0,05), tal como se muestra en la Figura 1. Al inicio del estudio el porcentaje de pacientes con un IMC > 25 en rango de sobrepeso fue del 38,2% y el de obesidad con IMC > 30 fue del 31,6%.
En la tabla III se muestran los resultados de las puntuaciones de las ocho dimensiones en cada grupo desde la medición basal, a los seis y a los 12 meses. Podemos observar que mejoran de forma global todas las escalas en el grupo intervención y que empeoran en el control.
En las Figura 2 y Figura 3 vemos cómo los componentes físico y mental también presentaron mejoría en sus puntuaciones en el grupo intervención y empeoraron en el control, con diferencias significativas en ambos.
El análisis multivariante de regresión logística se ha realizado relacionando la puntuación de los CSF y CSM con grupo, sexo e IMC como variables independientes cuantitativas y la VGS como variable independiente categórica.
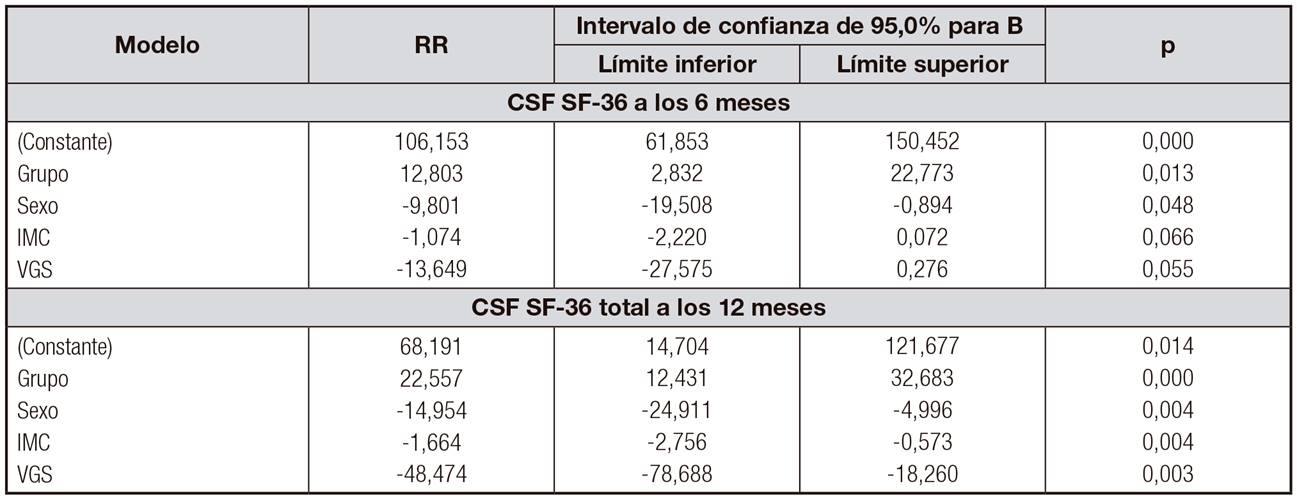
Para el CSF (Tabla III), a los seis meses y 12 meses mejora la puntuación ser grupo intervención y la empeoran ser mujer, tener un IMC elevado y ser categoría B o C de VGS respecto a ser A.
Tabla III. Puntuaciones de las escalas del cuestionario SF36 en los grupos control e intervención basal, a los 6 y a los 12 meses

Para el CSM (Tabla IV), a los seis meses mejora ser grupo intervención y empeora ser categoría B o C de la VGS. A los 12 meses, además, se añade el sexo; ser mujer empeora la puntuación.
DISCUSIÓN
El paciente renal presenta una menor CVRS que la encontrada en la población general debido a variables clínicas, sociodemográficas, diálisis, síntomas físicos, apoyo social y el impacto de la enfermedad. La sintomatología de la enfermedad renal limita las actividades físicas, interfiere en las actividades diarias, intensifica el dolor y hace que el paciente realice una peor valoración de su estado de salud. Además, una mala situación nutricional en pacientes en diálisis se ha relacionado fundamentalmente con el empeoramiento de los componentes de salud física y algo menos con los de salud mental.
La mayoría de estudios que muestran una estrecha relación entre los indicadores de CVRS y los índices de morbimortalidad están centrados en pacientes en diálisis 15,16 y solo el 5% de los artículos que relacionan calidad de vida y enfermedad renal crónica están realizados en la etapa prediálisis 12. En esta fase, un descenso del FG y un aumento de los síntomas urémicos se asocian con una reducción en la capacidad funcional y una peor puntuación en los cuestionarios de calidad de vida. En el estudio de Campbell 6, con población prediálisis, en general, la puntuación del componente físico global fue significativamente menor que los valores de la población general descritos en la literatura y el componente mental fue similar al de la población general.
Nuestro estudio pretendía mejorar la calidad de vida de los pacientes con ERCA al ayudarles en la nutrición, un aspecto clave de su enfermedad que crea mucho estrés a los pacientes en su tratamiento diario, objetivo que se cumplió con creces al encontrar mejoría en las puntuaciones de todos los parámetros de calidad de vida que se midieron.
El perfil nutricional en la ERC viene determinado por factores previos al estado urémico, como circunstancias relacionadas con la enfermedad de base y sus complicaciones, factores genéticos y ambientales y procesos agudos coexistentes y relacionados con el tratamiento sustitutivo renal, si es el caso. En los últimos años, viene apareciendo en la literatura el término protein energy wasting (PEW), que se define como el estado patológico en el que existe una disminución de los depósitos proteicos y energéticos 17. Se ha traducido al castellano como desgaste proteico energético (DPE) y otorga igual importancia al catabolismo y a la malnutrición 18.
La mayoría de estudios sobre nutrición y ERC están realizados en pacientes en diálisis, en los cuales la prevalencia de desnutrición en la ERC oscila en un amplio rango, entre el 12% y el 75% 3,4,19,20. Hasta la fecha, existen muy pocos estudios que describan la prevalencia de malnutrición en estadios prediálisis, con cifras que oscilan del 18% al 28%. En el estudio de Campbell y cols. 6, tras 12 semanas de seguimiento en 56 pacientes australianos con ERC estadio 4, hallaron una prevalencia de malnutrición del 12% 5. Lawson y cols. encuentran un 28% de prevalencia de malnutrición y Sanches y cols. 21, un 18%. En 2018 se publica un estudio español de 186 pacientes que reporta un 27,9% de desnutrición 7. Nosotros encontramos una malnutrición en forma de desnutrición medida por VGS de entre el 20 y el 29,3%, similar a la descrita en la literatura.
Por otro lado, el IMC nos muestra una población con obesidad y sobrepeso, reflejo de lo que está ocurriendo en la sociedad general. Según el estudio ENPE referido a población de entre 25 y 64 años (n = 3.966), la prevalencia de sobrepeso estimada en adultos es del 39,3% y la de obesidad general, del 21,6% 22. En las últimas actualizaciones de la Sociedad Española de Nefrología, se hace especial hincapié en esta epidemia y se describe que más de la mitad de los pacientes con ERCA presentan obesidad o sobrepeso con ERCA 23.
El concepto de malnutrición engloba tanto los problemas derivados del déficit como del exceso de ingesta de nutrientes y no debe considerarse exclusivamente sinónimo de desnutrición. La existencia de sobrepeso u obesidad no excluye, ni mucho menos, el déficit de la ingesta de proteínas y energía, encontrándose estos pacientes en riesgo de desnutrición 24.
Hasta hace poco se advertía exclusivamente de la malnutrición en forma de déficit como el DPE, pero debemos empezar a prestar atención a la malnutrición en forma de exceso y combatir la obesidad desde estadios precoces de la enfermedad renal para frenar el síndrome metabólico, ya que hay que recordar que la primera causa de mortalidad en los pacientes renales es la enfermedad cardiovascular 25,26.
Las recomendaciones sobre el estilo de vida siempre han sido una parte fundamental del tratamiento del paciente crónico. El asesoramiento nutricional debe ser la primera recomendación al paciente junto con la incentivación de la realización de ejercicio físico en la medida de sus posibilidades. Durante el seguimiento, en la etapa que antecede al inicio del tratamiento con diálisis, el asesoramiento dietético se emplea como medida renoprotectora y antiproteinúrica, así como para prevenir el sobrepeso y la desnutrición.
En nuestras consultas, el principal consejo dietético lo realiza el nefrólogo y es mayoritariamente en forma de restricciones. No contamos con dietistas especializados para la valoración y el tratamiento nutricional de los enfermos renales.
En los casos de sobrepeso y obesidad se recomienda perder peso mediante la restricción de energía en forma de hidratos de carbono y grasas. Por otro lado, se indican dietas bajas en calcio, fósforo, proteínas, sodio y potasio, y esto no siempre permite garantizar un adecuado soporte calórico, proteico y mineral. Muchas veces, el precio a pagar por una dieta, en teoría adecuada a la enfermedad del paciente, es una nutrición deficitaria.
Para una dieta hipopotasémica se recomienda la limitación de la ingesta de frutas y verduras y técnicas culinarias como la doble cocción. Esto es muy laborioso y conlleva la pérdida de sabor y de muchos nutrientes; además, existen muy pocos estudios científicos que demuestren la efectividad de estos métodos 27. Esto supone la mayoría de las veces una dieta insípida, monótona y baja en fibra y vitaminas. También se limita con frecuencia el consumo de lácteos en las dietas bajas en calcio y fósforo e hipoproteicas. Asimismo, se prohíben grasas saturadas, productos procesados, embutidos, bollería, panes y dulces.
Una de nuestras propuestas fue minimizar las restricciones o prohibiciones y facilitar la elección informada en los pacientes del grupo intervención, aumentando el consumo de fruta y verdura, fomentando el uso de alimentos frescos y animando a cocinarlos con distintas técnicas para evitar la monotonía. También se incentivó el empleo de microvegetales y condimentos (especias y similares) para mejorar la palatabilidad y por su bajo contenido en potasio. De esta manera, quisimos acercarnos a la dieta mediterránea y a hábitos destinados a la prevención y el control del síndrome metabólico.
Frecuentemente, las restricciones extremas no son necesarias o son demasiado estrictas e impersonales, y no solo no han demostrado ofrecer ventajas significativas en los pacientes ni en su pronóstico sino que podrían incluso empeorar la calidad de vida y el bienestar de nuestros pacientes 11. Los pacientes solo disponen muchas veces de la información por escrito con los alimentos prohibidos, y no de menús, recetas y técnicas culinarias específicas, ni de bases de datos fiables, y sobre todo, no saben cómo usarlas.
Esto lleva a los pacientes y familiares a preguntar en cada consulta: "Pero, doctor, ¿entonces qué puedo comer?", ya que la alimentación es el aspecto del tratamiento renal en el que más pueden participar.
Al instaurar este programa de educación nutricional, los pacientes se sintieron atendidos y muchos volvieron a comer alimentos que no probaban desde hacía años, mejorando su conocimiento sobre nutrición renal. Esta intervención personalizada tuvo en cuenta las preferencias alimentarias y los hábitos alimentarios, minimizando las restricciones y prohibiciones y facilitando una elección informada. Tras la intervención, mejoraron todos los parámetros de calidad de vida que se midieron, confirmando la influencia de la dieta en el bienestar de los pacientes. Encontramos una relación entre nutrición y calidad de vida, ya que empeoraron las puntuaciones tanto estar desnutrido como un IMC elevado, mientas que pertenecer al grupo intervención las mejoraba. No hemos observado diferencias importantes entre las puntuaciones de los componentes de salud física y los de salud mental, lo que podría deberse a que nuestros pacientes no se encontraban ante una mala situación nutricional que implicara desnutrición y no son pacientes en diálisis. Para contrastar nuestros datos, no hemos encontrado estudios que comparasen todas las subescalas de CVRS con valores de VGS en ERCA, o cualquier marcador nutricional relacionado con calidad de vida en ERCA en población que no estuviese ya en diálisis.
Como conclusión, la calidad de vida se puede mejorar en los pacientes con ERCA aplicando un programa de educación nutricional. Desde nuestros resultados nos parece lógico recomendar la mejora del conocimiento de los pacientes sobre nutrición renal mediante programas educativos estructurados personalizados según las preferencias alimentarias y los hábitos alimentarios, minimizando las restricciones y prohibiciones y facilitando una elección informada con ayuda de profesionales de la nutrición, así como el tratamiento de la malnutrición tanto por exceso como por déficit desde estadios precoces.