INTRODUCCIÓN
La obesidad ha aumentado de forma alarmante en los últimos 30 años, hasta el punto de ser considerada por la OMS como la epidemia del siglo XXI, con más de 1900 millones de adultos mayores de 18 años con sobrepeso y 650 millones con obesidad en el 2016. En EE. UU. representa la segunda causa de mortalidad, es responsable del 14 % de todas las muertes y provoca un coste sanitario de 238 mil millones de dólares (1).
Basterra y cols. han observado un aumento de la obesidad mórbida en España de más del 200 %, pasando entre 1993 y 2006 de 1,8 a 6,1/1000 habitantes, siendo la prevalencia mayor entre las mujeres. Tras ajustar la edad, en ambos sexos se mantiene un crecimiento significativo de la misma, con un aumento relativo anual del 4 % en hombres y del 12 % en mujeres (2).
El aumento de la mortalidad de la población obesa con respecto a la población con normopeso se produce principalmente como consecuencia del desarrollo de enfermedades cardiovasculares y síndrome metabólico, así como por la asociación de determinados tipos de cáncer (colon, recto, mama y útero).
Entre los posibles mecanismos responsables se han señalado los siguientes: el efecto mecánico del cúmulo de grasa visceral, la resistencia periférica a la insulina, el síndrome metabólico con diabetes mellitus de tipo 2 y dislipemia, el estrés oxidativo, el estado proinflamatorio y la disfunción endotelial (3).
La cirugía bariátrica es una alternativa terapéutica eficaz en la obesidad mórbida refractaria al tratamiento médico, consiguiendo pérdidas de peso importantes que se mantienen en el tiempo, algo muy difícil de lograr con un tratamiento conservador basado en la dieta y el ejercicio (4).
El bypass gástrico es una técnica quirúrgica considerada mixta, al combinar un mecanismo restrictivo con otro malabsortivo. En esencia, consiste en la confección de un reservorio gástrico de 30-35 cc de capacidad, aislado del estómago, que se anastomosa con un asa yeyunal; a una distancia de entre 100 y 150 cm de esta se realiza una segunda anastomosis yeyuno-yeyunal donde se mezclan el contenido gástrico y el biliopancreático.
Es, junto con la gastrectomía vertical, el procedimiento quirúrgico más utilizado y representa el 46,6 % del total de intervenciones de cirugía bariátrica realizadas entre 2013 y 2017 en el mundo.
Se considera de elección por su aceptable morbimortalidad, buenos resultados a largo plazo y excelente calidad de vida. Además, resulta más adecuada que otras técnicas en los pacientes con reflujo gastroesofágico, por un efecto antirreflujo del que carecen las técnicas restrictivas, y en los pacientes con DM2 y síndrome metabólico, por la respuesta hormonal secundaria al bypass gastrointestinal e independiente de la pérdida de peso (5).
El objetivo del estudio es determinar la presencia de factores de riesgo cardiovascular (FRCV) en los pacientes intervenidos mediante bypass gástrico antes de la cirugía, y la resolución de los mismos al final del seguimiento, así como calcular el riesgo de eventos cardiovasculares que tienen los pacientes antes y después de la cirugía, y la evolución de la pérdida ponderal.
MATERIAL Y MÉTODOS
Este fue un estudio retrospectivo observacional que incluyó a todos los pacientes intervenidos consecutivamente de bypass gástrico simplificado en Y de Roux laparoscópico según la técnica de Lonroth y Ramos, dejando un tamaño de asa común alimentaria de 150 cm, desde enero de 2005 a diciembre de 2014 (n = 303) en el Hospital Central de la Cruz Roja de San José y Santa Adela de Madrid.
A todos los pacientes se les realizó una valoración preoperatoria protocolizada que incluyó: historia clínica, exploración física, estudio antropométrico, bioquímico y hormonal, valoración complementaria para determinar la comorbilidad asociada, endoscopia o estudio radiológico esófago-gastro-duoudenal, pruebas funcionales respiratorias, valoración psiquiátrica, valoración anestésica y consentimiento informado.
La selección de los pacientes se hizo conforme a los criterios establecidos en el Documento de Consenso elaborado por las sociedades SEEDO (Sociedad Española para el Estudio de la Obesidad) y SECO (Sociedad Española de Cirugía de la Obesidad) en el 2004 (6).
El seguimiento después de la cirugía se llevó a cabo con la siguiente periodicidad: 1, 3, 6, 12, 18 y 24 meses, y posteriormente de manera anual. En cada visita se llevó a cabo un control ponderal y de las variables antropométricas, y se efectuaron las determinaciones analíticas y pruebas necesarias para el estudio de los FRCV.
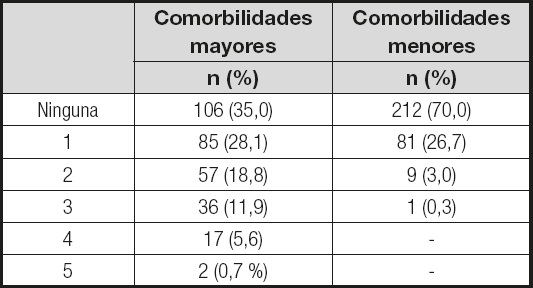
Se registraron las comorbilidades mayores: hipertensión arterial (HTA), diabetes mellitus de tipo 2 (DM2), dislipemia (DLP), enfermedad cardiovascular, síndrome de apnea-hipopnea del sueño (SAHS) y artropatía severa de las articulaciones de carga; y las siguientes comorbilidades menores: colelitiasis, reflujo gastroesofágico, esteatosis hepática, alteraciones mestruales/infertilidad, incontinencia urinaria de esfuerzo, varices e hipertensión intracraneal benigna (6).
Se siguieron los siguientes criterios para el diagnóstico de las comorbilidades mayores: HTA, si TA > 140/90 mmHg; DM2, si HbA1c > 6,5 % o glucosa en ayunas > 126 dl; DLP, si TG > 150 mg/dl o LDL-Col > 160 mg/dl o HDL-Col < 50 mg/dl en las mujeres o HDL-Col < 40 en los hombres o en caso de recibir tratamientos para estas patologías. El diagnóstico del SAHS se determinó mediante un estudio polisomnográfico si se observaban > 5 eventos/hora de apnea/hipopnea.
Los criterios que se siguieron para determinar la resolución de las comorbilidades mayores fueron: HTA si TAS ≤ 140 mmHg y TAD ≤ 90 mmHg; DM2 si HbA1c < 6 % y glucosa basal < 100 mg/dl sin tratamiento al menos durante un año; DLP si TG ≤ 150 mg/dl, LDL-Col ≤ 160 mg/dl y HDL-Col ≥ 50 mg/dl en las mujeres o HDL-Col ≥ 40 en los hombres. Para la resolución del SAHS fue necesario que en el estudio polisomnográfico se observaran ≤ 5 eventos/hora.
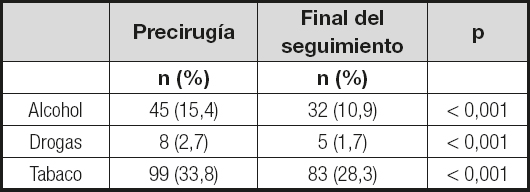
Se registró el consumo de tabaco, alcohol y drogas antes y después de la cirugía como FRCV. Para el cálculo del riesgo cardiovascular utilizamos la ecuación calibrada del Registre Gironí del Cor (REGICOR), cuya fórmula nos permite el cálculo del riesgo de cualquier acontecimiento coronario a los 10 años, adaptado a las características de prevalencia de los factores de riesgo y de la incidencia de acontecimientos coronarios de la población española; se expresa en forma de porcentaje (7).
Los factores de riesgo incluidos en el REGICOR son: edad, sexo masculino, tabaquismo, diabetes mellitus, colesterol total (mg/dl), colesterol-HDL (mg/dl), TAS (mmHg) y TAD (mmHg). La clasificación del riesgo a los 10 años es: muy alto (> 39 %), alto (20-30 %), moderado (10-19 %), ligero (5-9 %) y bajo (< 5 %).
Las fórmulas utilizadas para el cálculo de la pérdida ponderal son las recomendadas por la SECO (8):
– Índice de masa corporal: IMC = peso/talla2
– Porcentaje de sobrepeso perdido: PSP = [(P inicial – P actual) / (P inicial – P ideal)] x 100
– Porcentaje de exceso de índice de masa corporal perdido: PEIMCP = [(IMC inicial - IMC final) / IMC inicial - 25)] x 100
– Porcentaje de peso total perdido: PPTP = [(P inicial – P actual / P inicial] x 100
El análisis estadístico se realizó a partir de una base de datos creada en el programa SPSS para Windows, versión 23.0 (SPSS Inc., Chicago, IL, EUA).
Se realizó un estudio descriptivo de las variables basales de los pacientes. Las variables categóricas se describieron con frecuencias y porcentajes, y las variables continuas con la media y la desviación estándar.
Para comparar variables continuas utilizamos la prueba de la t de Student y para las variables categóricas se utilizó la prueba exacta de Fisher.
Para todos los análisis el nivel de significación estadístico se fijó en el 5 %, valor α = 0,05.
RESULTADOS
Se incluyeron 303 pacientes intervenidos de bypass gástrico en nuestro hospital, 221 mujeres y 82 hombres con una media de edad de 42,3 ± 10,0 años (20-68) y un IMC inicial de 48,2 ± 6,0 kg/m2 (35,4-71,6).
Al final del estudio, 10 pacientes se perdieron por traslado a otra comunidad. El tiempo medio de seguimiento desde la cirugía hasta finalizar el estudio fue de 5,7 ± 2,6 años (2,0 ± 11,7).
Veintiséis de los 303 pacientes habían sido sometidos previamente a tratamientos no conservadores para la obesidad: 16 (5,3 %) habían tenido previamente implantado un balón gástrico y 4 (1,3 %) una banda gástrica, y 6 pacientes (2 %) se habían sometido a gastroplastia vertical anillada.
La prevalencia de comorbilidades en los pacientes candidatos a cirugía bariátrica se expone en la tabla I; las adicciones antes de la cirugía y al final del seguimiento en la tabla II.
Tabla II. Prevalencia de adicciones en los pacientes intervenidos de bypass gástrico antes y al final del seguimiento
En nuestra serie, antes de la cirugía, el 76,9 % de los pacientes tenían un RCV bajo (< 5 %), el 19,5 % ligero (5-9 %) y el 3,6 % moderado. Al final del seguimiento, el 92,1 % tenían un RCV bajo, el 7,3 % ligero y el 0,6 % moderado, no teniendo ninguno riesgo alto o muy alto, ni antes ni después de la intervención.
La prevalencia de las comorbilidades mayores antes de la cirugía fue: HTA, 44,6 %; DM2, 19,1 %; GBA (glucosa basal alterada), 20,2 %; DLP, 34,7 %, y SAHS, 24,1 %. El tratamiento médico seguido por los pacientes antes de la cirugía y al final del seguimiento se muestra en la tabla III.
Tabla III. Tratamiento médico seguido por los pacientes
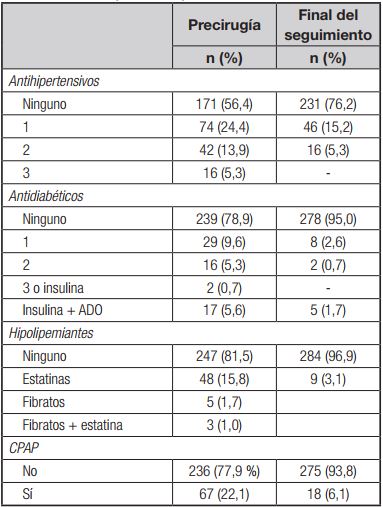
ADO: antidiabéticos orales; CPAP: presión continua positiva en la vía aérea.
La resolución de las comorbilidades al final del seguimiento fue del 53,4 % para la HTA, del 70,2 % para la DM2, del 83,9 % para la DLP y del 71,4 % para el SAHS (Tabla IV). Setenta de 132 (53,0 %) pacientes dejaron de tomar antihipertensivos, 49 de 64 (76,6 %) antidiabéticos orales y/o insulina y 47 de 56 (83,9 %) hipolipemiantes, y 49 de 67 (73,1 %) dejaron de utilizar CPAP para tratar el síndrome de apnea-hipopnea durante el sueño.
Tabla IV. Porcentaje de resolución de comorbilidades después del bypass gástrico

*Según criterios de la ADA. DLP: dislipidemia; DM 2: diabetes mellitus de tipo 2; HTA: hipertensión arterial; SAOS: síndrome de apnea obstructiva del sueño. Nota: el 20,1 % (n = 61) tenían GBA (glucemia basal alterada) antes de la cirugía, con normalización del 100 % posteriormente.
Al final del seguimiento, el porcentaje de eventos cardiovasculares a los 10 años estimado por REGICOR disminuyó en un 32,2 %. Todos los parámetros incluidos en el cálculo del riesgo cardiovascular disminuyeron significativamente al final del seguimiento salvo los niveles de HDL-colesterol, que no experimentaron ninguna variación significativa (Tabla V).
Tabla V. Comparación de los factores de riesgo cardiovascular y el riesgo cardiovascular a los 10 años antes de la cirugía y al final del seguimiento

La pérdida ponderal expresada en PSP, PEIMCP y PPTP es significativamente mayor a los 24 meses después de la cirugía que al final del seguimiento, al igual que el porcentaje de éxitos (PSP > 50 % del inicial), que es del 84,1 % a los 24 meses y disminuye al 64,7 % al final del seguimiento (p < 0,0001) (Tabla VI).
Tabla VI. Evolución ponderal de los pacientes a los 24 meses de la cirugía y al final del seguimiento
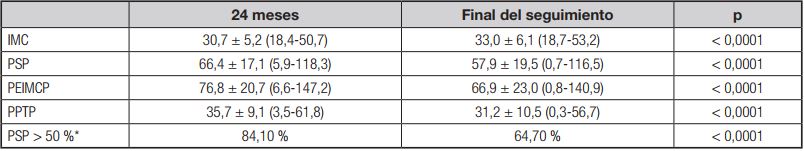
IMC: índice de masa corporal; PSP: porcentaje de sobrepeso perdido; PEIMCP: porcentaje de exceso de IMC perdido; PPTP: porcentaje de peso total perdido. *Criterio de éxito de la cirugía si PSP > 50 %.
El PSP al final del seguimiento es significativamente mayor en los pacientes intervenidos hace menos de 5 años (n = 140) que en los que han pasado al menos 5 años desde la cirugía (n = 153), siendo de 62,7 ± 17,3 vs. 53,5 ± 20,4, p < 0,0001, respectivamente.
DISCUSIÓN
Hay evidencia suficiente que relaciona la obesidad mórbida con una mayor morbimortalidad, fundamentalmente debida a enfermedades cardiovasculares. El objetivo que perseguimos con la cirugía es la reversión de los factores de riesgo cardiovascular con la pérdida de peso y la diminución del RCV en estos pacientes.
En un análisis publicado en JAMA en 2013, en el que se revisaron 270.000 muertes provenientes de 97 estudios, se observó un aumento significativo del riesgo relativo de muerte (RR: 1,34, IC: 1,21-1,74) para los rangos de IMC superiores a 35 kg/m2 (9).
En otro estudio publicado en Lancet en 2009, que registró la causa de muerte de una población de 1 millón de adultos reclutados desde los años 70 hasta la actualidad, se concluye que, a partir de un IMC de 25 kg/m2, la mortalidad aumenta en una media del 30 % por cada 5 kg/m2 de incremento del IMC, siendo esta relación máxima en el tramo de edad de 35 a 59 años.
El infarto agudo de miocardio estaba fuertemente relacionado con el IMC y, en el tramo de 25 a 50 kg/m2, cada aumento de 5 kg/m2 del IMC incrementaba la mortalidad un 40 % por infarto y por accidente cerebrovascular, y un 10 % por cáncer (10).
El estudio SOS (Swedish Obese Subjects Study), publicado en 2012 sobre 2010 pacientes suecos obesos con una mediana de seguimiento de 14,7 años, demuestra una reducción significativa del número de fallecimientos de origen cardiovascular y del número de sucesos cardiovasculares (infarto de miocardio e ictus) en los pacientes sometidos a cirugía bariátrica frente al grupo de control sometido a cuidados básicos habituales (11).
Estos datos se corroboran en un estudio publicado por Scott y cols., en el que aparece una reducción del riesgo de infarto agudo de miocardio, ictus o muerte del 25-50 % en comparación con los pacientes no intervenidos (12).
Hemos utilizado en el estudio el algoritmo REGICOR en lugar de la ecuación de Framingham (NM, EE. UU.), utilizada en otras series, porque esta última presenta diversas limitaciones cuando se aplica a nuestra población, debido a que sobreestima el riesgo cardiovascular más de 2,5 veces, puesto que asume la diabetes como equivalente de riesgo coronario y esto no parece cumplirse en nuestro entorno.
Es por ello por lo que en España se ha propuesto como alternativa la ecuación de REGICOR, que resulta de una calibración mediante una metodología contrastada de la ecuación de Framingham, y ha demostrado que en nuestra población realiza una estimación del riesgo cardiovascular a los 10 años más precisa que otras ecuaciones disponibles.
El RCV calculado en nuestra serie mediante el REGICOR es bajo, tanto antes como al terminar el seguimiento (3,2 % y 2,2 %, respectivamente), probablemente por tratarse de una población joven y exenta de enfermedad cardiovascular sintomática.
Corcelles y cols., en su serie de 403 pacientes, reportan con el mismo algoritmo un RCV antes y a los 12 meses de seguimiento del 4,1 % y 2,2 %, respectivamente (13). Mateo Gavira y cols. estudian el RCV de su serie, antes y a los 2 años del bypass, con ambas ecuaciones; con la de Framingham obtienen un riesgo de evento cardiovascular a los 10 años del 25,9 % y 4,3 %, respectivamente, significativamente mayor que cuando lo calculan mediante el REGICOR, que resulta del 3,0 % y 1,6 % antes y después de la cirugía, respectivamente (14).
Sin embargo, otros estudios que solo utilizan la ecuación de Framingham obtienen un RCV antes y a los 12 meses de la cirugía del 7 % vs. 3,5 % (Batsis y cols.), del 12 % vs. 6 % (Vogel y cols.), del 5,7 % vs. 2,7 % (Torquarti y cols.) (12) y del 4,5 % vs. 1 % (Ocon y cols.) (15).
La reducción del RCV en nuestro estudio, después de un seguimiento medio de casi 6 años, es del 32,2 %, comparable al descrito en otros trabajos con seguimientos de 12 meses, que muestran una disminución del 28 % en los pacientes sin síndrome metabólico y de alrededor del 50 % —en otros estudios— en el conjunto de los pacientes (13).
Esto es esperable puesto que la respuesta en cuanto a resolución de comorbilidades siempre es mayor en los pacientes operados con menor tiempo de evolución. Los resultados mejores suelen darse a los 2 años de la cirugía, pero los obtenidos a los 5 años son mucho más fiables para extraer conclusiones firmes, como afirman Baltasar y Fobi en sus estándares de calidad y criterios de mejora tras la cirugía (16).
Cuando analizamos la prevalencia de las comorbilidades en nuestros pacientes, esta es similar a la de otros estudios y la resolución de las mismas mantiene un porcentaje favorable, incluso superior a lo publicado en otras series con seguimiento inferior (17,18). La resolución de las comorbilidades, según los estándares de calidad referidos, define como resultados buenos la remisión de la DM2, la HTA y la DLP en > 70 % de los pacientes a los 2 años, y en un 25 % de los casos de SAHS a los 2 años. En nuestra serie superamos esos requerimientos con creces salvo en el caso de la HTA, que al final del seguimiento se resolvió en el 53,4 %, mostrando curación/mejoría el 82,3 % de los casos.
En una revisión sistemática que incluye 29 estudios y 428 pacientes sometidos a bypass gástrico laparoscópico, con un seguimiento del 80 % a los dos años, el porcentaje de resolución de la HTA es del 38,2 %, el de la DM2 del 66,7 % y el de la DLP del 60,4 % con un PSP del 65,7 % (19). Otros estudios reportan un porcentaje de resolución de la HTA de alrededor del 70 % a los dos años, pero con un porcentaje de pacientes seguidos escaso (20).
El seguimiento de nuestros pacientes es del 97 % de los operados durante casi 6 años, lo que justifica las cifras obtenidas ya que está descrito que hasta un 13,2 % de los pacientes con resolución de la HTA a los 2 años de la cirugía pueden recaer a los 6 años.
Con respecto al resto de comorbilidades, en nuestro caso se resuelven el 100 % de las GBA, el 70,2 % de las DM2, el 83,9 % de las DLP y el 71,4 % de los SAHS, porcentajes iguales e incluso superiores a los publicados en otras series con menor tiempo de seguimiento (21,22).
Hemos observado, al igual que otros autores (23), una mejoría de todos los FRCV menos de los niveles de HDL-colesterol, que no muestran variaciones significativas después de la cirugía (Tabla IV). Vest y cols., en su estudio de 2012, encuentran un aumento del HDL-colesterol después de la cirugía, con el siguiente efecto beneficioso cardiovascular que ello conlleva (24).
La SECO, en la Declaración de Salamanca del año 2003, se propone como deseable la evaluación del 75 % de los pacientes a los 2 y 5 años después de ser intervenidos para tener un estudio con fiabilidad. En la misma línea, la ASMBS (Standards Committee de la American Society for Metabolic and Bariatric Surgery) acepta, para valorar la pérdida ponderal, el PSP y el PEIMCP, y considera resultados definitivos de la cirugía bariátrica los obtenidos a los 10 años de seguimiento postoperatorio, con un seguimiento mínimo del 60 % de los pacientes intervenidos (25).
En una revisión sistemática de 2014 publicada en JAMA, Puzziferri y cols. observan que menos del 16 % de los estudios reportan resultados a más de 2 años y tan solo el 0,4 % de los mismos siguen al menos al 80 % de los pacientes (19). En otro estudio realizado por Higa y cols. con 242 pacientes, el 33 % siguen a los 2 años y tan solo un 7 % de ellos permanecen en seguimiento a los 10 años (26).
A pesar de contar en nuestro hospital con un registro exhaustivo y protocolizado de variables a registrar durante todo el seguimiento de los pacientes intervenidos de cirugía bariátrica desde hace 20 años, una debilidad del estudio es la de ser retrospectivo. Sin embargo, podemos afirmar que no hemos encontrado en la bibliografía otro trabajo con tan alto porcentaje de pacientes evaluados al final del seguimiento, con pérdida de tan solo 10 (3,3 %) durante un seguimiento medio de casi 6 años y con más del 50 % seguidos al menos 5 años, incluyendo los pacientes con reganancia de peso y fracaso, que con frecuencia dejan de acudir a revisión.
El Consenso SEEDO-SECO de 2004, que se basa en las publicaciones de Reinhold y MacLean, categoriza los resultados de la pérdida de peso como: excelente si el IMC < 30 kg/m2 y el PSP > 75 %; bueno si el IMC es de 30-35 kg/m2 y el PSP es el 50-75 %, y fracaso si el IMC > 35 kg/m2 y el PSP < 50 % (5).
La pérdida ponderal en nuestra serie se encuentra dentro del rango catalogado como resultado “bueno” si tomamos el PSP del 50-65 % con un IMC de 30-35 (el PSP a los 24 meses es del 66,4 %, al final del 58 % en nuestra serie), y como “excelente” si tomamos como referencia el PEIMCP > 65 % (en nuestra serie es, a los 24 meses, del 76,82 % y al final del 66,9 %). A los 2 años de la cirugía tenemos un 15,9 % de fracasos con un PSP < 50 %, y al final del seguimiento hay un 32 % de fracasos según este criterio, dato que corrobora la importancia del seguimiento a largo plazo.
CONCLUSIONES
El bypass gástrico es una técnica muy eficaz para perder peso de forma mantenida y resolver en un alto porcentaje las comorbilidades directamente involucradas en la aparición de eventos cardiovasculares.
Sin embargo, según nuestra experiencia, es muy importante que para evaluar la eficacia real de la técnica se reporten los resultados con un seguimiento mínimo de 5 años, ya que un porcentaje nada despreciable de pacientes con resultado excelente a los 2 años se convierten en fracasos a lo largo del seguimiento.