Señor Presidente de Honor, Presidenta y miembros de la Junta Directiva y del Comité Científico Educacional y socios de SENPE, congresistas, amigas y amigos:
Con gran honor y agrado dictaré esta Decimocuarta Lección Jesús Culebras que la SENPE ha decidido concederme en el 38 Congreso de la Sociedad que se celebra en la ciudad en que nací y en la que estudié Medicina. Este regalo no hace sino que vuelva a sentirme bienvenida y querida en esta sociedad científica en la que cabemos todos y a la que siempre estaré agradecida por todo lo que me ha enseñado.
He revisado las lecciones de mis predecesores en este reconocimiento y he aprendido de la historia de la SENPE y del papel desempeñado por Jesús Culebras, un cirujano apasionado de la nutrición, tanto en la fundación de la Sociedad en 1978 y la creación como boletín, en 1979, de la revista Nutrición Hospitalaria, como en el desarrollo posterior de ambas y en el posicionamiento de la revista en la escena internacional con la consecución del factor de impacto. Se necesita para ello ser una persona visionaria, perseverante e inasequible al desaliento…, cualidades que marcan a las personas que, como él, han tenido una gran proyección profesional, académica y científica en nuestro país y fuera de nuestras fronteras, principalmente en Latinoamérica.
Llegué al Hospital Niño Jesús en el año 1989 con la misión de crear y desarrollar la Unidad de Nutrición Clínica y Dietética al modo de las que existían en España en el campo de los adultos. Esta es la tarea que me encomendó el Prof. Hernández, catedrático de pediatría de la UAM y a la sazón mi jefe. No había en ese momento un ejemplo o campo de doctrina pediátrico de donde beber, pero sí encontré una buena referencia en los adultos y ahí conocí la SENPE. Esta Sociedad me ha acompañado durante toda mi vida profesional y he contribuido a su desarrollo siendo coordinadora del Grupo de Trabajo de Estandarización y Protocolos en Nutrición Clínica desde febrero 2007 hasta 2017.
El tratamiento con dieta cetogénica ha tenido gran importancia en mi vida profesional en el Hospital Niño Jesús gracias a una serie de personas que han permitido poder llevarlo a la práctica. Entre ellas destacaré, en primer lugar, a los pacientes con epilepsia, fundamentalmente debida a deficiencia de Glut-1, y en segundo lugar, a su médico, Luis González Gutiérrez Solana y su mujer Beatriz García-Alcolea, enfermera de nuestra unidad. Ella y Begoña Gómez han puesto todo su interés en el tratamiento de estos pacientes. Y, por último, a una médico como pocas, Jana Ruiz Herrero, quien con su interés ganó la beca de Investigación de la Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica Sira Carrasco de 2015, que la llevó a la lectura de su tesis Doctoral (1), al primer manual de dieta cetogénica en 2017 (2) y al segundo en 2021 (3).
He elegido este tema porque me parece apasionante y, aunque yo solo lo he desarrollado en niños, su proyección para el tratamiento de adultos con gran número de patologías es muy importante. Quiero dedicar esta “Decimocuarta Lección Jesús Culebras. Dieta cetogénica, un tratamiento a medio descubrir” a los pacientes y a sus familias.
INTRODUCCIÓN
El control de la epilepsia ha sido el punto de partida de la dieta cetogénica (DC) debido al efecto conocido del ayuno en su tratamiento desde tiempos remotos (4). Este efecto comenzó a observarse científicamente a principios del s. XX cuando, en 1911 en Francia (5) y 10 años más tarde en EE. UU. (6), se publican los primeros trabajos en los que, pensando que la epilepsia es una intoxicación, los pacientes se someten a periodos de ayuno prolongados para conseguir su depuración. Como es evidente, no se puede aplicar el ayuno durante mucho tiempo y es Wilder (7), en la Clínica Mayo, el primero en proponer una dieta capaz de conseguir la cetosis de un modo alternativo. Poco después, Talbot (8) es el que “pone a punto” el modo de diseñar y calcular una DC. Basándose en la capacidad cetogénica de los alimentos, define la razón cetogénica, expresada en g: grasa / proteína + carbohidratos, que conocemos en la actualidad.
Se define entonces la DC como aquella rica en grasa y pobre en proteínas y carbohidratos (CHO), cuyo objetivo es conseguir los cambios bioquímicos del ayuno y el efecto sobre el control de las crisis, y que permite un estado anabólico en una situación metabólica de ayuno. Este efecto lo consigue cambiando el metabolismo energético, potenciando la respiración mitocondrial (oxidación de grasa y producción y utilización de cuerpos cetónicos [CC]) frente a la glucólisis.
Para mejorar el cumplimiento de la dieta, al aumentar la palatabilidad y la diversificación alimentaria y disminuir los efectos secundarios, se han descrito distintos tipos de tratamientos dietéticos cetogénicos (TDC) (3). En ellos no solo puede variar la composición de la dieta sino también la frecuencia de las tomas y los intervalos entre ellas, como en el caso del llamado ayuno intermitente.
En la tabla I se muestran los diversos TDC ordenados en cuanto a su grado de restricción y aparición cronológica. Varias puntualizaciones en cuanto a la DC clásica (DCC): a) la mayoría de la grasa son triglicéridos de cadena larga (TCL), pudiendo administrarse preferentemente TCL poliinsaturados en vez de saturados para mejorar su perfil nutricional; b) la relación cetogénica puede modificarse según las necesidades del paciente; la dieta de relación cetogénica 2,5-2:1 recibe el nombre de modificada clásica; y c) la DCC 3:1 está indicada en los menores de 5 años, los adolescentes, los adultos y al inicio del tratamiento, para evitar que el aporte proteico pueda ser limitante, y la DCC 4:1 en el resto de edades.
Tabla I. Composición de los distintos tipos de dieta cetogénica (3).
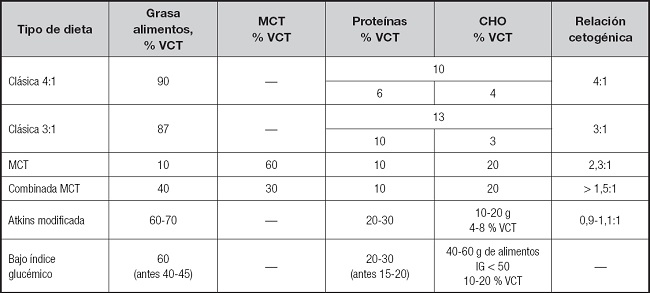
CHO: carbohidratos; IG: índice glucémico; MCT: triglicéridos de cadena media; VCT: valor calórico total de la dieta.
La absorción y metabolización de los triglicéridos de cadena media (MCT), menos compleja y más rápida que los TCL, llevó a Huttenlocher (9) a diseñar la dieta basada en MCT (D-MCT) para alcanzar el objetivo de cetosis con menores restricciones. Sin embargo, la presencia frecuente de efectos secundarios gastrointestinales ha llevado a modificaciones para evitarlos. En ellas es indispensable garantizar el aporte de ácidos grasos esenciales y con frecuencia pueden combinarse con la DCC.
La dificultad de mantener una DCC está en el origen del uso de la dieta de Atkins modificada (DAM) y la dieta de bajo índice glucémico (DBIG). La iniciativa del uso de la primera corresponde a la madre de un paciente, cuya experiencia fue capitalizada por el hospital John Hopkins (10), que comienza a usarla limitando el aporte de CHO a 10 g al día y, más tarde, añadiendo un preparado comercial de DCC que permite aumentar la ratio cetogénica y la cetosis (DAM modificada) (11). La utilidad de la DBIG se comprobó, además, al observar que los pacientes a la espera de comenzar la DCC a quienes se les indicaba esta dieta respondían a ella. Consiste en controlar rigurosamente la cantidad de CHO, escogiendo los alimentos cuyo índice glucémico es inferior a 50, prefiriendo aquellos con alto contenido en fibra (12). Esta dieta no consigue cetosis, aunque mantiene estables los niveles de glucosa, y con el tiempo ha sufrido variaciones, haciéndose más estricta.
Recientemente, el ayuno intermitente (13) empieza a considerarse también un TDC: bien ayunando (tomando agua libre) 1 o 2 días a la semana o a días alternos, o bien realizando todos los días entre 14-18 horas de ayuno. Su uso en pediatría no está reconocido actualmente.
En los casos en que no pueda usarse la vía digestiva se puede indicar la vía parenteral (14), usada por primera vez en 1970. Este tratamiento es siempre excepcional.
La elección del tipo de dieta se individualizará en cada paciente y será necesario tener en cuenta la edad, el tipo y gravedad de la enfermedad, la necesidad o no de conseguir una respuesta rápida, la existencia de accesos artificiales para nutrición enteral, las características de la familia y los hábitos dietéticos del enfermo, y la disponibilidad de personal entrenado (dietistas-nutricionistas) para la elaboración de las dietas. Un último comentario: a veces la dieta que reciben los pacientes no puede encuadrarse dentro de un determinado tipo, pero es rica en grasa y relativamente pobre en CHO, siendo cada vez más frecuente la mezcla de dietas y la adaptación a cada tipo de circunstancia: adición de fórmulas, de suplementos de MCT, de cetonas, etc. (15).
MECANISMO DE ACCIÓN
En 1921 el Dr. Geyelin (6) comunica, en la reunión de la Asociación Médica Americana, los buenos resultados del ayuno en una serie de 30 pacientes con epilepsia, tratamiento que había establecido basándose en las observaciones del osteópata Dr. Conklin. El éxito de este procedimiento llevó a implantarlo en diversos centros y a realizar una serie de investigaciones para conocer el porqué de sus efectos, que se atribuyeron a la acidosis, a la deshidratación y a la cetosis. Su aplicación en la Harriet Lane Home for Invalid Children (la primera clínica pediátrica asociada a una Escuela de Medicina en los Estados Unidos) del Johns Hopkins Hospital, sentó las bases del paradigma de la investigación clínica, el conocimiento de la fisiología de los electrólitos en pediatría y de la nefología moderna (4). El desarrollo de la DC (7,8) permite su aplicación con muy buenos resultados hasta la llegada de los fármacos antiepilépticos, pero luego su uso fue decayendo por la dificultad de seguir una dieta frente a la toma de una medicación oral. En 1993 el éxito obtenido en la curación de Charly, hijo de un director de cine, llevó al redescubrimiento del tratamiento. La creación de la Charly Fundation en 1994 en EE. UU. y la Mathew’s Friends Charity for Ketogenic Dietary Therapies en 2004 en Europa han alentado su desarrollo.
VÍAS METABÓLICAS IMPLICADAS EN LOS TRATAMIENTOS DIETÉTICOS CETOGÉNICOS (16-19)
La oxidación de ácidos grasos se realiza principalmente en la mitocondria del hígado y da lugar a acetil-CoA que se procesa en el ciclo de Krebs para la producción de adenosin trifosfato (ATP) vía fosforilación oxidativa.
Los CC (acetoacetato, β-hidroxibutirato y acetona) se producen como parte de las adaptaciones fisiológicas a la escasez de CHO durante el ayuno y el ejercicio prolongado. En estas circunstancias ocurre la lipolisis de los depósitos de grasa corporal y cuando los niveles de ácidos grasos son elevados y superan la capacidad metabólica del ciclo de Krebs, la acetil-CoA se deriva a la cetogénesis. La acetona se elimina a través de los pulmones y los riñones y los otros CC se transportan por la sangre a los tejidos extrahepáticos para proveer de una fuente de energía alternativa a la glucosa.
En el cerebro, estos CC cruzan la barrera hematoencefálica y llegan hasta el espacio intersticial de glía y neuronas mediante los transportadores específicos de ácidos monocarboxílicos. Allí se metabolizan en las mitocondrias llegando a producir acetil-CoA que se incorpora al ciclo de Krebs para producir energía (ATP).
Al instaurar una DC conseguimos una situación similar a la descrita: aumento de ácidos grasos y limitación de CHO. Este tratamiento condiciona el paso de la obtención de energía por el cerebro (que constituye el 2-3 % del peso corporal y es responsable del 25 % del consumo de O2 y el 20 % del consumo de glucosa del organismo), de una vía basada en la glucólisis a una vía basada en la oxidación de ácidos grasos a nivel mitocondrial. Además, en aquellas DC denominadas clásicas, con disminución importante del aporte proteico, la disponibilidad de CHO disminuye aún más al aumentar la captación de glucosa por los adipocitos debido al aumento del factor de crecimiento de fibroblastos. Por último, los TDC producen cambios importantes en la microbiota intestinal.
MECANISMOS DEL EFECTO ANTICONVULSIVANTE Y NEUROPROTECTOR (16-19)
En sus comienzos, la DCC perseguía emular el efecto anticonvulsivo del ayuno que se creía condicionado por los CC, como se demostró en 1935 en modelos animales. Sin embargo, pronto se comprobó una relación no constante entre los niveles de CC y el control de las crisis, sospechándose que otros efectos metabólicos podrían ser capitales tanto para dicho control como para los efectos antiepileptógenos que se observaban. Mucho más tarde, la efectividad de la DBIG, con la que no se produce cetosis, confirmó estas observaciones.
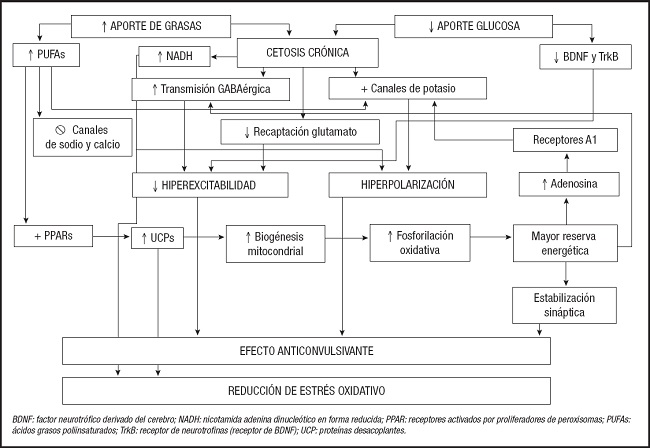
Los TDC condicionan una miríada de cambios y el efecto no es consecuencia de una sola modificación metabólica sino de su conjunto a distintos niveles. En la figura 1 se muestra un esquema de estos cambios.
Pero, es más, en los estudios preclínicos y clínicos, y en las aplicaciones traslacionales, se observa que la DC tiene, en los pacientes con epilepsia, no solo un efecto a nivel del control de las crisis, sino también un efecto neuroprotector con mejoría en el estado de alerta y conexión con el medio, del sueño, del desarrollo cognitivo, del estado de ánimo y del ajuste psicosocial, lo que amplía su aplicación a otras muchas enfermedades.
Los cambios en el metabolismo celular condicionados por la instauración del TDC permite una mejor adaptación (resiliencia) en las situaciones condicionadas por ciertas enfermedades en las que existe un desequilibrio en el metabolismo energético celular. La disminución de la glucosa en sangre y líquido cefalorraquídeo y el aumento de los ácidos grasos séricos son los dos hechos principales en este tipo de tratamiento y se traducen en aumento de los CC, restablecimiento del ciclo de Krebs (es decir, anaplerosis), de los canales iónicos, de la neurotransmisión, de la capacidad antioxidante, de la acetilación de histonas y de la función mitocondrial. Las consecuencias últimas de este tratamiento metabólico, que quizá pudiera cambiar la evolución de la enfermedad, son la mejora de la bioenergética mitocondrial, la disminución de la hiperexcitabilidad neuronal, la restauración de la integridad sináptica y la disminución de las especies reactivas de oxígeno, entre otras.
Alguno de los cambios observados parece ocurrir por variaciones en el perfil de expresión de genes relacionados con el sistema nervioso central (20). Al estudiarlo mediante microarrays y el análisis de componentes principales no dirigido, se observa tanto en el ARN mensajero como en los micro ARN cambios que nos permiten explicar la mayoría de los efectos encontrados en los pacientes estudiados, lo que apoya la complejidad de estas situaciones.
Por otra parte, estudios recientes en modelos animales han mostrado que los TDC producen cambios en la microbiota intestinal con efecto anticonvulsivante —algo de razón parece que tenían los primeros estudiosos del efecto del ayuno con su teoría de la intoxicación—, modificando la flora intestinal, reduciendo la actividad bacteriana de gamma-glutamilación y su efecto sobre los aminoácidos periféricos, y regulando el equilibrio GABA/glutamato en el hipocampo (21). Esta área de investigación abre un campo que puede ayudarnos a entender muchas cuestiones relacionadas con el eje intestino-cerebro e incluso la suplementación con distintos tipos de probióticos para controlar ciertas enfermedades neurológicas o psiquiátricas.
INDICACIONES Y CONTRAINDICACIONES, DEL NIÑO AL ADULTO
Los inicios de la DC se llevaron a cabo tanto en niños como en adultos –en estos últimos se mostraba un 56 % de control completo de las crisis (22)– pero el desarrollo posterior se realizó solo en niños. Su aplicación en lactantes fue más tardía y es a partir de 2001 cuando se empiezan a publicar sus resultados (23), que se completan con una guía (24). Nuestra experiencia muestra que este tratamiento, en 42 niños menores de 2 años, es eficaz y seguro, y que los mejores resultados se obtienen en el síndrome de West (25). En la tabla II se muestran las posibles indicaciones de los TDC en pediatría.
Tabla II. Posibles indicaciones de tratamientos dietéticos cetogénicos en pediatría (3).
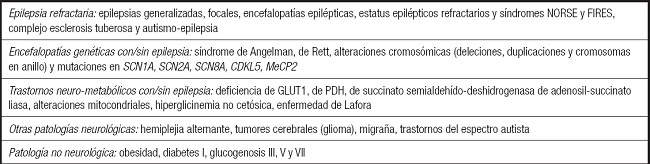
NORSE: new onset refractory status epilepticus; FIRES: febrile infection-related epilepsy syndrome; GLUT1: transportador de glucosa tipo 1; PDH: piruvato deshidrogenasa.
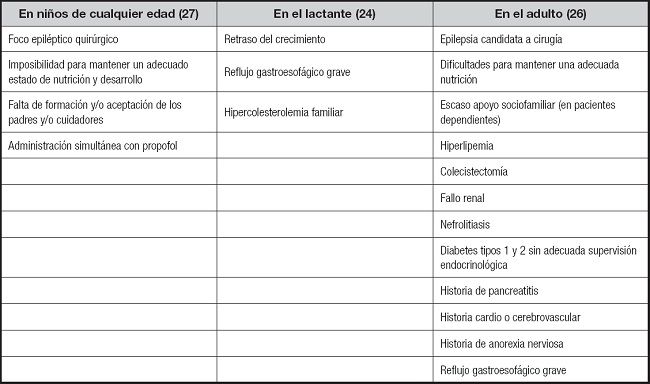
En 2021 se publican las primeras sugerencias de uso en adultos, como recomendación de expertos (26) y basadas en su experiencia en casi 2200 pacientes. La mayoría han comenzado el tratamiento siendo adultos, aunque en algún centro hasta el 42 % de los pacientes han sido trasladados desde pediatría. Concluyen que la indicación del TDC en la edad adulta es la epilepsia, como en los niños, excepto la epilepsia focal, cuyo tratamiento es la cirugía, y recomiendan ensayos antes de extender su uso a otras patologías. Llama la atención que el 40 % de las instituciones encuestadas ya prescriben TDC para otras enfermedades, mostrándose un resumen de estas en la tabla III. Los encuestados del panel identificaron los factores más importantes que influyen en la elección del tratamiento, tienen experiencia en todos sus tipos y usan más frecuentemente la DAM.
Tabla III. Posibles indicaciones de tratamientos dietéticos cetogénicos en adultos (3).
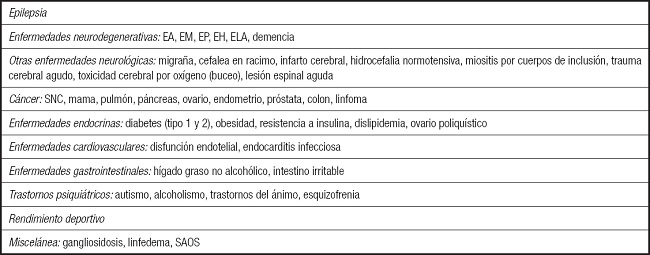
EA: enfermedad de Alzheimer; EM: esclerosis múltiple; EP: enfermedad de Parkinson; EH: enfermedad de Huntington; ELA: esclerosis lateral amiotrófica; SNC: sistema nervioso central; SAOS: síndrome de apnea obstructiva del sueño.
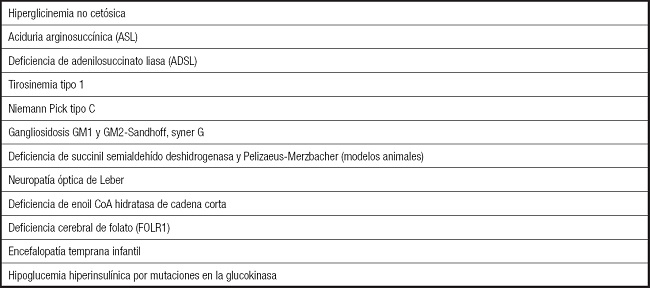
Las contraindicaciones absolutas (3,26,27) en todos los rangos de edad son aquellas en que la restricción de CHO o la oxidación de ácidos grasos están comprometidas y, por tanto, la instauración del TDC puede ser fatal (Tabla IV). Es imprescindible realizar un estudio metabólico para descartar estas alteraciones en los niños y valorar la conveniencia de llevarlo a cabo en los adultos, sobre todo en aquellos con deficiencias intelectuales o sin un diagnóstico de certeza (26). En el lactante (24) son también contraindicaciones absolutas los defectos de la glucogénesis, como es el déficit de fructosa-1,6-difosfatasa, las glucogenosis excepto la de tipo 2, el síndrome del QT prolongado y otras enfermedades cardíacas, las insuficiencias hepática, renal o pancreática, y los hiperinsulinismos excepto en el déficit de glucokinasa con hipoglucemia hiperinsulínica refractaria, en el que el tratamiento de elección en este momento es la DC (28). En el adulto (26) son el embarazo (aunque hay varias publicaciones que refieren un curso y desenlace normal), el fallo hepático, la pancreatitis aguda y la diabetes de tipo 1 sin indicación o supervisión por un endocrinólogo.
Tabla IV. Contraindicaciones absolutas de los tratamientos dietéticos cetogénicos a cualquier edad (3,26,27).

También existen contraindicaciones relativas en función de la edad, que se muestran en la tabla V.
Desde el punto de vista práctico, la evaluación previa y el seguimiento de los pacientes de cualquier edad debe realizarse de forma sistemática e individualizada, con un calendario reglado y por el equipo de profesionales implicado en cada caso (dietista-nutricionista, neurólogo, gastroenterólogo pediátrico o endocrinólogo de adultos, etc.), que inexcusablemente realizarán la educación del paciente y/o su familia. El control clínico y las determinaciones analíticas serán la base para la prevención y el abordaje de las complicaciones, y la duración mínima del tratamiento, excepto si existiera un empeoramiento claro de las crisis, será de 3 meses. Se recomienda aumentar la ingesta de líquidos al inicio del tratamiento y contemplar el suplemento de vitaminas, minerales y oligoelementos, especialmente el de vitamina D3 y calcio. Se remite al lector a publicaciones más extensas sobre este particular (3,24,26,27).
EPILEPSIA REFRACTARIA
Las indicaciones de los TDC en la epilepsia refractaria se han recogido muy bien en las recomendaciones pediátricas del año 2018 (27). En general, el 50 % de los pacientes reducen las crisis al menos en un 50 % y quedan libres hasta un 15-20 %; y en ciertas patologías (Tabla VI) los resultados son aún mejores, superiores al 70 %. Desde el punto de vista práctico, en toda epilepsia refractaria —aquella que no responde a dos antiepilépticos correctamente administrados— y también en ciertos casos de epilepsias muy graves debe plantearse la posibilidad del TDC y hay que tener en cuenta dos hechos: el primero, que la respuesta no depende de la semiología epiléptica y, el segundo, que el inicio del tratamiento debe realizarse lo antes posible. En los adultos, el consenso (26) recoge las mismas indicaciones que en pediatría, a excepción de la epilepsia focal, que tiene preferentemente tratamiento quirúrgico. Constantemente se van poniendo al día las recomendaciones como, por ejemplo, en el caso del estatus epiléptico superrefractario y el síndrome de epilepsia relacionada con infección febril (29,30).
Tabla VI. Patologías y síndromes epilépticos en los que los TDC han demostrado una respuesta superior al 70 % (27).

La última revisión Cochrane (31) reúne 13 ensayos clínicos de TDC y califica la evidencia para su uso como baja. Constata que la falta de cegamiento y los abandonos de la dieta son los dos problemas más importantes que afectan a la calidad de los estudios, y considera también el alto número de efectos adversos, aunque leves, como un inconveniente. Ciertamente, ninguno de ellos va a poder resolverse. Sin embargo, al hilo de la indicación en la epilepsia se han observado mejoras en otros aspectos que suponen un efecto neuroprotector (19,32), como ya se ha mencionado anteriormente, y que hasta el momento se han planteado como objetivos secundarios. Prueba del interés que despiertan, hay investigaciones o revisiones recientes en términos de calidad de vida (33), patología psiquiátrica acompañante (34), cognición (35), sueño (36), etc. En estas áreas es muy importante diseñar buenos estudios para poder sacar conclusiones que ayuden a perfilar las aplicaciones de estos tratamientos.
ERRORES INNATOS DEL METABOLISMO
Las características de los TDC –metabolización mitocondrial de las grasas frente a la oxidación de la glucosa para obtener energía– son una oportunidad para el tratamiento de ciertos errores innatos del metabolismo: aquellos que presentan una alteración en algún eslabón de la glucólisis. De esta forma, al sortear una ruta determinada y derivar a otra no comprometida, alcanzando modificaciones en el metabolismo o en la función mitocondrial, o consiguiendo un sustrato alternativo como los CC, se puede paliar el defecto primitivo y tratarlo de forma primaria (37-39). Este tratamiento con DC en general suele acompañarse de otras medidas.
Pero la DC puede también utilizarse para controlar ciertos síntomas (37-39), principalmente la epilepsia, y asimismo alteraciones musculares y del movimiento, retrasos del desarrollo o discapacidades intelectuales, etc. En estas circunstancias y una vez descartada la existencia de patología que la contraindique (Tabla IV), el control de los síntomas puede tener éxito.
En todos estos casos es fundamental instaurar el tratamiento de forma progresiva, sin someter al paciente a periodos de ayuno y procurándole un control riguroso.
Existe un gran número de patologías, pero en este texto se comentarán solo algunas de ellas.
USO DE TRATAMIENTOS DIETÉTICOS CETOGÉNICOS EN EL TRATAMIENTO DEL PROBLEMA METABÓLICO PRIMARIO
El síndrome de deficiencia del transportador de la glucosa tipo 1 (SD-glut 1) es el ejemplo clásico en que el TDC se considera como patrón oro. Al faltar el transportador de la glucosa en las células endoteliales de la barrera hematoencefálica y los astrocitos, se produce un síndrome de crisis cerebral de energía que se controla gracias al aporte de CC. Tanto es así que, en la publicación en que se describe esta patología, los pacientes ya están bajo tratamiento y han respondido favorablemente (40). El origen del trastorno son las mutaciones del gen SLCA1 (41), que es uno de los tres requisitos para el diagnóstico junto a la expresión clínica que varía con la edad (convulsiones, microcefalia, retraso del desarrollo y alteraciones complejas del movimiento) y la determinación de hipoglucorraquia con normoglucemia (42).
El comienzo del tratamiento debe ser inmediato a la sospecha y no es necesario esperar a la confirmación diagnóstica del estudio de mutaciones, ya que los pacientes con síntomas sugestivos en los que no se comprueba la mutación también se benefician del tratamiento (43). Se recomienda la DCC, de elección en lactantes y preescolares, manteniéndola el mayor tiempo posible. A partir de la edad escolar y en los pacientes con problemas de cumplimiento, la DAM también se ha mostrado eficaz. La DBIG no se aconseja ya que no consigue cetosis, pero su uso en pacientes con grandes dificultades de seguimiento de las indicaciones dietéticas ha mostrado resultados satisfactorios gracias a la estabilización de los niveles de glucosa en sangre (44). Este hecho abre la puerta a nuevos abordajes del tratamiento, menos restrictivos, sobre todo relacionados con su mantenimiento a largo plazo. El documento de consenso de Klepper y colaboradores (42) nos ilustra sobre las particularidades de esta enfermedad y hace un hincapié especial en los interrogantes que necesitarán una respuesta en el futuro, principalmente las repercusiones que se podrán observar en los pacientes adultos en los otros órganos en los que se expresa Glut-1: corazón, músculo, placenta y retina. También en la posibilidad de nuevos tratamientos de tipo genético o de administración de nuevos “combustibles” cerebrales.
En la deficiencia de piruvato-deshidrogenasa (PDH) por mutaciones del gen PDHA1 ligado a X, que es parte del complejo enzimático que permite el paso irreversible y aeróbico del piruvato a acetil-CoA, no se puede aprovechar la glucosa. Los TDC son de elección (45) al generar CC. Sin embargo, la heterogeneidad del trastorno bioquímico, que se plasma en una expresión clínica muy variable tanto en gravedad como en edad de presentación, hace que la respuesta no sea constante (46-48) y que precise otras medicaciones para controlar la enfermedad. La mayoría de los trastornos en niños son deficiencias en la subunidad E1 y también en la E3, mientras que, en los adultos, los tipos E1α y E2 que responden tienen clínica muscular o de alteración del movimiento. Es posible que en adultos el número de casos con este trastorno aumente bastante al mejorar los diagnósticos genéticos.
Otras enfermedades mitocondriales con repercusión en el abastecimiento de energía son debidas a mutaciones en el ADN mitocondrial o nuclear. Su presentación en cuanto a la clínica, momento de aparición y órgano afectado, sobre todo a nivel cerebral y con epilepsia, es muy diversa. La respuesta al TDC que condiciona, como se describía en el apartado de mecanismo de acción, una infinidad de cambios metabólicos a todos los niveles también es muy variable. Cada vez más patologías mitocondriales, sobre todo con epilepsia refractaria, son subsidiarias del TDC (11,37-39,49): síndromes de depleción del ADN mitocondrial tipo gammapolimerasa (POLG) con o sin síndrome de Alpers-Huttenloche, modificación de la traslación y transcripción como en el MELAS, y alteraciones de la cadena respiratoria no filiadas o de los complejos I, II, IV, I+IV. Sin embargo, ciertos casos en adultos con deleción del ADN mitocondrial y miopatía han mostrado resultados adversos.
Una muestra reciente de cómo se amplían las aplicaciones de los TDC en los casos de defectos en la provisión de energía mitocondrial es su indicación en las alteraciones en los defectos de la lanzadera mitocondrial malato-aspartato (MAS) y en el transportador del piruvato (MPC1) (50). MAS es el principal responsable del transporte de NADH a través de la membrana interna mitocondrial —que sustenta la glucólisis y la síntesis de serina— y MPC1 permite que el piruvato —último producto de la glucólisis— alcance la matriz mitocondrial, desde donde entra en el ciclo de Krebs. El análisis de los trastornos asociados a la expresión de las proteínas implicadas en estas vías metabólicas ha permitido diferenciar unos fenotipos complejos de tipo neurológico/epiléptico (MDH1, MDH2, GOT2, SLC25A12 y MPC1) y neuropsiquiátrico/hepático (SLC25A13). Mientras en este último, la deficiencia de citrina, ya estaba establecido el tratamiento con una dieta baja en CHO y rica en grasa, en el resto de las alteraciones genéticas este trabajo ha puesto de manifiesto su indicación.
Y, por último, las glucogenosis, de las que 4 tipos se han tratado con DC con el objetivo último de mejorar la provisión de energía mediante los CC (37,38). Las glucogenosis VII —enfermedad de Tauri o deficiencia de fosfofructoquinasa— y XII —deficiencia de aldolasa— están referidas en la literatura hace mucho tiempo sin publicaciones posteriores. En la de tipo IV, la enfermedad de McArdle o deficiencia de glucógeno-fosforilasa muscular, no se pueden movilizar las reservas de glucógeno muscular que se precisan para el ejercicio anaeróbico y de alta intensidad, lo que conduce a una tolerancia al ejercicio limitada. El tratamiento recomendado actualmente es una dieta con CHO complejos (65 % VCT), baja en grasa (20 % VCT), más sacarosa antes del ejercicio y entrenamiento progresivo. Numerosos pacientes informan de una mejora de sus síntomas con distintos tipos de TDC, por lo que se ha puesto en marcha un ensayo para conocer qué alternativa sería la mejor (51). En la glucogenosis de tipo III, enfermedad de Forbes, Cori o deficiencia de enzima desramificante, el tratamiento actual aceptado es una dieta rica en proteínas con suplementos de almidón de maíz para controlar la hipoglucemia, e incluso la administración de fuentes exógenas de CC (52). Sin embargo, la persistencia del daño a nivel muscular y cardíaco ha impulsado el uso de TDC (53) para, al disminuir el aporte de CHO, impedir la acumulación de glucógeno y evitar el hiperinsulinismo y, al proporcionar CC, mejorar el metabolismo mitocondrial. Este tratamiento debe monitorizarse cuidadosamente, sobre todo en los niños, debido a que sus repercusiones a nivel hepático y en los niveles de enzimas pueden ser muy variables.
USO DE TRATAMIENTOS DIETÉTICOS CETOGÉNICOS EN EL TRATAMIENTO DE LOS SÍNTOMAS DE CIERTOS ERRORES INNATOS DEL METABOLISMO
La causa principal de su uso es la existencia de convulsiones pero, como ya se indicó al principio, no es el único motivo. Esta área de indicación está en continua expansión, en primer lugar por la mayor supervivencia de los pacientes metabólicos y, en segundo lugar, por los mejores diagnósticos, el mayor conocimiento de los mecanismos bioquímicos básicos y, por último, la pérdida del miedo a esta terapia. En la tabla VII se muestran algunas de las indicaciones actuales, en muchos de los casos en combinación con otros procedimientos (37-39). Quisiera también llamar la atención sobre el uso de TDC en los casos de hipoglucemia hiperinsulínica por mutaciones en la glucokinasa (28), una muestra más del desarrollo de esta área.
TRATAMIENTOS DIETÉTICOS CETOGÉNICOS EN EL CÁNCER. ¿UN FUTURO PRÓXIMO?
Las indicaciones probadas de los TDC han ido aumentando en número, pero también su aplicación en patologías que hasta el momento no se han confirmado mediante estudios bien diseñados (Tablas II y III). El posible tratamiento del cáncer es un ejemplo que asocia una larga historia y un desarrollo clínico considerable, aunque sin un suficiente rigor científico.
En 1926, el bioquímico y médico alemán Warburg, que en 1931 recibiría el premio Nobel de Fisiología o Medicina por su descubrimiento del citocromo C en la respiración celular, publica su hipótesis sobre la etiología del cáncer, mostrando la diferencia entre el metabolismo de las células normales y de las cancerosas (55): en condiciones aeróbicas, los tejidos tumorales metabolizaban unas 10 veces más glucosa a lactato en un determinado tiempo que los tejidos normales. Este fenómeno, conocido más tarde como efecto Warburg, era el origen de la disfunción mitocondrial, principal causa del cáncer.
Hay que recordar (56) que las células normales no metabolizan la glucosa a lactato cuando disponen de oxígeno; solo recurren a esta vía metabólica (la glucólisis anaeróbica) cuando no lo hay o su disponibilidad está limitada. En contraste, las células tumorales la utilizan incluso cuando disponen de oxígeno pero, al ser mucho menos eficaz en la obtención de energía, las células cancerosas tienen gran voracidad por ella. Una aplicación práctica de esta hipótesis es la detección actual de los tumores mediante la tomografía por emisión de positrones, que mide la absorción de glucosa por una sustancia radiactiva, la fluorodeoxiglucosa. Además, mediante la glucólisis se generan los esqueletos de carbono en la síntesis de proteínas y ácidos nucleicos para así desarrollar una rápida proliferación celular.
La hipótesis de Warburg cayó en el olvido, sobre todo tras el descubrimiento de Watson y Crick de la estructura de doble hélice del ADN en 1953 y la apertura de la era de la biología molecular y la creencia de que el cáncer estaba condicionado por mutaciones genéticas. Aunque desde mediados de los años 50 ya se conocía que las células cancerosas no tenían alteraciones de su función mitocondrial y que esa (la alteración mitocondrial) no era la causa del trastorno metabólico que exhibían las células cancerosas, no es hasta los años 90 cuando Chi Van Dang se interesa por el efecto Warburg en la Universidad Johns Hopkins en Baltimore, y en sus estudios del gen MYC llega a la conclusión de que ambas hipótesis son posibles (56).
Para alcanzar sus importantes necesidades energéticas, la célula tumoral se esfuerza en adquirir los nutrientes que necesita por múltiples vías. En 2009 se describe el efecto Warburg inverso (58), un nuevo término para describir el metabolismo del cáncer como un parásito de las células normales, las células cancerosas como semillas que se siembran en un suelo fértil. Este suelo fértil, los fibroblastos, experimentan una transformación miofibroblástica y secretan lactato y piruvato (metabolitos energéticos resultantes de la glucólisis) que son transportados a las células cancerosas mediante transportadores específicos y se usan en el ciclo mitocondrial de Krebs, promoviendo así la producción eficiente de energía a través de la fosforilación oxidativa, lo que resulta en una mayor capacidad proliferativa. De ellas también obtienen otros nutrientes que necesitan, además de los producidos por la glucólisis, como ácidos grasos, glutamina y cetonas.
Una forma de combatir el crecimiento tumoral sería impedir selectivamente la adquisición de las necesidades metabólicas de estas células tumorales hambrientas mediante drogas específicas o terapias metabólicas. Estos tratamientos podrían ser menos tóxicos para las células normales que los habituales de quimio y radioterapia. La base teórica del uso de la DC en el tratamiento del cáncer es que la tumorigénesis depende en gran medida de la glucosa, mientras que las células normales mantienen su flexibilidad metabólica y pueden usar cetonas como fuel. Una DC restringida calóricamente u otras estrategias limitantes de la glucólisis fuerzan una alta producción de cetonas, sometiendo a un estrés máximo a las células cancerosas y mínimo a las células normales. Sus efectos a nivel tanto intra como extracelular son múltiples a nivel de su metabolismo, de la inflamación, de la transcripción génica y del microambiente (59).
La aplicación de la DC se ha realizado en varios tipos de cáncer y ha aumentado mucho en los últimos años (60). Los tumores más frecuentes son los gliomas, el cáncer de mama, el de próstata, el rectal, el pancreático, etc. Como pediatra, me centraré exclusivamente en los tumores cerebrales, en los que existen múltiples estudios preclínicos, en modelos animales, y clínicos que muestran efectos positivos en la aplicación del TDC (DCC y DAM): disminución del crecimiento tumoral, aumento de la supervivencia, mejoría de la calidad de vida, disminución de la cantidad de esteroides, control de la epilepsia… La limitación fundamental radica en el pequeño tamaño de las muestras, la variedad de los tipos de gliomas y la falta de grupo de control.
En el momento actual se puede resumir que, en los gliomas y glioblastomas (59), el resultado obtenido en los modelos animales contraindica la aplicación del TDC en los tumores renales asociados a esclerosis tuberosa y en aquellos con mutación BRAF V600E. Sin embargo, existen una serie de argumentos a favor (toxicidad limitada, bajo coste y fácil aplicación), otros en contra (escaso cumplimiento y efectos secundarios numerosos) y algunos puntos por aclarar, como la posible plasticidad de las células tumorales, que necesitan ensayos clínicos bien diseñados que nos despejen todas las dudas.
CONCLUSIONES
Disponemos de distintos tipos de TDC cuya elección depende de las características y necesidades de cada paciente. El conocimiento de su modo de acción está continuamente ampliándose, existiendo numerosas teorías bioquímicas, complementarias entre sí. Su aplicación inicial en el niño con epilepsia refractaria se ha ampliado a la edad adulta y está actualmente desarrollándose, y constituye el tratamiento primario en ciertos errores congénitos del metabolismo, siendo posible aplicarla en otros para la mejora de los síntomas. Además, existen muchas posibles indicaciones de los TDC, aunque son necesarios estudios clínicos rigurosos para poder confirmar su empleo.