Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.80 no.12 dic. 2005
ARTÍCULO ORIGINAL
ONCE AÑOS DE EXPERIENCIA EN EL MANEJO DE
LA RETINOPATÍA DEL PREMATURO EN LAS ISLAS BALEARES
ELEVEN YEARS EXPERIENCE IN THE MANAGEMENT OF RETINOPATHY
OF PREMATURITY IN THE BALEARIC ISLANDS
MONTAÑEZ FJ1, OLEA JL2
| RESUMEN Objetivo: Evaluar la incidencia y eficacia del tratamiento en Retinopatía del Prematuro (ROP) de los prematuros nacidos en Baleares. Palabras clave: Retinopatía del prematuro, prematuros, bajo peso al nacimiento. | ABSTRACT Purpose: To evaluate the incidence and effectiveness of the treatment of Retinopathy of Prematurity (ROP) in preterm births in the Balearic Islands. Key words: Retinopathy of prematurity, preterm, low birth weight. |
Recibido: 25/2/05. Aceptado: 30/11/05.
Hospital Universitario Son Dureta. Palma de Mallorca. España.
1 Licenciado en Medicina.
2 Doctor en Medicina.
Comunicación presentada en el LXXX Congreso de la S.E.O. (Córdoba 2004).
Correspondencia:
Francisco Javier Montañez Campos
Servicio de Oftalmología. Hospital Son Dureta
C/. Andrea Doria, 55
07014 Palma de Mallorca
España
E-mail: fjmontac@hotmail.com
INTRODUCCIÓN
Los avances en el campo de la neonatología en los últimos años, han logrado aumentar la supervivencia de los prematuros, provocando la aparición de nuevas complicaciones, casi especificas. Entre éstas se encuentra la retinopatía del prematuro (ROP), que es la primera causa de alteraciones retinianas en estos niños.
Consiste en la aparición de una retinopatía proliferante periférica debido a una isquemia retiniana. Se desencadenaría al producirse una hiperoxia extrauterina relativa que genera una regulación anómala en la producción del factor de crecimiento endotelial vascular (VEGF) (1). Se formarían unos neovasos retinianos en la periferia que pueden evolucionar a un desprendimiento de retina bilateral.
Aunque el proceso es multifactorial, el factor principal es la inmadurez vascular, relacionada inversamente con la edad de gestación y el peso al nacimiento; el principal factor desencadenante sería el oxígeno a concentraciones elevadas.
Existe una clasificación internacional, universalmente aceptada, publicada por el ICROP en 1984 (2), con una actualización en 1987. Basada en esta clasificación, un estudio multicéntrico, el CRYO-ROP, estandarizó los casos que debían ser tratados para disminuir el riesgo de la progresión a desprendimiento de retina del 51% al 31%, resaltando la importancia de diagnóstico y tratamiento precoces (3,4). Estos criterios, seguidos en este trabajo, se han visto modificados, recientemente, por la aparición de otro estudio multicentrico, el ETROP (5) y cuyos criterios de manejo y tratamiento han sido aceptados.
El CRYO-ROP efectuaba la ablación retiniana periférica con crioterapia, pero la posterior introducción de la fotocoagulación con láser de argón o diodo, a partir de 1992, ha permitido mejorar los resultados, disminuyendo los riesgos locales y generales.
A finales de 1991 se protocolizó en nuestro centro el manejo de los prematuros, poniendo en marcha un programa específico multidisciplinario con la colaboración de oftalmólogos y neonatólogos, y el almacenamiento de datos en una base de datos. Dado que nuestro centro es el único de la Comunidad Autónoma de las Islas Baleares con UCI neonatal, se ha producido una concentración de casos, entre los propios y los derivados de otros centro públicos y privados. Este trabajo pretende realizar una revisión del trabajo realizado, analizando los datos desde enero de 1992 hasta diciembre de 2003.
SUJETOS, MATERIAL Y MÉTODOS
Se puso en marcha un protocolo en el cual se incluían los recién nacidos con peso inferior a 1.501 o superior si requirieron oxigenoterapia intubada, nacidos en nuestro hospital, entre el 1 de enero de 1992 y el 31 de diciembre de 2003. La primera exploración se ha realizado a las semanas 4 tras el nacimiento, efectuándose controles posteriores cada 2 semanas y evaluando el estadio y localización, según la clasificación internacional. Las exploraciones se realizaron en el área de neonatología de nuestro hospital tras dilatación con colirio ciclopléjico al 0,5% y fenilefrina al 2,5% (1 gota cada 30 minutos, 2-3 veces), y anestesia tópica. Los que no han presentado criterios umbrales han sido seguidos cada 2 semanas hasta la vascularización completa. Aquellos que entraron dentro de los criterios de umbral se ha procedido al tratamiento bajo sedación con crioterapia (CT) o laserterapia (FC) según el momento histórico. Éstos se han seguido semanalmente hasta la resolución del proceso, y los que a pesar del tratamiento han progresado o no han regresado se ha valorado el retratamiento o si cabe la cirugía según su estadio.
Se estudiaron 446 niños, de 453 ya que por dificultades de seguimiento se excluyeron 7, de los cuales 237 niños y 209 niñas. Se ha examinado la incidencia de ROP para los pesos < 1.000 gr, 1.000-1.500 y >1.500, y para edad gestacional < 27, 27-30 y >30 semanas. Hemos evaluado en estadios III o superiores la incidencia de tratamiento en los dos períodos, donde del 92 al 95 se ha realizado crioterapia, y del 95 al 2003 se hace tratamiento con láser de diodo. También hemos evaluado el tiempo medio de inicio de tratamiento desde la fecha de nacimiento, así como en un subgrupo de casos el tiempo de vascularización periférica en aquellos no tratados.
Los resultados descriptivos se expresan con media y desviación estándar.
RESULTADOS
La edad media fue de 30,38 D.E. (desviación estándar) 2,22 semanas, y el peso medio de 1.178,38 D.E. 204,3 gr. La incidencia global de ROP en nuestro estudio es del 33,18%. En la tabla I aparecen los datos de las variables analizadas, fundamentalmente peso al nacimiento, y edad de gestación, relacionándolas con la presencia de ROP y la necesidad de tratamiento.
En las figuras 1 y 2 se muestran en un diagrama de barras la incidencia de ROP de acuerdo con los rangos establecidos, tanto en el peso al nacimiento como en la edad de gestación.
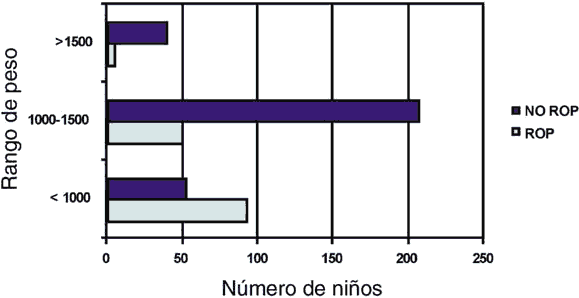
Fig. 1. N.º de niños con ROP para cada peso al nacimiento.
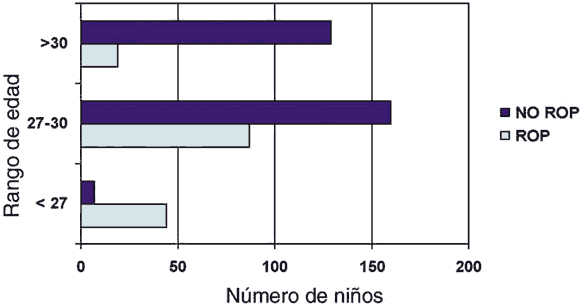
Fig. 2. N.º de niños con ROP para cada rango de edad gestacional.
Se aplicó crioterapia a 6 niños durante el período 1992-95, y 51 niños fueron sometidos a fotocoagulación con láser entre 1995 y 2003. De todos los niños que fueron tratados sólo en 5 (8,8%) se requirió tratamiento secundario dado que el proceso siguió progresando. En un caso (tratado con FC) se refotocoaguló; otro caso con estadio IV B (tratado con CT) que se realizó cerclaje en ambos ojos; un niño con estadio V (tratado con CT) que se hizo vitrectomía; y 2 niños (tratados con FC) con estadio IV B en el que en uno se hizo cerclaje + vitrectomía en ambos ojos, y en el otro niño se hizo cerclaje en ojo izquierdo y en el derecho cerclaje + vitrectomía.
El tiempo medio para la realización de tratamiento fue de 62,9 D.E. 27,53 días desde el momento de nacimiento.
En 298 niños que no presentaron ROP, se pudo efectuar el seguimiento hasta el desarrollo definitivo de vascularización periférica, que se presentó a una edad media de 37,5 D.E. 2,27 semanas.
DISCUSIÓN
El objetivo de los programas de despistaje de la ROP es detectar todos los casos umbral evitando exploraciones innecesarias y así optimizar los recursos. Nosotros seguimos las indicaciones de la Academia Americana de Pediatria y Academia Americana de Oftalmología (6) que recomiendan explorar a los pretérminos cuyo peso al nacimiento es igual o menor de 1.500 gr, realizándose la primera valoración, a las 4 semanas del nacimiento.
La incidencia global de ROP en nuestro estudio es del 33,18%. Ligeramente superior a lo publicado años atrás en nuestro hospital, 26,2% (7). Esta incidencia está entre los 22,8% de Grunauer et al (4), o los 27,3% del impresionante estudio realizado por Chiang et al de la incidencia de todo el estado de Nueva York publicado en julio de 2004 (8), y las más altas, como las que se describen en otros hospitales españoles que sitúan la incidencia en el 35%, o incluso del 65% como aparece en un estudio publicado hace 15 años por Palmer et al (9).
En este trabajo, aunque 1 de cada 3 tenían ROP, sólo la mitad de ellos alcanzan el estadio III, y de éstos el 70% precisaron tratamiento. Es decir que el programa de despistaje, en un proceso en el que la mayoría de los casos evoluciona favorablemente, está bien ajustado y desde el punto de vista de gestión de recursos, es rentable, aunque, como todo, mejorable.
El peso al nacimiento, es uno de los factores de riesgo que aparecen en todas las series. Los niños con peso inferior a 1.000 gr, tuvieron una incidencia superior al 60% y además presentan formas más graves ya que la mitad de los que presentaron ROP tuvieron que ser tratados.
Nuestro protocolo incluye a niños con más de 1.500 gr que han requerido oxigenoterapia a altas concentraciones y mantenidas en el tiempo. En realidad, queda a criterio del pediatra la inclusión de estos casos, y aunque un 11,8% presentaron ROP sólo 1 niño requirió tratamiento (láser). Nosotros mantenemos este criterio de selección en la actualidad.
El factor de la edad de gestación, está presente en todas las series, y al igual que el peso tiene una relación inversa con la incidencia de ROP, 1 de cada 3 niños con edad de gestación entre 27 y 30 semanas que presentaron ROP tuvieron que ser tratados, mientras que lo fueron 1 de cada 2 en los menores de 27 semanas. Es decir tienen más retinopatías y más graves.
Ambos factores pueden verse claramente en los diagramas de barras de las figuras 1 y 2 donde se expresa claramente su relación con la ROP.
El peso al nacimiento y la edad de gestación son factores incontrolables puesto que nos viene impuestos, otro factor constante pero en teoría modificable es la oxigenoterapia. La FiO2 máxima y el tiempo de FiO2 >0,60 (7) han demostrado estar directamente relacionados con la ROP, aunque una vez desarrollada no influye en la progresión de la retinopatía (10). Dado que los pediatras conocen perfectamente la problemática ROP, mantienen los parámetros respiratorios al límite imprescindible para la seguridad del niño en todos sus aspectos, por tanto es un factor que tenemos que asumir.
En nuestro estudio 3 de cada 4 niños que llegaron a estadio III requirieron tratamiento y hay que destacar que el 91,2% de éstos no requirieron ningún tratamiento añadido. Esta eficacia, es superior a la descrita en el CRYO-ROP Study (3) y fue obtenida utilizando fotocoagulación en casi todos los niños con el consiguiente ahorro económico y la reducción de riesgos.
Los primeros trabajos sobre tratamiento se basaron en la ablación retiniana con crioterapia (3) (en esta serie los 6 casos tratados en los 3 primeros años). Sin embargo la aplicación de esta técnica tiene varios inconvenientes: precisa de anestesia general, gran reacción inflamatoria local, y la actuación sobre la esclera puede favorecer la miopía del prematuro (10). Por otro lado, el tratamiento láser tiene unas características que lo hacen preferible: es más controlable, se hace bajo sedación en la unidad de neonatos por lo que se reducen las complicaciones, no requiere disecar la conjuntiva ni lesionar la esclera, y es menos agresiva localmente. Por tanto la crioterapia ha quedado obsoleta y ahora el tratamiento de elección es la fotocoagulación con láser, preferiblemente de diodo. El láser, además es mas eficaz, muchos estudios (11-16) han demostrado su superioridad sobre la crioterapia en el tratamiento de la ROP grave. Trabajos aleatorizados (11-12) demuestran que los pacientes tratados con láser presentan una mejor evolución tanto anatómica como funcional, incluyendo la menor frecuencia de complicaciones como miopía o estrabismos. Las posibilidades de cada hospital según los medios económicos disponibles provoca que en algunos casos todavía se siga haciendo crioterapia, especialmente en países con pocos recursos, aunque residualmente puede encontrarse algún centro aislado en Europa, incluida España.
Las indicaciones de tratamiento en nuestra serie son las que marcó el CRYO-ROP Study (3), en definitiva, ROP estadio III plus en zona I-II de 5 sectores horarios continuos u 8 en total. Recientemente se han ampliado éstas tras la publicación del estudio ETROP (Early Treatment on Retinopathy of Prematurity) en diciembre de 2003 (5). La indicación de tratamiento sería ahora ZI plus Ex, ZI no plus E III, ZII plus EII o III. En este trabajo también describe las situaciones de riesgo de evolución que denomina Tipo 2, y que aparecen en la tabla II. Las recomendaciones que aparecen en este estudio son las que seguimos actualmente.
Otro aspecto, que no suele ser muy comentado en los estudios, es el tiempo en el que se realiza el tratamiento. Hemos determinado que desde la fecha de nacimiento es de 62,9 D.E. 27,53 días. Teniendo en cuenta que el screening comienza a las 4 semanas y que se realiza el tratamiento a los dos meses aproximadamente del nacimiento, hay tiempo suficiente para adecuar el tratamiento.
Por último, en aquellos prematuros vistos en nuestro protocolo, y que no presentaron ningún grado de ROP, la vascularización periférica completa se alcanzó a las 37,5 D.E. 2,27 semanas de gestación.
Como conclusión, a pesar del aumento de los prematuros que haría pensar en un incremento de la frecuencia de ROP, la mejoría en los cuidados neonatales, los programas de screening mundialmente aceptados, los nuevos cambios de criterios, el adecuado tratamiento con láser , en definitiva la mejoría en el manejo, da lugar a una mejoría anatómica y funcional de esos niños.
BIBLIOGRAFÍA
1. Martin Begue N, Perapoch Lopez J. Retinopatía del prematuro: incidencia, gravedad y evolución. An Pediatr 2003; 58: 156-161. [ Links ]
2. Tasman W, McNamara JA. Retinopathy of Prematurity. Retinopaty of Prematurity. In: Tasman W, Jaeger EA. Duane´s Clinical Ophthalmology on CD-ROM. Philadelphia: Lippincott Williams and Wilkins. 2002. Vol 3. Chapter 20. [ Links ]
3. Cryotheraphy for Retinopathy of Prematurity Cooperative Group. Multicenter Trial of Cryotheraphy for Retinopathy of Prematurity: ophthalmological outcomes at 10 years. Arch Ophthalmol 2001; 119: 1110-1118. [ Links ]
4. Grunauer N, Iriondo Sanz M, Serra Castanera A, Krauel Vidal J, Jimenez Gonzalez R. Retinopatía del prematuro. Casuística de los años 1995-2001. An Pediatr 2003; 58: 471-477. [ Links ]
5. Early Treatment For Retinopathy Of Prematurity Cooperative Group. Revised indications for the treatment of retinopathy of prematurity: results of the early treatment for retinopathy of prematurity randomized trial. Arch Ophthalmol 2003; 121: 1684-1694. [ Links ]
6. Screening examination of premature infants for retinopathy of prematurity. A joint statement of American Academy of Pediatrics, the American Association for Ophthalmology and Strabismus, and the American Academy of Ophthalmology. Ophthalmology 1997; 104: 888-889. [ Links ]
7. Olea Vallejo JL, Corretger Ruhi FJ, Salvat Serra M, Frau Rotger E, Galiana Ferre C, Fiol Jaume M. Factores de riesgo en la retinopatía de la prematuriedad. An Esp Pediatr 1997; 47: 172-176. [ Links ]
8. Chiang MF, Arons RR, Flynn JT, Starren JB. Incidence of retinopathy of prematurity from 1996 to 2000: analysis of comprehensive New York state patient database. Ophthalmology 2004; 111: 1317-1325. [ Links ]
9. Palmer EA, Flynn JT, Hardy RJ, Phelps DL, Phillips CL, Schaffer DB, et al. Incidence and early course of retinopathy of prematurity. The Cryotherapy for Retinopathy of Prematurity Cooperative Group. Ophthalmology 1991; 98: 1628-1640. [ Links ]
10. Huntcheson KA. Retinopathy of prematurity. Curr Opin Ophthalmol 2003; 14: 286-290. [ Links ]
11. Connolly BP, McNamara JA, Sharma S, Regillo CD, Tasman W. A comparison of laser photocoagulation with trans-scleral cryoterapy in the treatment of threshold retinopathy of prematurity. Ophthalmology 1998; 105: 1628-1631. [ Links ]
12. Ng EY, Connolly BP, McNamara JA, Regillo CD, Vander FJ, Tasman W. A comparison of laser photocoagulation with cryoterapy for threshold retinopathy of prematurity at 10 years: part 1. Visual function and structural outcome. Ophthalmology 2002; 109: 928-935. [ Links ]
13. Banach MJ, Berinstein DM. Laser terapy for retinopathy of prematurity. Curr Opin Ophthalmol 2001; 12: 164-170. [ Links ]
14. Axer-Siegel R, Snir M, Cotlear D, Maayan A, Frilling R, Rosenbaltt I, et al. Diode laser treatment of posterior retinopathy of prematurity. Br J Ophthalmol 2000; 84: 1383-1386. [ Links ]
15. Pearce IA, Pennie FC, Gannon LM, Weindling AM, Clarck DI. Three year visual outcome for treated stage 3 retinopathy of prematurity: cryoterapy versus laser. Br J Ophthalmol 1998; 82: 1254-1259. [ Links ]
16. O´Keefe M, Burke J, Algawi K, Goggin M. Diode laser photocoagulation to the vascular retina for progressively advancing retinopathy of prematurity. Br J Ophthalmol 1995; 79: 1012-1014. [ Links ]















