Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.82 no.9 sep. 2007
Ptosis inducida por toxina botulínica como tratamiento de los defectos corneales persistentes
Peristent corneal defects treated with botulinum toxin-induced ptosis
Vleming E.N.1, Pérez-Rico C.2, Montes M.A.1, Pareja J.1
Servicio de Oftalmología del Hospital Universitario Príncipe de Asturias. Alcalá de Henares (Madrid).
1 Licenciado en Medicina.
2 Doctor en Medicina.
Dirección para correspondencia
RESUMEN
Objetivos: Evaluar el uso de la ptosis inducida mediante toxina botulínica (BTX) en el tratamiento de patología corneal.
Métodos: Se emplearon dos inyecciones de BTX sobre el párpado superior de diez ojos (nueve pacientes). Se estudió el grado de ptosis, su duración y la evolución de la lesión corneal.
Resultados: Conseguimos la ptosis completa en siete ojos y la resolución de la patología corneal también en siete ojos. No hubo complicaciones importantes con el tratamiento.
Conclusiones: Esta es una técnica sencilla y segura con la que tratar pacientes con patología corneal refractaria. Ofrece importantes ventajas sobre la tarsorrafia quirúrgica. Es además especialmente útil en pacientes que por diversas razones no puedan someterse a cirugía.
Palabras clave: Tarsorrafia, toxina botulínica, ptosis, defecto corneal persistente, lentes de contacto, suero autólogo.
ABSTRACT
Objectives: To evaluate the use of botulinum toxin (BTX) induced ptosis in the treatment of corneal pathology.
Methods: We employed two BTX injections into the superior lid of 10 eyes (9 patients). We evaluated the degree of ptosis, its duration and the effect on the corneal lesion.
Results: Complete ptosis resulted in seven eyes and the corneal pathology resolved in all of them. There were no relevant complications.
Conclusions: BTX treatment is a simple and safe technique for treating refractory corneal pathology. It has significant advantages over surgical tarsorrhaphy and is especially useful where the pathology does not require surgery (Arch Soc Esp Oftalmol 2007; 82: 547-550).
Key words: Tarsorrhaphy, botulinum toxin, ptosis, persistent corneal defect, contact lens, autologous serum.
Introducción
La toxina botulínica tipo A (BTX) es una de las diferentes toxinas producidas por el clostridium botulinum. La toxina comercializada está purificada y compuesta por dos cadenas polipeptídicas vinculadas por un puente disulfuro: cadena H (85-105 kDa) y cadena L (50-59kDa) esta última asociada a un átomo de Zn. Actúa inhibiendo la liberación de acetilcolina en la porción presináptica de la placa motora, produciendo una denervación funcional y reversible del músculo afecto (1).
Alan B. Scott fue pionero en el uso de la BTX A como una alternativa a la cirugía del estrabismo (2). Desde entonces su uso se ha extendido para el tratamiento de enfermedades neuromusculares como el blefarospasmo, espasmo hemifacial, distonía cervical, acalasia, etc. (3) y también para diferentes problemas oftalmológicos especialmente en el campo de la oculoplástica (4).
Los defectos corneales persistentes son fuente de gran morbilidad ocular. El retraso en la cicatrización, la tendencia a la infección y el adelgazamiento corneal, conllevan un riesgo importante de perforación y pérdida visual permanente. Las técnicas usadas para favorecer la reepitelización corneal, ante el fracaso del máximo tratamiento médico, incluyen el uso de lentes de contacto y la tarsorrafia quirúrgica (5,6). Las lentes de contacto terapéuticas entrañan un riesgo elevado de infección. La tarsorrafia quirúrgica dificulta el seguimiento de la lesión así como altera los márgenes palpebrales cuándo es revertida.
En el presente trabajo nos proponemos valorar la eficacia de la ptosis palpebral inducida mediante BTX tipo A como tratamiento coadyuvante de defectos corneales persistentes, en pacientes con mal estado general que no son candidatos a cirugía.
Sujetos, material y método
Se presenta un estudio descriptivo de una serie de casos clínicos de pacientes con defectos corneales persistentes. En todos los casos indicamos tarsorrafia quirúrgica, pero dado el estado general de los pacientes planteamos la opción de la tarsorrafia química.
Sujetos
Se ha incluido en el presente estudio nueve pacientes, un total de 10 ojos, que presentaban defectos corneales persistentes y refractarios a máximo tratamiento médico durante un periodo de al menos tres semanas. Este tratamiento médico incluía lubricación corneal y suero autólogo. En cuatro de los pacientes se había realizado trasplante de membrana amniótica que también había fracasado. Se planteo tarsorrafia química con BTX tipo A. Se entregó y explicó el consentimiento informado.
Los criterios de exclusión fueron:
Trastornos de la unión neuromuscular: miastenia gravis, esclerosis lateral amiotrófica, miopatías.
Interacciones medicamentosas que potencien el efecto de la BTX A: Antibióticos aminoglucósidos, espectomicina y relajantes musculares del tipo de la tubocuranina.
Los pacientes fueron revisados en el servicio de oftalmología de nuestro centro en el periodo comprendido entre febrero de 2004 y septiembre de 2005.
Material y métodos
Se utiliza BTX tipo A (BOTOX®; Allergan, Inc). Cada vial contiene 100 UI de BTX tipo A. Fueron reconstituidas en 2 ml de suero salino fisiológico, de modo que 0,1 ml de solución reconstituida contenía 5 UI de BOTOX.
Se inyectaron vía subcutánea 1,5 ml de solución (7,5 UI BOTOX) en la zona medial y en la zona lateral del borde superior de la placa tarsal superior. Se utilizó jeringa de insulina y aguja de 30G (fig. 1).

Fig. 1: Puntos de inyección de la BTX.
Clasificamos el grado de ptosis en completa cuando se obtiene un cierre palpebral total; parcial eficaz, cuando no obtenemos un cierre palpebral completo pero el defecto corneal es cubierto en su totalidad y parcial ineficaz cuando no obtenemos una completa oclusión del defecto corneal.
Los pacientes fueron revisados al día siguiente y posteriormente todos los días hasta conseguir una ptosis eficaz y después revisiones semanales. En cada visita se evaluó el grado de ptosis y la evolución de la lesión corneal, realizándose controles fotográficos previa instilación de fluoresceína (fig. 2). Se mantuvo en todos los casos el tratamiento lubricante. En los pacientes en los que la duración de la ptosis fue insuficiente se repitieron las inyecciones.
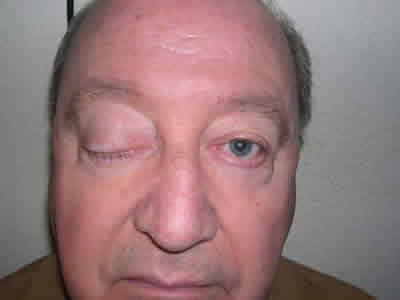
Fig. 2: Ptosis completa a los 5 días de la inyección.
Resultados
En nuestro estudio se incluyeron nueve pacientes, un total de 10 ojos, que presentaban defectos corneales refractarios al tratamiento médico. La duración del defecto fue de al menos 3 semanas en todos los casos.
Cinco de los pacientes presentaban úlcera neurotrófica, dos pacientes defectos corneales secundarios a infección microbiana, un paciente (dos ojos) queratopatía por exposición y un paciente insuficiencia límbica por uso de mitomicina C en trabeculectomía (tabla I).
Todos los pacientes habían sido tratados previamente con ungüentos lubricantes. Seis de los pacientes habían recibido además suero autólogo, y cuatro fueron tratados con trasplante de membrana amniótica (tabla I).
En todos los casos la aparición de la ptosis tuvo lugar entre el segundo y el sexto día tras la inyección de BTX (tabla II). La duración media de la ptosis fue de 40,6 días con una desviación estándar de 27,5 días (rango 29-56). El paciente que sufría de insuficiencia límbica requirió retratamiento al mes, utilizándose la misma dosis. Los pacientes siguieron utilizando el tratamiento médico durante este tiempo.
La resolución de la lesión corneal se consiguió en siete ojos en un tiempo medio de 42,71 días (rango 5-61). Un paciente, con enfermedad bilateral, falleció antes de la última revisión. En el paciente con insuficiencia límbica secundaria al uso de mitomicina C el tratamiento resultó ineficaz, persistiendo el defecto corneal a pesar del retratamiento y de la máxima lubricación (tabla II).
Ningún paciente sufrió complicaciones.
Discusión
Todos los pacientes incluidos en nuestro estudio presentaban defectos corneales refractarios al máximo tratamiento médico y mal estado general y/o bajo nivel de colaboración. Entre las medidas terapéuticas utilizadas se incluyeron lubricación, suero autólogo y trasplante de membrana amniótica. El uso de BTX en estos pacientes para inducir una ptosis protectora fue eficaz en siete de los 10 ojos.
En nuestro estudio la BTX ayudó a la resolución de la lesión corneal en los pacientes con ulceraciones neurotróficas y secundarias a infección bacteriana. Los resultados no fueron concluyentes en el paciente con queratopatía por exposición por su fallecimiento. En el paciente que presentaba insuficiencia límbica el tratamiento no resultó efectivo a pesar del retratamiento.
La BTX A actúa disminuyendo el roce del párpado superior, especialmente de su borde libre, sobre el defecto corneal, favoreciendo su cicatrización (7). Probablemente éste no sea el único mecanismo de acción. Se han postulado varias teorías, por una parte la disminución de la evaporación de la lágrima mejoraría la lubricación de la superficie ocular, por otra la liberación de factores de crecimiento y citoquinas a partir de la conjuntiva tarsal ayudaría a la cicatrización epitelial dado que la ptosis está muy próxima al defecto corneal (8).
Otras medidas que logran disminuir este roce presentan desventajas. El uso de lentes de contacto terapéuticas se ha relacionado con un elevado riesgo de infección microbiana (5). En cuanto a la tarsorrafia quirúrgica produce alteraciones anatómicas del borde palpebral cuando es revertida, como entropión cicatricial y distriquiasis, así como dificulta el seguimiento de la lesión (6). En la tarsorrafia química podemos inspeccionar perfectamente la córnea en la lámpara de hendidura mediante elevación manual del párpado superior, lo cual es una clara ventaja.
Kirkeness et al (7) consideraron la posibilidad de que la ptosis inducida mediante BTX A favoreciese la infección ocular al producir estancamiento de la lágrima. Es difícil valorar este riesgo con los casos que existen en la literatura, que por otra parte, también puede darse con el uso de lente de contacto terapéuticas y en la tarsorrafia quirúrgica.
En otras series publicadas en la literatura se ha usado la BTX inyectada directamente en el vientre del músculo elevador del párpado superior (7-9) para inducir ptosis protectora. Kirkness et al. (7,9) en una serie de 25 pacientes, comunicaron diplopía en un 12% y resolución del defecto corneal en un 90%. Ellis y Daniell (8), por otro lado, estudiaron a 21 pacientes, en un 24% tuvieron diplopía y el defecto corneal se solucionó en un 66%. Nuestros resultados son comparables a los de estas series. En cualquier caso nuestra técnica difiere de la utilizada por estos autores, no atravesando el septum orbitario, lo que explicaría que no tengamos ningún caso de diplopía.
Debido a que la etiología de los defectos corneales persistentes es muy variada, es difícil realizar estudios comparativos entre las diferentes opciones terapéuticas, pero en cualquier caso los resultados han sido muy buenos.
Consideramos que nuestra técnica es eficaz como terapia coadyuvante en el tratamiento de los defectos corneales persistentes, permitiendo en todo momento seguir la evolución de la lesión. Debido a su sencillez es especialmente útil en pacientes con mal estado general o escasa colaboración.
Bibliografía
1. López del Val LJ, Castro García A. Toxina botulínica: Aplicaciones terapéuticas. Barcelona: Masson SA; 2002. [ Links ]
2. Scott AB. Botulinum toxin injection into extraocular muscles as an alternative to strabismus surgery. Ophthalmology 1980; 87: 1044-1049. [ Links ]
3. Jankovic J, Brin MF. Therapeutic uses of botulinum toxin. N Eng J Med 1991; 324: 1186-1194. [ Links ]
4. Osako M, Keltner JL. Botulinum A toxin (Oculinum) in ophthalmology. Surv Ophthalmol 1991; 36: 28-46. [ Links ]
5. Poggio EC, Glynn RJ, Schein OD, Seddon JM, Shannon MJ, Scardino VA, et al. The incidence of ulcerative keratitis among users of daily-wear and extended-wear soft contact lenses. N Engl J Med 1989; 321: 779-783. [ Links ]
6. Cosar CB, Cohen EJ, Rapuano CJ, Maus M, Penne RP, Flanagan JC, et al. Tarsorrhaphy: clinical experience from a cornea practice. Cornea 2001; 20: 787-791. [ Links ]
7. Kirkness CM, Adams GG, Dilly PN, Lee JP. Botulinum toxin A-induced protective ptosis in corneal disease. Ophtalmology 1988; 95: 473-480. [ Links ]
8. Ellis MF, Daniell M. An evaluation of the safety and efficacy of botulinum toxin type A (BOTOX) when used to produce a protective ptosis. Clin Exp Ophthalmol 2001; 29: 394-399. [ Links ]
9. Adams GG, Kirkness CM, Lee JP. Botulinum toxin A induced protective ptosis. Eye 1987; 1: 603-608. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Eduardo Vleming Pinilla
C/. Arturo Soria, 337, 3B
28033 Madrid
España
E-mail: e_vleming@yahoo.es
Recibido: 6/9/06.
Aceptado: 17/7/07.
















