Introducción
La mamoplastia de aumento es una de las técnicas quirúrgicas más frecuentemente llevada a cabo en la Cirugía Estética. Su número va en aumento, y por lo tanto, el número total de pacientes portadoras de prótesis de mama también. Por otra parte, sabemos que 1 de cada 8 mujeres padecerá un cáncer de mama a lo largo de su vida. Teniendo en consideración estos dos hechos, observamos que existe una población de mujeres que se encontrarán en unas circunstancias diferenciadas respecto al resto en el manejo del cáncer de mama y su reconstrucción, especialmente en la reconstrucción mamaria inmediata (RMI).(1,2)
Con frecuencia se trata de pacientes más jóvenes, con índice de masa corporal menor, mayor porcentaje de fumadoras, mayor aceptación de utilización de prótesis, y escaso volumen mamario. También es habitual que tengan unas mayores expectativas respecto al resultado de la reconstrucción mamaria.(3) En estas pacientes, debido a su menor volumen mamario, las mastectomías parciales provocan una mayor distorsión; y si asociamos radioterapia (RT) a una tumorectomía o cuadrantectomía, conservando el implante mamario, sabemos que la posibilidad de desarrollar una contractura capsular es elevada.
Además, las pacientes deben saber que el tratamiento conservador, manteniendo el implante, con frecuencia consigue un resultado que dista bastante del que se espera de una cirugía estética. Por lo tanto, la mastectomía conservadora de piel (MCP) con extracción del implante, seguida de RMI, se ha convertido en una de las opciones más atractivas para la mayor parte de las pacientes que presentan cáncer de mama y aumento previo,(3) cuando por el estadio del tumor deben optar entre tumorectomía asociada a RT o mastectomía.
Algunos autores aconsejan la reconstrucción en dos tiempos quirúrgicos con la utilización inicial de expansores.(4) Actualmente hay una amplia aceptación del uso de matrices dérmicas acelulares (MDA) para reforzar el polo inferior mamario y llevar a cabo la reconstrucción en un solo tiempo.(5,6) Otros autores han presentado trabajos basados en la utilización de capsulotomías, capsuloplastias o injertos de cápsula para solucionar los problemas de cobertura de la prótesis y posibilitar la RMI evitando el uso de MDA o de expansores.(7 8 9-10)
El presente trabajo revisa la experiencia de los autores en RMI para las pacientes previamente sometidas a aumento mamario con implantes después de una MCP, con o sin conservación del complejo areola-pezón, utilizando implantes anatómicos definitivos en combinación con una técnica que utiliza un colgajo capsular retropectoral periprotésico que permite el soporte y la cobertura total de la prótesis.
Material y método
Entre diciembre de 2014 y febrero de 2016, hemos seleccionado a todas las pacientes con cáncer de mama que previamente eran portadoras de prótesis mamarias por aumento y que, valoradas por el Comité de Patología Mamaria de nuestro hospital, fueron candidatas a MCP pudiendo conservar la cápsula periprotésica. Todas ellas dieron su consentimiento para la participación en el estudio y la publicación de sus fotografías.
Excluimos las pacientes con implantes de menos de 1 año, los implantes colocados en plano subglandular, los casos de contractura capsular grados III y IV, las roturas protésicas, las pacientes fumadoras y aquellas subsidiarias de RT.
El periodo mínimo de seguimiento postoperatorio establecido para inclusión en el estudio fue de 1 año.
Valoramos el resultado estético y las complicaciones, principalmente: contractura, seroma, hematoma e infección.
Técnica quirúrgica
La técnica quirúrgica fue aprobada por el Comité de Patología Mamaria de nuestro centro hospitalario.
Todas las pacientes recibieron profilaxis antibiótica.
La mastectomía debe preservar el tejido periprotésico intacto (Fig. 1). Realizamos la disección submuscular entre el músculo pectoral mayor y la cápsula periprotésica en su superficie anterior, con especial cuidado para mantener íntegra la cápsula (Fig. 2A).

Figura 1. A. Dibujo preoperatorio: cápsula periprotésica en rojo. Línea de puntos rojos mostrando el área retropectoral de la cápsula. B. Imagen postmastectomía. C. Despegamiento del músculo pectoral mayor de la cápsula periprotésica. Flecha señalando el nivel de realización de la capsulotomía, por donde será extraída la prótesis. D. Prótesis extraída por capsulotomía en pliegue superior. E. Cápsula periprotésica retropectoral desplegada caudalmente hasta el borde del músculo pectoral mayor. F. Colocación del nuevo implante bajo el músculo pectoral mayor y la cápsula periprotésica
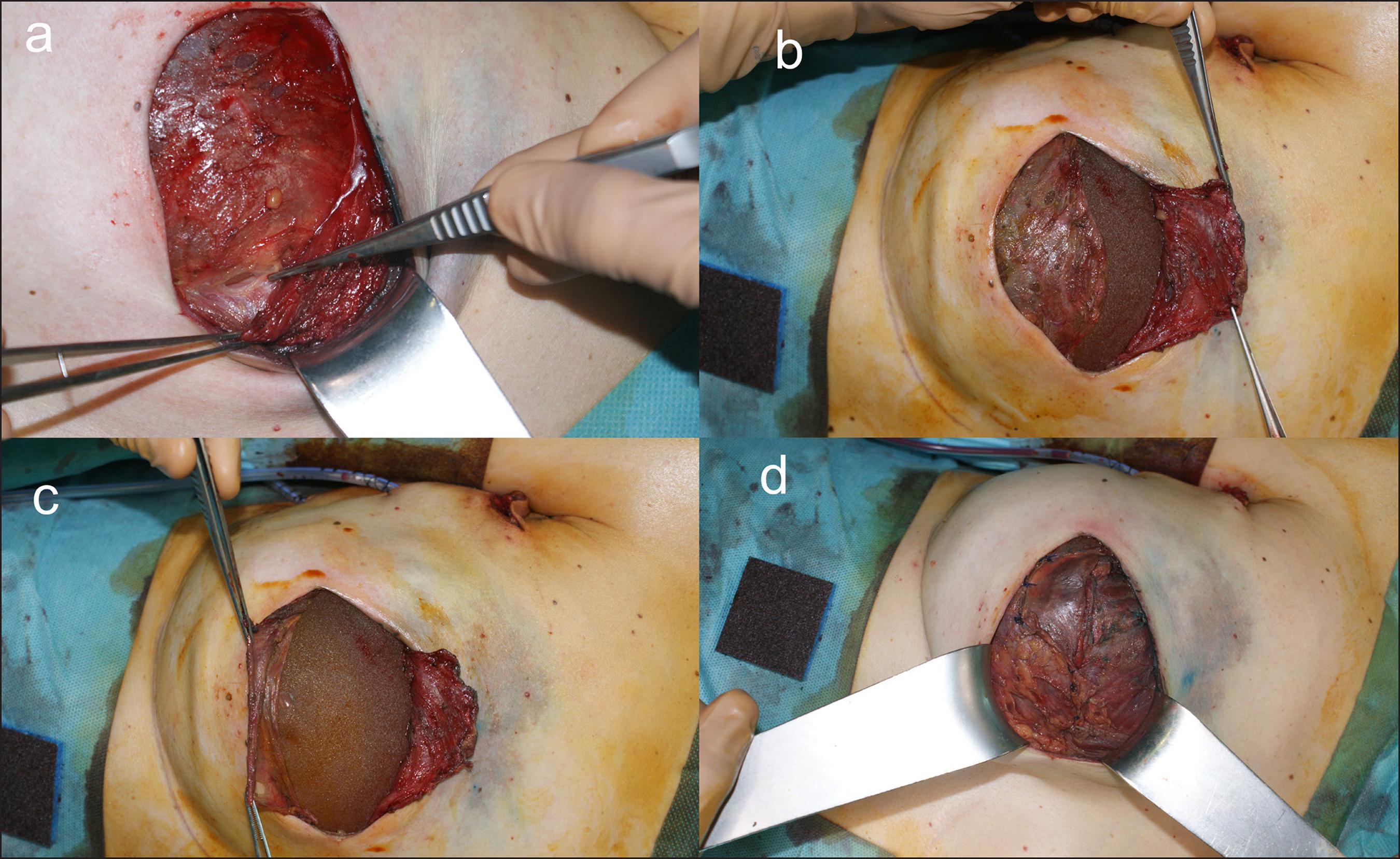
Figura 2. Imágenes intraoperatorias: surco inframamario a la izquierda de la imagen, músculo pectoral mayor disecado y elevado de la cápsula periprotésica a la derecha. A.Cápsula cubriendo la prótesis. Pinza de disección señalando el inicio de la capsulotomía en el borde cefálico.B. Músculo pectoral mayor elevado. Cápsula periprotésica desplegada inferiormente después de haber realizado la capsulotomía en la mitad cefálica de la cápsula.C.Cápsula y músculo pectoral mayor evertidos para mostrar la nueva prótesis.D.Sutura de la cápsula al músculo pectoral mayor para permitir la cobertura total de la prótesis.
Una vez levantado el músculo pectoral mayor, realizamos una capsulotomía hemicircunferencial superior en el borde de repleción cefálico de la cápsula, para a continuación abatirla inferiormente (Fig. 2B). Calculamos el volumen aproximado del nuevo implante sumando el volumen de la prótesis previa al volumen de tejido mamario resecado, y haciendo comprobación intraoperatoria mediante el medidor del volumen final que mejor se adapte a la reconstrucción.
A continuación, introducimos el nuevo implante y lo cubrimos en su polo inferior con la cápsula previamente abatida y en su polo superior por el músculo pectoral mayor (Fig. 2C). Suturamos la cápsula al borde inferior del músculo pectoral mayor, cubriendo por completo el nuevo implante (Fig. 2D). Cerramos por planos dejando 2 drenajes aspirativos a vacío, uno en el plano subcapsular y otro en el subcutáneo, que mantenemos hasta que el débito es inferior a 30 cc tras 2 días consecutivos.
Resultados
Llevamos a cabo reconstrucción mamaria mediante la técnica descrita en 4 pacientes durante el periodo de estudio. La edad media fue de 44 años (máxima de 61 y mínima de 34). El volumen medio de los implantes utilizados fue de 410 cc (máximo de 520 y mínimo de 375).
Tras un periodo de medio de seguimiento de 17 meses (máximo de 22 y mínimo de 12), ninguna paciente sufrió complicaciones mayores, considerando como tales hematoma, seroma o infección, no se desarrolló contractura capsular en ningún caso y no fue preciso reintervenir a ninguna de las pacientes por complicaciones o para mejorar el resultado estético, considerado por las pacientes como equiparable a la mama contralateral portadora de la prótesis para aumento (Fig. 3).

Figura 3. Paciente de 34 años. Prótesis por aumento mamario 7 años antes. Superior. Preoperatorio. Inferior. Postoperatorio al año tras mastectomía conservadora de piel con reconstrucción inmediata mediante la técnica descrita y colocación de implante mamario anatómico de alto perfil de 370 cc.
En una de las pacientes apreciamos pliegues (rippling) en el polo superior, área cubierta por el músculo pectoral mayor. Consideramos que esto fue secundario al adelgazamiento del colgajo cutáneo por la mastectomía, pero sin relación con el área reconstruida con el colgajo capsular (Fig. 4).
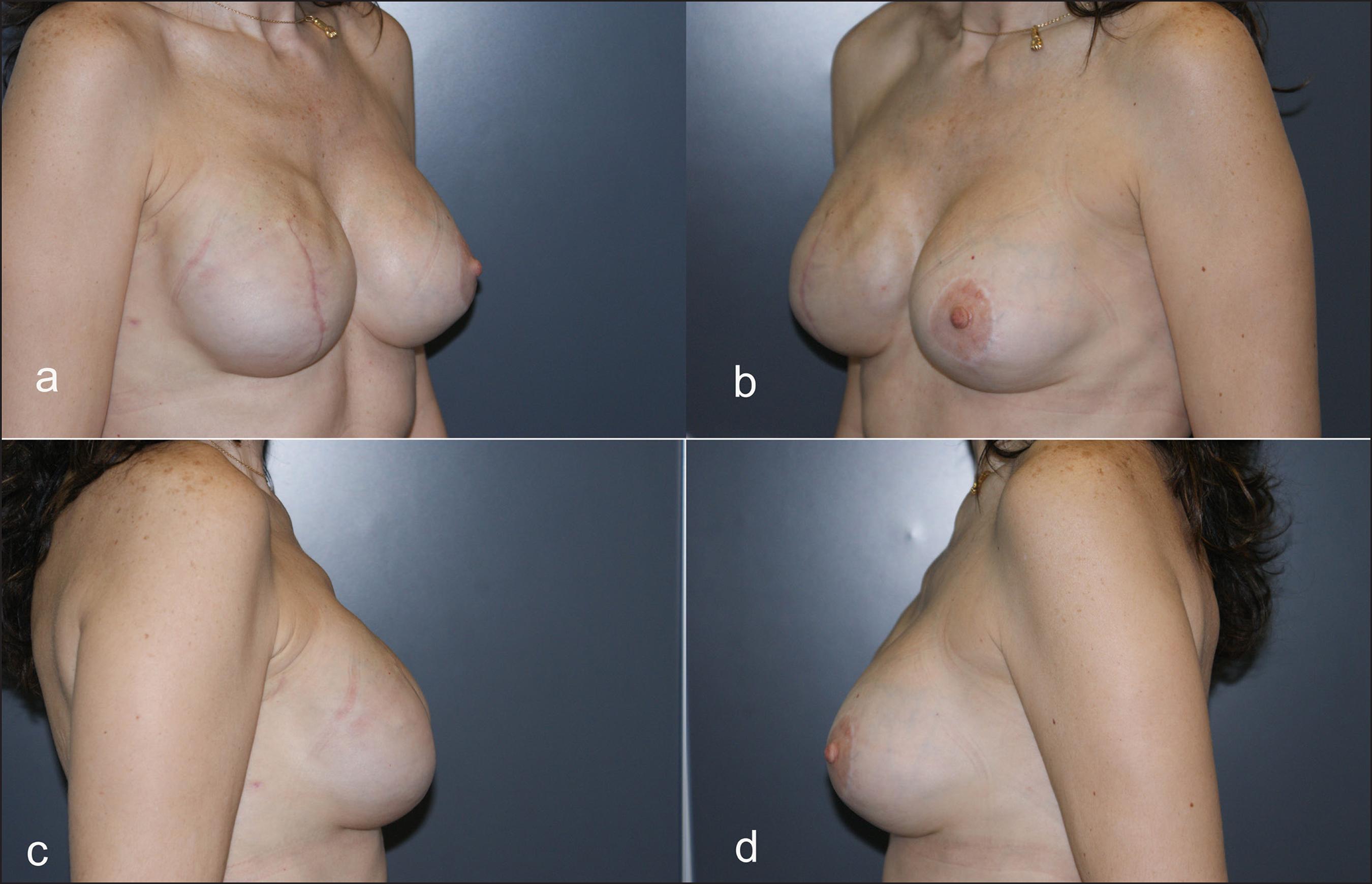
Figura 4. Paciente de 46 años con mastopexia y aumento mamario subpectoral 10 años antes. Superior. Preoperatorio. Inferior. Postoperatorio al año tras mastectomía conservadora de piel con reconstrucción inmediata mediante la técnica descrita y colocación de implante mamario anatómico de alto perfil de 410 cc. Obsérvese el rippling en el polo superior, área cubierta por el músculo pectoral mayor.
Discusión
La cobertura de la porción inferior del implante en reconstrucción de mama es aún un tema controvertido, especialmente cuando se realiza una RMI aloplástica en un solo tiempo quirúrgico tras la mastectomía ahorradora de piel.
Están descritas un gran número de técnicas para solventar este problema.(7 8 9 10 11-12) Recientemente, el uso de MDA ha conseguido aportar mayor soporte al polo inferior mamario, demostrándose la buena adecuación del tejido y poniendo en evidencia la existencia de neovascularización en los exámenes histológicos. Pese a los buenos resultados obtenido con este producto, su elevado coste y la aparición de complicaciones dificultan su uso estandarizado.(7)
Otros autores han recurrido a la utilización del tejido periprotésico, empleando la cápsula como injerto o en forma de colgajos. Sin embargo, ninguno de los trabajos que hemos podido revisar permite la cobertura de la prótesis por dos planos de tejido totalmente independientes.(6,7)
La técnica que presentamos recurre a la utilización de un tejido cada vez más valorado, la cápsula periprotésica, pero de una zona y en una extensión que, en base a la búsqueda bibliográfica realizada (hemos revisado en: Scopus y PubMed empleando las palabras clave: breast augmentation, breast cancer, breast reconstruction, capsule, capsulotomy, implants), no hemos hallado descrita con anterioridad, como es el área retropectoral. Esto nos ha permitido diseñar un amplio colgajo que facilita la total cobertura del polo inferior de la prótesis, permitiendo la RMI en un único tiempo quirúrgico. Técnicamente es simple de realizar, prolonga la intervención solo unos 15 minutos más y obtiene dos planos completamente diferenciados. La prótesis descansa sobre el colgajo capsular, liberando a los colgajos cutáneos de posibles tensiones que pudieran comprometer su viabilidad (Fig. 1 y 2).
La presencia de pliegues en el polo superior de la mama (rippling), presente en una de nuestras pacientes, consideramos que puede mejorar mediante infiltrado graso, de la misma forma que se hace en otras pacientes con reconstrucción protésica. Al estar cubierta la prótesis por el músculo pectoral mayor en su polo superior, presenta un menor riesgo de rotura de la prótesis durante esta maniobra. Sin embargo, en nuestro caso, la paciente presentada rechazó llevar a cabo esta nueva cirugía.(13,14)
Entre las contraindicaciones para utilizar esta técnica incluimos a aquellas pacientes con contractura capsular periprotésica grados III-IV o con implantes rotos, en las que optamos por realizar una capsulectomía completa. Igualmente descartamos su realización en pacientes que se hayan sometido a aumento mamario protésico en el año anterior a la mastectomía por considerar que la cápsula puede carecer de la mínima resistencia necesaria a la tracción.
Analizamos como un punto débil de nuestro trabajo el escaso número de pacientes recogidas. Esto se debe a que los criterios de selección que seguimos son necesariamente restrictivos. Las pacientes con aumento mamario previo mediante prótesis son un pequeño subgrupo dentro de las afectadas por cáncer de mama, grupo que al aplicar los criterios de exclusión indicados se reduce aún más.
Aunque nuestro estudio debe ser valorado como preliminar, los resultados obtenidos en nuestras pacientes creemos que justifican la presentación de nuestra experiencia hasta la fecha al poder aportar nuevas ideas en el tratamiento reconstructivo postmastectomía, con una baja tasa de complicaciones y un resultado estético satisfactorio (Fig. 3 y 4). Teniendo en consideración que en la realización de la técnica presentada recurrimos a la utilización de prótesis mamarias anatómicas, así como de la cápsula periprotésica, nuestra actitud ante el linfoma anaplásico de célula grandes asociado a implantes mamarios (LACG-AIM) es la misma que seguimos para con el resto de nuestras pacientes. Siguiendo las recomendaciones de las agencias sanitarias, en pacientes que presenten seroma tardío o masa asociada a la prótesis, procedemos a la punción guiada por ecografía del seroma y/o al estudio anatomopatológico de las posibles tumoraciones asociadas a la cápsula o de los ganglios. Si cuando llevamos a cabo la técnica de reconstrucción descrita no encontramos ningún hallazgo de sospecha de LACG-AIM, no biopsiamos la cápsula por no considerar que esté justificado.(15 16-17)
Conclusiones
La utilización de la cápsula periprotésica disecada de la superficie posterior del músculo pectoral mayor, permite la realización de un amplio colgajo que dará cobertura y soporte a la prótesis mamaria en su polo inferior, consiguiendo un bolsillo músculo-cápsular totalmente cerrado e independiente del plano subcutáneo.
Se trata de una técnica segura, de fácil realización y los resultados estéticos obrtenidos son comparables a la mama no reconstruida. No obstante, se trata de una aportación de datos preliminares que sin duda requieren un mayor tiempo de seguimiento así como un mayor número de pacientes para obtener mayor validez.















