Introducción
Las células madre mesenquimales son candidatas terapéuticas para una amplia gama de enfermedades humanas. Estas células pueden migrar a zonas de injuria tisular para facilitar la reparación del tejido. Una vez en el lugar, pueden diferenciarse en distintos componentes del tejido lesionado. Sin embargo, su efecto clave es probablemente su capacidad para ejercer efectos inmunomoduladores y para secretar factores que promueven la reparación de tejidos.(1)
El uso de células madre se ha investigado como tratamiento complementario para una gran variedad de enfermedades tales como: accidente cerebrovascular isquémico, esclerosis múltiple, isquemia miocárdica, enfermedad pulmonar obstructiva crónica, fibrosis pulmonar idiopática, insuficiencia hepática crónica, insuficiencia renal aguda, enfermedad inflamatoria intestinal y osteoartritis.(1) En Cirugía Plástica también han generado gran interés, especialmente para el tratamiento de heridas crónicas,transferencia de tejido adiposo para procedimientos estéticos y reconstructivos con mejora en la retención de injerto graso y por ende disminución de su reabsorción(2) y para el aumento en la vitalidad de los colgajos.(3)
Existen distintas fuentes disponibles para la obtención de células madre: células troncales embrionarias (Embryo- nic Stem Cells, ESCs) y células troncales adultas.(4) A pesar del gran potencial terapéutico encontrado en las ESCs por su capacidad de autorrenovación y pluripotencialidad, presentan limitaciones en la práctica clínica por consideraciones éticas, manipulación genética y regulación celular.(5) En contraste, las células madre adultas, por naturaleza, son inmunocompatibles y no presentan limitaciones éticas para su uso.(5) Estas últimas inicialmente se aislaron en médula ósea (Bone Marrow Mesenchymal Stem Cells, BM-MSCs),(6) luego en el cordón umbilical y últimamente en el tejido adiposo (ASCs).(5)
Las ASCs tienen la ventaja de encontrarse en grandes cantidades en el individuo, poseen una extensa capacidad de autorrenovación, se pueden aislar fácilmente y poseen potencial de diferenciación en distintas líneas celulares, tales como: adipocitos, osteoblastos, condrocitos, neuronas o miocitos en respuesta a distintos factores inductores.(7)
Estas células se caracterizan por su morfología que recuerda a los fibroblastos, presentan propiedades adhesivas y de autorrenovación, así como la capacidad de diferenciarsein vitro en tres tejidos mesodérmicos tales como óseo, cartilaginoso y adiposo. Expresan marcadores de superficie CD29, CD44, CD90 y CD105 con ausencia de expresión de marcadores hematopoyéticos y HLA-DR.(7,8) Otro marcador es la vimentina, proteína que se encuentra en los filamentos intermedios de las células mesenquimales.(9,10)
Gimble y col.(11) sugieren que para que las células madre se apliquen en Medicina Regenerativa deben cumplir los siguientes criterios:
Encontrarse en abundantes cantidades (de millones a billones de células).
Obtenerse a través de un procedimiento mínimamen- te invasivo.
Poseer la capacidad de diferenciarse en múltiples li- najes celulares de una manera regulable y reproduci- ble.
Trasplantarse en forma segura y efectiva a un huésped autólogo o alógenico.
Ser manipulables de acuerdo a las guías de buena práctica.
La aplicabilidad de las ASCs resulta atractiva por su fácil obtención a través de lipoaspirado, que va desde 100 ml a más de 3 l. y que rutinariamente es eliminado.(11,12) Para la obtención de tejido adiposo es preferible la región abdominal en comparación a otras áreas, como de la cadera y el muslo, por la mayor cantidad en forma significativa de ASCs. Las células ASCs en distintas áreas corporales no varían su potencial de diferenciación en otras líneas celulares ni en la expresión de marcadores de superficie celular, ni tampoco influye la edad en la frecuencia de aparición de ASCs.(13)
El uso de BM-MSCs para aumentar la supervivencia del colgajo no parece ser mejor respecto al de ASCs, sin embargo corresponde a un procedimiento invasivo y doloroso para la recolección de estas células, encontrarse proporcionalmente en menor cantidad en el individuo en comparación al tejido adiposo, y por su disminución de la capacidad de proliferación y diferenciación en otros linajes celulares con la edad.(7)
El uso de células madre ha resultado promisorio y llama la atención por su efecto potencial global. A diferencia de los métodos farmacológicos que actúan frente a un factor en específico (angiogénesis, vasodilatación, simpaticolíticos, secuestro de radicales libres, inhibición de prostaglandinas, etc.), estas células, en teoría por su capacidad de diferenciación en múltiples linajes celulares, capacidad de anidamiento (homing) o de localizarse en el tejido de interés y permanecer allí, inmunomodulación, promoción de la reparación y regeneración directa de los tejidos dañados, por su habilidad de autorrenovación y diferenciación en múltiples linajes celulares, se convierten en candidatas terapéuticas prometedoras.(1)
A pesar de que rápidamente el tratamiento con células madre se ha desarrollado como un tratamiento regenerativo potencial para varias enfermedades, se han ignorado varios aspectos y problemas tales como: diferenciación celular, sobrevida de las células trasplantadas en un lugar hostil sometidas a isquemia e hipoxia, citotoxicidad, especies reactivas de oxígeno, respuesta inflamatoria, activación de cascada apoptótica, entre otros.(14) Es por ello que se ha podido potenciar el efecto de las células madre a través del precondicionamiento.
Se han empleado varios agentes precondicionantes en las células madre mediante un insulto subletal a través de isquemia, hipoxia, anoxia, ácido sulfhídrico (H2S), peróxido de hidrógeno (H2O2) monóxido de carbono (CO)(14) y fotobiomodulación.(15)
La exposición a hipoxia a un nivel no letal aumenta significativamente la tolerancia celular y presenta una mejora en las propiedades regenerativas de las células madre. A través de características de mejora en la sobrevida, en los efectos paracrinos con obtención de un mejor soporte trófico, expresión de factores tróficos estimulantes de la angiogénesis, activación de mediadores antioxidantes, mejor tolerancia en el sitio de lesión tras su administración, aumento de la proliferación y capacidad de migración a regiones isquémicas o alrededor de un tejido infartado.(14)
La exposición a hipoxia se puede realizar a concentraciones del 1 al 5% de O2. La exposición a concentraciones del 1% es óptima para la promoción de las propiedades proangiogénicas a través de un aumento de la expresión del VEGF, mientras que la exposición al 5% de O2 presenta mayor proliferación celular.(16,17)
El propósito de este estudio es describir el método de aislamiento y cultivo de células madre derivadas de tejido adiposo (ASCs), caracterización morfológica y mediante inmunofluorescencia y cómo estas pueden precondicionarse con hipoxia y generar cambiosin vitro en su capacidad proliferativa y migratoria. Esta metodología ya fue utilizada por nosotros en un estudio publicado en esta misma revista en el que comparamos distintos métodos para disminuir la necrosis del colgajo cutáneo aleatorio, utilizando células madre derivadas de tejido adiposo con y sin precondicionamiento con hipoxia, retardo de colgajo y grupo control. Además proponemos una clasificación de necrosis del colgajo según hallazgos macroscópicos e histopatológicos.(17)
Material y método
Obtención de ASCs
Obtenemos el tejido adiposo en ratas Sprague-Dawley de sexo masculino, de peso entre 300-500 gr, intervenidas bajo las normas bioéticas del ICBM (Instituto de Ciencias Biomédicas de Santiago, Chile) para la experimentación con animales de laboratorio: 10 ratas para células madre derivadas de tejido adiposo adultas (ASCs) y 10 ratas para células madre derivadas de tejido adiposo adultas precondicionadas con hipoxia (ASCs-H). Las ratas son anestesiadas con ketamina 80 mg/kg y xilacina 8 mg/kg vía intramuscular. Preoperatoriamente se les administra penicilina benzatina 40.000 U/Kg también intramuscular.
Fraccionamos el tejido adiposo del área abdominal de la rata y lo lavamos con solución buffer-fosfato 1x (DPBS, GIBCO, Cod: 14190144) (Fig. 1), digerido con colagenasa tipo II al 0.15% (Sigma-Aldrich, Cod: C6885) durante 60 min a 37 ºC y neutralizado con medio de cultivo (DMEM, GIBCO, Cod:11995) 10% de suero bovino fetal (FBS, GIBCO, Cod: 10270), 1% de antibióticos y antimicóticos (Antibiotic-Antimycotic 100X, GIBCO, Cod: 15240). Posteriormente se centrifuga durante 10 min a 1200 g. Elpellet obtenido es resuspendido en medio de cultivo y analizado (Fig. 2). Mantenemos las ASCs en condiciones de normoxia (21%O2-5%CO2), mientras que con las ASCs-H, en la mitad del proceso de expansión, realizamos tripsinización (0.25% Trypsin-EDTA (1X), GIBCO,Cod:25200) de las células para luego colocarlas en DMEM preparado y sometido a hipoxia durante 24 horas en cámara de hipoxia (Modular Incubator Chamber). Tras 72 horas en estas condiciones (2% O2-5% CO2) procedemos a la tripsinización nuevamente para realizar el conteo celular con hemocitómetro.

Figura 1. A. Rata en posición supina con rasuración del área ínguino-abdominal. B. Incisión con bisturí y exposición de tejido graso subcutáneo. C. Tejido graso fraccionado en placa de Petri con solución buffer fosfato 1x.

Figura 2. A. Recolección de tejido adiposo fraccionado en solución buffer fosfato 1x y colagenasa tipo II. B. Tejido graso digerido mediante colagenasa tipo II. C. Obtención delpellet tras la centrifugación. C. Resultado final tras la expansión de las ASCs al cabo de 10 días, tripsinización y centrifugación.
Inmunohistoquímica
Colocamos un cubreobjeto estéril sobre cada uno de los cultivos durante el segundo pasaje para la adhesión celular. Después de 3 días, extraemos el cubreobjeto y sumergimos en una placa de Petri durante 6 minutos en metanol a -20 ºC y 1 minuto en acetona a -20 ºC, para luego pasarlo por tampón fosfato durante 5 minutos y cubrirlo con suero de cabra 1/10 en PBS-BSA al 2%, dejándolo en cámara húmeda durante 30 minutos. Utilizamos el anticuerpo primario vimentina (Dako) 1/100 y el anticuerpo CD90 (Thy-1) 1/100 (Chemicon). Lo dejamos 1 noche en refrigeración. Posteriormente empleamos IgG FITC (Vector) 1/200 como anticuerpo secundario. Utilizando la técnica de Propidio (Polysciences) 1/500 es posible destacar la cromatina de los núcleos en color rojo. Montaje en medio acuoso (Dako Faramount, S3025). Visualización en microscopio de fluorescencia UV con filtro mixto.
Estudio de proliferación celular
Durante el segundo pasaje de un cultivo celular en condiciones de normoxia, se tripsiniza y tomamos 2 muestras que colocamos en 2 frascos de cultivo celular en concentraciones equivalentes, uno se mantiene en condiciones de normoxia (21% O2-5% CO2) y el otro en hipoxia (2% O2-5% CO2) (Modular Incubator Chamber). Mantenemos durante 24 horas en estas condiciones y nuevamente procedemos a la tripsinización, obteniendo 10 muestras de ambos cultivos para luego realizar el conteo celular mediante hemocitómetro. A partir de otro cultivo celular, realizamos este mismo procedimiento pero haciendo el conteo celular a las 72 horas en las condiciones descritas.
Estudio de migración celular
De un cultivo celular, durante el segundo pasaje en condiciones de normoxia, se tripzinizan las células y se colocan sobre 16 cubreobjetos en cantidades equivalentes. Colocamos 8 cubreobjetos en placas de Petri en condiciones de normoxia (21% O2-5% CO2) y las 8 restantes en hipoxia (2% O2-5% CO2). Esperamos confluencia celular del 90% para posteriormente, de un vértice del cubreobjeto, retirar 10 mm de células adheridas con micropipeta y tomar registro fotográfico con cámara Canon Power Shot A640. A las 24 horas realizamos un nuevo registro fotográfico y mediante el programa ImageJ 1.45 medimos en milímetros la migración celular (Fig. 3).

Figura 3. A. A la izquierda, retirada de 10 mm de las células adheridas al cubreobjeto con micropipeta, tomando como referencia el borde del cubreobjeto (Microscopio óptico invertido, visualización directa y sin tinción. Aumento 10X). B y C. Fotografías obtenidas a las 24 horas: estudio de migración de las células que se alejaron respecto al punto de partida (línea negra). (Microscopio óptico invertido, visualización directa y sin tinción. Aumento 10X).
Resultados
Aislamiento y cultivo de las ASCs en condiciones de normoxia y en hipoxia
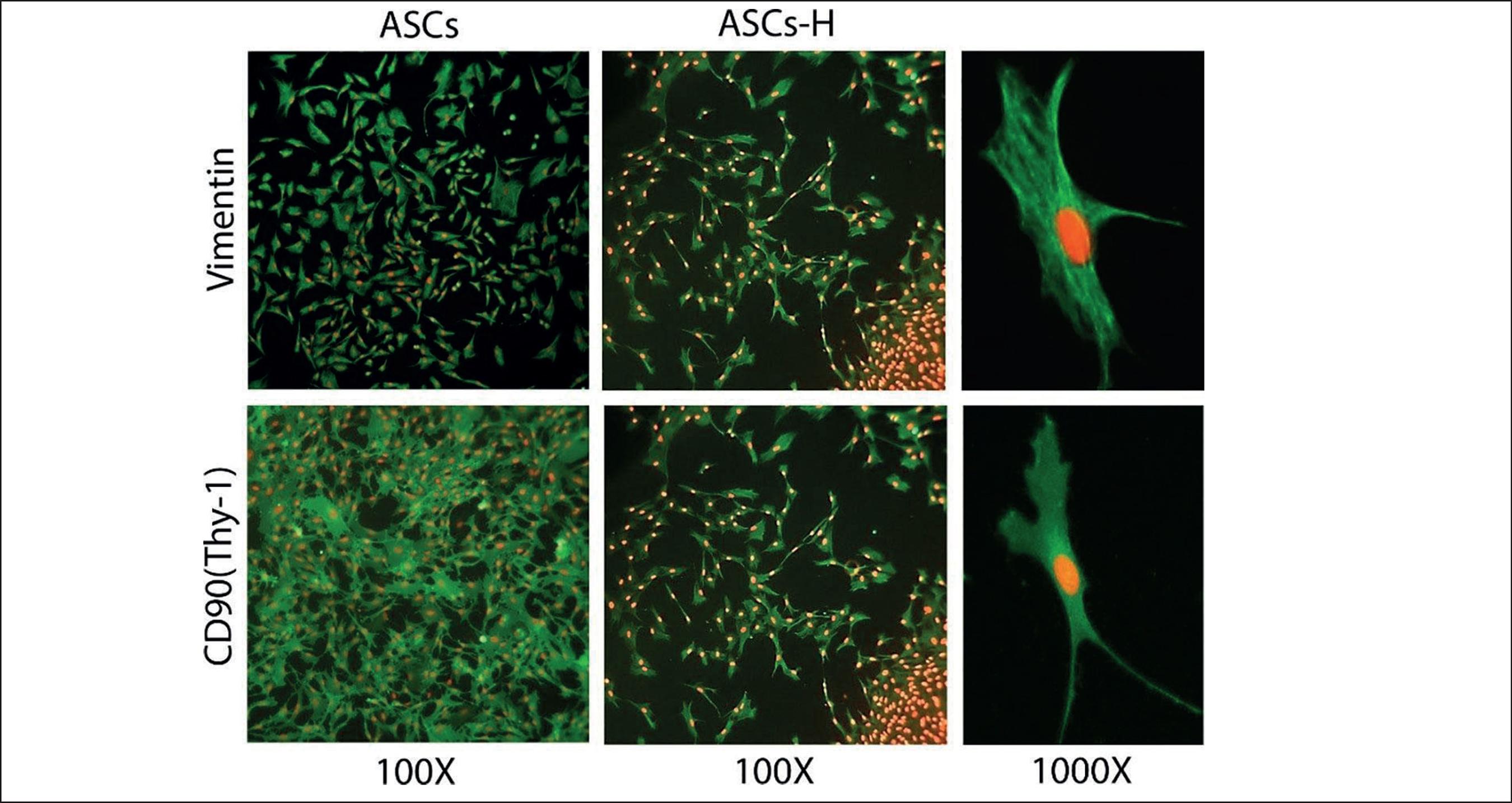
Utilizamos en promedio 1.64 +/- 1.13 gr de tejido adiposo del área ínguinoabdominal en el grupo de ASCs y 0.93 +/- 0.34 gr en el grupo ASCs-H para el aislamiento de ASCs. Logramos una concentración celular de ASCs 9.95 x106 +/- 7.3 x 106 céls/ml y en el grupo de ASCs-H 1.5 x107 +/- 1.5 x 107 céls/ml, manteniendo una viabilidad celular >99%. Bajo visualización directa mediante microscopio invertido, observamos su adherencia al plástico y la morfología característica tipo fibroblasto a partir del primer cambio de medio de cultivo; al cuarto día, estas células se agrupan formando colonias y al séptimo día ya se puede observar confluencia celular cercana al 90% (Fig. 4). Mediante inmunofluorescencia, obtuvimos tinción positiva indistintamente para el grupo ASCs como para el grupo ASCs-H para el anticuerpo primario vimentina (Dako) 1/100 (marcador de los filamentos intermedios) y CD90 (Thy-1) 1/100 (marcador de proteína de superficie celular). Este último presentó positividad en más del 90% de las células tanto en condiciones de normoxia como en hipoxia al 2% de O2 (Fig. 5).
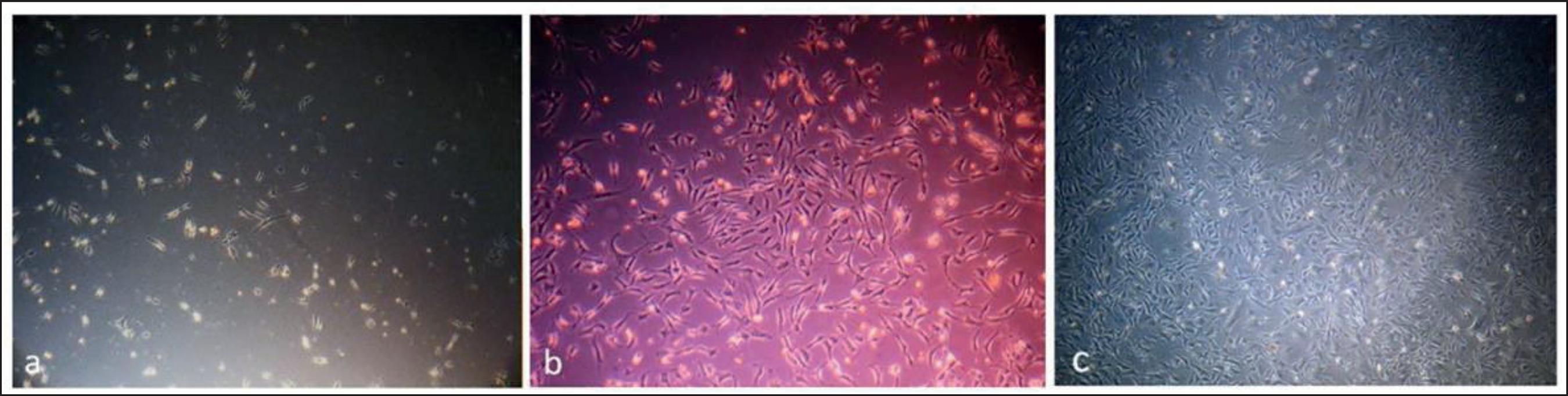
Figura 4. Visualización directa y sin tinción de las ASCs mediante microscopio invertido al segundo día (A), cuarto día (B) y al séptimo día (C) de cultivo celular (Aumento 40X).
Estudio de proliferación celular
Durante el segundo pasaje de cultivo celular de ASCs en condiciones de normoxia hicimos la tripsinización y división en 2 frascos en concentraciones equivalentes, 3.61 x 105 +/- 1.50 x 105 céls/ml y 3.63 x 105 +/- 1.14 x 105 céls/ml respectivamente (p= 0.96). Después de 24 horas obtuvimos como resultado un aumento significativo de la concentración celular en condiciones de hipoxia (5.42 x 105 +/- 1.03 x 105 céls/ml) en comparación con el grupo en normoxia (3.26 x 105 +/- 8.61 x 104 céls/ml) (p≤0.001).
Realizamos este mismo procedimiento a las 72 horas con otro cultivo celular, logrando la misma tendencia de aumento de proliferación celular en hipoxia con 3.04 x 105 +/- 1.13 x 105 céls/ml en comparación con el grupo normoxia con 1.31 x 105 +/- 3.71 x 104 céls/ml (p≤0.01) (Gráfico 1).
Estudio de migración celular
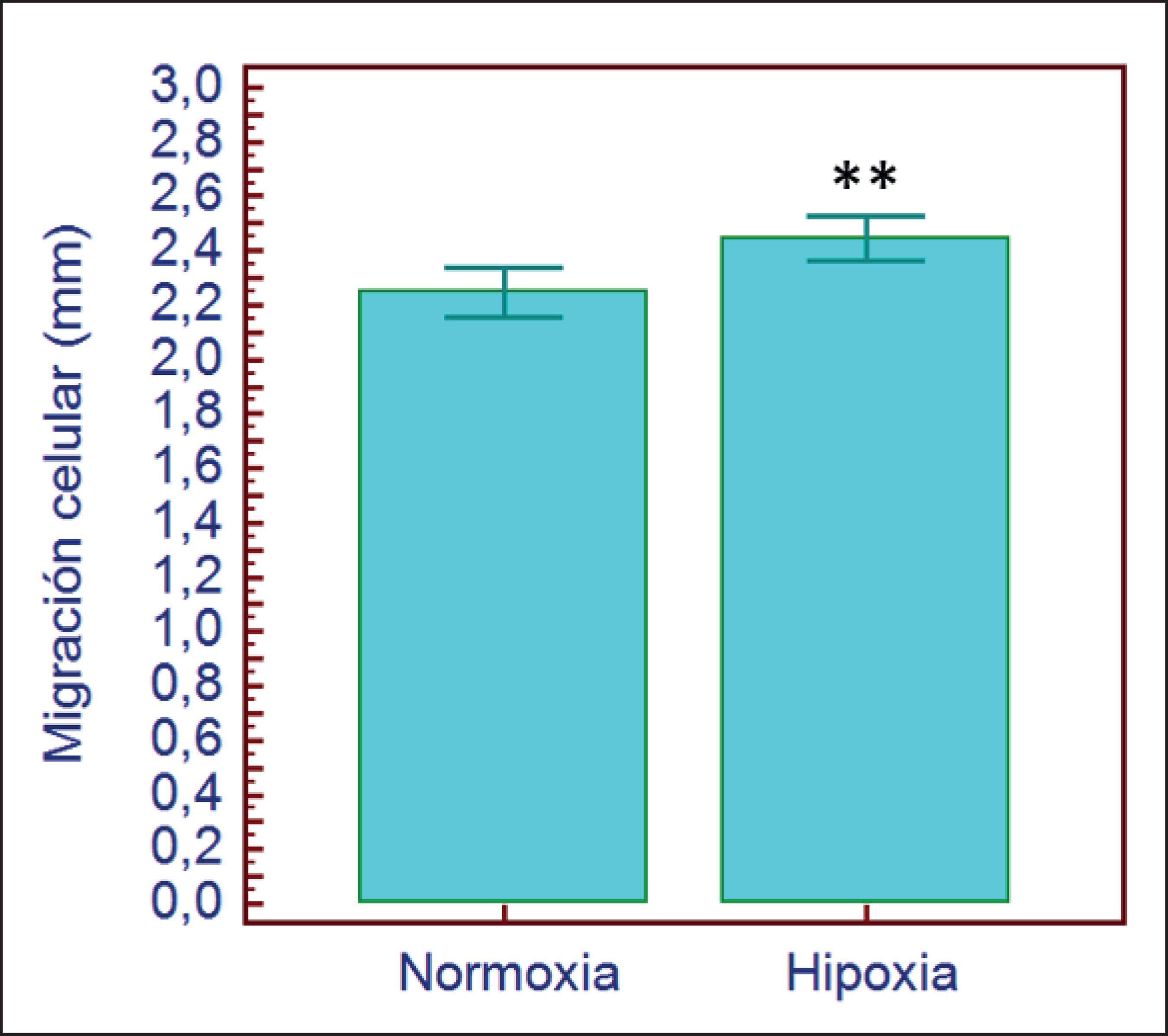
Medimos la migración celular a las 24 horas de cada cubreobjeto, obteniendo mayor capacidad migratoria en el grupo en condiciones de hipoxia (2.24 +/- 0.82 mm) en comparación con el grupo que se mantuvo en hipoxia (2.44 +/- 0.85 mm) (p≤0.01) (Gráfico 2).
Discusión
Las células madre son una opción terapéutica promisoria para el tratamiento de reparación y regeneración de tejidos. En la actualidad se pueden obtener de distintos tejidos con características similares a las originalmente aisladas de médula ósea. Las células madre derivadas de tejido adiposo adultas cobran importancia ya que se encuentran en forma abundante, son de fácil acceso y es posible lograr diferenciación celular de distintos linajes mesodérmicos.(5) Además es posible lograr inducción para la expresión de marcadores ectodérmicos para la producción de neuronas; por lo tanto se podrían considerar estas células con capacidad pluripotencial.(19) En este trabajo logramos obtener células madre derivadas de tejido adiposo adultas de la zona ínguino-abdominal de ratas. Para poder caracterizar y garantizar que corresponden a células madre, estas presentan características morfológicas que recuerdan a los fibroblastos, poseen capacidad de adherirse al plástico y expresión de marcadores de superficie celular como el CD90 en una proporción mayor al 90%(7,8,20) y expresión de vimentina que corresponde a filamentos intermedios del citoesqueleto que se encuentra particularmente en células indiferenciadas.(9,10)
Uno de los mayores problemas del tratamiento con células madre es el que una gran proporción de estas células mueren en el sitio trasplantado isquémico, situación que podría reducir su eficacia.(3) Es por ello que optamos por potenciar estas células en hipoxia al (2% O2 y 5% CO2). Las células madre precondicionadas con hipoxia aumentarían la resistencia a las injurias a través de la expresión de señales protectoras tales como el factor inducible a hipoxia (HIF-1). El complejo HIF-1 está compuesto por 2 subunidades proteicas: HIF-1β que se expresa constitutivamente y HIF-1α que no está presente en las células normales, se induce y acumula en condiciones hipóxicas, y se degrada en condiciones de normoxia y se acumula rápidamente tras exposición a baja tensión de oxígeno.(21) La expresión de este factor de transcripción contribuiría a la activación de genes proangiogénicos, genes promotores de la migración celular, genes antioxidantes y protectores de la apoptosis, con mayor tolerancia al trasplante en zonas isquémicas.(21)
Dentro de las propiedades de las células madre precondicionadas con hipoxia, pudimos constatar un aumento significativo de la proliferación celular, así como su capacidad migratoria respecto a las células sin precondicionamiento. El aumento de la capacidad migratoria se podría explicar por una regulación al alza de proteínas involucradas en la movilidad celular,(14) así como la expresión de receptores quimiotácticos CXCR4, CXCR7, y CX3CR1 que desempeñarían un rol importante para el reclutamiento de células madre hacia el tejido dañado y su asentamiento.(22) La capacidad de autorrenovación de las células madre es una de sus características clave, por lo tanto es necesario un aumento de la tasa de proliferación para su eficiencia en la terapia regenerativa.(22) Las células madre sometidas a una concentración de oxígeno entre el 2 al 5% mejorarían la capacidad proliferativa por medio de la expresión del HIF-1α y el aumento de la expresión de NANOG, que es un regulador de la entrada de la fase S del ciclo celular.(23)
Dentro de las propiedades de las células madre precondicionadas con hipoxia, pudimos constatar un aumento significativo de la proliferación celular, así como su capacidad migratoria respecto a las células sin precondicionamiento. El aumento de la capacidad migratoria se podría explicar por una regulación al alza de proteínas involucradas en la movilidad celular,(14) así como la expresión de receptores quimiotácticos CXCR4, CXCR7, y CX3CR1 que desempeñarían un rol importante para el reclutamiento de células madre hacia el tejido dañado y su asentamiento.(22) La capacidad de autorrenovación de las células madre es una de sus características clave, por lo tanto es necesario un aumento de la tasa de proliferación para su eficiencia en la terapia regenerativa.(22)
Pudimos corroborar un aumento de la proliferación celular ya a las 24 horas de exposición a hipoxia celular.(23) La translocación y la activación a nivel nuclear sería la causante de la producción de varios genes “río abajo” codificadores de eritropoyetina (Epo), VEGF entre otros, los cuales estimularían los mecanismos endógenos de la angiogénesis.(14,21)
Otros genes diana de la HIF-1, como el CXCR4 y codificadores de proteínas de la matriz extracelular (MMPs), estarían involucrados en la migración celular; y otros responderían a mediadores inflamatorios y distintas citoquinas, aumentarían la producción del óxido nítrico sintetasa (iNOS) y la activación de genes antioxidantes.(14),24
También está descrito un aumento de la tolerancia a la apoptosis reflejado por una disminución de la muerte celularin vitro y en el área isquémica o peri-infarto.(14,25)
En relación al uso de estas células en heridas y colgajos, Lee y col.(26) en un estudio en 4 ratas sometidas a 2 lesiones de espesor completo de 8 mm de diámetro en el área dorsal, evidenciaron que la herida tratada con ASCs precondicionadas con hipoxia mejoraba significativamente su capacidad de curación por medio de una regulación al alza de VEGF y bFGF (factor de crecimiento fibroblástico básico) respecto a la herida tratada con ASCs en condiciones de normoxia. Es interesante que tras la inhibición de VEGF y bFGF por medio de anticuerpos, revirtieron los efectos de migración de los fibroblastos y el proceso de curación de la herida. El efecto de la hipoxia (1% O2) en las BM-MSCs durante las 48 horas previas al trasplante en colgajo random en ratas, representó un aumento significativo del área de supervivencia del colgajo y de la densidad microvascular respecto al grupo trasplantado de BM-MSCs en condiciones de normoxia (21% O2).(3)
En el estudio publicado anteriormente por nosotros en esta misma revista, utilizamos esta metodología de precondicionamiento con hipoxia de células madre derivadas de tejido adiposo en colgajos cutáneos aleatorizados en ratas y comparamos respecto al grupo de retardo de colgajo de 5 días y el grupo control.(18) Observamos una disminución significativa en el área de necrosis global del colgajo en los grupos tratados con células madre derivadas de tejido adiposo, con y sin precondicionamiento. Por otra parte, en el grupo de retardo del colgajo y según los patrones de necrosis identificados por medio de características macroscópicas y microscópicas, otorgando una clasificación a esta, observamos necrosis de bajo grado en mayor proporción. Esto significa que se involucra parcialmente y en forma superficial a la dermis, con atrofia y focos de desprendimiento epitelial al séptimo día, que se traducen en una mayor capacidad de reepitelización en comparación al resto de los grupos en los que principalmente el compromiso necrótico del colgajo involucró la dermis en su totalidad.
Conclusiones
El precondicionamiento de células madre derivadas de tejido adiposo es posible mediante la exposición a hipoxia al 2% O2- CO2 5%. Objetivamos un aumento en su capacidad proliferativa y migratoriain vitro de forma precoz tras la exposición a hipoxia en el cultivo. Resulta ser un método reproducible para la aplicación de estas células madre precondicionadas a fin de potenciar el tratamiento de distintas enfermedades en humanos.
Este mismo método ya había sido comprobado por nuestro mismo equipo en un modelo experimental en ratas para disminución de la necrosis en colgajos cutáneos aleatorizados.