INTRODUCCIÓN
Según la tercera edición de la Clasificación Internacional de las Cefaleas (ICHD-III) de la Sociedad Internacional de Cefaleas, la cefalea en racimos (CR) pertenece al grupo de cefaleas primarias trigémino-autonómicas y ha recibido numerosos nombres, tales como cefalea de Horton, cefalalgia histamínica, eritroprosopalgia de Bing o neuralgia esfenopalatina, entre otros 1.
Esta entidad se caracteriza por la aparición cíclica de dolor unilateral orbitario, supraorbitario y/o temporal, breve e intenso, y que se acompaña de inquietud y/o agitación y/o al menos uno de los siguientes síntomas o signos homolaterales: hiperemia conjuntival y/o lagrimeo, congestión nasal y/o rinorrea, sudoración frontal y/o facial, miosis y/o ptosis, edema palpebral. Los episodios duran entre 15 y 180 minutos y recurren con frecuencia variable, entre un ataque cada dos días y ocho ataques diarios. De acuerdo con su periodicidad, puede clasificarse en episódica o crónica, según si los periodos de remisión entre los ataques ocurridos en un año son mayores o menores de tres meses 1.
La prevalencia de la CR es del 0,1-0,4 % de la población general y la edad de comienzo suele estar comprendida entre los 20 y los 40 años. Por motivos que se desconocen, en general, los varones se ven afectados tres veces más que las mujeres; no obstante, estudios epidemiológicos recientes indican que esta diferencia es cada vez menor 2. Algunas investigaciones sugieren que en el 5 % de los casos la CR puede estar transmitida de forma autosómica dominante 1.
La última actualización de la guía para el tratamiento de la CR de la American Headache Society (AHS) 3 recomienda el empleo de oxigenoterapia al 100 %, sumatriptán subcutáneo y/o zolmitriptán intranasal en las crisis. Para los pacientes que no responden ni toleran esta medicación de primera línea, las opciones alternativas incluyen sumatriptán intranasal, zolmitriptán oral, estimulación del ganglio esfenopalatino, anestésico tópico nasal y octreotida subcutánea (Tabla I).
Tabla I. Evidencia y niveles de recomendación para el tratamiento agudo de la cefalea en racimos según la American Headache Society
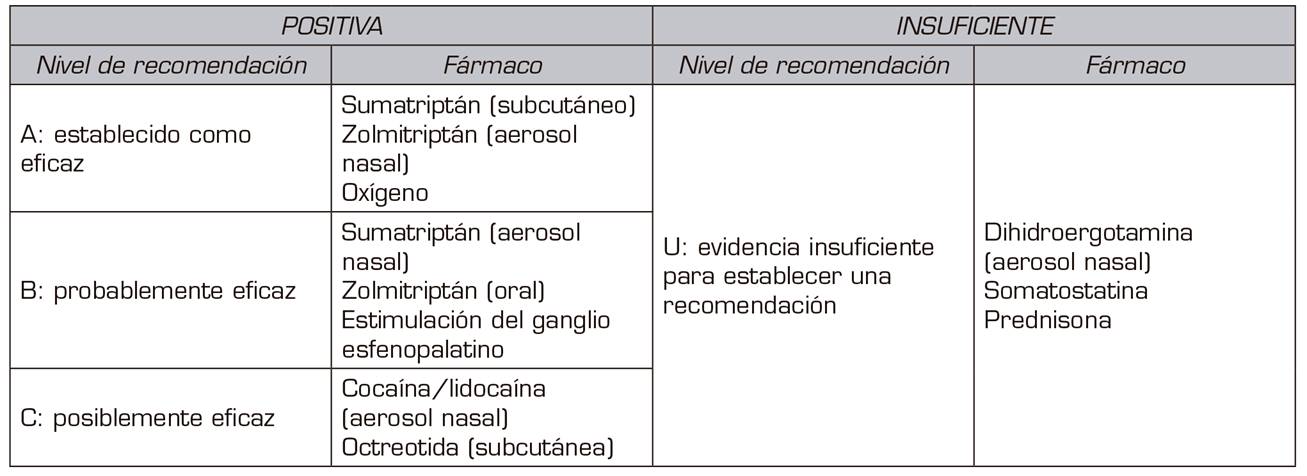
Traducida y adaptada de Robbins et al.3
Los corticoides son considerados como tratamiento profiláctico de transición, debido a su corta latencia y duración del efecto, contemplándose como una terapia puente mientras la medicación de mantenimiento es escalada hasta alcanzar dosis máximas y/o eficaces. La inyección subcutánea suboccipital o bloqueo del nervio occipital mayor ipsilateral al dolor con corticoides goza del nivel más alto de recomendación de la AHS dentro de las opciones terapéuticas profilácticas de la CR.
Como tratamiento preventivo a largo plazo existe evidencia positiva sobre la aplicación de una solución, no disponible en España, de civamida (zucapsaicina) intranasal y sobre la administración de carbonato de litio, verapamilo, warfarina y melatonina (Tabla II).
Tabla II. Evidencia y niveles de recomendación para el tratamiento profiláctico de la cefalea en racimos según la American Headache Society

Traducida y adaptada de Robbins et al.3
Otras alternativas que han demostrado eficacia pero que no cumplieron los criterios de inclusión y exclusión para elaborar la revisión sistemática de la AHS son las siguientes: metisergida, metilergonovina, flunarizina, topiramato, gabapentina, baclofeno, clonidina, pizotifeno, histamina, kudzu, ácido 2-bromo-lisérgico, tratamiento hormonal como testosterona y clomifeno, inyecciones de toxina botulínica y bloqueo y/o radiofrecuencia del ganglio esfenopalatino 3.
Actualmente, en aquellos casos rebeldes al tratamiento estándar, la ketamina parece ser un fármaco efectivo ya que bloquea el receptor glutamatérgico N-metil-d-aspartato (NMDA). Además, este efecto analgésico podría verse potenciado gracias a la combinación con sulfato de magnesio, que actúa bloqueando la misma vía 4.
CASO CLÍNICO
Mujer de 65 años, con historia previa de CR episódica, fumadora de 10 paquetes/año y sin otros antecedentes médico-quirúrgicos de interés, que fue remitida a la Unidad del Dolor por Neurología. En el momento de ser valorada por nosotros, la paciente presentaba un brote de CR de 2 meses de evolución con una media de seis crisis diarias de predominio nocturno. Al inicio del cuadro había sido evaluada por su neurólogo, que le había pautado tanto medicación abortiva (oxigenoterapia al 100 %, zolmitriptán intranasal, diazepam) como profiláctica (verapamilo y topiramato). Se reajustó el tratamiento y se añadió: lidocaína intranasal al 4 % aplicada con una torunda colocada lo más próxima al cornete medio, 6 mg de sumatriptán subcutáneo para el control de las crisis, 1 mg/kg/día de prednisona con posterior pauta descendente, 25 mg/día de amitriptilina y 2 mg/día de melatonina para su prevención. Además, se le realizaron tres infiltraciones (la primera por parte del Servicio de Neurología y las dos siguientes, ecoguiadas, por parte de la Unidad de Dolor) del nervio occipital mayor con levobupivacaína al 0,25 % y 20 mg de triamcinolona acetónido (el máximo periodo de remisión fue de 6 días, tras la segunda infiltración, en la que se infiltró también el nervio occipital menor), precediéndose la tercera, además, de una radiofrecuencia pulsada, a 45 voltios durante 6 minutos, de dicho nervio.
Transcurridos 4 meses desde el comienzo del episodio y ante la no mejoría clínica y el deseo expreso de la paciente de intentar evitar otros procedimientos intervencionistas, se decidió realizar, (previo consentimiento informado y bajo monitorización estándar [pulsioximetría, presión arterial no invasiva, electrocardiograma] y oxigenoterapia con gafas nasales a 3 l/min con capnografía, previa administración de 0,1 mg/kg de midazolam en bolo lento durante 5 minutos) una perfusión de 1 mg/kg de ketamina y 3 g de sulfato de magnesio en un suero fisiológico de 100 ml durante 60 minutos, que aconteció sin incidencias. Después de este tratamiento las crisis cedieron durante 3 días, tras los cuales se reiniciaron. En un principio fueron de menor intensidad, pero terminaron exacerbándose, por lo que se decidió repetir la perfusión al mes. Tras la misma tuvieron lugar dos crisis en total, que se controlaron con oxigenoterapia y lidocaína intranasal. Se decidió proceder a una tercera y última perfusión 4 semanas después de la segunda.
Actualmente, a los 6 meses de la última perfusión, la paciente refiere que ha abandonado el hábito tabáquico, únicamente toma 80 mg/día de verapamilo y 2 mg/día de melatonina como tratamiento profiláctico y, en los momentos en los que ella percibe que se puede desencadenar una crisis (momentos de estrés, ansiedad, agitación, etc.) o comienza con lo que parecen pródromos de un episodio de CR (la paciente lo describe "como si el ojo fuera empujado a salir de su órbita"), se autoadministra oxígeno y lidocaína intranasal tópica, manteniéndose hasta la fecha libre de crisis.
DISCUSIÓN
La CR, cefalea trigémino-autonómica más frecuente 3, es considerada una de las más intensas e invalidantes dentro del grupo de las cefaleas primarias, y aunque se dispone de tratamientos sintomáticos y preventivos eficaces, estos pueden no ser suficientes en casos rebeldes, tal y como ocurrió en el caso que presentamos.
Un dato relevante en esta patología es que en torno al 85 % de los pacientes son fumadores crónicos y, aunque dejar de fumar no parece tener ningún efecto sobre la enfermedad una vez establecida, el hábito tabáquico puede ser un factor de riesgo para su desarrollo, posiblemente sobre la base de una predisposición genética 5. Por otro lado, sí parece haber una relación entre ser fumador y formas más intensas de CR 6. Por consiguiente, basándonos en la bibliografía consultada, podríamos inferir que la mejoría sintomatológica en la paciente se debe principalmente al tratamiento médico instaurado y no al abandono del hábito tabáquico, sin poder descartar, por supuesto, que esta última medida no contribuya a la magnífica evolución del cuadro.
Es sabido que la administración de ketamina, debido a su acción anti-NMDA y a sus probables efectos antiinflamatorios y de potenciación de las vías inhibitorias descendentes, entre otros, puede ser efectiva en el tratamiento del dolor crónico, incluyendo la cefalea refractaria a tratamiento 4. Además del alivio del dolor, una sola infusión de ketamina parece ser efectiva para reducir rápidamente la ideación suicida, que puede ser un problema relevante en pacientes con CR. Asimismo, la combinación con sulfato de magnesio produciría un efecto analgésico sinérgico 7. Tomando estas premisas como base, y al igual que procedió el grupo de Moisset et al. 8, pero con dosis (1 mg/kg de ketamina en lugar de 0,5 mg/kg) e intervalos entre perfusiones (1 mes lugar de 8 semanas) diferentes, se decidió instaurar el tratamiento con ketamina y sulfato de magnesio intravenoso, tras lo que se obtuvo buena respuesta, cediendo las crisis de CR hasta el momento actual. Investigaciones recientes demuestran niveles reducidos de ácido quinurénico (antagonista del receptor NMDA) en pacientes con CR, lo que refuerza la hipótesis de la supuesta hiperactividad de los receptores NMDA en esta patología 9. No obstante, aún son necesarios estudios para poder determinar la eficacia y seguridad de este tratamiento en pacientes con CR.
Actualmente se están analizando nuevas opciones de tratamiento con resultados prometedores 10. Las líneas de investigación tienen el punto de mira en la terapia con anticuerpos monoclonales, que actuarían bloqueando el receptor CGRP (péptido relacionado con el gen de la calcitonina) y otros receptores implicados en la fisiopatología de la CR. Además, se estudia el uso de nuevos dispositivos para administración de medicamentos ya aprobados (como el parche transdérmico de zolmitriptán con microagujas 11)), nuevas formas de neuroestimulación (por ejemplo, estimulación no invasiva del nervio vago 12)) y otras líneas que podrían ser el futuro en el tratamiento de la CR.














