INTRODUCCIÓN
Las quemaduras lesionan la piel y/o afectan a otros tejidos corporales. Pueden ser causadas por agentes térmicos, químicos, radioactivos, eléctricos, biológicos (anguilas eléctricas) o por frío1.
El diagnóstico, gravedad, tratamiento y riesgo vital de la quemadura los marcarán la superficie corporal quemada (SCQ), la profundidad y tipo de tejidos afectados, la intensidad de las energías destructivas, el tiempo de exposición a estas2,3, la edad, localización y primeros auxilios recibidos, entre otros.
Las quemaduras se pueden clasificar según su afectación tisular en:
Quemadura epidérmica o de primer grado: epidermis.
Quemadura dérmica superficial o de segundo grado superficial: hasta dermis papilar.
Quemadura dérmica profunda o de segundo grado profundo: la lesión afecta a todos los estratos epidérmicos, llegando hasta la dermis reticular, pero sin afectación del tejido subcutáneo.
Quemadura subdérmica o de tercer grado: destrucción completa de todo el espesor de la piel, llegando a afectar tejido subdérmico e incluso estructuras subyacentes (fascia, músculo, tendón, vasos, nervios, periostio, etc.). Queda afectada la totalidad de los anejos cutáneos (glándulas, folículos, etc.). No queda ninguna célula epidérmica viable. Las terminaciones nerviosas también resultan destruidas3.
En las quemaduras subdérmicas extensas o de zonas sensibles, por el alto riesgo vital, o de producir secuelas, que conllevan, se debe añadir al tratamiento tópico y sistémico, el quirúrgico4. Las quemaduras en extremidades inferiores (EE II) pueden complicarse y causar síndrome posflebítico, cicatrices retráctiles o disfunciones motoras. Son necesarios el diagnóstico precoz de las complicaciones y su tratamiento adecuado5.
La evidencia indica que la cura en ambiente húmedo (CAH)6,7 es la mejor opción, pues genera un microambiente propicio de reparación tisular fibroblástica y regeneración epidérmica. Además, la utilización de vendajes compresivos en la fase inflamatoria profundiza la lesión3.
Tras búsqueda bibliográfica sin casos precedentes, consideramos que la exposición de este caso refleja las consecuencias de un manejo inicial inadecuado. El objetivo es exponer el abordaje terapéutico, que puede ayudar a otros profesionales a conocer la importancia del tratamiento inicial de estas lesiones para prevenir y/o resolver futuras complicaciones.
PRESENTACIÓN DEL CASO
Historia clínica
Varón de 37 años con paraplejia desde 2011 tras accidente. Lesión neurológica por fractura y estallido de vértebra D12. Lesión medular en vértebra lumbar L2 derecha y L1 izquierda de grado A. Sin más hallazgos de interés. Presenta quemadura en pierna derecha por contacto prolongado con el tubo de escape de un motor de explosión (fig. 1 A).
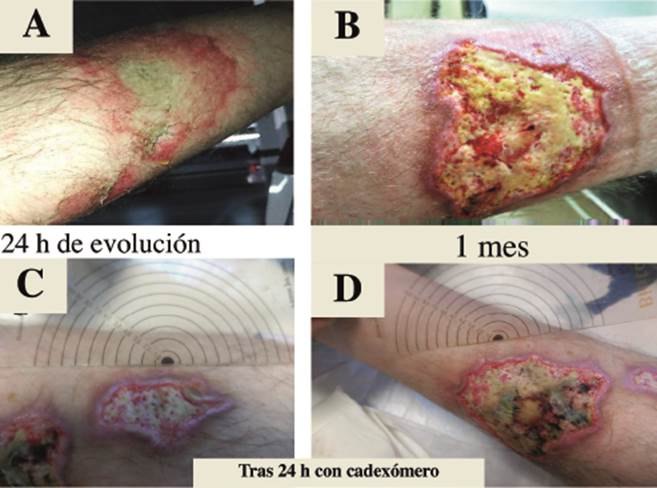
Figura 1 A) Al día siguiente ya se apreciaba un lecho blanquecino. Aunque no se diagnosticó como de espesor total. B) A los 30 días presentaba el lecho con gran cantidad de tejido inviable, fibrina y con mucha probabilidad, biopelícula bacteriana. C) La lesión proximal se resolvió con descarga bacteriana de 5 días con cadexómero, y apósito de fibras detersivas hasta la epitelización. D) Tejido necrótico y esfacelos.
Valoración
Quemadura en zona gemelar medial de pierna derecha de 1,5% de SCQ, con dimensiones de 8 cm de ancho por 9 cm de largo, sin profundidad valorable, destrucción del espesor de la epidermis con tejido subdérmico expuesto y anestesia a la exploración de la sensibilidad dolorosa. Tras un mes de evolución (fig. 1 B) presenta flebolinfedema en la extremidad, eritema perilesional, fibrina, esfacelos y sospecha de biopelícula en el lecho de la herida. En zona proximal presenta otra quemadura de características similares, pero inferior al 0,5% de SCQ y de 3 cm de largo por 2 cm de ancho y 0,5 cm de profundidad con lecho fibroso (fig. 1 C).
PLAN DE CUIDADOS
Durante el primer mes se realizó vendaje compresivo en fase inflamatoria con venda de crepé y curas regulares con la pauta de curas descrita en la tabla 1.
A continuación, la herida se manejó en tres fases:
1.ª fase de limpieza de la herida (fig. 1 D) y descongestión del flebolinfedema:
Uso de apósitos bactericidas (tabla 2) y productos enzimáticos o hiperosmolares.
En lesión menor se utiliza apósito de fibras detersivas con hidrocoloide (Urgoclean®) hasta su resolución.
Terapia de compresión con vendas de tracción corta (Comprilan® y/o Putterbinde®).
2.ª Fase de reparación tisular:
Preparación del lecho de la herida con CAH, control de carga bacteriana con apósitos bactericidas y del exudado mediante dispositivo de un solo uso de terapia de presión negativa (DSUTPN) (PICO®).
3.ª Fase de epitelización y remodelación:
Apósitos de espuma y silicona hasta epitelización.
Apósitos bactericidas en uso intermitente según evolución de la carga bacteriana.
Apósitos de silicona para cicatrices y prendas de presoterapia para remodelación.
Educación para la salud (EPS):
Utilizar medias de compresión ligera en ambas extremidades.
Movilización pasiva de dorsiflexión del pie.
Elevar EE II en reposo.
Fomentar abandono de los hábitos tóxicos.
Tabla 2 Pauta de curas de los 91 días restantes hasta la epitelización.*

PHMB: polihexametileno biguanida.
*Desde la primera cura se emplearon productos de cura en ambiente húmedo. Se procuró realizar una rotación de apósitos bactericidas. La gran carga bacteriana se apreció en la cura 3, con proteasa, y la cura 8 con malla con NOSF (Nano-Oligo Saccharide Factor). Al eliminar los apósitos bactericidas se produjo reaparición de tejido necrótico y aumento del exudado. La utilización de cadexómero (cura 1) tras el desbridamiento cortante es una alternativa a la cura hemostásica tradicional con gasa y antiséptico.
EVOLUCIÓN
Durante el primer mes, la quemadura involucionó a herida compleja con abundante tejido necrótico y fibrina (fig. 1 A). Entre el segundo y el tercer mes, se aplicaron las técnicas y recursos necesarios para abordar la herida (figs. 2 A-C).

Figura 2 A) Tras el desbridamiento cortante se tuvo que cauterizar algunos puntos sangrantes con nitrato de plata. B) Ya se aprecia borde de epitelización y la profundidad de la lesión. C) La lesión proximal está epitelizada en un 90%. La quemadura principal tiene buenos bordes epiteliales y lecho con abundante tejido de granulación. D) Apósito de terapia de presión negativa tras 4 días de uso. Se aprecia la utilización del vendaje de compresión con vendas de tracción corta. Protección de áreas expuestas con espuma adhesiva y venda de algodón.
RESULTADOS
El DSUTPN (fig. 2 D) redujo un 80% la extensión de la quemadura8. Con vendajes de tracción corta, CAH y descarga bacteriana intermitente, se logró la epitelización (figs. 3 A-D). Se previnieron las cicatrices patológicas con apósitos Mepiform® y medias ortostáticas de baja compresión de 18-23 mmHg.

Figuras 3 A y B) Evolución de la herida con la terapia de presión negativa. C) Lesión inferior a 1 cm. Se decide dar apósitos con tecnología nano-oligo-sacárida y lípido coloidal (UrgoStart Border®, UrgoTul Absorb Border®) y que realice las curas su cuidadora. Sufre una gran involución debido a que deja de utilizar las medias de compresión (temperaturas elevadas que no bajan de los 30 ºC). Se da continuos baños de mar con la silla de ruedas y no acude a las citas con su enfermero. D) Tras la desbridación de la hiperqueratosis perilesional, se reinicia el tratamiento con apósitos de plata nanocristalina y aplicación de vendaje elástico tubular (en dos tamaños distintos, ancho en pierna y estrecho en pie) que soporta mejor que la media de compresión.
DISCUSIÓN
La complejidad de la lesión, y los datos previos, manifestaron la escasa utilización de apósitos de CAH y variabilidad del manejo inicial de esta quemadura.
La variabilidad del tratamiento de una lesión puede relacionarse, entre otros, con un déficit de formación, actitud de los profesionales y la discontinuidad de los cuidados9. Fueron 15 profesionales de enfermería los que manejaron la herida, lo que originó la discontinuidad en su atención, valoración y cuidado, y pudo favorecer el agravamiento de la quemadura (fig. 1 B). En este sentido, sería interesante emprender estudios cuantitativos que reflejen el coste-consecuencia de la variabilidad profesional en la evolución de las quemaduras.
Inicialmente, la mezcla de apósitos incompatibles inactivó sus principios activos (colagenasa con polihexametileno biguanida)10. Utilizar desbridamiento enzimático con cura seca11 sin respetar la vida útil de la pomada, junto al escaso control del exudado y carga bacteriana, pudo causar aumento de tejido inviable (fig. 1C) y entorpecer la cicatrización.
Utilizar pomadas antibióticas, sin respetar los plazos de actividad bactericida, pudo favorecer el aumento de la carga bacteriana y las resistencias bacteriológicas. Así se refleja en la involución y agravamiento que sufrió la herida cuando, con el lecho de la herida limpio, se retiró el tratamiento bactericida (figs. 3 C y D, tabla 2).
La aplicación sistemática de antisépticos y/o pomadas bactericidas12 y la utilización de técnicas cruentas como la cura seca, vendajes compresivos en fase inflamatoria o limpiezas agresivas con cepillo3 pudieron enlentecer y/o complicar el proceso de cicatrización (figs. 1 A y B). La evidencia encontrada en guías y protocolos certifica3 que cualquier presión ejercida en la fase inflamatoria de la quemadura dificulta la buena perfusión tisular y produce profundización de la lesión. Los vendajes compresivos en las primeras curas, con gran probabilidad, habrán profundizado la lesión tisular de capas profundas. Sin embargo, la eficiente utilización de la terapia de compresión a partir del primer mes (al reducir el flebolinfedema) y de los DSUTPN (PICO®) ayudaron a la cicatrización.
Queda patente en la literatura científica6 que un tratamiento quirúrgico precoz reduce las complicaciones y costo del tratamiento, por lo que una rápida intervención quirúrgica habría sido lo indicado para la resolución de este caso.
CONCLUSIONES
Un buen manejo inicial de la quemadura determina una evolución positiva (fig. 4). El diagnóstico correcto, apoyado por la aplicación de técnicas de exploración y valoración de la sensibilidad, del tipo de tejido expuesto y de signos y síntomas que presenta, permite un correcto abordaje de la lesión y una posible derivación oportuna a servicios más especializados, de los que el paciente se puede beneficiar. Asimismo, la detección y corrección de complicaciones surgidas durante la evolución de la herida, mediante la aplicación de los diferentes tratamientos mencionados, promovió una cicatrización favorable.

Figura 4 Se consigue el cierre cutáneo y a los 30 días se inicia el tratamiento con apósitos reductores de cicatrices y prendas terapéuticas.
Desde la primera cura se emplearon productos de cura en ambiente húmedo. Se procuró realizar una rotación de apósitos bactericidas. La gran carga bacteriana se apreció en la cura 3, con proteasa, y la cura 8 con malla con NOSF (Nano-Oligo Saccharide Factor). Al eliminar los apósitos bactericidas se produjo reaparición de tejido necrótico y aumento del exudado. La utilización de cadexómero (cura 1) tras el desbridamiento cortante es una alternativa a la cura hemostásica tradicional con gasa y antiséptico.















