INTRODUCCIÓN
La salud pública es la disciplina que se ocupa de planear, ejecutar y evaluar programas de salud que busquen resolver los problemas de salud pública que afectan a la sociedad1. Desde la perspectiva biopsicosocial, la demencia es una enfermedad que produce muchos cambios a nivel tanto biológico como psicológico y social. Con el aumento del porcentaje de personas de más de 75 años en las poblaciones industrializadas, el deterioro cognitivo es un problema que crece, y también crece el interés social para entender el porqué de determinadas patologías2.
Desde la visión de la salud pública, las demencias representan un problema creciente de demandas de servicios de salud en prácticamente todo el mundo3, con lo que crece la necesidad de crear un consenso efectivo para reconocerlo, conocer sus causas, los factores de riesgo y de protección y, en última instancia, tratarlo. Desde la perspectiva de la familia, dependiendo de quién es el miembro enfermo y en función de la fase de enfermedad, el impacto dentro de este sistema es mayor o menor4.
Para planear y evaluar los programas de salud, es necesario conocer qué causas son las que ocasionan el fenómeno, así como desarrollar estrategias para intervenir sobre las causas modificables.
Uno de los síndromes más comúnmente conocidos por causar un deterioro cognitivo importante es la demencia. La demencia es un síndrome de etiología múltiple2 que afecta a diversas funciones mentales. Esta ocasiona un declive significativo comparado con el nivel previo de funcionamiento, en uno o más dominios cognitivos (atención compleja, función ejecutiva, aprendizaje y memoria, lenguaje, habilidad perceptual motora o cognición social5). Este declive de las funciones mentales se presenta de forma insidiosa, crónica y generalmente progresiva. Para que dicho deterioro cognitivo sea diagnosticado como demencia, uno de los criterios sine qua non es que el declive no debe darse exclusivamente durante un síndrome confusional, también llamado delírium6.
El Manual Diagnóstico y Estadístico de los Trastornos Mentales (DSMIV TR) explica los criterios diagnósticos para el diagnóstico de delírium en personas mayores6. El criterio A establece que debe existir una alteración de la conciencia, referida a los niveles de atención y alerta; el criterio B exige la presencia de cambios en las funciones cognitivas (memoria, orientación, lenguaje, etc.) o presencia de alteraciones perceptivas (alucinaciones, ideaciones delirantes, etc.) que no se expliquen por una demencia previa o en desarrollo. El criterio C indica que debe presentarse de forma aguda (horas o días) y tiende a fluctuar durante el mismo día. Por último, el criterio D menciona que el cuadro clínico debe ser efecto de una enfermedad médica, del consumo de sustancias o de ambas. El diagnóstico de delírium exige el cumplimiento de los 4 criterios.
Algunos autores, como Fong7 y Krogseth8, hablan sobre la actual y gran controversia del diagnóstico de delírium ¿Es un simple marcador de vulnerabilidad de la demencia? ¿Es el delirium el enmascaramiento de una demencia no reconocida? ¿O por el contrario es un diagnóstico aparte con la capacidad de causar un daño neuronal permanente y encaminar a la persona hacia la demencia? No entraremos en detalle, pero para dar respuesta a estas preguntas, se ha hipotetizado en unos mecanismos sobre cómo el delírium contribuiría al daño neuronal permanente; estos incluyen neurotoxicidad (p. ej., anestesia), inflamación, estrés crónico, daño neuronal (p. ej., isquemia prolongada o septicemia), aceleración de la demencia (p. ej., beta-amiloide o tau) y reserva cognitiva disminuida9. La evidencia emergente sobre estudios epidemiológicos, clinicopatológicos, de neuroimagen, biomarcadores y estudios experimentales apunta a la idea de una fuerte interrelación entre ambos síndromes, pero a la vez también apunta hacia una diferenciación de los mecanismos patológicos de cada uno10.
Actualmente, la prevalencia de delírium en personas mayores residentes en la comunidad oscila entre el 1% y el 2%. Esta cifra aumenta a medida que aumenta la edad, alcanzándose hasta un 14% en personas mayores de 85 años11. Junto con la demencia, ambos procesos coinciden con frecuencia en un mismo paciente, formando parte de los llamados grandes síndromes geriátricos12. El delírium es el síndrome más frecuente de presentación de enfermedad en personas mayores, ligado claramente al envejecimiento, donde la edad avanzada y la aparición en pacientes con demencia hace que se produzca un infradiagnóstico13,14.
Aunque aún queda camino, lo que se sabe ahora es que hay algunos factores de riesgo que contribuyen a la aparición de un síndrome confusional agudo (delírium). Algunos de los factores se muestran a continuación15,16, representados en la tabla 1.
Tabla 1 Síntesis abreviada de factores predisponentes y precipitantes para el desarrollo de un delírium o síndrome confusional agudo
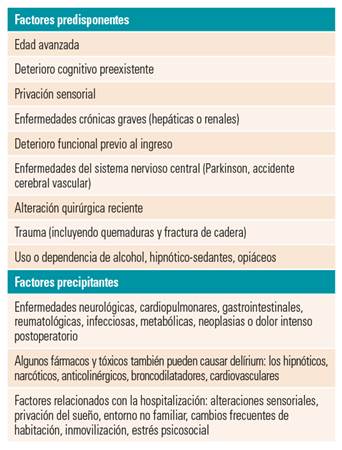
En la población con un daño cerebral previo (p. ej., tumores), los índices de delírium en la fase aguda notificados aumentan entre un 15% y un 48%17. Otro de los factores de riesgo más importantes se descubrió a raíz de las operaciones por fracturas de cadera en ancianos de más de 70 años. Gracias a esto, se observó la aparición de delírium postoperatorio (POD, Post Operative Delirium) entre un 15% y un 53% de los intervenidos quirúrgicamente18. Otro factor de riesgo que también cabe tener en cuenta es la hospitalización, donde se ha estudiado que en el momento de ingreso o en las primeras 24 horas se produce una prevalencia del 14-24% y pasadas 24 horas19, esta prevalencia pasa a ser del 6-56%.
Actualmente, la relación entre un desarrollo cognitivo pobre y el riesgo de sufrir episodios de delírium está bien establecida20. Por el contrario, la relación de dichos episodios con el desarrollo posterior de demencia no lo está tanto21. Este artículo pretende resumir la evidencia escrita hasta la fecha, mediante un metaanálisis, y extraer una conclusión lo más ajustada posible a la realidad de la influencia de una variable sobre la otra.
El objetivo de este estudio fue el de realizar una revisión sistemática con metaanálisis, para determinar la influencia de los episodios de síndrome confusional agudo o delírium en el desarrollo posterior de una demencia o un deterioro cognitivo grave en personas mayores.
MATERIAL Y MÉTODOS
Para este trabajo, se realizó en primer lugar una búsqueda en la base de datos Cochrane con el objetivo de encontrar revisiones sistemáticas ya realizadas sobre esta misma temática. A continuación, se realizó una búsqueda a través de las bases de datos PsycInfo, PubMed y Psicodoc incluyendo las palabras clave “delirium”, “acute confusional state”, “dementia”, “delirium risk factor”, “cognitive impairment”, “alzheimer disease”, “post stroke”, “oldest old”. Estas palabras clave se combinaron de la siguiente forma: “delirium and dementia”, “delirium and oldest old”, “delirium and cognitive impairment”, “delirium and risk factor”, “stroke/post stroke and delirium”, “delirium and alzheimer’s disease”. La búsqueda en las bases de datos se limitó a la lengua española e inglesa. Se determinó un año de publicación superior a 2004.
Los criterios de inclusión y evaluación fueron los siguientes:
Que el estudio evaluara la asociación entre los episodios de delírium en pacientes no demenciados con la demencia, para estudiar si se producía un deterioro cognitivo pasado un tiempo del episodio de delírium.
Que la edad de los participantes fuera de más de 70 años, ya que el estudio va dirigido a la asociación anteriormente mencionada en pacientes geriátricos.
Que los pacientes no estuviesen sufriendo una enfermedad mental concurrente al estudio (depresión, esquizofrenia) y que no hubiesen sufrido otros episodios confusionales agudos en el pasado.
Que el diseño del estudio fuese explicitado.
Utilizar medidas objetivas de la función cognitiva en la primera evaluación, y que fueran las mismas medidas en el seguimiento. También que el diagnóstico de delírium y demencia estuviese hecho por varios profesionales del ámbito de la salud según los criterios del DSM-IV TR.
Que en los resultados de los estudios seleccionados se explicitara el número de personas en cada una de las cuatro condiciones (delírium y demencia, delírium y no demencia, no delírium y demencia, no delírium y no demencia).
La combinación de las bases de datos identificó un total de 2.334 archivos. Los duplicados se eliminaron (537). A continuación se hizo una selección mediante la lectura de los títulos y los abstracts, en la cual 1.780 fueron eliminados por no incluir las variables que se querían estudiar en este artículo (estudios con una variable cualitativa binomial), por deficiencias en la metodología (usar diferentes test en la medida pre y la medida post, no explicar la pérdida de muestra durante el estudio, no explicar cómo ni de dónde se extrajo la muestra) o por haber diferencias muy significativas en cuanto a la edad intergrupos.
En total quedaron 17 artículos potencialmente relevantes para el presente trabajo. Después de leer totalmente los documentos, 9 artículos fueron excluidos porque no cumplían con los requisitos mínimos que se impusieron para la inclusión en este metaanálisis o porque los datos que aportaban eran incompatibles con la de los otros artículos. Finalmente, se seleccionaron 8 estudios que cumplían los criterios de inclusión. El proceso por el cual se seleccionaron los artículos se muestra en la figura 1.
El análisis de los resultados se ha llevado a cabo con el programa estadístico R Commander. Se realizó un modelo de efectos fijos y aleatorios para estudiar qué diferencias se daban. No se observaron grandes diferencias, pero aun así se asumió un modelo de efectos aleatorios, ya que en las pruebas estadísticas referentes al estudio de la homogeneidad (fig. 2), los estadísticos Tau (T2) y Q, sí daban un valor muy cercano a 0 pero no lo incluía, por lo que se creyó oportuno aplicar el modelo de efectos aleatorios para tener en cuenta el margen de aleatoriedad.
Todo metaanálisis debe valorar la posibilidad de la existencia de un sesgo de publicación que pudiese comprometer sus resultados y conclusiones. Hay varios métodos para explorar la posibilidad y la cuantía del sesgo de publicación. Con el objetivo de ser más visual, en este estudio se ha realizado un diagrama de embudo o Funnel Plot que se muestra en la figura 3. Como puede observarse, el embudo tiene una forma de V invertida, donde los estudios se agrupan en torno a la cima de este, lo que indica ausencia de sesgo de publicación, excepto un estudio22 que queda fuera del embudo, ya que por la OR que presenta se espera que tenga un menor error estándar. Esto es debido probablemente a su pequeño tamaño muestral que aumenta la probabilidad de heterogeneidad en el grupo.
RESULTADOS
Ocho artículos fueron incluidos en el estudio por cumplir los criterios de selección (tabla 2). Todos los estudios fueron longitudinales, con entre 6 y 120 meses de seguimiento. A todos los participantes se les pasó el MMSE (Mini-Mental State Examination) de Folstein, así como una entrevista diagnóstica siguiendo los criterios del DSM-IV TR, realizada por diferentes profesionales del ámbito de la salud en momentos diferentes, para descartar la posible presencia de demencia en la línea base. La mayoría de estudios hacen referencia a un delírium posterior a hospitalización debida a una fractura, pero también se incluyen estudios con población general, accidente vascular cerebral (AVC) y pacientes de la unidad de cuidados intensivos.
Tabla 2 Resumen de los artículos incluidos en el metaanálisis
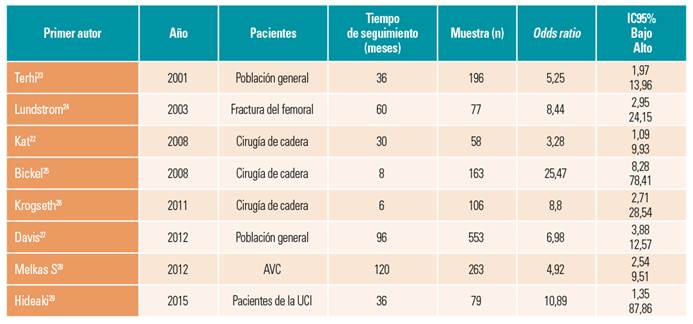
AVC: accidente vascular cerebral; UCI: unidad de cuidados intensivos.
En la tabla 3 puede observarse un resumen de la distribución de pacientes que presentaron delírium y acabaron desarrollando o no demencia y aquellos pacientes que no presentaron ningún episodio de delírium y acabaron presentando o no demencia.
Tabla 3 Resultados observados pasado el tiempo de seguimiento en cada uno de los cuatro grupos: delírium (demencia o no) y no delírium

Para la obtención de los resultados se realizó un contraste de hipótesis. La hipótesis nula (Ho) toma la explicación de que la proporción de personas con demencia en el grupo de delírium es igual a la proporción de pacientes con demencia en el grupo no delírium. La hipótesis alternativa (H1) implicaría que ambos grupos son diferentes entre sí. Para realizar el contraste de hipótesis se llevaron a cabo dos pruebas. En primer lugar se realizó la prueba no paramétrica de los rangos con signo de Wilcoxon. En segundo lugar, se realizó la prueba de la χ2 de Pearson. Ambas pruebas coinciden en descartar la hipótesis nula, por lo que se concluye que la proporción de pacientes con demencia en el grupo delírium es diferente que en el grupo no delírium (fig. 4).

Figura 4 Contraste de hipótesis H0 y H1. Tabla resumen del sumatorio de los pacientes de todos los estudios incluidos en cada grupo de comparación. Pruebas no paramétricas de Wilcoxon y χ2 de Pearson.
Los resultados obtenidos apuntan hacia un efecto positivo del hecho de haber sufrido delírium con el posterior efecto de desarrollar deterioro cognitivo. Como puede observarse en el Forest Plot de la figura 5, todos los estudios quedan a la derecha de la línea del “no efecto”, por lo que indica una muy baja heterogeneidad. Además, ninguno de los estudios incluye el valor 1 en sus intervalos de confianza, lo que indica que los resultados son estadísticamente significativos. En resumen, y como puede observarse en el resultado global, se observa que el hecho de haber sufrido episodios previos de delírium sí que tiene un efecto positivo en el riesgo de desarrollar posteriormente una demencia.
DISCUSIÓN
Delírium y demencia son síndromes clínicos neurocognitivos de alta prevalencia en el anciano30. Se definen sobre la base de los criterios clínicos de consenso6 y se diferencian en función de características clínicas recogidos en ellos. En los últimos años, son numerosos los autores13,30,31 que apuestan por un cambio de paradigma en el abordaje del delírium en personas mayores, y que enfatizan la necesidad de desarrollar nuevos criterios formales de definición y abordaje de los síndromes geriátricos en general, y delírium entre ellos en concreto, ya que existe mucha polémica sobre si este es un síndrome en sí mismo o es un marcador de fragilidad en la persona de edad avanzada31,32.
Esta revisión tenía el objetivo de determinar si, como ya apuntaba Cunningham10, existe relación entre estas dos grandes patologías geriátricas. O dicho de otro modo, si el impacto de haber sufrido uno o varios episodios de delírium es un factor de riesgo para el posterior desarrollo de demencia.
Para ello se ha llevado a cabo una búsqueda exhaustiva de todos los artículos científicos encontrados en las bases de datos PsycInfo, PubMed y Psicodoc que hacían referencia a este tema, y se ha hecho la lectura completa de los que cumplían los criterios de inclusión de esta revisión. A continuación, se extrajo la información necesaria y se hicieron las pruebas estadísticas pertinentes con el fin de observar qué relación existía entre ambas variables (delírium y demencia).
En el presente metaanálisis se ha evidenciado que el hecho de haber padecido un síndrome confusional agudo en el pasado es un importante factor de vulnerabilidad a tener en cuenta en el desarrollo de demencia posterior en personas mayores. Estos resultados parecen ser lógicos, ya que algunos mecanismos de los estudiados hasta ahora y etiquetados de ser factores de riesgo para la demencia, lo son también para el delírium33,34,35.
Estos hallazgos pueden ser de utilidad en el futuro para establecer una prevención secundaria, de cara a las personas mayores que sufran un episodio de síndrome confusional agudo, para estar alerta tanto a nivel individual como sociofamiliar y socioambiental, y tratar de empezar cuanto antes actividades profilácticas para el mantenimiento de las capacidades mentales. También, a nivel más general, puede ser útil para la creación de planes específicos de acción preventiva orientados a estos pacientes que, como hemos visto, tienen un mayor riesgo de desarrollar demencia.
Para finalizar, han sido varias las limitaciones que se han encontrado a lo largo de este trabajo. En primer lugar, la búsqueda de información se ha realizado únicamente en las lenguas inglesa y castellana, aunque la mayoría de la literatura especializada esté escrita en estas lenguas, puede haberse obviado algún artículo escrito en alguna otra lengua. El hecho de que los pacientes no provinieran del mismo origen (unos eran pacientes de fractura de cadera, otros de la UCI, etc.) puede haber sesgado en alguna medida los resultados, ya que también había pacientes de población general y estos tienen menos probabilidades de desarrollar un episodio de delírium que los hospitalizados. Además, algunas de las muestras tienen un tamaño de muestra pequeña en comparación con otros artículos, donde la muestra máxima es de 553 y la mínima es de Lo mismo pasa con el tiempo de seguimiento, en el cual el más corto es de 1,3 meses y el más largo es de 2 años. Por último, este estudio iba enfocado a personas con más de 65 años de edad, lo que incluye un gran rango de edades, lo que podría haber creado diferencias entre los grupos debido a la diferencia de esta variable.


















