INTRODUCCIÓN
El estrés psicológico, aunque nos ha salvado la vida como especie durante siglos, puede tener efectos devastadores en la salud1. Este, además de relacionarse con trastornos psicopatológicos es un buen predictor de enfermedades cardiovasculares, inmunes y endocrinas2.
El estrés perinatal, aquel que ocurre en torno al embarazo, conlleva grandes modulaciones endocrinas e importantes repercusiones sobre la salud3,4,5,6. Estudios longitudinales han evidenciado que los cambios ocurridos en el eje Hipotalámico-Pituitario-Adrenal (HPA) durante el embarazo producen alteraciones en la futura madre y en el feto que pueden perdurar hasta la edad adulta7 (figura 1). Los niveles de cortisol materno están mediados por la concentración de hormona liberadora de corticotropina (CRH) hipofisaria y placentaria, que elevan los niveles de cortisol a lo largo de la gestación, disminuyendo los mismos tras el parto8. Distintos grados de activación del eje HPA se relacionan con diferentes estados de salud física y psicológica durante el embarazo, lo que afecta al normal curso del mismo, así como a diferentes resultados en el desarrollo del parto y puerperio9.
Múltiples observatorios e instituciones relacionadas con la Salud Pública nacional e internacional incluyen en sus protocolos el control del estrés y ansiedad perinatal10,11,12.
El objetivo de este artículo fue presentar el protocolo del estudio longitudinal sobre el efecto del estrés perinatal desde la concepción hasta un año de vida en España. Este artículo sigue las recomendaciones de la declaración de la iniciativa STROBE (Strengthening the Reporting of Observational Studies in Epidemiology) para la comunicación de estudios de cohortes en epidemiología observacional analítica13.
El estrés psicológico y la activación del eje hipotalámico hipofisario adrenal (HPA). El estrés psicológico durante el embarazo se ha relacionado con consecuencias negativas para la madre y su descendencia14. Como parte de la respuesta al estrés, el cortisol prepara al organismo para soportar y superar un estímulo estresante. En parte debido a la presencia de la placenta, el eje HPA está profundamente alterado durante la gestación. La placenta, órgano endocrino de origen fetal, favorece la secreción de cortisol15. Además, durante el embarazo aumenta de tamaño la glándula pituitaria y aumenta la producción de cortisol desde la glándula adrenal8. Sin embargo, algunos estudios afirman que la percepción del estrés por la mujer embarazada no se correlaciona con la secreción de cortisol en sangre ni con prematuridad16, mientras otros sugieren que ciertos niveles de estrés durante el embarazo pueden incluso favorecer un más rápido desarrollo cognitivo y motor en la descendencia17.
Estrés perinatal materno y sus consecuencias en el feto y el bebé. Modelos animales han encontrado relación entre estrés materno y la activación del eje HPA en su descendencia. Estos estudios mimetizan los efectos del estrés prenatal administrando a las hembras embarazadas corticoides y comprobando posteriormente sus efectos18,19. Así, se propone que altos niveles de estrés materno aumentan los niveles de cortisol en la madre, que al atravesar la placenta pueden afectar al desarrollo del cerebro fetal3.
Niveles elevados de estrés materno durante el embarazo se relacionan con que sus bebés tendrán un mayor riesgo de alteraciones del neurodesarrollo, asma, bajo peso al nacer, prematuridad, autismo e incluso un mayor riesgo de esquizofrenia en la edad adulta3,8,20. Por otro lado, factores asociados con la duración de la lactancia materna pueden favorecer un mejor desarrollo cognitivo y motor de los bebés21.
La evaluación de los niveles de cortisol materno se ha llevado a cabo en diferentes medios, como sangre, orina y líquido amniótico. Estas medidas informan de la cantidad de cortisol en un momento concreto mediante técnicas invasivas y están influenciadas por variables contextuales. Sin embargo, la medición de cortisol en pelo ofrece una serie de ventajas como informar de los niveles de estrés crónico de forma retrospectiva22. Esta técnica innovadora, es altamente recomendada como método no invasivo y efectiva en la evaluación de la activación del eje HPA en la mujer embarazada al no estar influenciada por variables situacionales ni ritmos circadianos23,24. Además, por su carácter no invasivo y retrospectivo, es también aplicable a recién nacidos, ya que puede informar de los niveles de estrés a los que han estado expuesto durante su vida intrauterina25.
Objetivos:
Estudiar la relación entre la secreción de cortisol (ej. HPA) en pelo materno y distintas variables de salud psicológica en la mujer embarazada a lo largo de los 3 trimestres de embarazo, parto y puerperio.
Describir si existe asociación entre los niveles de cortisol en pelo materno y la salud física (pre-eclampsia, diabetes gestacional, etcétera) en la mujer embarazada durante los 3 trimestres de embarazo, parto y puerperio.
Comprobar la relación existente entre el cortisol en pelo de la mujer a lo largo de todo el embarazo, lactogénesis y duración de lactancia materna.
Estudiar la relación entre la secreción de cortisol (ej. HPA) en pelo materno a lo largo del embarazo con diferentes variables fetales: longitud del fémur, circunferencia abdominal, diámetro bi-parietal, peso estimado y riesgo de cromosomopatías.
Estudiar la asociación entre la secreción de cortisol (ej. HPA) en pelo materno a lo largo del embarazo con diferentes variables de salud neonatal: semanas de gestación al nacimiento, peso al nacer, diámetro cefálico, diámetro torácico, talla y test de Apgar.
Comprobar la relación entre los niveles de cortisol en pelo materno durante todo el embarazo con los niveles de cortisol en el neonato en el puerperio.
Analizar si la secreción de cortisol de la madre durante todo el embarazo, así como su perfil psicopatológico, el cortisol del pelo del bebé al nacer y el cortisol de la madre en los meses posteriores son predictores del temperamento, estrés y neurodesarrollo del bebé a la edad de 6 y 12 meses.
SUJETOS Y MÉTODOS
Diseño. Estudio prospectivo de cohortes de base poblacional, en el que se evalúa a las mujeres embarazadas y a los fetos durante el primer, segundo, tercer trimestre de embarazo y en el puerperio. Además se realizará un seguimiento de los bebés a los 6 y 12 meses de edad.
El tamaño muestral se calculó con el programa G*Power 3.1.326, para una potencia estadística del 80%, poder detectar diferencias estadísticamente significativas en el contraste de la hipótesis nula H :μ1=μ2 para 2 muestras independientes y asumiendo un nivel de significación del 5%. Con estos datos se estimó un tamaño muestral de 807 mujeres embarazadas.
Se capta a las embarazadas durante el primer trimestre de gestación en las consultas de control del embarazo de los centros de atención primaria. Posteriormente se les entrega el documento con la información del estudio y el consentimiento informado, que deben leer, entender y firmar.
Los criterios de inclusión fueron mujeres embarazadas en el primer trimestre de gestación, mayores de 18 años y con un alto nivel del idioma castellano. Se excluyeron a las que padecían alguna enfermedad previa al embarazo.
El estudio comenzó en enero de 2016 y pretende tener una duración de 3 años. La selección de participantes se llevará a cabo durante 21 meses para asegurar la inclusión del total de la muestra.
Las instituciones colaboradoras de este estudio son la Universidad de Granada, el Centro de Investigación Mente, Cerebro y Comportamiento (CIMCYC), centro de salud Góngora (Granada), centro de salud Mirasierra (Granada), Hospital Clínico (Granada), Agencia Pública Empresarial Sanitaria Poniente de El Ejido (Almería), centro de salud Roquetas de Mar (Almería), Hospital Comarcal Antequera y Queen´s University Belfast.
Medidas. Para valorar la exposición al estrés se utilizan las medidas de cortisol en pelo, que se toman y analizan en concordancia con las guías recomendadas23,24. Para la obtención de la muestra de pelo se toma un pequeño mechón de la parte posterior de la cabeza, de un diámetro de medio centímetro, cortándose lo más cerca posible de la base del cráneo. La muestra se introduce en un pliego de papel de aluminio y lo introducimos en una bolsa de plástico con auto-cierre correctamente identificada con el código asignado a cada participante. Finalmente, se entrega en el laboratorio colaborador para su análisis mediante método ELISA. En el momento del nacimiento se toma también una muestra de pelo del neonato siguiendo el mismo protocolo que el descrito. El procedimiento de toma de muestra de pelo es un método no invasivo, que no supone realizar ningún daño a los participantes y que está descrito en varios estudios23,24.
Los datos sociodemográficos y obstétricos se obtienen de la historia de salud de cada una de las mujeres seleccionadas. La valoración de variables psicopatológicas y de estrés psicológico se basa en las escalas que se muestran en el anexo 1.
Con el propósito de evaluar la variables fetales, se usan las técnicas ecográficas y screening bioquímico de cromosomopatías que se indican en el Documento de Salud de la Embarazada27. En lo referente a variables ecográficas fetales, se evalúan los siguientes: biometría fetal en tres momentos diferentes, una por cada trimestre donde los principales parámetros que se calculan son: CRL (mm), longitud cráneo-caudal, TN (mm) translucencia nucal, DBP (mm) diámetro biparietal, LF (mm) longitud del fémur, peso (gramos), circunferencia abdominal, estática fetal (posición, presentación). De estas medidas se obtienen los siguientes índices: longitud, circunferencia cefálica, circunferencia abdominal y peso estimado. En lo que respecta al screening bioquímico de cromosomopatías, se valoran translucencia nucal (mm), CRL (mm), MoM Beta HCG-libre (Ul/L), MoM PAPP-A (Ul/L), MoM translucencia nucal y presencia o ausencia de hueso nasal. Estos parámetros generan tres índices de riesgo de cromosopatías: Índice Riesgo Síndrome de Down, Índice Riego Síndrome Edwards, Índice Riesgo Síndrome Patau. Esta prueba se realiza entre las semanas 10 y 12 de embarazo.
En lo referente a datos del parto y nacimiento se toman de las historias de salud de las mujeres embarazadas.
Para la valoración de los bebés a los 6 y 12 meses se usan las escalas de neurodesarrollo y conductuales que aparecen en el anexo 2.
Análisis estadístico. El análisis de los datos se lleva a cabo mediante χ2 y t-student para evaluar si existen diferencias estadísticamente significativas en las variables descriptivas. Las variables longitudinales se analizan mediante ANOVA de medidas repetidas, incluyendo como covariables las variables estadísticamente significativas en el análisis descriptivo de los datos. Igualmente, el uso de regresión múltiple informa de las variables de salud, psicológicas y de niveles de cortisol en pelo durante el embarazo que pueden predecir niveles de cortisol en pelo en recién nacidos, y niveles de temperamento y neurodesarrollo en los bebés a los 6 y 12 meses de edad.
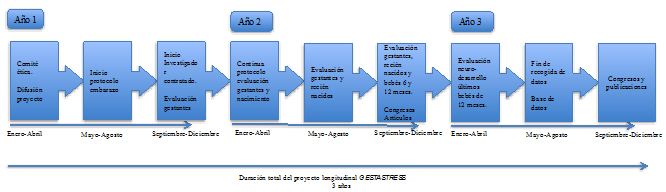
Cronograma. El cronograma del estudio desde su inicio en Enero de 2016 y con una duración de 3 años se muestra en la figura 2.
Consideraciones éticas. El protocolo de este estudio ha sido evaluado favorablemente por el Comité de Ética en Investigación Humana de la Universidad de Granada, el Comité de Ética de Centro de Granada y la conformidad de la dirección del Distrito Sanitario de Poniente de Almería.
Posibles impactos. La implantación de la técnica de cortisol en pelo, que actualmente solo se realiza en 5 centros de investigación en el mundo y no se ha realizado hasta ahora en España, supondrá un gran avance. Mediante esta técnica será posible medir el cortisol de las mujeres embarazadas a lo largo de los 3 trimestres. Además, es una gran innovación la posibilidad de valorar mediante la extracción de cortisol en pelo del bebé sus niveles de estrés intrauterino en el último trimestre y de forma inocua y no invasiva. Estudiaremos su relación con el estrés de la madre y con su posterior neurodesarrollo y temperamento.
Los resultados encontrados serán de gran importancia en el ámbito de la Salud Pública al permitir establecer puntuaciones promedio de cortisol en pelo de las mujeres embarazadas y sus bebés, para así hacer un screening de estrés en esta población y permitir su intervención. Estos factores tienen importantes implicaciones económicas en el sistema de salud a corto plazo y en la sociedad en general a largo plazo. Futuras investigaciones pueden incluir en sus protocolos la influencia del estrés fisiológico y psicológico durante el embarazo sobre determinantes tóxicos, nutricionales y genéticos en la salud maternal y en el desarrollo fetal e infantil35.