Introducción
La enfermedad cerebrovascular (ECV) es una patología causada por un trastorno de la circulación sanguínea a nivel cerebral, que ocasiona alteraciones permanentes o temporales en el funcionamiento total o parcial del cerebro1. La ECV es muy prevalente en la sociedad actual. Según la Sociedad Española de Neurología (SEN), esta patología afecta a 110.000-120.000 personas al año en España, especialmente en edades avanzadas. Según los datos aportados por el Instituto Nacional de Estadística (INE), en el año 2018 las ECV fueron la cuarta causa de muerte en la población general, observándose un progresivo incremento a partir de los 40-45 años. Además, se prevé que la incidencia de este grupo de patologías se incremente, como consecuencia del envejecimiento poblacional. En este sentido, la Organización Mundial de la Salud (OMS) augura un aumento de la incidencia del ictus de un 27% en los próximos 25 años2,3.
Tras una ECV, los pacientes que sobreviven al evento sufren importantes secuelas físicas y mentales, lo que se traduce en un aumento del gasto sanitario y, a nivel personal, un cambio radical en su situación funcional que influye en el entorno social. Entre las secuelas más frecuentes son destacables los déficits motores totales o parciales, las alteraciones sensitivas y del lenguaje, la fatiga, la osteoporosis, las caídas/fracturas, la espasticidad, la incontinencia urinaria, las contracturas, la depresión, la ansiedad, la demencia, las alteraciones de la memoria, los déficits de atención o la disfunción sexual, entre otras1,4,5.
Las oclusiones arteriales de gran vaso (OAGV) son un tipo de infarto cerebral, es decir, una ECV isquémica con déficit neurológico mantenido durante más de 24 horas, de causa aterotrombótica que ocasiona una oclusión de arterias de gran calibre. Las arterias consideradas de gran calibre, a nivel intracraneal, son la arteria carótida interna intracraneal, la arteria vertebral intracraneal, la arteria basilar y/o las arterias cerebrales proximales posterior, media y anterior1,4,6-8.
Las OAGV tienen una alta prevalencia dentro de los ictus isquémicos agudos. Rai y col9 estimaron una incidencia anual de OAGV del 24 % por cada 100.000 habitantes. Rennert y col7 y Bathia y col10 afirmaron que estas oclusiones se asociaban a una mayor morbimortalidad y peor pronóstico. Por este motivo, y teniendo en cuenta que la ECV es una urgencia neurológica tiempo dependiente, es esencial la instauración temprana del tratamiento pertinente. La evidencia científica demuestra que, para pacientes con OAGV, el tratamiento más efectivo es la trombectomía, con o sin tratamiento fibrinolítico asociado, aunque algunos autores, como Bathia y col10 demostraron que el tratamiento trombolítico con activador tisular plasminógeno (Tissue Plasminogen Activator, t-PA) no es muy efectivo porque presenta resistencia a la trombólisis farmacológica. En definitiva, para determinar el tratamiento óptimo (trombectomía o fibrinolisis) y planificar el traslado del paciente al centro mejor capacitado, es conveniente emplear escalas de OAGV.
En el ámbito extrahospitalario, se emplean diversas escalas que predicen la presencia de una OAGV, como Melbourne Ambulance Stroke Scale (MASS)11, Los Angeles Motor Scale (LAMS)12 o Rapid Arterial oCclusion Evaluation (RACE)13; esta última es el instrumento de elección por los servicios de emergencias sanitarias españoles. Al igual que MASS y LAMS, RACE permite identificar la gravedad del estado de los pacientes con sospecha de una ECV isquémica aguda, y reconocer aquellos que, con alta probabilidad, estén sufriendo una OAGV, a fin de seleccionar el tratamiento adecuado y su traslado al centro médico mejor capacitado para su tratamiento. La escala RACE valora cinco ítems (parálisis facial, paresia braquial, paresia crural, desviación oculocefálica y afasia/agnosia), obteniéndose una puntuación final que oscila entre 0 y 9; con puntuaciones superiores a 4 se sospecha, con alta probabilidad, la existencia de una OAGV13.
Debido a que una de las características esenciales de los equipos de emergencias sanitarias es el trabajo en equipo, es fundamental ampliar los conocimientos y habilidades necesarios para el manejo y empleo de estos instrumentos, especialmente de la escala RACE que es la empleada por los servicios de emergencias españoles, permitiendo una prestación óptima de servicios a la población general.
El objetivo de esta revisión fue comparar el valor predictivo de la escala RACE con el de otras escalas destinadas al ámbito extrahospitalario para reconocer la presencia de una OAGV en pacientes que sufren una ECV, con la finalidad de seleccionar el tratamiento más beneficioso para el paciente y su traslado al centro médico mejor capacitado.
Material y métodos
Se ha realizado una revisión rápida (Rev Rap) sobre la evaluación de escalas prehospitalarias destinadas a la detección de una OAGV en pacientes que han sufrido una ECV, centrando la investigación, especialmente, sobre la escala RACE.
En la actualidad no existe consenso para el término Rev Rap, aunque para algunos autores deben seguir la metodología de las revisiones sistemáticas convencionales (RS) a fin de mantener la calidad de los resultados obtenidos, evitando el sesgo de inclusión y realizando una exhaustiva evaluación y síntesis de los estudios, por lo que las principales conclusiones de las Rev Rap y de las RS no difieren significativamente14,15,17-19. Sin embargo, las Rev Rap permiten simplificar etapas respecto a las RS, pudiendo completarse en un periodo inferior a seis meses manteniéndose el rigor metodológico19, lo que se logra limitando las fuentes de información, realizando el cribado de los estudios un único evaluador, o no evaluando la calidad de los estudios incluidos. También suelen ser menos extensas y su lenguaje no suele ser tan técnico.
Se decidió realizar este tipo de revisión porque se disponía de escaso tiempo y, además, se trata de un tema de investigación crítico del que se necesitan revisiones en profundidad. Se siguieron las directrices de un protocolo preestablecido para las Rev Rap14,15 (exceptuando la evaluación del riesgo de sesgo) y de la declaración PRISMA (Preferred Reporting Items of Systematic Reviews and Meta-Analyses Guidelines)16.
La elaboración de la pregunta de investigación central de esta Rev Rap siguió el esquema PICO:
- P - población: Pacientes con una oclusión arterial de gran vaso (OAGV) en los que se ha empleado una escala para su valoración.
- I - intervención: Utilización de la Escala Rapid Arterial oCclusion Evaluation (RACE).
- C - comparación: Diferentes escalas destinadas a la valoración de pacientes que sufren una OAGV.
- O - resultado (outcome): Rendimiento predictivo y utilidad de la escala RACE.
Resultando: ¿la escala RACE es un instrumento válido en la valoración de pacientes que sufren una OAGV, comparando su valor predictivo con el de diferentes escalas destinadas al mismo fin?
La búsqueda de artículos se llevó a cabo en la base de datos de MEDLINE vía PubMed hasta el 3 de enero de 2020. Las palabras clave seleccionadas, según la terminología MeSH (Medical Subject Headings), se combinaron en dicha base de datos junto con los operadores booleanos AND y OR. La ecuación de búsqueda seleccionada reproducible fue la siguiente: (“stroke” [MeSH Terms] OR “stroke” [All Fields]) AND (“occlusion” [All Fields]) AND (“emergencies” [MeSH Terms] OR “emergencies”[All Fields] OR “emergency” [All Fields]) AND (“humans” [MeSH Terms] AND English[lang]).
Se incluyeron artículos en inglés sobre la validez y fiabilidad de escalas de uso extrahospitalario empleadas para detectar una OAGV.
Se recopilaron los conceptos de OAGV proporcionadas por los autores de los diferentes estudios incluidos en esta revisión y se extrajeron los siguientes datos:
- autor, país, año de publicación, características de la muestra (tamaño, edad, sexo y diagnóstico), diseño epidemiológico y duración del estudio, escalas evaluadas, puntos de corte (PC), intérpretes y principales resultados;
- principales ítems y puntaciones de las escalas clínicas para predecir OAGV;
- rendimiento predictivo de las escalas: precisión, sensibilidad (S), especificidad (E), valor predictivo positivo (VPP), valor predictivo negativo (VPN), curvas ROC (Receiver Operating Characteristic) y área bajo la curva (area under the curve), razón de verosimilitud positiva (RVP), razón de verosimilitud negativa (RVN), coeficiente de correlación (r / rho) y otros estimadores estadísticos de interés.
Resultados
La estrategia de búsqueda recuperó 562 artículos. Tras la revisión de los títulos y, posteriormente, los resúmenes de estos, se preseleccionaron 36 publicaciones. Tras la lectura completa de estos manuscritos y aplicando los criterios de inclusión mencionados anteriormente, se seleccionaron 16 artículos. Además, se realizó una búsqueda inversa mediante la revisión manual de la lista de referencias de cada uno de los artículos seleccionados previamente, incorporándose otros cuatro estudios que cumplían dichos criterios. La Figura 1 muestra el diagrama de flujo que detalla el proceso de selección de artículos, elaborado a partir de la metodología PRISMA16.
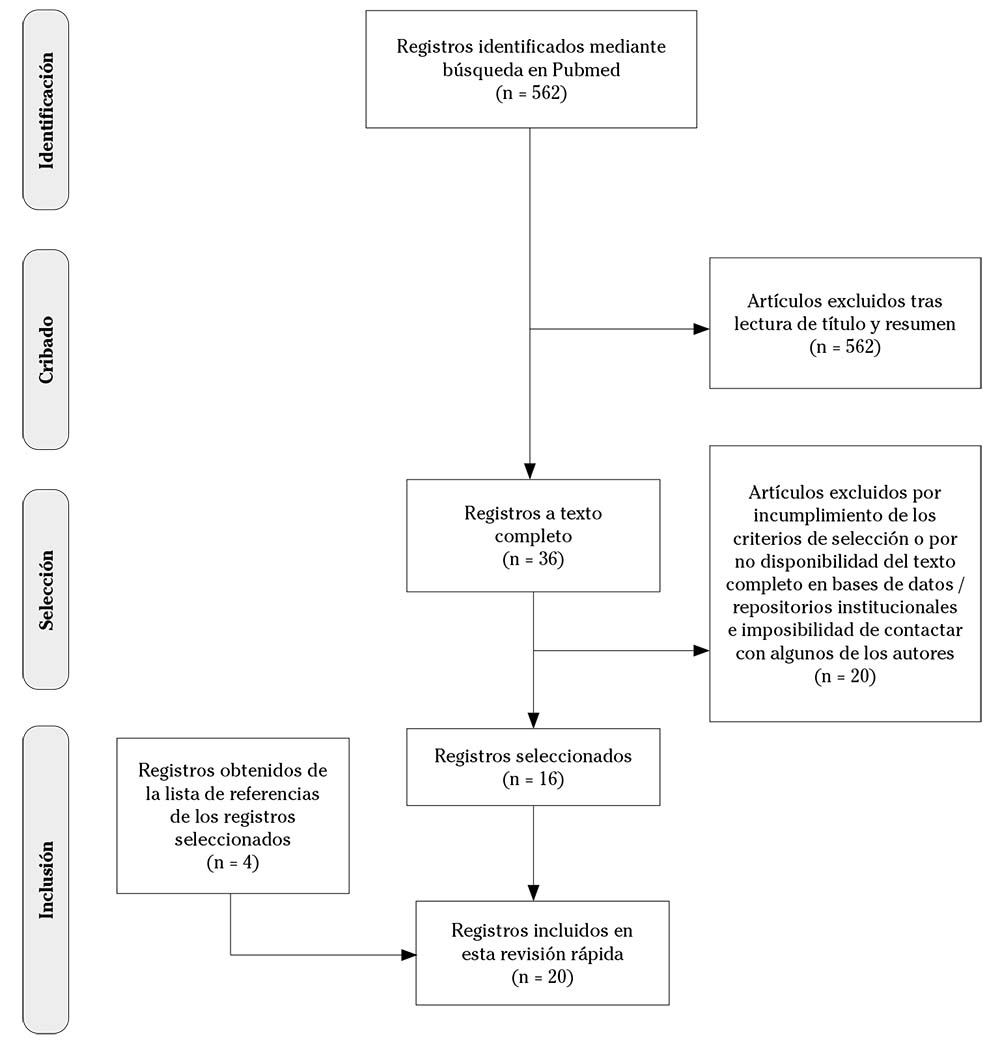
Figura 1. Diagrama de flujo del proceso de búsqueda y selección de artículos según la metodología PRISMA.
En la Tabla 1 se muestran las características (tamaño de muestra, diseño epidemiológico, duración, escala e intérpretes) y principales resultados de los 20 artículos incluidos en esta revisión.
Tabla 1. Tamaño y características de la muestra, diseño y duración de los estudios, escalas evaluadas e intérpretes de estas, y principales resultados de los artículos incluidos
| Autor/País/Año | Tamaño/Edad media (DE)/% hombres/Diagnóstico | Diseño/Duración | Escala y PC Evaluadores | Principales resultados |
|---|---|---|---|---|
| Singer y col | n: 171 | Cohortes retrospectivo | 3I-SS ≥4 | Diseño y validación de la escala 3I-SS, demostrando su eficacia en la identificación de una OAGV. Evaluación de la NIHSS, fuertemente correlacionada con la 3I-SS. |
| Alemania | 68 (15) | 11 meses | NIHSS ≥14 | |
| 200535 | 64% | - | URG (neur) | |
| - | sospecha de ECV | - | - | |
| Nazliel y col | n: 119 | Cohortes retrospectivo | LAMS ≥4 | Evaluación de las escalas LAMS y NIHSS. Buen rendimiento de LAMS para predecir una OAGV pero ligeramente inferior al de la NIHSS. |
| EEUU | 67 (18) | - | NIHSS ≥11 | |
| 200832 | 45% | - | URG (neur) | |
| - | ECVI | - | - | |
| Pérez y col | n: 357 | Cohortes ambispectivo | RACE ≥5 | Valoración de las escalas RACE y NIHSS. Ambas eran capaces de predecir una OAGV con una precisión similar. |
| España | 73 (13) | 24 meses | NIHSS ≥11 | |
| 201313 | 54% | - | SEM (TES) | |
| - | sospecha de ECV | - | - | |
| Katz y col | n: 624 | Cohortes retrospectivo | CPSSS ≥2 | Diseño y validación de la escala CPSSS. Buen rendimiento para predecir una OAGV y orienta sobre la gravedad de la ECV. |
| EEUU | - | - | URG (neur) | |
| 201533 | - | - | - | |
| - | ECVI | - | - | |
| Cooray y col | n: 11.632 | Cohortes retrospectivo | NIHSS ≥11 | Evaluación de la escala NIHSS. Precisión ligeramente superior al resto de escalas para predecir una OAGV. Fuerte relación con mRS. |
| Europa | 68,2 | - | URG (neur) | |
| 201538 | 56,40% | - | - | |
| - | ECVI | - | - | |
| Lima y col | n: 727 | Cohortes prospectivo | FAST-ED | Validación de la escala FAST-ED. Precisión comparable a NIHSS para predecir una OAGV. Predice el grado de dependencia funcional de los pacientes. |
| EEUU | 68,1 (15,4) | - | ≥4 y ≥3 | |
| 201621 | 52% | - | URG (neur) | |
| - | ECVI | - | - | |
| Kummer y col | n: 664 | Cohortes retrospectivo | CPSSS ≥2 | Diseño y validación de la escala CPSSS. Gran capacidad discriminante para predecir una oclusión y una ECV grave. |
| EE UU | 68,4 (10) | 12 meses | URG (neur) | |
| 201631 | 54% | - | - | |
| - | ECVI | - | - | |
| Hastrup y col | n: 3.127 | Cohortes retrospectivo | PASS | Diseño y validación de la escala PASS. Precisión similar a otras escalas de uso extrahospitalario para predecir una OAGV. |
| Dinamarca | 69 (14) | - | URG (neur) | |
| 201636 | 60% | - | - | |
| - | ECVI | - | - | |
| Vanacker y col | n: 848 | Cohortes retrospectivo | ASTRAL ≥16 | Creación de la escala ASTRAL para mejorar el rendimiento de NIHSS añadiendo variables. Buen poder discriminatorio respecto al uso exclusivo de NIHSS. |
| Suiza | 59-79 | - | NIHSS ≥ 10 | |
| 201620 | - | - | URG (neur) | |
| - | ECV | - | - | |
| Purrucker y col | n:1.430 | Cohortes retrospectivo | sNIHSS-EMS | Diseño y evaluación de la escala sNIHSS-EMS. Buen rendimiento para predecir una OAGV, y permite orientar sobre la gravedad de la ECV. |
| Alemania | - | 24 meses | ≥6 | |
| 201727 | - | - | SEM | |
| - | sospecha de ECV | - | - | |
| Teleb y col | n: 62 | Estudio piloto prospectivo | VAN | Desarrollo y evaluación de la escala VAN. Su precisión para predecir una OAGV es comparable al de NIHSS. |
| EEUU | - | - | SEM (enf) | |
| 201726 | - | - | - | |
| - | sospecha de ECV | - | - | |
| Andsberg y col | n: 78 | Estudio piloto | Pre-HAST ≥2 | Diseño y validación de la escala Pre-HAST. Similar rendimiento para predecir una OAGV al de NIHSS y permite orientar sobre la gravedad de la ECV. |
| Suecia | - | 12 meses | SEM (enf) | |
| 201729 | - | - | - | |
| - | sospecha de ECV | - | - | |
| Suzuki y col | n: 413 | Cohortes prospectivo | ELVOs | Diseño y validación de la escala ELVOs. Precisión en la identificación de una OAGV similar a otras escalas, ligeramente inferior a NIHSS. |
| Japón | 74 (13) | 12 meses | SEM (param) | |
| 201823 | 57% | - | - | |
| - | sospecha de ECV | - | - | |
| Richards y col EE. UU | n: 138 | Cohortes retrospectivo | CPSS = 3 | Evaluación de la escala CPSS. Gran precisión para predecir una OAGV. Rendimiento era comparable a NIHSS. |
| 201822 | 69 (58-81)* | 24 meses | SEM (param) | |
| - | 50,70% | - | - | |
| - | ECVI | - | - | |
| Zhao y col Australia | n: 162 | Cohortes retrospectivo | ACT-FAST | Diseño y validación de la escala ACT-FAST. Buen rendimiento para identificar una OAGV, comparable al de otras escalas, incluida NIHSS. |
| 201837 | 69 | 10 meses | SEM (param) | |
| - | 49,10% | - | - | |
| - | sospecha de ECV | - | - | |
| Noorian y col | n: 94 | Cohortes prospectivo | LAMS ≥4 | Evaluación de las escalas LAMS y Glasgow (GCS) para predicción de una OAGV. Bajo rendimiento y pobre precisión, respectivamente. |
| EEUU | 70 (13) | - | URG (neur) | |
| 201834 | 51% | - | - | |
| - | ECV | - | - | |
| Carrera y col | n: 1.822 | Estudio observacional | RACE ≥5 | Evaluación de la escala RACE. Buena capacidad para identificar una OAGV con precisión similar a NIHSS. |
| España | - | 12 meses | SEM | |
| 201824 | - | - | - | |
| - | sospecha de ECV | - | - | |
| Václavík y col | n: 435 | Estudio multicéntrico prospectivo | FAST-PLUS | Diseño y evaluación de la escala FAST-PLUS. Rendimiento para predecir una OAGV comparable al de NIHSS y ligeramente superior al de otras escalas. |
| República Checa | 73 | - | SEM (param) | |
| 201830 | 51% | - | - | |
| - | sospecha de ECV | - | - | |
| Jumaa y col | n: 1.639 | Cohortes prospectivo | RACE ≥5 | Validación de la escala RACE. Buen rendimiento para identificar una OAGV, ligeramente inferior al de la NIHSS. |
| EEUU | 73 (63-82)* | 36 meses | SEM | |
| 201925 | 44,50% | - | - | |
| - | sospecha de ECV | - | - | |
| Vidale y col | n: 145 | Estudio piloto | LARIO-SS >3 | Validación de la escala LARIO-SS para identificar una OAGV. Alto rendimiento, comparable a NIHSS y superior a otras escalas. |
| Italia | 75 (11) | 12 meses | SEM (enf) | |
| 201928 | 60,70% | - | - | |
| - | sospecha de ECV | - | - |
DE: desviación estándar; PC: punto de corte; *: mediana (rango intercuartílico); ECV: enfermedad cerebrovascular; ECVI: enfermedad cerebrovascular isquémica; OAGV: oclusión arterial de gran vaso; URG: urgencias; SEM: servicio de emergencias médicas; neur.: neurólogo; TES: técnico de emergencias sanitarias; enf: enfermero; param.: paramédico.
3I-SS : 3-Items Stroke Scale ; ACT-FAST : Ambulance Clinical Triage-Face, Arms, Speech and Time;ASTRAL : Acute STroke Registry and Analysis of Lausanne; CPSS : Cincinnati Prehospital Stroke Scale; CPSSS : Cincinnati Prehospital Stroke Severity Scale; ELVOs : Emergent Large Vessel Occlusion screen; FAST-ED : Field Assessment Stroke Triage for Emergency Destination; FAST-PLUS : Face, Arms, Speech and Time modified Test; GCS : Glasgow Coma Scale; LAMS: Los Angeles Motor Scale; LARIO-SS : Large ARtery Intracranial Occlusion Stroke Scale; mRS: modified Rankin Scale; NIHSS: National Institutes of Health Stroke Scale; PASS : Prehospital Acute Stroke Scale; Pre-HAST: Pre-Hospital Ambulance Stroke Test; RACE : Rapid Arterial oCclusion Evaluation; sNIHSS-EMS : shortened National Institutes of Health Stroke Scale for Emergency Medical Services; VAN : Vision, Aphasia, Neglect.
Los autores expusieron diferentes definiciones de OAGV. Algunos de ellos, como Vanacker y col20 o Lima y col21, nombraron bajo este término a aquellas oclusiones que afectan a la arteria basilar, la carótida interna y el segmento proximal de la arteria cerebral media. En cambio, otros, como como Richards y col22 o Suzuki y col23, ofrecieron una definición más amplia, incluyendo aquellos bloqueos que se producían en la arteria cerebral posterior y la cerebral anterior. Algunos autores demostraron que las puntuaciones más elevadas de las escalas correspondían a OAGV y, una parte significativa, a hemorragias intracraneales e imitadores de ECV13,23-25. Además, observaron una diferencia importante en las puntuaciones en función del lugar donde se había producido la oclusión; la mayoría de estos bloqueos afectaron a la arterial cerebral media y la arteria carótida interna intracraneal21,23-27.
En cuanto a la población a estudio y los intérpretes de las escalas clínicas, como se puede observar en la Tabla 1, nueve de los 20 estudios incluidos se realizaron en poblaciones con diagnóstico confirmado de ECV isquémica, siendo los intérpretes neurólogos de los servicios de urgencias20-22,31-34,36,38. En cambio, el resto de los estudios, aplicaron las escalas en poblaciones con sospecha de ECV, siendo los intérpretes personal del servicio de emergencias sanitarias23-30,35,37, y solamente en tres de ellos se mencionó explícitamente al personal de enfermería26,28,29. En la mayoría de los artículos incluidos, los intérpretes de las escalas sometidas a estudio no recibieron ningún tipo de formación para aplicar dichos instrumentos, a excepción de seis de ellos, cuyos autores mencionaron haber impartido sesiones teóricas y/o prácticas a los intérpretes de estas13,25,26,28-30.
En total se encontraron 16 escalas de predicción de OAGV: National Institutes of Health Stroke Scale (NIHSS)20,25,32,35,38, Rapid Arterial oCclusion Evaluation (RACE)13,24,25, 3-Items Stroke Scale (3I-SS)35, Los Angeles Motor Scale (LAMS)32,34, Cincinnati Prehospital Stroke Severity Scale (CPSSS)31,33, Field Assessment Stroke Triage for Emergency Destination (FAST-ED)21, shortened National Institutes of Health Stroke Scale for Emergency Medical Services (sNIHSS-EMS)27, Cincinnati Prehospital Stroke Scale (CPSS)22, Large ARtery Intracranial Occlusion-Stroke Scale (LARIO-SS)28, Pre-Hospital Ambulance Stroke Test (Pre-HAST)29, Acute STroke Registry and Analysis of Lausanne (ASTRAL)20, Emergent Large Vessel Occlusion screen (ELVOs)23, Vision, Aphasia, Neglect (VAN)26, Face, Arms, Speech and Time modified Test (FAST-PLUS)30, Ambulance Clinical Triage-Face, Arms, Speech and Time (ACT-FAST)37, y Prehospital Acute Stroke Scale (PASS)36.
Todos los instrumentos descritos anteriormente se derivan de la escala NIHSS a excepción de FAST-PLUS y ACT-FAST, que se derivan del conocido método FAST, y LAMS, derivada de la escala prehospitalaria LAPSS. De todas ellas, solo NIHSS es de uso hospitalario, el resto están diseñadas para su aplicación en el entorno extrahospitalario. Tres de ellas fueron evaluadas en más de un estudio: RACE13,24,25, LAMS32,34 y CPSSS31,33, los mismos que evaluaron también el rendimiento de la escala hospitalaria NIHSS para predecir una OAGV.
En la Tabla 2 se resumen los ítems valorados por las 16 escalas de predicción de OAGV incluidas en esta revisión. Estas investigaciones demostraron que la función motora de las extremidades superiores era la variable que más fuertemente se asociaba con una OAGV; también señalaron otros ítems como predictores fundamentales de dicho evento, como la desviación de la mirada, la parálisis facial y la presencia de afasia y agnosia20,26-29,31,33,36,37.
Tabla 2. Ítems y puntuaciones de las escalas clínicas destinadas a la predicción de oclusiones arteriales de grandes vasos
| Items | NIHSS 38 | RACE 13,24,25 | 3I-SS 35 | LAMS 32,34 | CPSSS 31,33 | FAST-ED 21 | sNIHSS-SEM 27 | CPSS 22 | LARIO-SS 28 | Pre-HAST 29 | ASTRAL 20 | ELVOS 23 | VAN 26 | FAST-PLUS 30 | ACT-FAST 37 | PASS 36 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nivel de consciencia/ preguntas / órdenes | 0-7 | 0-2c | 0-1 | 0-3 | 0-2e | √ | ||||||||||
| Mirada | 0-2 | 0-1 | 0-2 | 0-2 | 0-2 | 0-2 | √ | √ | √√b | √ | ||||||
| Visión | 0-3 | 0-2 | √ | |||||||||||||
| Parálisis facial | 0-3 | 0-2 | 0-1 | 0-1 | 0-3 | 0-1 | 0-1 | 0-1 | √ | |||||||
| Función motora braquial | 0-8 | 0-2 | 0-1 | 0-2 | 0-1 | 0-2 | 0-8 | 0-1 | 0-1 | 0-4 | √ | √ | √ | √ | ||
| Función motora crural | 0-8 | 0-2 | 0-1 | 0-8 | 0-4 | √ | ||||||||||
| Ataxia | 0-2 | |||||||||||||||
| Sensibilidad | 0-2 | 0-2 | 0-2 | |||||||||||||
| Afasia /lenguaje | 0-3 | 0-2a | 0-2 | 0-3 | 0-1 | 0-2 | √ | √ | √ | √a | ||||||
| Disartria | 0-2 | 0-2 | 0-1 | |||||||||||||
| Agnosia /negligencia | 0-2 | 0-2b | 0-2 | 0-1 | 0-5 | √ | √ | √d | ||||||||
| Fuerza de agarre | 0-2 | 0-1 | ||||||||||||||
| NIHSS al ingreso | 0-42 | |||||||||||||||
| mRS ≤ 2 | 0-3 | |||||||||||||||
| Fibrilación auricular | 0-2 | |||||||||||||||
| Sexo femenino | 0-3 | |||||||||||||||
| Rango de puntuación | 0-42 | 0-9 | 0-6 | 0-5 | 0-4 | 0-9 | 0-29 | 0-3 | 0-5 | 0-19 | 0-55 | Positivo/negativo | ||||
mRS: Modified Rankin Scale; a: si hay hemiparesia derecha; b: si hay hemiparesia izquierda; c: solo nivel de consciencia; d: si hay desviación de la mirada; e: sólo órdenes motoras.
3I-SS : 3-Items Stroke Scale ; ACT-FAST : Ambulance Clinical Triage-Face, Arms, Speech and Time; ASTRAL : Acute STroke Registry and Analysis of Lausanne; CPSS : Cincinnati Prehospital Stroke Scale; CPSSS : Cincinnati Prehospital Stroke Severity Scale; ELVOs : Emergent Large Vessel Occlusion screen; FAST-ED : Field Assessment Stroke Triage for Emergency Destination; FAST-PLUS : Face, Arms, Speech and Time modified Test; GCS : Glasgow Coma Scale; LAMS: Los Angeles Motor Scale; LARIO-SS : Large ARtery Intracranial Occlusion Stroke Scale; mRS: modified Rankin Scale; NIHSS: National Institutes of Health Stroke Scale; PASS : Prehospital Acute Stroke Scale; Pre-HAST: Pre-Hospital Ambulance Stroke Test; RACE : Rapid Arterial oCclusion Evaluation; sNIHSS-EMS : shortened National Institutes of Health Stroke Scale for Emergency Medical Services; VAN : Vision, Aphasia, Neglect.
En la Tabla 3 se muestra el rendimiento diagnóstico (S, E, VPP, VPN, RVP y RVN, AUC y los coeficientes de correlación de cada una de las escalas analizadas en los estudios incluidos en esta Rev Rap. Los autores determinaron el umbral óptimo de cada instrumento para identificar pacientes con una OAGV mediante curvas ROC y, en algunos casos, el índice de Youden (J)13,24,25,31-34.
Tabla 3. Rendimiento predictivo de las escalas clínicas en la identificación de una oclusión arterial de gran vaso.
| Escala | PC | Prec | S | E | VPP | VPN | AUC (IC 95%) | RVP | RVN | Correlación (p) | J Youden |
|---|---|---|---|---|---|---|---|---|---|---|---|
| RACE13 | ≥5 | 0,72 | 0,85 | 0,68 | 0,42 | 0,94 | 0,82; 0,77-0,87 | rho= 0,76 <0,001 | |||
| RACE24 | ≥5 | 0,84 | 0,6 | 0,35 | 0,94 | 0,77; 0,75-0,80 | rho= 0,93 <0,001 | ||||
| RACE25 | ≥5 | 0,77 | 0,75 | 0,25 | 0,97 | 0,75; 0,73-0,77 | |||||
| 3I-SS35 | ≥4 | 0,86 | 0,67 | 0,92 | 0,74 | 0,89 | CCI= 0,95 | ||||
| LAMS32 | ≥4 | 0,85 | 0,81 | 0,89 | 0,74 | 0,89 | 0,85 | 7,36 | 0,2 | ||
| LAMS34 | ≥4 | 0,72 | 0,76 | 0,65 | 0,79 | 0,61 | 0,79 | 2,18 | 0,37 | ||
| NIHSS35 | ≥14 | 0,86 | 0,95 | 0,86 | 0,95 | ||||||
| NIHSS32 | ≥11 | 0,89 | 0,91 | 0,87 | 0,93 | ||||||
| NIHSS25 | ≥11 | 0,76 | 0,88 | 0,72 | 0,85; 0,81-0,89 | ||||||
| NIHSS38 | ≥11 | 0,65 | 0,65 | 0,64 | 0,65 | 0,68 | |||||
| NIHSS20 | ≥10 | 0,86 | 0,69 | 0,43 | 0,95 | 0,83 | |||||
| ASTRAL20 | ≥16 | 0,84 | 0,68 | 0,41 | 0,94 | 0,84 | |||||
| CPSSS31 | ≥2 | 0,7 | 0,87 | 5,3 | 0,3 | ||||||
| CPSSS33 | ≥2 | 0,83 | 0,4 | 0,67 | 1,38 | 0,42 | |||||
| FAST-ED21 | ≥3 | 0,76 | 0,71 | 0,78 | 0,62 | 0,84 | 0,81 (p<0,001) | ||||
| ≥4 | 0,79 | 0,6 | 0,89 | 0,72 | 0,82 | 0,49 | |||||
| sNIHSS-SEM27 | ≥6 | 0,77 | 0,7 | 0,81 | 0,7 | 0,81 | 0,81; 0,77-0,84 | 0,51 | |||
| Pre-HAST29 | ≥2 | 1 | 0,4 | 0,5 | 1 | 0,77; IC 95%: 0,66-0,88 | r= 0,92 | ||||
| ELVOs23 | 0,76 | 0,85 | 0,72 | 0,54 | 0,93 | rho= 0,74 <0,001 | |||||
| FAST PLUS30 | 0,93 | 0,47 | 0,41 | 0,94 | 0,65 | ||||||
| ACT-FAST37 | 0,92 | 0,85 | 0,93 | 0,53 | 0,99 | 0,9 | K= 0,61 (0,51-0,71) | ||||
| CPSS22 | =3 | 0,41 | 0,88 | 0,64 | 3,44 | 0,67 | K= 0,80 rho= 0,56 <0,001 | 0,29 | |||
| VAN26 | 1 | 0,9 | 0,74 | 1 | |||||||
| PASS36 | 0,73 | 0,61 | 0,83 | 0,66 | 0,8 | 0,72; IC 95%: 0,69-0,75 | 3,59 | 0,47 | |||
| LARIO-SS28 | >3 | 1 | 0,82 | 0,77 | 1 | 0,95; IC 95%: 0,90-0,98 | K= 0,96 <0,001 | ||||
PC: punto de corte; Prec: precisión; S: sensibilidad; E: especificidad; VPP: valor predictivo positivo; VPN: valor predictivo negativo; AUC: area under curve; IC 95%: intervalo de confianza al 95%; RVP: razón de verosimilitud positiva; RVN: razón de verosimilitud negativa; CCI: coeficiente de correlación intraclase; ROC: Receiver Operating Characteristic; K: coeficiente Kappa de Cohen; r: coeficiente de correlación de Pearson; rho: coeficiente de correlación de Spearman; J: índice J de Youden.
3I-SS : 3-Items Stroke Scale ; ACT-FAST : Ambulance Clinical Triage-Face, Arms, Speech and Time; ASTRAL : Acute STroke Registry and Analysis of Lausanne; CPSS : Cincinnati Prehospital Stroke Scale; CPSSS : Cincinnati Prehospital Stroke Severity Scale; ELVOs : Emergent Large Vessel Occlusion screen; FAST-ED : Field Assessment Stroke Triage for Emergency Destination; FAST-PLUS : Face, Arms, Speech and Time modified Test; GCS : Glasgow Coma Scale; LAMS: Los Angeles Motor Scale; LARIO-SS : Large ARtery Intracranial Occlusion Stroke Scale; mRS: modified Rankin Scale; NIHSS: National Institutes of Health Stroke Scale; PASS : Prehospital Acute Stroke Scale; Pre-HAST: Pre-Hospital Ambulance Stroke Test; RACE : Rapid Arterial oCclusion Evaluation; sNIHSS-EMS : shortened National Institutes of Health Stroke Scale for Emergency Medical Services; VAN : Vision, Aphasia, Neglect.
Los tres estudios que analizaron la escala RACE obtuvieron valores similares de S en la identificación de pacientes con OAGV13,24,25, aunque el de Jumaa y col25 fue ligeramente inferior. La mayor parte de las escalas mostraron valores de S similares a RACE, a excepción de LARIO-SS28, VAN26 y Pre-HAST29 que describieron los valores más elevados. La escala RACE mostró similares valores de E < 0,80 en los tres estudios incluidos13,24,25, a diferencia de las otras escalas evaluadas21,27,31,32,35,36.
Los VPP de la escala RACE fueron inferiores a 0,5013,24,25, mientras que otras escalas mostraron un VPP ≥ 0,70: sNIHSS-EMS27, VAN26, LARIO-SS28, LAMS32,34, FAST-ED21, 3I-SS y NIHSS35. La escala RACE obtuvo VPN ≥ 0,9013,24,25, muy similares a los obtenidos por NIHSS y ASTRAL20,35.
El AUC de la escala RACE fue >0,80 en uno de los estudios incluidos13, con valores similares a los obtenidos en ASTRAL20, LARIO-SS28 y ACT-FAST37. Estas dos últimas, junto con NIHHS evaluada por Nazliel y col32, mostraron un valor superior al resto (AUC ≥ 0,90).
Las razones de verosimilitud solamente se analizaron para las escalas LAMS32,34, CPSSS31,33, PASS36 y CPSS22. Las escalas clínicas con las cifras más elevadas de RVP fueron la LAMS y la CPSSS, de los grupos de estudio Nazliel y col32 y Kummer y col31, respectivamente.
Se emplearon distintas pruebas para evaluar la correlación entre la escala hospitalaria NIHSS de referencia y el instrumento sometido a evaluación. El coeficiente rho de Spearman se utilizó para las escalas ELVOs23, CPSS22, FAST-ED21 y RACE13,24,25, con valores altos en las dos últimas. Andsberg y col29, empleando el coeficiente de correlación de Pearson (r), encontraron una fuerte correlación entre NIHSS y Pre-HAST (Tabla 3).
Algunos estudios evaluaron la concordancia entre intérpretes para las escalas sometidas a validación; esta fue alta para 3I-SS35, LARIO-SS28 y CPSS22, mientras que para la escala ACT-FAST fue buena pero inferior a las anteriores37.
Discusión
En esta Rev Rap, cuyo objetivo principal ha sido comparar el valor predictivo de la escala RACE frente a otras escalas, destinadas al ámbito extrahospitalario y empleadas para predecir el tratamiento adecuado al paciente y su traslado al centro médico mejor capacitado, se han encontrado múltiples instrumentos de evaluación clínica con capacidad para predecir una OAGV en el ámbito extrahospitalario. No obstante, es destacable que solamente tres de estas herramientas han sido validadas con mayor frecuencia: RACE, CPSSS y LAMS. Aunque muchas de las escalas que se han encontrado predicen, con una precisión razonable, la presencia de una OAGV, algunas no fueron diseñadas específicamente para este fin33, mientras que otras solo se centraron en oclusiones que afectaban a arterias concretas29,32.
Una de las principales cuestiones que puede haber influido en los resultados obtenidos en esta revisión es el concepto de OAGV. Al diseñar una escala enfocada en oclusiones que afectan a unas arterias en concreto, no se puede saber si es igualmente precisa para el resto de los vasos. Por otro lado, hay autores que consideraron que los pacientes con hemorragia intracraneal que forman parte de la muestra influyeron positivamente en los resultados obtenidos y, además, pudieron beneficiarse de la atención hospitalaria temprana13. En cambio, otros, defendieron que no deberían haber formado parte de la muestra, porque obstaculizaron la identificación de una OAGV y retrasaron el transporte de pacientes subsidiarios de terapias recanalizadoras39. Con respecto a la formación de los intérpretes de las escalas, fueron pocos los autores que impartieron clases teóricas y/o prácticas sobre cómo llevar a cabo estos instrumentos de valoración, a pesar de que la formación es esencial para una mejor identificación de estos eventos40.
En numerosos estudios se ha observado que la escala NIHSS era el mejor instrumento clínico hospitalario capaz de orientar sobre la gravedad de una ECV y predecir una OAGV, pero no consideraron factible su uso en el ámbito extrahospitalario, ya que requería más tiempo y un mayor entrenamiento20,26-29,31,33,36,37. Por ello, todas las escalas prehospitalarias se derivaron de esta; mediante el análisis de los ítems de la NIHSS se escogieron aquellos que guardaban mayor relación con la OAGV, coincidiendo algunos autores en que los signos corticales eran los que reflejaban lesiones isquémicas mayores y estaban altamente relacionados con dicho evento, permitiendo su diferenciación de otros diagnósticos como la hemorragia intracraneal40. La escala NIHSS evalúa siete ítems relacionados con el lenguaje y dos ítems vinculados con la agnosia; debido a que considera menos signos característicos de las lesiones que se producen en el hemisferio derecho, podría pasar por alto eventos que afecten a dicha zona. Esto no sucede con la escala RACE, que evalúa por igual ambos ítems13,39.
En general, las escalas establecían puntuaciones concretas para cada ítem en función de las alteraciones que estuvieran presentes en el paciente en el momento de la valoración, excepto cinco de ellas (FAST-PLUS, VAN, PASS, ACT-FAST y ELVOs) que clasificaron los resultados como positivos o negativos sin otorgar puntuaciones concretas, lo que puede haber facilitado tanto el aprendizaje como la enseñanza y su aplicación23,26,30,36,37. Los autores de los artículos incluidos en esta revisión justificaban el empleo de este tipo de instrumentos en el ámbito prehospitalario y la elegibilidad de unos frente a otros, por el rendimiento diagnóstico observado13,20-38. Otras investigaciones, aunque encontraron un buen rendimiento, no hallaron evidencias suficientes de la superioridad de un instrumento frente a los demás41-43.
Los tres estudios que evaluaron la escala RACE observaron un rendimiento similar de esta en el umbral ≥513,24,25. Justificaban que aquellos pacientes que no fueron clasificados por la escala estaban levemente afectados y que el retraso en el tratamiento no fue en exceso perjudicial, argumentando que, en estas situaciones, las terapias de recanalización no han demostrado una eficacia muy elevada. Además, demostraron que el empleo de PC inferiores evitaba que los pacientes con una OAGV no recibieran el tratamiento oportuno, aunque muchas de estas transferencias no serían útiles, lo que aumentaría la carga de trabajo y muchos pacientes potencialmente tratables no serían atendidos adecuadamente13,24,25,27-29. Otros autores argumentan que estos umbrales podrían variar en función de las necesidades del medio donde sea valorado el paciente. En el medio prehospitalario, donde es necesario no pasar por alto pacientes potencialmente tratables, la prueba debe ser más sensible (disminuye el umbral a ≥3). A nivel hospitalario, como interesa más reconocer quien es subsidiario del tratamiento, debe ser más específica (sube el umbral a ≥6)44. Autores como Requena y col42 consideraron la escala RACE como un instrumento de valoración ideal debido a que permitía reconocer una OAGV e identificar a los pacientes que podían optar a los tratamientos de reperfusión. Otras investigaciones sostuvieron que la escala RACE mostraba un rendimiento inferior a otras como CPSS o NIHSS en la identificación de oclusiones e, incluso, en la identificación de pacientes subsidiarios del tratamiento endovascular, por lo que no debería emplearse en el medio prehospitalario y defendían el uso de la escala CPSS frente a esta44. Algunos autores consideraron que la escala RACE era extensa y plantearon una simplificación de esta eliminando ciertos ítems; sin embargo, se demostró que la mayor precisión en la identificación de pacientes con una OAGV se conseguía con la escala original45.
En cuanto a las limitaciones, fueron escasos los artículos que analizaron la eficacia pronóstica de las escalas. Esta información solo estuvo disponible en seis estudios y ninguno de ellos analizó la escala RACE22,31,32,33,34,36. Únicamente en el estudio de Lima y col21 se aplicaron diversas escalas prehospitalarias existentes a la población de estudio, mientras que la mayoría se sirvieron de datos de otros artículos y los compararon con los obtenidos para el instrumento que diseñaron y/o evaluaron. En la evidencia científica actual, existe una escasa valoración de la reproductibilidad de las escalas, tan solo en cuatro estudios se analizó la concordancia entre intérpretes, y ninguno de ellos se llevó a cabo en la escala RACE22,28,35,37. Por otra parte, las muestras de los estudios fueron heterogéneas en cuanto al número y el diagnóstico. En numerosos casos se preseleccionaron los pacientes con un determinado diagnóstico, generalmente ECV isquémica21,22,31-33,36,38. El resto incluyeron a pacientes con sospecha de ECV, aunque solamente dos de ellos no especificaron qué tipos de eventos incluía dicho término28,30. También la escasa formación de los intérpretes de la prueba fue otra de las limitaciones. En muy pocos estudios se ofreció educación adicional sobre la ECV y sobre las escalas a validar, a pesar de que en muchos casos se consideraba como un elemento que garantizaba un mejor rendimiento de las escalas13,25,26,28-30. Otra limitación del presente manuscrito se relaciona con la disponibilidad de algunos artículos localizados en la búsqueda inicial, debido a que algunos de ellos no estuvieron disponibles a texto completo mediante la consulta en bases de datos, repositorios institucionales o a los propios autores y podrían haber sido manuscritos elegibles. Sin embargo, el número de artículos encontrados en esta situación fue muy limitado, lo que no implicaría modificaciones sustanciales en la conclusión de esta Rev Rap. Por otro lado, solo en uno de los artículos incluidos se tuvo en cuenta la opinión de los intérpretes de las escalas sobre la utilidad de estos instrumentos29.
En relación con el tipo de diseño de esta revisión, es necesario recalcar algunas limitaciones de las Rev Rap. La búsqueda no fue tan exhaustiva como en una RS, restringiéndola a la base de datos MEDLINE (PubMed) por ser la base de datos de referencia para estudios biomédicos. El cribado fue realizado por un solo autor, aunque gran parte de las cuestiones metodológicas se llevaron a cabo junto a un autor con experiencia en RS. No obstante, las Rev Rap cada vez están cobrando mayor relevancia y repercusión para recopilar la evidencia en menor tiempo manteniendo la rigurosidad metodológica.
En cuanto a las fortalezas, se debe destacar que 17 de los 20 artículos incluidos en esta revisión son de los últimos cinco años20-31,33,34,36-38. En la mayoría de los artículos incluidos se especifica qué tipo de profesionales fueron los encargados de interpretar las escalas sometidas a validación13,20-23,26,28-38, muchos de los cuales, fueron profesionales del servicio de emergencias sanitarias13,22-30,37 quienes, en algunos casos, habían recibido formación adicional sobre el empleo de dichas escalas13,22-29,37. Además, en numerosos estudios la muestra de pacientes estaba constituida por sujetos de diferentes centros hospitalarios, lo que refuerza la confiabilidad de los resultados obtenidos por estas investigaciones20,21,23,24,27,30,33,38. Otra de las fortalezas a resaltar es el análisis del rendimiento de las escalas; en todos los artículos incluidos se analizó la precisión diagnóstica de estos instrumentos13,20-38 y, además, aquellos que analizaron las mismas escalas obtuvieron datos muy similares13,24,25,31-34.
Una de las principales líneas de investigación futuras, sería la aplicación de una nueva escala durante un largo periodo de tiempo en el medio extrahospitalario. Esta herramienta podría elaborarse a partir de ítems que evalúan signos corticales, ya que son los que más se correlacionan con la OAGV y son fáciles de evaluar. Los resultados podrían ser clasificados como positivos o negativos, sin puntuaciones específicas, lo que podría resultar más eficiente y sencillo, con un riesgo menor de errores y sin presentar la necesidad de consultar material adicional. Por otra parte, sería aconsejable que los intérpretes fueran profesionales del servicio de emergencias sanitarias, individuos que deberían recibir una formación previa, tanto teórica como práctica, sobre la utilización y las actualizaciones más importantes. Finalmente, durante el periodo de estudio, sería aconsejable evaluar la capacidad de la escala para predecir una OAGV, en base al mayor rendimiento conseguido.
Aunque estas escalas en la práctica habitual se aplican en el servicio de emergencias sanitarias, en algunas comunidades autónomas no las llevan a cabo ni los profesionales de enfermería ni los técnicos de emergencias. Es necesario conocer y saber utilizar estas escalas para emplearlas de manera correcta, siendo imprescindible la actualización de los conocimientos sobre este tipo de instrumentos y el grupo de patologías a los que van dirigidos. De este modo, se conseguirá mejorar la calidad de los cuidados proporcionados a los pacientes que lo precisen.
Según los resultados de esta Rev Rap, la mayoría de las escalas evaluadas son capaces de clasificar correctamente a gran parte de los pacientes. La escala RACE es un instrumento clínico que permite detectar una OAGV en pacientes que sufren una ECV isquémica en un corto periodo de tiempo, siendo factible su uso en el medio extrahospitalario. Además, este instrumento muestra una precisión similar a otras escalas prehospitalarias, aunque ligeramente inferior a la NIHSS de uso hospitalario, y una buena capacidad pronóstica en la identificación de tal evento, al igual que la gran mayoría de escalas evaluadas. Los estudios sobre la eficacia pronóstica y la reproductibilidad de las escalas son escasos y ninguno se llevó a cabo en la escala RACE. La utilización de esta escala plantea una ventaja generalizada debido a que, al ser una prueba cuya realización no conlleva mucho tiempo, no se retrasa el acceso de los pacientes a los tratamientos pertinentes; de hecho, permite determinar el traslado del paciente al centro médico adecuado en función del tipo de tratamiento que precise, mejorando de este modo la eficacia y la evolución clínica.














