Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Medicina Oral, Patología Oral y Cirugía Bucal (Internet)
versión On-line ISSN 1698-6946
Med. oral patol. oral cir.bucal (Internet) vol.11 no.1 ene./feb. 2006
Reacción granulomatosa facial por rellenos cosméticos inyectados:
presentación de cinco casos
Rafael Poveda 1, José V. Bagán 2, Judith Murillo 3, Yolanda Jiménez 1
(1) Médico Estomatólogo. Adjunto del Servicio de Estomatología
(2) Catedrático de Medicina Bucal, Universidad de Valencia. Jefe del Servicio de Estomatología.
Hospital General Universitario de Valencia.
(3) Cirujano Maxilofacial. Adjunta del Servicio de Estomatología del Hospital general Universitario de Valencia.
Dirección para correspondencia
RESUMEN
El uso de sustancias para el aumento de tejidos blandos por motivos estéticos puede ocasionar la aparición de granulomas a cuerpo extraño, entre otros efectos indeseables. Las mejoras introducidas en dichas sustancias han conseguido la disminución de la incidencia de reacciones adversas pero no su desaparición. Presentamos cinco casos de reacción a cuerpo extraño por tres productos diferentes, dimetilpolisiloxano (silicona), colágeno bovino, y ácido poliláctico, que habían sido infiltrados en el tejido celular subcutáneo de las pacientes (las cinco eran mujeres) entre dos y dieciséis años antes de la aparición de la reacción a cuerpo extraño. Las cinco presentaron un cuadro de tumefacción facial difusa, no dolorosa y de consistencia duroelástica. Los estudios de imagen con resonancia magnética mostraron signos de reacción inflamatoria intensa de la zona afectada.
La histología mostró la presencia de granulomas a cuerpo extraño con células gigantes multinucleadas.
Las pacientes fueron tratadas con corticoides administrados por vía sistémica, excepto una de ellas que no precisó tratamiento farmacológico.
Palabras clave: Granuloma, siliconoma, ácido poliláctico, silicona, colágeno bovino.
ABSTRACT
The use of substances to augment soft tissues as aesthetic purpose is associated with, among other undesirable effects, the appearance of foreign body granulomas. The improvements made to these substances have reduced the incidence of adverse reactions, but not eliminated them. We present five cases of foreign body reactions to three different products, dimethylpolysiloxane (silicone), bovine collagen, and polylactic acid, which were injected into the subcutaneous cellular tissue of the patients (all five were women), between two and sixteen years before the appearance of the foreign body reaction. All five presented painless, diffuse facial tumefaction, of firm, elastic consistency. The magnetic resonance image (MRI) studies showed signs of intense inflammatory reaction in the affected areas.
The histology revealed the presence of foreign body granulomas with giant multi-nucleated cells.
The patients were treated with systemically administered corticoids, except in one case which did not require pharmacological treatment.
Key words: Granuloma, siliconoma, polylactic acid, silicone, bovine collagen.
Introducción
La utilización de sustancias de relleno para aumento de tejidos blandos data de finales del Siglo XIX. Se utilizó inicialmente grasa autóloga, posteriormente parafina, silicona, colágeno bovino y una larga lista de productos que sigue creciendo en la actualidad (1). El mecanismo de acción es similar en todos ellos: se trata de materiales supuestamente inertes que al ser introducidos en los tegumentos provocan un aumento de volumen "per se" y una infiltración progresiva por una matriz de colágeno que a su vez contribuye al aumento de volumen (2).
La silicona líquida está formada por polímeros de dimetilsiloxano. Se utiliza siguiendo la técnica de inyección de microgotas descrita por Orentreich (3).
El colágeno bovino es la sustancia más utilizada actualmente. Constituye el patrón de referencia para el resto de sustancias de relleno. Se han ensayado múltiples presentaciones del producto (asociado a esferas de polimetacrilato, a péptidos de elastina solubilizada, en forma monomolecular al 2% en solución acuosa, etc.).
El ácido poliláctico es un producto de origen no animal que se presenta liofilizado y precisa ser reconstituido con agua previamente a su infiltración (1).
El uso de estos productos se asocia con ciertos efectos indeseables de los que nos interesa particularmente la reacción a cuerpo extraño.
Casos clínicos
Caso 1
Mujer de 55 años, fumadora de dos paquetes de cigarrillos al día y consumo ocasional de alcohol. Es diabética insulinodependiente y padece úlcera de estómago. En tratamiento con insulina, citalopram, loracepam, dobesilato cálcico, raloxifeno y atorvastatina.
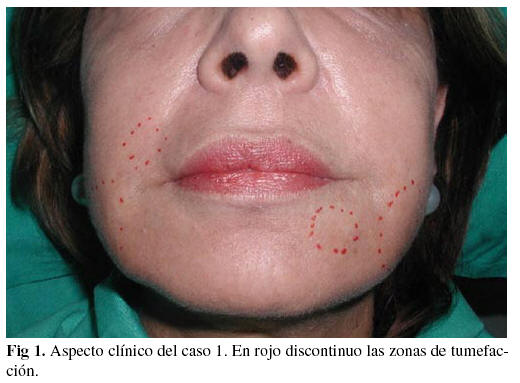
Es remitida a nuestro Servicio por presentar tumefacción en parte inferior de ambas regiones genianas, labio inferior izquierdo y surco nasogeniano derecho de un mes de evolución, consistencia elástica, indolora, de aparición lenta y crecimiento progresivo (fig.1). La paciente notaba que se encontraba peor por las mañanas. Relató que había recibido primero infiltraciones locales de ácido poliláctico y luego toxoide botulínico A (Botox®) hacía nueve años y año y medio respectivamente. Se solicitó analítica ortopantomografía, RM y biopsia. La analítica y la ortopantomografía no mostraron alteraciones significativas. La RM informó de imágenes hiperintensas de la grasa subcutánea mandibular y submandibular con discreta trabeculación en relación a cambios inflamatorios. La biopsia informó de infiltrado inflamatorio crónico con eosinófilos y células gigantes multinucleadas a cuerpo extraño por silicona situadas en la submucosa y fascículos del músculo estriado. Se inició tratamiento con deflazacort 15 mg al día durante 10 días para ir disminuyendo la dosis progresivamente hasta retirarlo por completo un mes y diez días después. La paciente había notado una franca mejoría aunque persistía la palpación de tumoraciones bilaterales de consistencia firme.
Caso 2
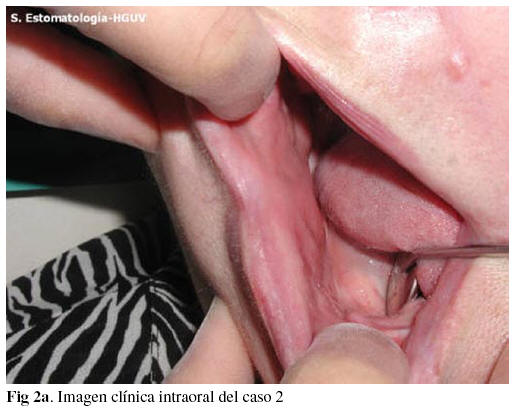
Mujer de 72 años no fumadora ni bebedora de alcohol y sin antecedentes clínicos de interés que acude a nuestro Servicio por presentar desde hace 8 días tumefacción facial difusa, dura, mal definida aunque más marcada en labio y mentón, sin adenopatías ni alteración del estado general (fig. 2a).
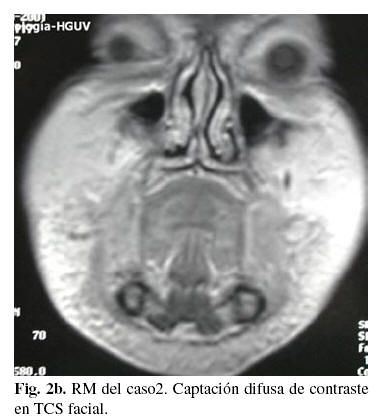
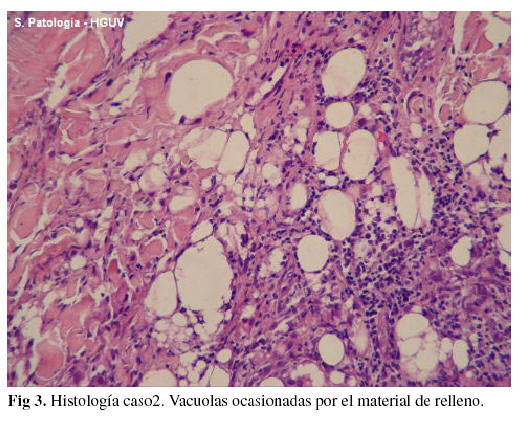
La paciente informa que 16 años antes se había sometido a un tratamiento de infiltraciones con dimetilpolisiloxano (silicona) en labios, pómulos y mentón. Se solicita analítica, ortopantomografía, PAAF, resonancia magnética y biopsia. Las tres primeras no aportan datos que ayuden al diagnóstico. La RM informa de un intenso proceso inflamatorio que afecta a la práctica totalidad del tejido celular subcutáneo que recubre los maxilares y el suelo de la boca así como gran parte de la mucosa de las mejillas (fig. 2b). La afectación es difusa y capta abundante contraste. La biopsia informa de lesión compatible con granuloma a cuerpo extraño por silicona (fig. 3).
Se inicia tratamiento con deflazacort 30 mg/día que fue rebajado a 15 y 7,5 mg a los tres y dos días respectivamente. Un mes después la paciente nota una reagudización por lo que se vuelve a instaurar tratamiento con deflazacort 30 mg/día. Tres meses después aún persiste la tumefacción por lo que sigue tomando 7,5 mg/día de deflazacort. 10 meses después se procede a la retirada de la medicación. La paciente no nota molestias pero persiste el tacto duro de las zonas infiltradas.
Caso 3
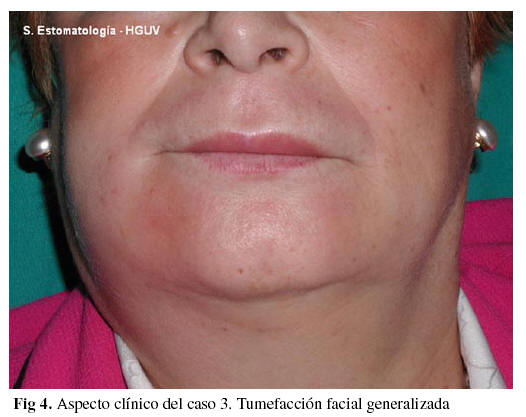
Mujer de 70 años de edad, consumidora ocasional de alcohol y tabaco y con antecedentes de artrosis, cataratas, desprendimiento de retina y depresión. Acude a consulta por presentar tumefacción facial bilateral generalizada que no remite tras tratamiento antibiótico (fig. 4). Dos años antes había sido sometida a un tratamiento de infiltraciones faciales con colágeno en labio superior. Relata la paciente que un año antes tuvo un brote que cedió con la exodoncia de un molar. Se solicitó ortopantomografía y se realizó una biopsia. El estudio radiográfico no mostró signos de interés. La biopsia evidenció discretos infiltrados linfoides perivasculares junto a foco de esteatonecrosis y célula gigante multinucleada de tipo reacción a cuerpo extraño. El diagnóstico final fue de infiltración por colágeno bovino. Se inició tratamiento con Deflazacort 30 mg/día. Se produjo una paulatina mejoría de los síntomas en las dos semanas siguientes. Se retiró la medicación y dos semanas después apareció un nuevo brote en zona mandibular derecha que requirió nuevamente tratamiento con corticoides hasta su resolución 10 días después.
Caso 4
Mujer de 54 años con antecedentes de osteoporosis, pólipos y cáncer de mama. En tratamiento con oseína-hidroxiapatita (Osteopor®), extracto de meliloto (Esberiven®) y un preparado homeopático para la alergia (Limphomyosot®). La remite su odontólogo porque, desde hace 15 días, presenta hinchazón en labios y mejillas que ha ido variando de intensidad y localización. A veces lo nota más en un lado que en otro. La paciente está preocupada por si se trata de una metástasis oral del cáncer de mama. 12 años antes había recibido infiltraciones con silicona en los pliegues nasolabiales superiores.
Presenta tumefacción de consistencia dura en ambas mucosas yugales hasta la zona retrocomisural. Se solicita analítica, cuyos resultados son normales, y se realiza biopsia que confirma la reacción a cuerpo extraño por silicona. Dado la mejoría de la paciente se decide no instaurar tratamiento y realizar revisiones periódicas.
Caso 5
Mujer de 43 años sin enfermedades previas de interés que había recibido infiltraciones de silicona en labios y carrillos 10 años antes. A los 2-3 años de las infiltraciones comenzó a hinchársele la cara por lo que recibió tratamiento antiinflamatorio. Dado que el tratamiento no resultaba eficaz fue sometida a cirugía para retirar el cuerpo extraño. Le quedó, como secuela de la cirugía, una parálisis facial sin que se resolviera la hinchazón. Cuando acude a nuestro Servicio la paciente relata episodios continuos de inflamación que requieren tratamiento con corticoides de forma permanente (deflazacort) lo que le ha provocado un aumento de 5 kg de peso. En la exploración física la paciente presenta tumefacción labial y de mucosa bucal sobre todo en lado derecho. Es de consistencia dura. Se realiza biopsia que es informada como reacción a cuerpo extraño por silicona.
Discusión
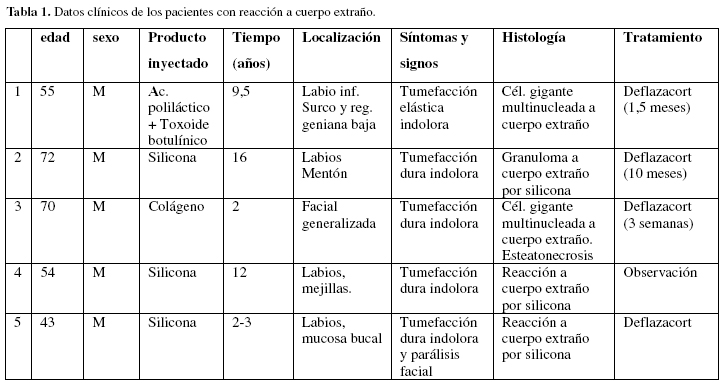
Las característica epidemiológicas y clínicas de los casos presentados en el presente trabajo se recogen en la tabla 1.
Con independencia de producto de relleno empleado en cada caso, el mecanismo de acción y la finalidad es similar en todos ellos. El producto inyectado induce una reacción en el tejido conjuntivo circundante con depósito de colágeno más o menos estable que persiste independientemente de que el material de relleno sea fagocitado (2). Se produce, en definitiva, un aumento de volumen de los tejidos blandos que es el efecto deseado.
La supuesta inocuidad de estos productos (se consideraron inertes inicialmente) se vio rápidamente cuestionada al observarse reacciones adversas directamente relacionadas con su uso. Dado que la silicona fue el primer material utilizado masivamente y con poco control sanitario acapara la mayor parte de las reacciones adversas descritas y también las más virulentas (4). Conviene señalar, sin embargo, que se han descrito reacciones adversas con la práctica totalidad de los productos utilizados y, por supuesto, con los tres implicados en el presente trabajo (5).
Aunque se ha sugerido la posible toxicidad sistémica de alguno de estos productos y en particular de la silicona, al detectarse depósitos en hígado, bazo y riñones tras la inyección subcutánea, lo cierto es que no se ha podido establecer relación con enfermedades del tejido conjuntivo ni con otras enfermedades (6,7). Tampoco se han podido detectar anticuerpos antisilicona (8).
La toxicidad local incluye dolor, edema, equimosis, eritema, discromía, alteraciones en la textura cutánea, sobrecorrección y fenómenos embólicos locales (3). En algunos casos, afortunadamente raros, se pueden llegar a producir úlceras extensas que pueden llegar a afectar músculo, hueso y estructuras nerviosas (9,10).
La reacción granulomatosa a cuerpo extraño aparece tras un periodo de tiempo variable (2, 9,10, 12 y 16 años en los casos presentados) desde los 5 meses hasta los 15 años en la literatura revisada (11).
El mecanismo de acción permanece desconocido aunque se ha sugerido que una infección podría desencadenar una reacción inmunológica cruzada (12) o que podría existir una estimulación de la inmunidad retardada (13).
La clínica incluye tumefacción de consistencia normalmente dura. Aunque hay descritas otras manifestaciones como enrojecimiento, sensación urente, dolor y sensibilidad a la palpación (11), no aparecieron en los casos que presentamos.
La histología es característica mostrando células gigante multinucleadas como reacción a cuerpo extraño. Es frecuente encontrar las vacuolas correspondientes al material de relleno, particularmente con la silicona. Con otros productos puede no detectarse el material de relleno (2).
El diagnóstico diferencial debe incluir la erisipela, la dermatitis alérgica de contacto, el edema facial con eosinofilia, la queilitis glandular apostematosa, el síndrome de Ascher, las granulomatosis orofaciales como la enfermedad de Crohn, el síndrome de Melkersson-Rosenthal o la sarcoidosis (11,14). Asimismo leismaniasis cutánea, lepra o tuberculosis pueden presentarse también como inflamación granulomatosa de la piel (13).
El tratamiento etiológico (remoción del producto inyectado) presenta dificultades difícilmente soslayables en la actualidad. Para el tratamiento sintomático se han descrito los corticoides locales, sistémicos (12), la minociclina (15) y el imiquimod al 5% (16). Nuestros casos fueron tratados con corticoides sistémicos durante los brotes ya que se consideró que el producto de relleno no podía ser eliminado quirúrgicamente.
Bibliografía
1. Klein A, Elson M. The history of substances for soft tissue augmentation. Dermatol Surg 2000;26:1096-105 [ Links ]
2. Lemperle G, Morhenn V, Charrier U. Human histology and persistence of various inject able filler substance for soft tissue augmentation. Aesthetic Plast Surg 2003;27:554-66. [ Links ]
3. Orentreich D. Liquid injectable silicone. Clin Plast Surg 2000;27:595-612. [ Links ]
4. Allevato MA, Pastorale EP, Zamboni M, Kerdel F, Woscoff A. Complications following industrial liquid silicone injection. Int J Dermatol 1996;35:193-5. [ Links ]
5. Lombardi T, Samson J, Plantier F, Husson C, Kuffer R. Orofacial granulomas after injection of cosmetic fillers. Histopathologic and clinical study of 11 cases. J Oral Pathol Med 2004;33:115-20. [ Links ]
6. Sanchez-Guerrero J, Colditz G, Karlson E, Hunter D, Speizer F, Liang M. Silicone breast implants and the risk of connective tissue diseases and symptoms. N Eng J Med 1995;332:1666-70. [ Links ]
7.Gabriel S, OFallon M, Kurlan L, Beard CM, Woods JE, Melton LJ. Risk of connective-tissue diseases and other disorders after breast implantation. N Eng J Med 1994;330:1697-702. [ Links ]
8.Oliver DW, Walker MS, Walters AE, Chatrath P, Lamberti BGH. Antisilicone antibodies and silicone containing breast implants. Br J Plast Surg 2000; 53:410-4. [ Links ]
9.Rapaport M, Vinnik C, Zarem H. Injentable silicone: cause of facial nodules, cellulitis, ulceration and migration. Aesth Plat Surg 1996;20:267-76 [ Links ]
10.Mastruserio N, Pesqueira M, Cobb M. Severe granulomatous reaction and facial ulceration occurring after subcutaneous silicone injection. J Am Acad Dermatol 1996;34:849-52 [ Links ]
11.Ficarra G, Mosqueda-Taylor A, Carlos R. Silicone granuloma of the facial tissues: A report of seven cases. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2002;94:65-73. [ Links ]
12.Bigatà X, Ribera M, Bielsa I, Ferrándiz C. Adverse granulomatous reaction after cosmetic dermal silicones injection. Dermatol Surg 2001;27:198-200. [ Links ]
13.Maas C, Papel I, Greene D, Stoker D. Complications of Injectable Synthetic Polymers in Facial Augmentation. Dermatol Surg 1997;23:871-7. [ Links ]
14.Yanagihara M, Fujii T, Wakamatu N, Ishizaki H, Takehara T, Nawate K. Silicone granuloma on the entry points of acupuncture, venopuncture and surgical needles. J Cutan Pathol 2000;27:301-5. [ Links ]
15.Senent P, Bachelez H, Ollivaud L, Vignon-Pennamen D, Dubertret L. Minocycline for the treatment of cutaneous silicone granulomas. Br J Dermatol 1999;140:985-7 [ Links ]
16.Baumann L, Halem M. Lip silicone granulomatous foreign body reaction treated with Aldara (Imiquimod 5%). Dermatol Surg 2003;29:429-32. [ Links ]
![]() Dirección para correspondencia
Dirección para correspondencia
Rafael Poveda Roda
Hospital General Universitario de Valencia
Av/ Tres Cruces s/n
46.014 Valencia
E-mail: poveda_raf@gva.es
Recibido: 30-03-2004
Aceptado: 25-03-2005











 texto en
texto en