INTRODUÇÃO
Conforme dados do Instituto Nacional do Câncer, as doenças e agravos não transmissíveis, incluindo as neoplasias malignas, representam a maior parte dos adoecimentos e óbitos em todo o mundo, provocando as chamadas transições demográfica e epidemiológica1,2.
Neste contexto, as doenças onco-hematológicas, representam 7% das hemopatias e estão relacionadas ao comprometimento funcional hematopoiético de linhagens mielóide, linfoide, mastócitos, macrófagos e seus precursores3. As alterações na produção de células hematopoiéticas da medula óssea são responsáveis pela origem das neoplasias hematológicas, que compreendem principalmente as leucemias, linfomas e mieloma múltiplo (MM)4.
O MM é uma neoplasia maligna de células linfoides medulares, a segunda doença onco-hematológica com maior prevalência, e representa 1% de todas as doenças oncológicas. Também conhecido como doença do idoso, a incidência do MM é maior a partir dos 40 anos, com discreto predomínio em pessoas do sexo masculino. Acredita-se que alguns agentes infecciosos, exposição a agrotóxicos, radiação ionizante e benzeno sejam algumas das possíveis causas para o surgimento da doença3,5-7.
O MM ainda é uma neoplasia incurável e o tratamento tem por objetivo o controle da doença, com redução dos efeitos no organismo e melhoria da qualidade de vida. A farmacoterapia é a base do tratamento e envolve a utilização de esquemas quimioterápicos que combinam de 2 a 4 fármacos diferentes8.
Dentre os medicamentos que compõem a quimioterapia do paciente com MM inclui-se a talidomida e bortezomibe, os quais podem provocar um tipo de reação adversa que consiste em lesão dos nervos do sistema nervoso periférico: a neuropatia periférica induzida por quimioterapia (NIPQ). A NPIQ é relatada entre 10 e 55% dos pacientes em uso de talidomida e entre 31 e 64% daqueles em uso de bortezomibe. Nesses pacientes a NIPQ se manifesta por meio de sintomas como formigamento, dormência em extremidades, disestesia, dor neuropática, eventos gastrointestinais, desordens motoras e neurodegenerativas9,10.
Não existem agentes terapêuticos preventivos para a NPIQ, por isso, é de suma importância a identificação e manejo farmacoterapêutico do paciente, com diminuição da dose ou suspenção do quimioterápico neurotóxico, antes que sintomas incapacitantes acometam o paciente.
Diante do exposto, o objetivo do estudo foi identificar, por meio da revisão de literatura, instrumentos que avaliem a NPIQ e que possam ser adaptados ou traduzidos para ser utilizados na prática clínica do cuidado ao paciente com MM.
MÉTODO
O presente estudo trata-se de uma Revisão Narrativa. Esse tipo de estudo permite, sob ponto de vista teórico ou contextual, discorrer de forma analítica e crítica sobre determinado assunto que se deseja explorar11. Para isso o roteiro dessa revisão foi dividido em seis etapas: 1. Escolha do tema e delineamento da pergunta norteadora; 2. Seleção das bases de dados e construção das estratégias de busca; 3. Seleção e categorização dos estudos; 4. Análise crítica dos artigos incluídos; 5. Interpretação dos resultados; 6. Discussão detalhada dos artigos que atenderam aos critérios de inclusão12.
O levantamento bibliográfico foi realizado por meio de fontes de informações secundárias da Biblioteca Virtual em Saúde BVS, Scopus, Scientific Electronic Library Online – SciELO e U.S. National Library of Medicine . PubMed.
Considerando a importância das estratégias de busca foram realizadas combinações entre descritores do Medical Subject Headings (MeSH) e Descritores em Ciências da Saúde (DeCS), com termos em inglês e português para pesquisas na BVS, e apenas em língua inglesa para as bases SciELO, Scopus e PubMed. Os descritores utilizados foram: Efeitos Colaterais e Reações Adversas Relacionados a Medicamentos (Drug-Related Side Effects and Adverse Reactions), Lista de checagem (Checklist), Antineoplásicos (Antineoplastic Agents), Tratamento farmacológico (Drug Therapy), Doenças do Sistema Nervoso Periférico (Peripheral Nervous System Diseases) e Doenças Hematológicas (Hematologic Diseases). Embora não encontrado no DeCs e MeSH o descritor Neuropatia (Neuropathy), é um termo importante para o contexto do estudo, e por isso, foi incluído. Aos descritores foram associados os operadores booleanos “AND” e “OR”.
O levantamento bibliográfico transcorreu no período de julho de 2018 a maio de 2019. Foram elegíveis artigos publicados em inglês e português, disponíveis na íntegra de maneira livre ou em periódicos assinados pelo Portal de Coordenação de Aperfeiçoamento de Pessoal de Nível Superior com abrangência temporal de junho de 2007 a janeiro de 2019. Foram excluídos estudos realizados com animais, monografias, guidelines, teses, casos clínicos e estudos que não são da área da saúde.
Após analisar cada artigo quanto à sua pertinência ao tema, foram excluídos aqueles que não dispunham na introdução, resumo ou íntegra, instrumentos para avaliação de NPIQ. De forma complementar, foram incluídas manualmente outras referências que atendiam ao propósito do estudo, que eram de conhecimento prévio dos próprios pesquisadores e/ou que foram identificadas a partir das referências dos artigos incluídos e analisados.
Os dados referentes ao levantamento bibliográfico e categorização do material foram armazenados em planilha eletrônica Microsoft Excel.
RESULTADOS
As buscas retornaram um total de 127 publicações. Após aplicados os critérios de elegibilidade, 40 foram excluídas por duplicidade, 54 após leitura do título e 14 após leitura do resumo. Outros três estudos também foram excluídos: um guideline sobre manejo do linfoma linfoplasmocitário, e dois por não estarem disponíveis na íntegra.
Ao final do processo, 16 artigos foram avaliados na íntegra quanto ao seu conteúdo. Destes, 14 foram excluídos pois, embora discorressem sobre a NPIQ, não apresentavam instrumentos que permitissem a avaliação do paciente. Portanto, após a exploração do material e aplicação dos critérios de elegibilidade, apenas dois artigos foram válidos. A partir das referências dos artigos incluídos e analisados, foram incorporados manualmente quatro artigos, e um outro estudo que era do conhecimento dos pesquisadores. Por fim, sete artigos contemplaram o objetivo desse trabalho, e todo o processo metodológico de inclusão e exclusão de artigos estão descritos nafigura 1.
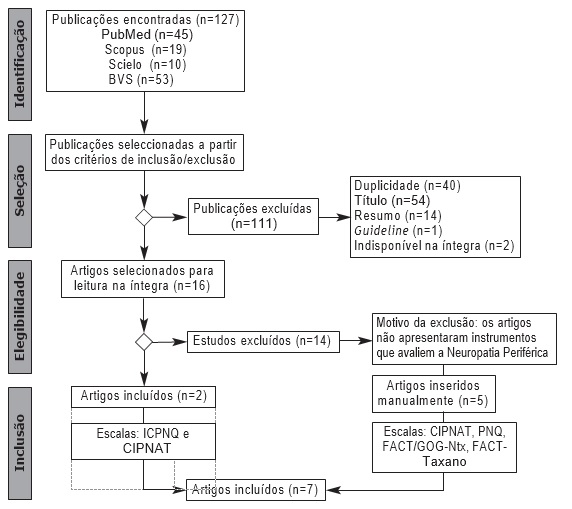
Figura 1. Fluxograma de identificação, seleção, elegibilidade e inclusão de publicaçõesencontradas no PubMed, Scopus, SciELO e BVS.
Os objetivos dos sete estudos foram claramente explicitados pelos autores, conforme apresentados no tabela 1. De modo geral, os estudos buscaram avaliar resultados de intervenções, verificar fatores preditores da NPIQ, bem como outros fatores relacionados à ocorrência, incidência, impacto na vida do paciente e validade dos instrumentos apresentados. Ao final, cinco instrumentos foram apresentados nos sete estudos avaliados.
Tabela 1. Estudos de avaliação da neuropatia periférica induzida por quimioterapia (NPIQ) empregando diferentes instrumentos clínicos.
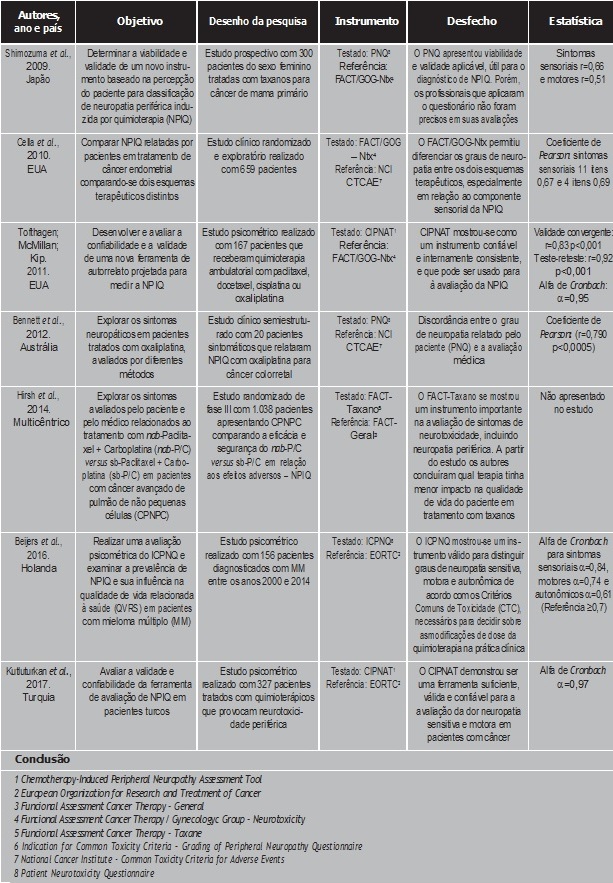
Os estudos foram realizados na Holanda (n=1), Estados Unidos (n=2), Austrália (n=1), Japão (n=1), Turquia (n=1), e um Multicêntrico – Celgene Corporation (n=1).
Um total de 2.667 participantes, maiores de 18 anos foram envolvidos nos sete estudos analisados, sendo a maior parte constituída por pessoas do sexo feminino. Dentre os tipos de cânceres considerados nas pesquisas incluiu-se o de mama, pulmão, estômago, pâncreas, colorretal, carcinoma endometrial e mieloma múltiplo. Uma variedade de agentes quimioterápicos foi descrita, como a talidomida, bortezomibe, lenalidomida, vincristina, taxanos (docetaxel, paclitaxel), derivados da platina (oxaliplatina, cisplatina e carboplatina) e doxorrubicina.
Instrumentos de avaliação da neuropatia periférica induzida por quimioterápicos (NPIQ)
O presente estudo permitiu identificar cinco instrumentos de avaliação de NPIQ que foram descritos no tabela 2, são eles: Patient Neurotoxicity Questionnaire (PNQ); Funcional Assessment of Cancer Therapy/Gynecologyc Group . Neurotoxicity (FACT/GOG-Ntx); Chemotherapy-Induced Peripheral Neuropathy Assessment Tool (CIPNAT); Funcional Assessment Cancer Therapy/Taxane (FACT-Taxano); Indication for Common Toxicity Criteria . Grading of Peripheral Neuropathy Questionnaire (ICPNQ).
Patient Neurotoxicity Questionnaire (PNQ)
Em um dos estudos apresentados o PNQ foi aplicado em pacientes com neoplasia colorretal submetidos previamente ao tratamento com oxaliplatina que mesmo após interrupção ou término da terapia antineoplásica apresentavam algum grau de NP. O corpo clínico utilizou a classificação do NCI CTCAE versão 3.0 para avaliar a gravidade de neuropatia: grau 1: leve ou assintomático; 2: moderado, com alterações sensoriais como formigamento e parestesia; 3: grave, com limitações para o autocuidado; 4: risco de morte; 5: morte relacionada a evento adverso. A pontuação máxima obtida frente os sintomas apresentados foi utilizada pelo médico como referência para determinar o maior nível de neuropatia13.
O PNQ é um questionário simples, respondido pelo paciente e consiste de duas seções que identificam a incidência e gravidade de distúrbios sensoriais e motores. Cada seção dispõe de cinco itens que são respondidos pelo paciente sobre os níveis de neuropatia por ele experimentado. As respostas referidas pelo paciente são subjetivas e dependem de sua percepção a respeito dos sintomas observados. Na primeira seção são avaliados sintomas sensoriais como dormência, dor, queimação, formigamento, alterações táteis e, também alterações de sensibilidade nos pés e boca. A seção 2 avalia sintomas motores como a deglutição, respiração e mastigação. Cada um dos cinco itens corresponde: “A” ausência de neuropatia, “B” leve, “C” moderada, “D” moderada a grave e “E” neuropatia grave. É possível também que o paciente indique quais sintomas interferem nas atividades de vida diária13,14.
Funcional Assessment of Cancer Therapy/Gynecologyc Group – Neurotoxicity (FACT/GOG-Ntx)
O instrumento FACT/GOG-Ntx é uma subescala produzida a partir da escala FACT, e foi criada para avaliação de NP em pacientes de ginecologia. O instrumento foi utilizado em um estudo clínico randomizado para avaliar a toxicidade entre dois esquemas de tratamento em pacientes com câncer endometrial. Destes, um grupo foi tratado com cisplatina e doxorrubicina e o outro grupo com cisplatina, doxorrubicina e paclitaxel. A escala foi aplicada no início, durante e após seis meses de tratamento e evidenciou que o sistema sensorial foi o mais afetado (Cella et al., 2010).
A subescala FACT/GOG-Ntx é um instrumento validado, composto por 11 itens específicos que avaliam sintomas neurotóxicos (mãos, pés, deambulação e desconforto auditivo) e o impacto que eles produzem nas atividades diárias, tendo por referência os sete dias que antecedem à avaliação. Outros 27 itens que compõem a escala são específicos para mensurações gerais sobre a qualidade de vida (bemestar físico/social/familiar e emocional). No total, a escala é composta por 38 itens15.
A cada item da escala é possívelatribuir pontos em um intervalo de 0a 4, sendo 0 (nenhum), 1 (um pouco),2 (pouco), 3 (moderado), 4 (muito). Paralelamente foi aplicado pelo médico a classificação de gravidade de reação adversa para neurotoxicidade do CTCAE. O instrumento é limitado pois a maioria dos itens são de avaliação de sintomas sensoriais15.
Funcional Assessment Cancer Therapy/Taxane (FACT-Taxano)
O questionário FACT-Taxano foi aplicado em um estudo multicêntrico comparativo entre esquemas de tratamento com paclitaxel e carboplatina (nab-P/C e sb-P/C) em pacientes com câncer de pulmão de não pequenas células. O objetivo foi avaliar qual esquema apresentava menos sintomas relacionados ao tratamento16.
O FACT-Taxano é uma subescala e foi elaborado pelos mesmos autores do FACTGeral, com acréscimo de itens para avaliação específica da toxicidade por taxanos. O FACTGeral é um instrumento validado composto por 11 itens que avaliam a neurotoxicidade durante o tratamento com quimioterápicos. A partir da escala primária foi produzido o FACT-Taxano que contempla cinco itens adicionais com perguntas para avaliação de sintomas como artralgia, mialgia e lesões cutâneas. Juntas as duas escalas somam 16 itens.
A escala utilizada no estudo considerou a classificação do NCI CTCAE versão 3.0 e do Dicionário Médico de Atividades Reguladoras (MedDRA) e foi aplicada no início do tratamento e a cada novo ciclo. Os itens da escala de neurotoxicidade (11 itens) avaliam a dormência ou formigamento em mãos e pés, desconforto em mãos e pés, dores articulares ou câimbras, fraqueza, dificuldades para ouvir, zumbido no ouvido, dificuldades para abotoar roupas, dificuldade de sentir pequenos objetos e dificuldade para andar16.
A escala específica para taxanos (5 itens) avalia a presença de edema em mãos, pernas e pés, dor na ponta dos dedos e desconforto nos pés. A cada pergunta o paciente deve responder 0 (nenhum), 1 (um pouco), 2 (pouco), 3 (moderado), 4 (muito) e quanto maior o número, maior o risco. Em seguida, os itens foram reagrupados em neuropatia periférica (dormência, formigamento, dificuldade para abotoar e sentir a forma de pequenos objetos), dor (dor ou desconforto ponta dos dedos e mãos), audição (dificuldade para ouvir ou zumbido) e edema (corpo, mãos e pés)16.
De forma complementar, os médicos realizaram a cada ciclo à avaliação da neuropatia sensorial, para isso, foi utilizada a classificação do NCI CTCAE versão 3.0: grau 1, presença de sintomas sensoriais/ formigamento ou parestesia, mas que não interfere nas atividades da vida diária; 2, presença de sintomas sensoriais que interferem nas atividades da vida diária; 3, os sintomas sensoriais prejudicam o autocuidado; 4, coloca em risco a vida do paciente; 5, morte16.
Chemotherapy-Induced Peripheral Neuropathy Assessment Tool (CIPNAT)
O instrumento CIPNAT foi desenvolvido e validado nos Estados Unidos, por médicos e enfermeiros17. Outro estudo foi conduzido com o objetivo de testar a validade e confia-bilidade de CIPNAT na NPIQ em pacientes turcos em tratamento ambulatorial18.
A versão final do instrumento contempla 36 itens e dispõe de duas seções. A primeira seção avalia sintomas neuropáticos específicos quanto a sua gravidade, intensidade e frequência. Desses, nove são específicos para avaliação de sintomas neuropáticos como dormência e formigamento em mãos e pés, sensibilidade ao frio, perda de equilíbrio, dor muscular e articular. As seis primeiras perguntas são relacionadas a neuropatia sensitiva, o sétimo, oitavo e nono versam sobre sintomas motores. A segunda seção é composta de 14 itens que avaliam o impacto que os sintomas de NP sensitiva e motora produzem na qualidade de vida do paciente. Esses sintomas incluem: dormir, caminhar, destreza manual, pegar objetos, escrever, atividades de lazer, relacionamentos, atividades domésticas, exercícios trabalho, atividade sexual e dirigir17,18.
É possível, ainda, que sejam acrescentados ao CIPNAT 19 itens que não são pontuados, mas permitem uma melhor descrição anatômica e localização dos sintomas reportados pelo paciente, onde ele descreve com detalhes o sintoma apresentado17.
Indication for Common Toxicity Criteria – Grading of Peripheral Neuropathy Questionnaire (ICPNQ)
O instrumento ICPNQ foi desenvolvido e validado na Holanda para avaliação da NPIQ em pacientes com mieloma múltiplo. Foram envolvidos profissionais da área de hematologia e neurologia19.
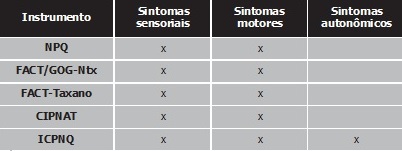
O instrumento contém três subescalas hipotéticas que avaliam sintomas sensoriais, autonômicos e motores. A escala sensorial inclui cinco itens referentes à percepção do paciente sobre alterações no tato, dormência, formigamento e alterações na sensação de temperatura e dor. A escala autonômica contém nove itens referentes à percepção do paciente sobre alterações nas funções autonômicas. A escala motora é dividida em três itens que avaliam a força em membros, o seu comprometimento para atividades instrumentais e autocuidado19.
A avaliação das respostas do paciente ao questionário permite uma indicação em relação ao grau CTCAE da NPIQ: grau 0, assintomático; grau 1, a presença de sintomas sensoriais na ausência de sintomas motores e autonômicos; grau 2, presença de sintomas autonômicos e/ou perda de força, e/ou problemas vivenciados em atividades instrumentais acompanhadas de sintomas sensoriais e/ou dor; e grau 3, presença de problemas nas atividades de autocuidado acompanhadas de sintomas sensoriais e/ou dor e/ou perda de força. A neuropatia de grau 1 e 2 pode ser dividida em categorias com ou sem dor neuropática associada19.
DISCUSSÃO
A partir da avaliação dos instrumentos acima apresentados e considerando o objetivo do estudo foi realizado uma análise da validade, aplicabilidade e viabilidade de cada instrumento.
O instrumento PNQ se mostrou útil na tomada de decisões clínicas e alterações na farmacoterapia como interrupção do tratamento, alterações de dose ou medidas profiláticas para evitar uma NPIQ. Quanto à validade do instrumento os sintomas sensoriais (r=0,66) e motores (r=0,51) do PNQ e do FACT/GOG-Ntx se mostraram significativos (Shimozuma et al., 2009). Outro estudo apontou que, o instrumento, quando aplicado pelo avaliador de pesquisa expressou melhores resultados se comparado a aplicação realizada pelo médico. A correlação do PNQ com NCI foi feita pelo coeficiente de Pearson (r=0,790, p<0,0005)13.
Os pesquisadores concluíram que apesar de o PNQ ser um instrumento viável e aplicável, ele apresenta limitações. Os autores descreveram discordância entre os resultados de NPIQ detectados quando médicos utilizavam o FACT/GOGNtx comparado aos do PNQ, com resultados maiores de NPIQ detectada pelo instrumento respondido pelo próprio paciente. Essa falta de sensibilidade dificulta a tomada de decisões para o manejo adequado da NP. Uma outra limitação do estudo é que os pacientes apresentaram dificuldade na distinção de seus sintomas o que leva a um preenchimento inadequado no instrumento13,14.
Outro instrumento apresentado é o FACT/GOG-Ntx. Para fins de comparação e validade, o número total de itens (11) foi subdividido em neuropatia sensorial (4 itens), problemas funcionais relacionados a neuropatia (3 itens), problemas auditivos (2 itens) e mialgia (2 itens). A validade do instrumento foi verificada considerando os critérios de neuropatia definidos pelo NCI CTCAE. Para isso, foi aplicado o coeficiente de Pearson para avaliação de sintomas sensoriais, com valores de 0,67 para os 11 itens e 0,69 para 4 itens. Embora haja correlação entre o FACT/GOG-Ntx e os critérios de toxicidade do NCI CTCAE os itens avaliados são distintos (sensorial e motora), e assim essa avaliação é mais específica para sintomas sensoriais15.
O instrumento FACT-Taxano foi construído15 a partir da FACT-G, com acréscimo de itens específicos para avaliação de pacientes em tratamento com taxanos. Ao aplicar o instrumento, foram observadas diferenças significativas na neuropatia relatada, dor neuropática nas mãos e pés e perda auditiva entre pacientes em terapia antineoplásica para CPNPC, porém, é uma escala limitada, com avaliação majoritária de sintomas sensoriais16.
De modo geral, as escalas FACT (FACT/GOG-Ntx e FACTTaxano) avaliam a qualidade de vida do paciente relacionada a neuropatia que pode se manifestar durante ou após o tratamento com antineoplásicos20. Por isso ela dispõe de poucos itens que se aplicam a NPIQ, não sendo viável para aplicação em pacientes onco-hematológicos.
O instrumento CIPNAT foi correlacionada ao FACT/GOGNtx (r=0,83, p<0,001, n=167) e atestou fortes evidências de validade convergente. A confiabilidade do instrumento foi mensurada por meio de teste-reteste (r=0,92, p<0,001) e alfa de Cronbach total (α=0,95) para consistência interna. Juntos os dois procedimentos de análise forneceram forte evidência de validade e confiabilidade do construto17.
O CIPNAT foi aplicado em uma amostra de 327 pacientes com o objetivo de analisar a validade e aplicabilidade do instrumento na NPIQ. Os resultados estatísticos para este estudo correlacionaram CIPNAT e EORTC com valor para alfa de Cronbach (α=0,97) que se mostrou satisfatória e confiável para CIPNAT, evidenciando a confiabilidade do instrumento18.
Em razão do número de itens e o tempo necessário para aplicação do CIPNAT (cerca de 15 minutos), os autores sugerem que o instrumento seja replicado e aprimorado, para que, assim, se torne mais objetivo e demande menos tempo para aplicação, o que é fundamental na prática clínica17. Os autores reportaram ainda dificuldades no levantamento de estudos que aplicaram o instrumento, demonstrando que, mesmo sendo um instrumento confiável e aplicável, ele ainda é pouco utilizado18.
E, por fim, o instrumento ICPNQ foi construído e validado em 2016 pela hematologista Dra. Monique Minnema e sua equipe. A confiabilidade do ICPNQ foi confirmada pelo de Cronbach (referência ≥0,7) para sintomas sensoriais (0,84) e motores (0,74). O de Cronbach para sintomas autonômicos (0,61) ficou abaixo de 0,7, o que foi considerada uma limitação do estudo em relação a esse item. De modo geral, os autores confirmam que há evidencias altas de correlação com o instrumento EORTC. A confiabilidade testereteste e validade do construto foram positivas para todas as subescalas. O instrumento pode ter sua avaliação prejudicada se o paciente não for capaz de identificar a presença de sintomas neuropáticos pré-existentes e outras condições de saúde como deficiência de vitaminas e diabetes mellitus19.
O instrumento se mostrou de fácil compreensão pelo paciente e pelo profissional aplicador, objetivo, rápido e, em razão disso, o tempo médio para o preenchimento foi de até cinco minutos. Assim, o ICPNQ demonstra ser válido para distinguir entre os graus mais altos e mais baixos dos Critérios Comuns de Toxicidade (CTC), necessários para decidir sobre as modificações de dose da quimioterapia na prática clínica diária19.
Os instrumentos preenchidos pelos profissionais de saúde empregam escalas de classificação ordinal, que se tornam uma limitação na detecção de pequenas mudanças na NPIQ. Além disso, embora sejam instrumentos utilizados na prática clínica, geralmente a interpretação com precisão é dificultada devido aos diferentes parâmetros usados para descrever a neurotoxicidade periférica por essas escalas21,22. Ainda, as escalas podem ser interpretadas de maneira diferente levando a divergências entre os resultados encontrados23.
A ausência de um instrumento simples, clinicamente útil, válido, em uma linguagem universalmente conhecida na oncologia e que possa ser implementado pelos diferentes profissionais de saúde torna-se necessário. Além disso, o desenvolvimento de novos instrumentos ou validação e aplicação de questionários já disponíveis, faz-se importante para um melhor manejo, detecção e resolução da NPIQ, em especial nos centros oncológicos no Brasil.
Portanto, a partir dos instrumentos apresentados é possível inferir que aquele que mais se aproxima do objetivo desse trabalho é o instrumento ICPNQ, por ser um instrumento objetivo, rápido e capaz de avaliar os três tipos de neuropatia periférica associados à quimioterapia em pacientes onco-hematológicos – sensorial, motora e autonômica. Esse é um instrumento que pode ser incorporado facilmente pelo farmacêutico e profissional médico na prática clínica19.
O instrumento permite avaliar graus diversos de neuropatia, o que auxilia na tomada de decisões frente a mudanças ou suspensão da farmacoterapia, e, assim, melhorar a qualidade de vida e o tratamento do paciente.
CONCLUSÃO
Foram identificados instrumentos de avaliação da NPIQ em pacientes com mieloma múltiplo, no entanto nenhum deles está em língua portuguesa. É sugerível que seja realizada a tradução e validação do instrumento ICPNQ para o português, para que assim, ele possa ser aplicado na prática clínica em pacientes onco-hematológicos, especialmente de mieloma múltiplo.