Introducción
Las Técnicas Continuas de Reemplazo Renal son aquellas técnicas que incluyen la circulación continua de sangre por circuitos extracorpóreos con el fin de depurarla, y forman parte del tratamiento y cuidado integral de pacientes con lesión renal aguda1. Algunos autores prefieren el término más genérico de Técnicas Continuas de Depuración Extracorpórea (TCDE), ya que existen algunas modalidades que no son necesariamente continuas y otras que no suplen una deficiente función del riñón2. En este artículo hablaremos en todo momento de TCDE.
Esas técnicas permiten realizar una eliminación lenta y continuada de ultrafiltrado, con buena tolerancia hemodinámica en pacientes críticos3.Además, tienen una mayor rentabilidad depurativa y una mayor seguridad para el paciente4), (5. Actualmente las TCDE son veno-venosas, y las más utilizadas son la ultrafiltración, hemodiálisis, hemo-filtración, hemodialfiltración y diálisis continua de alto flujo6. En nuestra UCI, mayoritariamente utilizamos la hemodiafiltración vena-venosa continua (HDFVVC); es una técnica asociada con ratios elevados de ultrafiltración y difusión a través de una membrana altamente permeable5.
Existen estudios que recomiendan cambios electivos del hemofiltro según la patología a tratar; a las 12 h en pacientes sépticos, a las 24 h cuando el objetivo es realizar depuración renal, y a las 72 h para la eliminación de líquido7. Pero a veces la teoría y la práctica no siempre confluyen por igual. Los estudios que han analizado la vida media de hemofiltros son antiguos y la media de duración descrita es variable7. La duración del hemofiltro y los factores que pueden influir, son de vital importancia dado los costes que puede ocasionar el correcto manejo del hemofiltro por parte del profesional. La aparición y desarrollo del dialytrauma, engloba todos los eventos adversos dañinos relacionados con la TCDE, cómo son las alteraciones metabólicas, hidroelectrolíticas y/o terapéuticas8), (9. Pueden surgir problemas derivados del propio hemofiltro o complicaciones derivadas de la clínica. Las complicaciones derivadas de la técnica son: la obstrucción y/o acodamiento del catéter, el calibre y localización de los accesos vasculares, la pauta de anticoagulación, la velocidad de flujo sanguíneo, el volumen de reemplazo de fluidos y electrolitos (descritos como factores que influyen en la vida útil del hemofiltro) (10)-(12. De hecho, una de las complicaciones más frecuentes durante las TCDE es la coagulación del filtro, que se describe como una caída de presión superior a 100 mmHg y una presión transmembrana (PTM) superior a 200 mmHg, de forma mantenida, lo que obliga a cambiar de manera precoz el sistema, sin cumplir a veces el tiempo de permanencia establecido por el fabricante, que son a las 72 horas13. Las complicaciones derivadas de la propia clínica son la hemorragia al canalizar el acceso vascular, alteraciones del balance hídrico, hipotermia, trombosis y anemia por sustituciones repetidas de hemofiltros6), (7. La coagulación del hemofiltro conlleva la pérdida hemática subyacente al no retorno del volumen sanguíneo remanente del sistema5. Se ha estimado que la pérdida de sangre cada vez que se coagula el hemofiltro M100 PRESET® sin posibilidad de retorno, es de 150 ml, cantidad que varía según modelo de máquina y tamaño del mismo, lo que podría favorecer la aparición de anemia iatrogénica14), (15. El cambio frecuente de los circuitos (hemofiltro y sistemas) interrumpe el tratamiento, supone un aumento de las cargas de trabajo, pueden aumentar el coste económico y ser perjudiciales para la atención al paciente16.
A pesar de los factores descritos en la bibliografía que pueden influir en la optimización de la vida útil del hemofiltro, continúa siendo un aspecto de vital importancia realizar un diagnóstico de situación del entorno donde trabajamos para detectar aspectos de mejora en el cuidado de pacientes que precisan TCDE. Conocer las causas permitirá prevenir, lo que aumentará la duración de los equipos, reducirá costos económicos, optimizará la carga de trabajo de los profesionales de enfermería y permitirá aplicar estrategias de mejora en la atención y cuidado de pacientes portadores de hemofiltro.
Los objetivos de este estudio fueron determinar la vida media de los hemofiltros en el paciente crítico ingresado en la UCI y los principales factores asociados a su duración.
Material y Método
Diseño: Estudio descriptivo observacional transversal, realizado en la Unidad de Cuidados Intensivos (UCI) de un hospital público terciario, que dispone de 32 camas, distribuidas en 4 unidades: cirugía cardiaca, coronarias, médico quirúrgica y neurotraumatología. La recogida de datos se realizó desde enero hasta noviembre de 2019.
Población y muestra: La población a estudio fueron todos los hemofiltros utilizados en pacientes mayores de 18 años ingresados en la UCI. El servicio de Medicina Intensiva del Hospital Son Espases dispone de un consentimiento informado para el registro y uso de un conjunto mínimo de datos del paciente, obtenidos a partir de la historia clínica y gráficas evolutivas, y que es solicitado al paciente o familia al ingreso en la unidad. Este consentimiento fue evaluado favorablemente por el Comité de Ética de la Investigación de las Islas Baleares en sesión del día 27 de junio de 2019, referencia IB 3909/19 PI.
Variables: En nuestra unidad utilizamos el monitor de hemofiltración PrismaFlex®, circuitos M100 y M150 PRESET® con membrana AN69, y Oxiris® de Hospal®. Se recogieron variables sociodemográficas al inicio de la terapia: edad, sexo, índice de masa corporal (IMC) y peso, unidad de ingreso, velocidad de flujo sanguíneo (ml/h), fracción de filtrado (FF), débito horario, terapia de anticoagulación utilizada para el sistema: heparina sódica (Heparina Sódica Sala® 5000UI/ml), citratos (Prismocitrate®) o sin terapia de anticoagulación, tiempo de tromboplastina activada (TTPA), motivo de la retirada (coagulación del hemofiltro, problemas con el catéter, recambio del circuito por caducidad), hora de inicio y finalización de la terapia.
El catéter utilizado para las TCDE es GamCath® Gambro de doble luz de 11,5 Fr y 150 mm para yugular, de 13 Fr y 200 mm para femoral y de 13 Fr y 150 mm para subclavia.
La administración de heparina sódica se realiza a través del hemofiltro en perfusión continua, a una velocidad 2,1 ml/h y dosis de heparina ajustada al peso del paciente. La dosis de citrato objetivo son de 2 a 5 mmol/l de sangre. La velocidad de flujo de citrato se ajusta en proporción correcta con la velocidad de flujo sanguíneo.
Recogida de datos: El proceso de recogida de datos se realizó mediante una hoja auto diseñada. La cumplimentación de los registros fue llevada a cabo por los profesionales de la unidad y los investigadores, al inicio y finalización de la terapia. Posteriormente fueron transcritos a una base de datos.
Análisis estadístico: Se realizó un análisis descriptivo para las variables cuantitativas: medidas de tendencia central (media y mediana) y de dispersión (desviación estándar y rango intercuartílico). Para las variables cualitativas se calculó medidas de frecuencias y porcentajes. Para el análisis de las variables se utilizó la pruebas de Kruskal-Wallis y el coeficiente de correlación Rho de Spearman. Se consideró significación estadística valores de p<0,05. El análisis estadístico se realizó con el software IBM SPSS vs. 24.
Consideraciones éticas: El estudio fue presentado y aprobado por el comité de investigación del hospital el 14 de diciembre de 2018, referencia nº CI-286-18. Se ha garantizado la confidencialidad en todo momento siguiendo la Ley Orgánica de Protección de Datos y Garantía de Derechos Digitales (LOPDGDD) 3/2018 de 6 de diciembre. Los autores declaran no tener conflictos de intereses.
Resultados
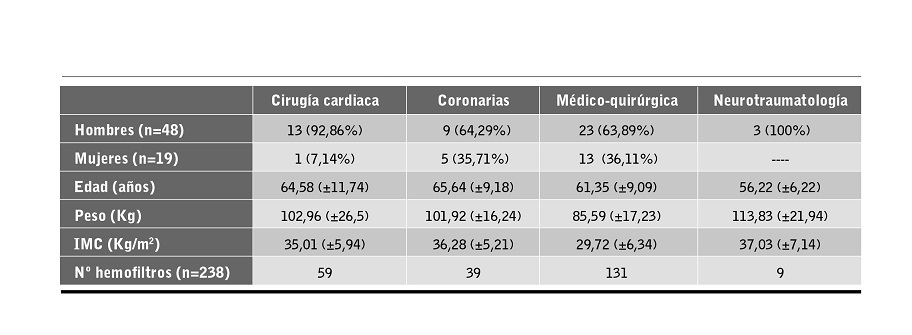
Se recogieron datos de 238 hemofiltros en una muestra de 67 pacientes. Se descartaron otros tres hemofiltros por problemas en el montaje/cebado. La edad media de los pacientes fue de 62,66 años (±9,95), el 80,1% fueron hombres. En la tabla 1 se representan las características de los pacientes y unidad de ingreso.
Tabla 1. Características de los pacientes y unidad de ingreso. Hemodiafiltración venovenosa continua (HDFVVC).
En relación al abordaje de accesos vasculares, 189 (80,1%) se insertaron en vena femoral, con un flujo medio de 193,39 ml/min (±52,98); 46 (19%) en vena yugular interna con flujo medio de 178,67 ml/min (±53,62), y 2 (0,8%) en la vena subclavia, con flujo medio de 175 ml/min (±106,07) (tabla 2).
Se calculó una media de 3,57 filtros (±5,95) por paciente. Según la indicación médica para iniciar tratamiento de TCDE, 154 (63,5%) fue por insuficiencia renal, 45 (18,5%) por shock séptico, 16 (6,6%) sobrecarga hídrica, 13 (5,4%) por alcalosis/acidosis metabólica, 4 (1,66%) por shock distributivo, 3 (1,24%) por hiperpotasemia, 2 (0,8%) por depuración por intoxicación, 2 (0,8%) en postoperatorio de cirugía cardiaca y 3 (1,24%) por otras patologías.
La velocidad media de flujo sanguíneo (VMFS) fue de 190,08 ml/min (±53,48), con una FF media (cantidad de suero que ultrafiltramos del total de plasma que pasa por el filtro en un determinado período de tiempo) de 19,02 (±7,45), y vida media del filtro de 26,28 horas (±22,8).
En relación con la terapia de anticoagulación, se empleó la heparina sódica en 105 (44,12%) de los hemofiltros, en 48 (20,17%) se utilizó citratos, y en 81 (34,03%) no se utilizó anticoagulación por contraindicación médica (presencia o riesgo aumentado de sangrado, alteraciones de la coagulación, uso de anticoagulantes sistémicos, plaquetopenia, trombocitopenia inducida por heparina). En uno de los hemofiltros (0,42%) la heparina fue aportada junto a la terapia ECMO y en 3 (1,26%) la heparina se suministró a través del catéter central. Las dosis medias de heparina pautada fueron de 5,60 U/kg/h (±2,88). El valor medio de TTPA del paciente se mantuvo de media en 37,69 (±13,5) segundos.
En relación a los factores que motivaron la interrupción de la terapia, en 128 (53,9%) de los casos la causa fue la coagulación del hemofiltro con una duración media de este de 22,72 (±16,82) horas, en 32 (13,3%) de los casos el hemofiltro llegó al final de su vida útil con una duración media de estos de 63,23 (±23,72) horas y, en otros 32 (13,3%) la causa fue problemas con el catéter y su duración media fue de 11,97 horas (±7,60).
Por problemas relacionados con el acceso vascular (presiones, obstrucción, acodamientos…) fueron retirados y sustituidos 14 (18,8%) de los circuitos tratados con citratos, 23 (11,4%) en los de heparina y 9 (11,1%) en los que no llevaron anticoagulación.
En relación con la asociación de variables, no se encontraron diferencias estadísticamente significativas entre la durabilidad de los hemofiltros sin anticoagulación, los anticoagulados con heparina y citratos (p=0,6) (figura 1).
Se encontró relación estadística entre la velocidad del flujo sanguíneo y la durabilidad del hemofiltro (rs=0,208; p=0,001); flujos más altos tuvieron duraciones más elevadas del hemofiltro. Los hemofiltros con catéteres localizados en vena yugular izquierda perduraron más horas que los de localización femoral y subclavia (figura 2). En la tabla 2 se representa la duración del hemofiltro respecto a la localización de los distintos catéteres.
No se encontró relación estadística entre la vida media del hemofiltro y los valores de TTPA (r=0,037, p=0,6.). En la tabla 3 están representados el anticoagulante utilizado, VMFS, FF, pérdida horaria y duración del hemofiltro.
Tabla 3. Anticoagulación utilizada, vida media de los hemofiltros utilizados, velocidad media de flujo sanguíneo (VMFS), fracción de filtrado (FF).

VMFS: Velocidad media del flujo de sangre.
Posterior a determinar la relación entre las variables, se aplicó el análisis de regresión lineal múltiple para determinar la relación entre aquellas que podían influir en la duración del hemofiltro. La variable flujo de sangre es un determinante que se asoció a la duración del filtro (tabla 4).
Discusión
La utilización de las TCDE en el paciente crítico y los continuos avances en este tipo de terapias tanto en los materiales como en los dispositivos, han permitido ampliar las indicaciones de las TCDE17. Una de las principales ventajas de la HDFVVC es que permite su utilización en pacientes inestables ya que es un tratamiento lento y continuado, que evita cambios bruscos en la volemia y permite una gran flexibilidad en el manejo hidroelectrolítico y el control metabólico5.
En nuestro servicio durante la realización de este estudio solo se utilizó la hemodiafiltración como terapia de TCDE, esta modalidad se utiliza en varios de los estudios consultados10), (18)-(21. La localización del acceso vasculares es una variable a tener en cuenta en la planificación de la técnica por su relevancia sobre la presencia de complicaciones. La diversidad de catéteres disponibles en función del punto de inserción proporciona los flujos de sangre necesarios para la terapia10. El sitio de elección para la inserción del catéter temporal para la terapia es la vena yugular interna derecha, debido a que el recorrido intravascular es recto y existe menor riesgo de trombosis6), (22. Así pues, el tipo de acceso vascular y el lugar de inserción son elementos a tener en cuenta para un óptimo funcionamiento del circuito, ya que para poder realizar TCDE es necesario disponer de un acceso que proporcione un buen flujo de sangre y baja resistencia al retorno23. En nuestro estudio, se registró un mayor número de catéteres insertados en la vena femoral. Es uno de los accesos de elección en pacientes críticos con escasa movilización, porque resulta fácil de abordar y es bastante segura24. Se observó una asociación entre el número de hemofiltros coagulados y dicha localización, siendo este resultado similar a otros estudios consultados10), (20), (25. A pesar de que hay un mayor número de catéteres femorales, según el análisis los de mayor durabilidad fueron los insertados en yugular izquierda. En una revisión bibliográfica reciente, se recomienda utilizar catéteres de acceso yugular debido a la anatomía del vaso, ya que es más corto y recto, por lo que favorecen la optimización y rendimiento del hemofiltro26. Un aspecto en el uso de las TCDE es la variación de la velocidad del flujo sanguíneo en función del anticoagulante utilizado. En nuestro estudio las velocidades oscilaron de 110 a 225 ml/min. La bibliografía encontrada, describe una velocidad media de flujo que oscila entre 100 ml/min y 300 ml/min, donde la modalidad principal utilizada es la HDFVVC, lo que indica una gran variabilidad para estos tratamientos10), (19)-(21),(25), (27), (28. Cabe destacar que los hemofiltros con mayor durabilidad se habían asociado a una mayor velocidad del flujo sanguíneo. En el estudio de Mottes se calculó que por cada 10 ml/min de aumento de flujo sanguíneo, equivale a un aumento del 5,8% en la supervivencia del hemofiltro29.
El número así como la vida media de los hemofiltros difieren de otras series consultadas, aunque próximos a los márgenes descritos en estos estudios (3,57 frente a 4,4 y 6,8 filtros por paciente, con una duración media de 26,28 horas frente a 17,72 y 49,4 horas) (7), (18. En nuestro estudio no observamos diferencias significativas entre la duración del hemofiltro con anticoagulación y sin anticoagulación. En los estudios consultados, la vida media oscila entre 18,7 y 49,9 h, y en hemofiltro con citratos llegan hasta las 92,8 h7), (16.
Cabría esperar que a valores más elevados de TTPA, la vida media del hemofiltro fuese mayor. Según el estudio de Bouman, existe una asociación positiva entre el TTPA y la vida media de los hemofiltros30. Nuestros datos reflejaron que valores más bajos de TTPA coincidieron con hemofiltros de vida media más corta, pero no se ha podido demostrar estadísticamente.
La coagulación del hemofiltro implica la retirada de la terapia o el recambio del circuito y continuar con la terapia. Existen estudios que afirman que la coagulación es una de las principales causas de retirada (22,6%; 29,6%)7), (10, siendo en nuestro estudio muy superior (53,9%). Entre los factores asociados a la coagulación del hemofiltro, el mal funcionamiento del catéter puede ser un factor de riesgo de coagulación del hemofiltro31 nuestros resultados también son superiores a los encontrados en la bibliografía (13,3% vs 5,8%)32.
Para prolongar la vida media de los hemofiltros es necesario una monitorización constante de las presiones del circuito (especialmente la tendencia, que proporciona información sobre el estado del sistema), utilización de catéteres apropiados, modificación de la fracción de filtración para mantenerla por debajo del 20% o realizar 1/3 de la reposición prefiltro6. El número de alarmas, los problemas mecánicos que puedan surgir durante la terapia y la falta de formación se han asociado a peor vida útil del hemofiltro9), (33. En un estudio realizado en nuestra unidad sobre formación en TCDE, las enfermeras y médicos manifestaron la necesidad de formación y reciclaje continuo34), (35. A pesar de haber realizado formación, la incorporación de nuevo personal, y una continua rotación de parte de los profesionales de enfermería, hacen que la formación recibida quede obsoleta a corto-medio plazo34. Una auditoría de la vida útil del hemofiltro es una información útil y necesaria para las estrategias de formación del personal de enfermería. Quizás se debería insistir en realizar más formación en el control de la técnica y conocimiento de aquellas variables que puedan predecir y detectar una coagulación precoz. La coagulación del hemofiltro es un evento adverso por lo que fomentar una actitud proactiva y promover estrategias para prevenir riesgos asociados a la terapia, puede mejorar la eficacia de la terapia y mejorar la seguridad del paciente.
Como limitaciones del estudio, hay que destacar el tamaño muestral, al tratarse de un estudio realizado en un único centro. En nuestra UCI, a pesar de disponer de un protocolo de anticoagulación con citratos, existe mucha variabilidad a la hora de prescribir la terapia de anticoagulación, no existiendo un consenso cuando se prescribe una terapia con otro anticoagulante, como por ejemplo la heparina sódica. Aún siendo referencia en el campo de las TCDE, la obsolescencia de algunas de las publicaciones científicas consultadas han dificultado poder comparar los resultados con estudios más actuales.
A partir de los resultados obtenidos en nuestro estudio podemos apreciar que la vida media de los hemofiltros estudiados está en torno a 26 h, situándose dentro de los rangos descritos por otros autores. Los hemofiltros sin anticoagulación presentan valores similares en cuanto a duración y velocidad media respecto a los hemofiltros con anticoagulación. Los hemofiltros en los que el acceso vascular era un catéter yugular izquierdo registraron mayor número de horas de supervivencia respecto al resto de localizaciones.
Debemos plantearnos mejorar el tiempo de duración de los hemofiltros e invertir esfuerzos en mejorar la formación de enfermeras y médicos, para reducir riesgos y costes asociados a las TCDE.


















