Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de Zootecnia
versión On-line ISSN 1885-4494versión impresa ISSN 0004-0592
Arch. zootec. vol.60 no.231 Córdoba sep. 2011
https://dx.doi.org/10.4321/S0004-05922011000300064
Estructura genética y cuello de botella de la población bovina Guaymí mediante microsatélites
Genetic structure and bottleneck of the Guaymi bovine population by means of microsatellites
Villalobos Cortés, A.I.1*, Martínez, A.M.2, Vega-Pla, J.L.3 y Delgado, J.V.2
1Instituto de Investigación Agropecuaria. Estación Experimental El Ejido. Los Santos. Panamá. z62vicoa@uco.es
2Departamento de Genética. Universidad de Córdoba. Córdoba. España. ib2mamaa@uco.es
3Laboratorio de Investigación Aplicada. Cría Caballar de las Fuerzas Armadas. Córdoba. España. jvegpla@oc.mde.es
RESUMEN
Se caracterizó la población bovina Guaymí con un panel de 27 microsatélites seleccionados a partir de las recomendaciones hechas por la FAO/ISAG. Se analizaron muestras aleatorias de ADN obtenidas de la población bovina criolla Guaymí que se encuentran ubicadas en el área que comprende la comarca indígena Ngöbe-Buglé en la zona montañosa de la provincia de Chiriquí en la República de Panamá. Para cada microsatélite se calcularon el contenido de información polimórfica (PIC), el número medio de alelos (Na), la heterocigosis observada (Ho), la heterocigosis esperada (He), el estadístico FIS, y equilibrio Hardy-Weinberg (HWE). Además se calculó si existía cuello de botella en esta población. Los valores obtenidos fueron: PIC: 0,6899; Ne: 4,04; He: 0,7243; Ho: 0,7088; FIS: 0,0356. Se observaron tres microsatélites en desequilibrio (p<0,05). Los valores encontrados se consideran dentro de los rangos obtenidos en otras poblaciones criollas, exóticas y autóctonas españolas. Se requiere realizar estudios más detallados de estas poblaciones y su relación con otras poblaciones bovinas. No se observa cuello de botella en el pasado reciente de esta población.
Palabras clave: Criollo. Conservación.
SUMMARY
Guaymi creole cattle were characterized by a 27 microsatellite panel, selected from a recommendation of FAO/ISAG. Random samples of DNA were taken from Guaymi creole cattle population in the highlands of the Chiriqui province in Ngöbe-Buglé region in the Panama Republic. From each microsatellite, was calculated the polymorphic information content (PIC), mean number of alleles (Na), observed heterozygosity (Ho), expected heterozygosity (He), the FIS statistic, the exact test for Hardy-Weinberg equilibrium (HWE). Besides a bottleneck study was calculated in this population. The result of the analysis show a PIC: 0.6899; Ne: 4.04; He: 0.7243; Ho: 0.7088; FIS: 0.0356. Three microsatellites were in unbalance (p<0.05). The Results are considered in the same range of values from other creoles, exotics and Spanish native populations. It requires more detailed studies of these populations and its relation to other cattle populations. No bottleneck was showed in the recent past.
Key words: Creole. Conservation.
Introducción
Los primeros informes oficiales de entrada de bovinos en Panamá se observan en la Cédula Real de Burgos del 6 de septiembre de 1521, desde la isla de Santiago (Jamaica)a solicitud de Pedro Arias de Ávila, de importar cincuenta reses y otros bastimentos para repartir entre los vecinos de la ciudad (Archivo General de Indias, 1521). A raíz de este hecho y con la rápida proliferación de estos animales dentro del nuevo territorio y la fundación de nuevas ciudades, se llevaron a cabo migraciones desde Panamá hacia el oeste llegando hasta Chiapas, México y desde Panamá hacia la región de Perú en Suramérica (Archivo General de Indias, 1532; Cortés, 2002). En Panamá existen dos poblaciones criollas, la Guabalá que se encuentra ubicada en manos de productores privados en zonas de trópico húmedo a nivel del mar en la provincia de Chiriquí y que fue identificada en el año 2006 (Villalobos et al., 2009) y la Guaymí que está en manos de productores de la región indígena Ngöbe-Buglé. Ambas poblaciones son de gran importancia dentro de los estudios de biodiversidad y su potencial utilización en la producción animal de tipo ecológico. Las últimas poblaciones de bovinos criollos Guaymí se encuentran ubicadas en el área que comprende la comarca indígena Ngöbe-Buglé en la zona montañosa de la provincia de Chiriquí y se han identificado una diversidad de colores de la capa como berrendo en negro, berrendo colorado, cenizo, negro, negro cariblanco y presenta gran diversidad en el tamaño de pelo. El tamaño medio de estos animales es de 1,20 m a la altura de la cruz y 1,79 m de longitud corporal. El peso medio al nacimiento es de 27 y 28 kg hembras y machos respectivamente y un peso medio de 465 kg en estado adulto (Villalobos, 2010). Esta población de animales convive con las comunidades indígenas Ngöbe-Buglé en la que existe un importante aislamiento geográfico de la zonas urbanas, no hay caminos de acceso y se practica una agricultura de subsistencia con altos niveles de pobreza. Estos animales son aprovechados como fuente de proteína animal ya que debido a la llegada de las poblaciones bovinas a Panamá en 1521, se han logrado adaptar perfectamente al medio y no requiere manejo sanitario especializado, además por su alta fertilidad requiere un mínimo manejo reproductivo. Aprovechan pastos de baja calidad y se observan en zonas a nivel del mar y por encima de los 1000 metros. Por su gran capacidad de adaptación, estos bovinos criollos serían muy importantes para los sistemas de producción de carne y en sistemas de cruzamientos donde se requiera un componente de adaptación y resistencia ambiental. En cuanto a la cantidad de bovinos Guaymí en el territorio panameño, se estima que existen menos de 1000 hembras, por lo que se encontrarían en la categoría de población en peligro según la clasificación de la FAO (2000). Los marcadores moleculares tipo microsatélites de ADN han sido utilizados para estudios de caracterización y diversidad genética, relaciones genéticas entre poblaciones, influencia de una raza sobre otra (admixture), pruebas de paternidad, consanguinidad y cuellos de botella genéticos entre otros (Spencer et al., 2000; Quiroz et al., 2004; Martínez et al., 2005; Quiroz et al., 2007). El objetivo de este trabajo es caracterizar genéticamente, la población bovina Guaymí mediante micro-satélites y determinar si existe cuello de botella.
Material y métodos
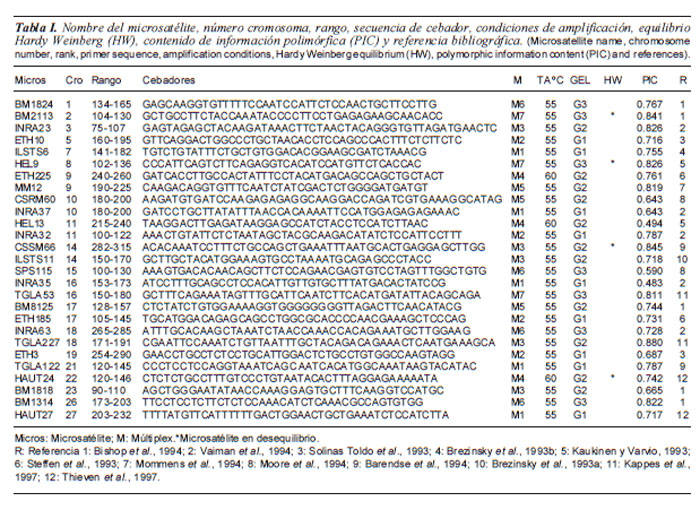
En el presente trabajo se estimaron algunos parámetros de diversidad genética en la población bovina Guaymí con un panel de 27 microsatélites seleccionados a partir de las recomendaciones hechas por la FAO/ ISAG (Food and Agriculture Organization/ International Society of Animal Genetics) para realizar estudios de biodiversidad genética bovina (FAO, 2004). La tabla I muestra los datos generales de los microsatélites utilizados.
Se analizó el ADN obtenido de un muestreo aleatorio de 50 hebras de pelo de la zona caudal de 36 individuos de las poblaciones bovinas criollas Guaymí en la región occidental de la república de Panamá, dentro de la Comarca Ngöbe-Buglé (8o26" de latitud Norte y 81o51' longitud Oeste); en el Laboratorio de Genética Molecular Aplicada del Grupo de Investigación AGR-218 de la Universidad de Córdoba. Se tomaron 10 hebras de pelo con folículo de la zona caudal de los animales muestreados, seguidamente se procedió a la extracción de ADN utilizando el kit BLOODCLEAN (Biotools-Biotechnological & Medical Laboratorios, S.A). Los microsatélites se amplificaron mediante la técnica de la reacción en cadena de la polimerasa (PCR) según la metodología de Martínez et al. (2000). Los fragmentos obtenidos de la PCR se separaron por medio de una electroforesis en un gel de poliacrilamida utilizando un secuenciador automático ABI Prism 377XL (Applied Biosystems, Foster City, CA, USA). Se utilizó el reactivo comercial ReprogelTM 377 (Amersham Pharmacia Biotech) de acrilamida/bisacrilamida con una concentración final de 6%, que contiene un desnaturalizante a base de Urea, un iniciador para luz ultravioleta y TBE. Se diseñaron varias reacciones denominadas múltiplex (M1-7) para reducir el número de reacciones y los costes de los experimentos. Con el programa Genescan (Genescan 672 v.3.1.2) se analizaron los datos obtenidos del secuenciador automático que proporciona información del tamaño de los fragmentos estudiados. El empleo del secuenciador automático y de las aplicaciones informáticas, ofrecen la posibilidad de marcar los cebadores de ADN con fluorocromos de tres colores diferentes (amarillo, azul y verde), usando un cuarto color (rojo) que marca un estándar de tamaños. Una vez que se ha calculado el tamaño de cada banda se seleccionan aquellas que representen un alelo y las demás se descartan y se procede a enviar al programa Genotyper 3.7 NT. El programa Genotyper, analiza las gráficas de las bandas obtenidas con el programa Genescan e identifica los diferentes alelos presentes en cada uno de los microsatélites.
La metodología estadística utilizada se basó en el cálculo de la variabilidad genética intrapoblacional y la determinación del cuello de botella. Para evaluar la variabilidad genética de la población Guaymí, se calcularon los siguientes parámetros: la heterocigosis observada y esperada (He, Ho), total de alelos por población (Ap), número efectivo de alelos (Ne), el contenido de información polimórfica (PIC) y las desviaciones del equilibrio de Hardy-Weinberg por población. Para calcular las frecuencias alélicas, las heterocigosis y el valor de FIS (Wright, 1965; Weir and Cockerham, 1984) se utilizó el programa Genetix v. 4.02 (Belkhir et al., 2003). Para el cálculo del equilibrio Hardy-Weinberg (HW) se utilizó el programa Genepop v.3.1c (Raymond and Rousset, 1995) mediante la aplicación del test exacto de FIS her usando el método en cadena de Monte Carlo Markov, dememorización= 5000, 100 lotes y 10000 iteraciones por lote (Guo and Thompson, 1992). Para el cálculo del Contenido de Información Polimórfica (PIC) de cada microsatélite se aplicó la fórmula propuesta por (Botstein et al., 1980) empleando el complemento The Excel Microsatellite Toolkit (Park, 2001), utilizando el programa MS EXCEL® 2003.
Para estimar si la población ha sido afectada por una disminución en su tamaño y la generación de un cuello de botella, se utilizaron dos métodos. El primer método se basa en tres pruebas que son: la de signos, de diferencias estandarizadas y de rangos de Wilcoxon, que se utilizan para determinar el exceso de Heterocigosis (Cornuet and Luikart, 1996). El otro método, es una representación gráfica del indicador de cambio de moda (Luikart et al., 1998). Este consiste en agrupar alelos de una muestra con un mínimo de 5 loci polimórficos en un histograma de frecuencias de 10 clases. La conclusión que una población ha sufrido cuello de botella se basa en que pocos alelos se encuentren en la frecuencia más baja en relación a las frecuencias medias y altas. La distribución de He bajo el modelo de mutación y deriva para cada locus y población fue obtenida mediante la simulación de un proceso de coalescencia (el tiempo en el que se lleva a un ancestro común).
Debido a que un microsatélite puede evolucionar a través de mutaciones, se utilizaron tres modelos: El modelo de alelos infinitos (IAM) que asume que cada mutación produce un alelo nuevo, diferente a los que previamente existían (Kimura and Crow, 1964). El modelo de mutación por pasos SMM, es un modelo estricto en el cual los cambios se realizan un paso hacia delante o hacia atrás, con igual probabilidad (Ota and Kimura, 1973). Ambos modelos, el IAM y SMM son modelos extremos dentro del rango de posibles modelos de mutación. El modelo de mutación de dos fases TPM (Di Rienzo et al., 1994), es un modelo intermedio entre ambos IAM y SMM, se aplicó combinando 70% SMM y 30% (Luikart and Cornuet, 1998). Para analizar los tres modelos se utilizó el programa informático Bottleneck v1.2.02, http://www.ensam.inra.fr/URLB (Piry et al., 1999).
Resultados y discusión
Se encontró que la desviación de equilibrio de Hardy-Weinberg fue estadísticamente significativa (p<0,05) para los loci Bm2113, HEL9 y HAUT24 (3/27) con lo cual estaríamos estimando que la población Guaymí tiene menos microsatélites desequilibrados que los encontrados en la población Guabalá (Villalobos et al., 2009). Es importante que en la mayoría de los loci estudiados exista este equilibrio, dado que es prerrequisito para realizar evaluaciones posteriormente, como el uso de modelos bayesianos (Pritchard et al., 2000). El número medio de alelos obtenido fue de 7,4 y un total de alelos en la población de 202; el locus con mayor valor fue TGLA227 con 0,8553 y el menor valor se encontró en INRA35 con 0,4048. Todos los marcadores empleados estuvieron en la categoría de altamente informativos, a excepción de HEL13 e INRA35 quienes mostraron valores medianamente informativos de 0,455 y 0,405 respectivamente. Los valores de heterocigosis media esperada y observada fueron de 0,7346 y 0,7088 respectivamente. La heterocigosis media esperada y heterocigosis media observada, el número medio de alelos y el valor de Fis. La tabla II muestra que los valores de He son mayores a los publicados para las razas Hereford (0,589), Mostrenca (0,593), Criollo Patagónico (0,611), Guabalá (0,646), Criollo Argentino (0,651) y Pajuna con 0,706. Por otro lado son menores a los reportados en las poblaciones criollas colombianas, BON (0,800) Romosinuano (0,780) y Costeño (0,770). En lo que se refiere a Ho la población Guaymí resultó con el segundo valor más alto (0,709) detrás de la BON (0,720) En lo que se refiere al Ne, la población Guaymí presenta los valores más altos (4,04) mayor a la Pajuna que reporta un valor de Ne de 3,60 seguido del Guabalá con 3,51 (Barrera et al., 2006; Quiroz-Valiente, 2007; Martínez, 2008; Villaloboset al., 2009). Cabe destacar que la población Guaymí presenta una mayor diversidad genética que la población, Guabalá aunque no se debe descartar que podría existir una alteración de estos índices por efecto de las razas cebuínas y exóticas que influenciaron a las poblaciones criollas en Latinoamérica, con cruzamientos mal dirigidos como el caso de Panamá en el año 1914 (Jaén, 1998). El valor de Fis reportado muestra que esta población presenta bajos índices de endogamia y son susceptibles, todavía, de ser recuperadas y montar programas de conservación, reestructuración y mejoramiento en beneficio de las poblaciones indígenas de las que depende para su subsistencia y además ser utilizadas como fuente de variabilidad genética en sistemas de cruzamientos donde se requiere un tipo animal que aporte resistencia y rusticidad, como es el caso de los sistemas de doble propósito, que aprovechan la producción de leche y carne en las zonas tropicales.
Los resultados de los análisis de cuello de botella (tabla III) muestran diferencias en cuanto a las probabilidades en las pruebas y modelos que fueron utilizados. En el caso de la prueba de signos, el número esperado de loci con exceso de heterocigosis y las respectivas probabilidades fue de 16,01; 16,21 y 16,01, y 0,0037; 0,4397 y 0,0000 para los modelos IAM, TPM y SMM respectivamente. En este caso se rechaza la hipótesis nula en el modelo IAM y SMM. En cuanto a la prueba de diferencias estandarizadas, se observa que se rechaza la hipótesis nula en los modelos IAM y SMM (0,0006 y 0,0000) pero no en el TPM (0,3252). La prueba de rangos de Wilcoxon mostró rechazo en la hipótesis nula en el modelo IAM (0,0005) y no se mostró rechazo en el modelo TPM (0,1010) y SMM (0,9995). Como el modelo IAM muestra rechazo en la hipótesis nula (p<0,05), se concluye que el equilibrio de mutación y deriva no se cumple. Di Rienzo et al. (1994) observaron que el modelo IAM se ajusta mejor que el SMM cuando se trata de microsatélites dinucleotídicos por lo que los resultados que obtenemos con este modelo son más creíbles que los otros.
En lo que se refiere al análisis de cambio de moda (figura 1), se observan contradicciones con el modelo anterior ya que mostró la existencia de una alta proporción de alelos en las frecuencias alélicas más bajas, por lo que según el mismo, las poblaciones bovinas Guaymí no han sufrido cuello de botella en el pasado reciente. Mediante el análisis de cuello de botella se confirma que la población bovina Guaymí no ha sufrido cuello de botella en el pasado reciente. Estos resultados son similares a los reportados por Quiroz-Valiente (2007) quien encontró influencia cebuínas en los bovinos criollos de Chiapas (24%) y Nayarit (10%) lo que reforzaría la posible presencia de alelos nuevos en el proceso de formación de estas poblaciones antes de su posterior aislamiento geográfico o el posible movimiento de animales hacia las montañas por parte de los propios indígenas, por lo que el estudio comparativo mediante otras técnicas como modelos de distancias genética, árboles de relaciones o NeighborNet y modelos bayesianos (Nei, 1972; Pritchard et al., 2000; Huson and Bryant, 2006) serían útiles para dilucidar estas interrogantes. Es posible que este mismo fenómeno se podría estar presentando, ya que durante décadas pasadas los cebuínos fueron utilizados como modelos de mejoramiento genético y fueron dispersados por todo el continente americano y utilizados dentro de sistemas de cruzamientos de forma indiscriminada.
Conclusiones
El bovino criollo Guaymí presenta una alta variabilidad genética y niveles de endogamia relativamente bajos pero es recomendable estudiar mediante otros modelos si existe influencia de otras poblaciones sobre este resultado. No se detectó efecto de cuello de botella sobre las poblaciones estudiadas. Debido a la importancia socioeconómica que representan estas poblaciones dentro de las comarcas indígenas del territorio panameños, el interés por la búsqueda de nuevas fuentes de biodiversidad de animales domésticos y la importancia histórica para el país, se recomienda profundizar los estudios de la población Guaymí con el fin de establecer programas de conservación, estructuración y mejoramiento genético.
Bibliografía
Archivo General de Indias. 1521. Despacho para la ciudad de Panamá. Portal de Archivos Españoles. Sevilla. Panamá. 233, L.1, F.288V-290R. http://pares.mcu.es/ (20/08/07). [ Links ]
Archivo General de Indias. 1532. Licencia a Diego de Almagro para pasar ganados a Túmbez. Portal de Archivos Españoles. Sevilla. Panamá. 234, L.5, F.34R. http://pares.mcu.es/ (20/08/07). [ Links ]
Barendse, W.S., Armitage, M., Kossarek, L.M., Shalom, A., Kirkpatrick, B.W., Ryan, A.M., Clayton, D., Li, L., Neibergs, H.L., Zhang, N., Grosse, W.M., Weiss, J., Creighton, P., McCarthy, F., Ron, M., Teale, A.J., Fries, R., McGraw, R.A., Moore, S.S., Georges, M., Soller, M., Womack, J.E. and Hetzel, D.J.S. 1994. A genetic linkage map of the bovine genome. Nat. Genet., 6: 227-235. [ Links ]
Barrera, G.P., Martínez, R., Pérez, J.E., Polanco, N. y Ariza, F. 2006. Evaluación de la variabilidad genética en Ganado Criollo Colombiano mediante 12 marcadores microsatélites. AGRI, 38: 35-45. [ Links ]
Belkhir, K., Borsa, P., Chikhi, L., Raufaste, N. et Bonhomme, F. 2003. Genetix: 4.05 Logiciel sous Windows TM pour la genetique des populations. In: U.d. Montpellier (ed.). Laboratoire Genoma Populations, Interactions, Adaptations. Montpellier. France. [ Links ]
Bishop, M.D., Kappes, S.M., Keele, J.W., Stone, R.T., Sunden, S.L., Hawkins, G.A., Toldo, S.S., Fries, R., Grosz, M.D., Yoo, J. and Beattie, C.W. 1994. A genetic linkage map for cattle. Genetics, 136: 619-639. [ Links ]
Botstein, D., White, R.I., Skolnich, M. and Davis, R.W. 1980. Construction of a genetic linkage map in man using restriction fragment length polymorphism. Amer. J. Hum. Genet., 32: 324-331. [ Links ]
Brezinsky, L., Kemp, S.J. and Teale, A.J. 1993a. Five polymorphic bovine microsatellites (ILSTS010-014). Anim. Genet., 24: 75-76. [ Links ]
Brezinsky, L., Kemp, S.J. and Teale, A.J. 1993b. ILSTS006: a polymorphic bovine. Anim. Genet., 24: 73. [ Links ]
Cornuet, J.M. and Luikart, G. 1996. Description and power analysis of two tests for detecting recent population bottlenecks from allele frequency data. Genetics, 144: 2001-2014. [ Links ]
Cortés, R. 2002. Sociedad y naturaleza antes y después de la conquista y colonización de América Central. Intercambio. Universidad de Costa Rica. No1. [ Links ]
Di Rienzo, A., Peterson, A.C., Garza, J.C., Valdes, A.M. and Slatkin, M. 1994. Mutational processes of simple sequence repeat loci in human populations. Proc. Nat. Acad. Sci. USA., 91: 3166-3170. [ Links ]
FAO. 2000. World watch list for domestic animal diversity. 3rd ed. Rome. Italy. pp. 726. http://www.fao.org/docrep/009/x8750e/x8750e00.HTM. (10/08/09). [ Links ]
FAO. 2004. Secondary guidelines for development if natural farm animals genetic resources management plans: Measurement of domestic animal diversity (MoDAD): Recommended microsatellite markers. FAO ed. Roma. Italy. [ Links ]
Guo, S.W. and Thompson, E.A. 1992. Performing the exact test of Hardy-Weinberg proportion for multiple alleles. Biometrics, 48: 361-372. [ Links ]
Huson, D.H. and Bryant, D. 2006. Application of phylogenetic networks in evolutionary studies. Mol. Biol. Evol., 23: 254-267. [ Links ]
Jaén, O. 1998. La población del istmo de Panamá. 1aed. Agencia Española de Cooperación Internacional. Panamá. [ Links ]
Kappes, S.M., Keele, J.W., Stone, R.T., McGraw, R.A., Sonstegard, T.S., Smith, T.P., Lopez-Corrales, N.L. and Beattie, C.W. 1997. A secondgeneration linkage map of the bovine genome. Genome Res., 7: 235-249. [ Links ]
Kaukinen, J. and Varvio, S.L. 1993. Eight polymorphic bovine microsatellites. Anim. Genet., 24: 148. [ Links ]
Kimura, M. and Crow, J.F. 1964. The number of alleles that can be maintained in a finite population. Genetics, 49: 725-38. [ Links ]
Luikart, G. and Cornuet, J.M. 1998. Empirical evaluation of a test for identifying recently bottlenecked populations from allele frequency data. Cons. Biol., 12: 228-237. [ Links ]
Luikart, G., Allendorf, F.W., Cornuet, J.M. and Sherwin, W.B. 1998. Distortion of allele frequency distributions provides a test for recent population bottlenecks. J. Hered., 89: 238-247. [ Links ]
Martínez, A.M., Delgado, J.V., Rodero, A. and Vega-Pla, J.L. 2000. Genetic structure of the Iberian pig breed using microsatellites. Anim. Genet., 31: 295-301. [ Links ]
Martínez, A.M., Calderón, J., Camacho, E., Rico, C., Vega-Pla, J.L. and Delgado, J.V. 2005. Caracterización genética de la raza bovina Mostrenca con microsatélites. Arch. Zootec., 54: 357-361. [ Links ]
Martínez, R.D. 2008. Caracterización genética y morfológica del bovino Criollo argentino de origen patagónico. Tesis. Universidad Politécnica de Valencia. Valencia. [ Links ]
Mommens, G., Coppieters, W., Van de Weghe, A., Van Zeveren, A. and Bouquet, Y. 1994. Dinucleotide repeat polymorphism at the bovine MM12E6 and MM8D3 loci.Anim. Genet., 25: 368. [ Links ]
Moore, S.S., Byrne, K., Berger, K.T., Barendse, W., McCarthy, F., Womack, J.E. and Hetzel, D.J.S. 1994. Characterization of 65 bovine microsatellites. Mamm. Genome, 5: 84-90. [ Links ]
Nei, M. 1972. Genetic distances between populations. Am. Nat., 106: 283-292. [ Links ]
Ota, T. and Kimura, M. 1973. A model of mutation appropiate to estimate the number of eletrophoretically detectable alleles in an finite population. Genet. Res., 22: 201-204. [ Links ]
Park, S.D.E. 2001. Trypanotolerance in West African Cattle and the population genetic effects of selection. Thesis doctoral. University of Dublin. Dublin. [ Links ]
Piry, S., Luikart, G. and Cornuet, J.M. 1999. Computer note. BOTTLENECK: a computer program for detecting recent reductions in the effective size using allele frequency data. J. Hered., 90: 502-503. [ Links ]
Pritchard, J., Stephens, M. and Donnelly, P. 2000. Inference of population structure from multilocus genotype data. Genetics, 155: 945-959. [ Links ]
Quiroz, J., Martínez, A., Marques, J., Calderón, J. y Vega-Pla, J. 2007. Relación genética de la vaca Marismeña con algunas razas andaluzas. Arch. Zootec., 56: 449-454. [ Links ]
Quiroz, V.J., Martínez, M.A., Martínez, R.D., Armstrong, E., Calderón, J. y Delgado, J.V. 2004. Relaciones genéticas de la raza Mostrenca con otras razas bovinas. IV Congreso Ibérico sobre Recursos Genéticos Animales. Ponte de Lima. Portugal. [ Links ]
Quiroz-Valiente, J. 2007. Caracterización genética de los bovinos Criollos mexicanos y su relación con otras poblaciones bovinas. Tesis. Universidad de Córdoba. Córdoba. [ Links ]
Raymond, M. and Rousset, F. 1995. GENEPOP (version 1.2): A population genetics software for exact test and ecumenicism. J. Hered., 86: 248-249. [ Links ]
Spencer, C.C., Neigel, J.E. and Leberg, P.L. 2000. Experimental evaluation of the usefulness of microsatellite DNA for detecting demographic bottlenecks. Mol. Ecol., 9: 1517-1528. [ Links ]
Steffen, P., Eggen, A., Dietz, A.B., Womack, J.E., Stranzinger, G. and Fries, R. 1993. Isolation and mapping of polymorphic microsatellites in cattle. Anim. Genet., 24: 121-124. [ Links ]
Solinas Toldo, S., Fries, R., Steffen, P., Neibergs, H.L., Barendse, W., Womack, J.E., Hetzel, D.J. and Stranzinger, G. 1993. Physically mapped, cosmidderived microsatellite markers as anchor loci on bovine chromosomes. Mamm. Genome, 4: 720-727. [ Links ]
Thieven, U., Solinas-Toldo, S., Friedl, R., Masabanda, J., Fries, R., Barendse, W., Simon, D. and Harlizius, B. 1997. Polymorphic camicrosatellites for the integration of the bovine genetic and physical map. Mamm. Genome, 8: 52-55. [ Links ]
Vaiman, D., Mercier, D., Moazamigoudarzi, K., Eggen, A., Ciampolini, R., Lepingle, A., Velmala, R., Kaukinen, J., Varvio, S.L., Martin, P., Leveziel, H. and Guerin, G. 1994. A Set of 99 cattle microsatellites. Characterization, synteny mapping, and polymorphism. Mamm. Genome, 5: 288-297. [ Links ]
Villalobos, A., Martínez, A.M., Vega Pla, J. y Delgado, J.V. 2009. Caracterización genética de la población bovina Guabalá mediante microsatélites. Arch. Zootec., 58: 485-488. [ Links ]
Villalobos, A. 2010. Caracterización genética de la población bovina Guabalá mediante microsatélites. Tesis Doctoral. Universidad de Córdoba. España. pp. 24. [ Links ]
Weir, B.S. and Cockerham, C.C. 1984. Estimating F-statistics for the analysis of population structure. Evolution, 38: 1358-1370. [ Links ]
Wright, S. 1965. The interpretation of population structure by F-statistics with special regard to systems of mating. Evolution, 19: 395-420. [ Links ]
Recibido: 14-9-09
Aceptado: 29-3-10