Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos Españoles de Urología (Ed. impresa)
versión impresa ISSN 0004-0614
Arch. Esp. Urol. vol.60 no.3 abr. 2007
TRASPLANTE
Autotrasplante renal: Una alternativa válida en la resolución de casos complejos
Renal autotransplantation: a valid option in the resoltion of complex cases
Luis López-Fando Lavalle, Javier Burgos Revilla, Javier Sáenz Medina1, Ana Linares Quevedo1, Jorge Vallejo Herrador1,
Cristina De Castro Guerin, Julio Pascual Santos2 y Roberto Marcén Letosa2
Servicio de Urología Ramón y Cajal, Madrid.
Servicio de Urología Hospital de Fuenlabrada1. Madrid.
Servicio de Nefrología2. Hospital Ramón y Cajal. Madrid. España.
Dirección para correspondencia
RESUMEN
Objetivo: Analizar las indicaciones actuales del auto-trasplante renal (ATR), así como los aspectos técnicos, complicaciones y seguimiento a largo plazo de esta técnica.
Métodos: Desde 1990 a 2005 se han llevado a cabo un ATR en 10 pacientes, 7 adultos y 3 niños. La indicación fue por patología del pedículo vascular en 8 casos y por lesión ureteral en 2. En los 8 casos con patología vascular, ésta se distribuyó en: estenosis por ateromatosis (4), estenosis por displasia (2), estenosis por enfermedad de Takayasu (1) y aneurisma de arteria renal (1). Los dos pacientes con lesión ureteral correspondieron a una estenosis ureteral secundaria a Enfermedad de Crohn inicialmente resuelta mediante stent ureteral, que posteriormente se obstruyó por incrustación litiásica; y una por avulsión ureteral yatrógena post-ureteroscopia. En los 8 casos en que fue necesaria la reconstrucción vascular los injertos vasculares utilizados fueron: en 7 pacientes arteria hipogástrica y en 1 vena sáfena. En 5 casos fue necesario llevar a cabo una reimplantación ureteral tras la cirugía de banco, mientras que en otros 5 la reconstrucción vascular se realizó sin desinsercción ureteral. En todos los casos los injertos fueron perfundidos con Ringer Lactato o Wisconsin a 4ºC y protegidos con isquemia fría de superficie. Los tiempos de isquemia oscilaron entre 42 y 89 min.
Resultados: Nueve (90%) riñones fueron funcionantes tras el ATR teniendo 8 de ellos función inmediata tras la intervención y uno de ellos función retardada tras un período de necrosis tubular de 6 días de duración. El riñón nunca funcionante correspondió al de la estenosis arterial secundaria a enfermedad de Takayasu. La causa de la pérdida del injerto fue la trombosis de la vena renal. La mortalidad postoperatoria de la serie fue nula (0%).Con un tiempo medio de seguimiento de 72+-13 meses la creatinina media es de 1,6+-0,4 mg/dl (1,1-2,4) y el 70% (7/10) de los pacientes están normotensos sin necesidad de medicación hipotensora.
Conclusiones: El ATR, con o sin reconstrucción vascular extracorpórea, es una técnica compleja que tiene indicaciones excepcionales en la actualidad, pero que permite rescatar unidades renales afectas de patología vascular no subsidiarias de angioplastia o revascularización in situ. Así mismo, es una alternativa válida a la interposición de ileon en casos de lesión ureteral extensa.
Palabras clave: Autotrasplante renal. Lesión ureteral. Lesión vascular.
SUMMARY
Objectives: To analyze the current indications for renal autotransplantation, as well as the technical features, complications and long-term follow-up of the technique.
Methods: From 1990 to 2005 we have performed autotransplantation in 10 patients, 7 adults and 3 children. The indication was established due to vascular pedicle pathology in 8 cases and ureteral lesion in 2. The cause of vascular pathology was: atherosclerotic stenosis (4), dysplastic stenosis (2), Takayasus disease stenosis (1), and renal artery aneurysm (1). The patients with ureteral lesion had ureteral stenosis secondary to Crohns disease in one case, initially solved by ureteral stent and subsequently obstructed by lithiasic encrustation, and ureteral avulsion in the other case. The vascular grafts employed in the 8 cases with vascular reconstruction were: hypogastric artery 7 cases, and saphena vein in one case. Ureteral reimplantation was necessary in 5 cases after bench surgery; in other five cases vascular reconstruction was performed without ureteral division. All grafts were perfused with 4ºC lactate ringer or Wisconsin solution and protected with surface cold ischemia. Ischemia times ranged from 42 to 89 minutes.
Results: Nine kidneys (90%) functioned after autotransplantation, 8 of them had immediate function, and one had delayed graft function after a six-day period of acute tubular necrosis. The kidney with arterial stenosis secondary to Takayasus disease never functioned. The cause of graft loss was renal vein thrombosis. Postoperative mortality was zero. After a mean follow-up of 72+/- 13 months mean serum creatinine is 1.6+- 0.4 mg/dl (1.1-2.4) and 70% (7/10) of the patients have normal blood pressure without antihypertensive medication.
Conclusions: Currently, renal autotransplantation, with or without extracorporeal vascular reconstruction, is a complex technique with exceptional indications, but it allows recovering renal units with vascular pathology not amenable to angioplasty or in situ revascularization. It is also a valid alternative to ileal ureteral substitution in cases of extensive ureteral lesion.
Keywords: Renal Autotransplantation. Ureteral lesion. vascular lesion.
Introducción
El avance y la introducción de nuevas técnicas de revascularización mínimamente invasivas, como la angioplastia transluminal percutánea (ATP) y la implantación de prótesis autoexpandibles (stent) han limitado la realización de la cirugía reconstructiva del pedículo vascular renal y por tanto las indicaciones del autotrasplante renal (ATR) (1).
En el momento actual el ATR es un procedimiento infrecuente, con indicaciones excepcionales que se reserva para la resolución de casos seleccionados y complejos.
Las indicaciones del ATR son excepcionales. Básicamente éstas serían 3: La reconstrucción extracorpórea de patología compleja del pedículo renal, la lesión ureteral extensa y la cirugía conservadora del cáncer renal en pacientes con riñón único o insuficiencia renal con tumores no extirpables sin reconstrucción extracorpórea en banco (1).
Desde que Hardy en 1963 (2) describió por primera vez la técnica del ATR para el tratamiento de la lesión ureteral extensa, las indicaciones han ido variando a lo largo de los últimos años reservándose en la actualidad para casos complejos.
Novick y cols. (3) en 1980 aportó su experiencia en el ATR tanto para el tratamiento de la enfermedad renovascular como de lesiones ureterales, demostrando la seguridad y la eficacia de este procedimiento. Posteriormente se ha contemplado como opción de tratamiento para el manejo principalmente de la enfermedad renovascular con o sin cirugía extracorpórea (4) pero también se ha considerado para el tratamiento de lesiones del tracto urinario superior (5), para el tratamiento de tumores renales o litiasis no extirpables sin reconstrucción extracorpórea en banco (6,7) y para el tratamiento del síndrome de hematuria-dolor lumbar (8,9). Recientemente Wotkowicz y Libertino (1) publicaron una revisión histórica de las indicaciones y su propia experiencia a cerca del ATR.
El objetivo de este estudio retrospectivo es analizar las indicaciones, las variantes técnicas, los resultados y las complicaciones de una serie de diez ATR realizados que presentaban patología renovascular o lesión ureteral extensa.
Material y métodos
Desde 1990 hasta 2005 se han realizado 10 ATR, 7 de ellos fueron adultos y 3 niños. La indicación fue por patología del pedículo vascular en 8 (80%) casos y por lesión ureteral en 2 (20%). (Tabla I).
De los 7 adultos que precisaron ATR, 5 fueron por patología vascular no subsidiaria de tratamiento percutáneo, y 2 por lesión ureteral. La patología vascular correspondió a: estenosis de arteria renal por ateromatosis en 4 casos, y aneurisma de arteria renal en 1 caso.
Dos pacientes adultos que requirieron ATR presentaban una lesión ureteral extensa y se prefirió la realización de esta técnica como alternativa a la interposición de ileon. Estos pacientes correspondieron a una estenosis ureteral secundaria a Enfermedad de Crohn inicialmente resuelta mediante stent ureteral, que posteriormente se obstruyó por incrustación litiásica; y el otro caso a una avulsión ureteral yatrógena post-ureteroscopia en el intento de extracción de una litiasis ureteral lumbar. (Figura 1).
En los 3 niños la indicación fue por estenosis de arteria renal secundaria a displasia en 2 casos y en otro caso por estenosis de arteria renal por enfermedad de Takayasu.
En los 8 casos en que fue necesaria la reconstrucción vascular, los injertos vasculares utilizados fueron: en 7 pacientes arteria hipogástrica y en 1 vena sáfena. En 5 pacientes fue necesario llevar a cabo una reimplantación ureteral tras la cirugía de banco, mientras que en otros 5 la reconstrucción vascular fue llevada a cabo sin ser necesaria la desinsercción ureteral. (Tabla II).
Los injertos fueron perfundidos con Ringer Lactato o Wisconsin a 4ºC y protegidos con isquemia fría de superficie mediante hielo pilé. (Figura 2).
Los tiempos de isquemia oscilaron entre 42 y 89 minutos, siendo el tiempo medio de 56 +- 3,2 minutos.
Se evaluaron las complicaciones postoperatorias menores y mayores, así como la función renal posterior y la necesidad de medicación hipotensora que precisan estos pacientes para regular su tensión arterial, utilizando como límite superior de la normalidad una presión arterial de 130/85 mmHg según el criterio propuesto por la Organización Mundial de la Salud (32).
En los 10 casos de nuestra serie se utilizó como vía de abordaje la lumbotomía con prolongación pararrectal hacía la espina iliaca anterosuperior para acceder al espacio retroperitoneal tanto de fosa renal como fosa iliaca homolateral sin acceder a la cavidad peritoneal.
Tras la disección del pedículo vascular y del uréter y previo a su sección, se realizó la disección de los vasos iliacos para disminuir el tiempo de isquemia al que se somete al riñón (en 5 casos no fue necesario interrumpir la vía urinaria).
El trasplante renal fue realizado en todos los casos en la fosa iliaca homolateral (ATR heterotópico) mediante la misma técnica reglada utilizada en los alotrasplantes. Se realizó anastomosis terminolateral de vena y arteria renal con los vasos iliacos y posterior ureteteroneocistostomía posterior si había sido necesario seccionar la vía urinaria.
Resultados
Nueve (90%) riñones fueron funcionantes tras el ATR teniendo 8 de ellos función inmediata tras la intervención y uno de ellos función retardada tras un período de necrosis tubular de 6 días de duración. El riñón nunca funcionante correspondió al de la estenosis arterial secundaria a enfermedad de Takayasu. La causa de la pérdida del injerto fue la trombosis de la vena renal.
La mortalidad postoperatoria de la serie fue nula (0%).
Con un tiempo medio de seguimiento de 72+-13 meses la creatinina media es de 1,6+-0,4 mg/dl (1,1-2,4) y el 70% (7/10) de los pacientes están normotensos sin necesidad de medicación hipotensora. (Tabla III).
Discusión
Desde que Hardy en 1963 (2), realizó el primer ATR renal con éxito para el tratamiento de una lesión ureteral extensa, como alternativa a la sustitución ureteral con ileon, este tratamiento ha sido considerado como una posibilidad en el manejo de estas lesiones del tracto urinario superior, pero su indicación principal ha sido la enfermedad renovascular con o sin cirugía extracorpórea (1).
En el momento actual es un procedimiento seguro y efectivo que se reserva para casos complejos. La técnica quirúrgica no difiere del trasplante renal, por tanto la mayor experiencia de los equipos de trasplante en nuestros días hace que esta técnica tenga una mortalidad prácticamente nula, con baja morbilidad y excelentes resultados.
Las dos indicaciones fundamentales del ATR son la alteración del pedículo vascular y la lesión ureteral extensa. Estas indicaciones han ido variando con el avance de las técnicas percutáneas, la radiología intervencionista y la endoscopia, que hace que en el momento actual el ATR sea un procedimiento infrecuente.
La enfermedad renovascular sigue siendo la indicación principal del ATR. En la mayoría de las series supone entre el 60-80% de los casos realizados. En la tabla IV se resumen las series con mayor número de casos publicadas en la literatura (1,3-5,10,11) observando que en los últimos años se ha convertido en una indicación excepional. Las nuevas vías de abordaje de estas enfermedades hacen que se reserve este tratamiento para aquellos pacientes con enfermedad vascular del pedículo renal (Displasia fibromuscular, Aneurisma de arteria renal, Enfermedad de Takayasu, Arteriosclerosis, ) refractarias a tratamiento percutáneo. Se aconseja realizar esta técnica en aquellos casos en los que la reparación requiera un tiempo de isquemia superior a los 45 minutos y estén afectas las arterias renales distales (12).
La serie más extensa de ATR corresponde la Novick y cols. (3), incluyendo un total de 108 ATR renales (67 por lesiones vasculares, 27 lesiones ureterales y el resto por distintas indicaciones). Los resultados fueron satisfactorios en el 96% de las lesiones arteriales, en el 92% de las lesiones ureterales y en el 85% de los carcinomas renales que precisaron cirugía de banco para su exéresis con ATR ulterior.
Chiche y cols. (4) publicaron los resultados de 68 ATR realizados en 57 pacientes con enfermedad vascular, siendo los resultados óptimos en todas las indicaciones excepto en estenosis de arteria renal debido a arterioesclerosis en los que la supervivencia del injerto a los cinco años era del 54%, respecto al 94-96% del resto de indicaciones (displasia fibromuscular, Takayasu, ). La morbimortalidad era similiar en todos los grupos y esta diferencia en la efectividad del ATR, probablemente fuese debida a la generalización de la propia enfermedad arteriosclerótica.
Wotkowicz y cols. (1) realizaron 21 ATR con éxito de 24 realizados, recalcando que para casos seleccionados la cirugía extracorpórea renal es una mejor alternativa para el paciente que el tratamiento con diálisis crónica o la realización de un alotrasplante con sus potenciales complicaciones.
En relación con la patología ureteral en la literatura se han descrito muchas alternativas para la reconstrucción de su continuidad (13).
1) anastomosis ureteral término-terminal,
2) transuretero-ureterostomía,
3) ureteroplastia con íleon o colon,
4) autotrasplante renal (ATR),
5) lateralización vesical (vejiga psoica o ureteroplastia distal tipo Boari).
6) descenso renal y
7) la asociación de cualquiera de los procedimientos anteriormente descritos.
La indicación principal del ATR en las lesiones ureterales será en aquellas que afecten al tracto urinario superior que sean suficientemente extensas como para precisar interposición de intestino para la reparación.
La decisión en este tipo de lesiones debe basarse en la viabilidad de intestino, la longitud y localización de lesión ureteral, la preferencia del paciente y la experiencia del cirujano.
La interposición con ileon debe evitarse en pacientes con cirugía abdominal previa o en aquellos que presentan antecedentes de enfermedades inflamatorias del intestino. Es un procedimiento con una eficacia similar al ATR (81-88,5%) siendo este resultado mejor cuando se realiza de forma diferida a la lesión. El principal problema a largo plazo es el potencial deterioro funcional renal debido a la secreción mucosa, la reabsorción electrolitos y la bacteriuria crónica (14,15).
Los dos casos incluidos en nuestra serie de lesión ureteral, el ATR se realizó como alternativa a las otras alternativas técnicas para: evitar el abordaje intraperitoneal, reconstruir la continuidad del urotelio sin interponer intestino, no comprometer el sistema excretor contralateral e intentar preservar el órgano y la función del mismo.
Bodie y cols. (5) comunicaron los resultados de 23 pacientes sometidos a ATR. La totalidad de los casos publicados en esta serie presentaban lesiones ureterales extensas con un seguimiento de 14 años. Todos los pacientes habían sufrido una o más intervenciones previas. Ningún paciente falleció en el postoperatorio y todos los implantes menos uno funcionaron inmediatamente. Dos de los riñones tuvieron que ser retirados por sangrado postoperatorio. De los 20 restantes, todos se mantuvieron con función renal estable.
El resto de las series con mayor número de casos publicadas están integrados por casos aislados a lo largo de años de experiencia en los distintos centros. La nuestra es una serie de casos aislados acumulados desde hace 15 años, como lo son la serie de casos de Plas y cols. (11) desde 1977 a 1994 y la de Webster (10) desde 1997 a 2005.
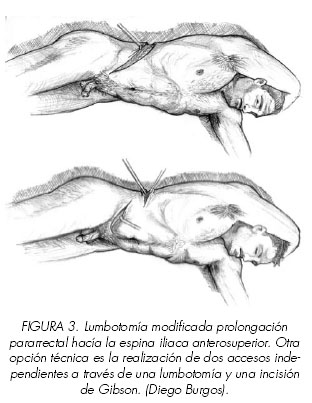
La vía de abordaje más frecuentemente utilizada es la lumbotomía con prolongación pararrectal hacía la espina iliaca anterosuperior por sus ventajas al acceder al espacio retroperitoneal tanto de fosa renal como fosa iliaca homolateral sin acceder a la cavidad peritoneal. Esta vía presenta menor morbilidad postoperatoria y menor estancia hospitalaria que la vía transperitoneal (16). Otra opción técnica es la realización de dos accesos independientes a través de una lumbotomía y una incisión de Gibson, la primera para realizar la nefrectomía y la segunda para el trasplante. (Figura 3).
En los últimos años en la literatura se han publicados casos de ATR realizando la extracción renal por vía laparoscópica transperitoneal (17-19), bien sea pura o mano asistida (20), realizando posteriormente el trasplante con la técnica habitual mediante una incisión de Gibson. Los casos publicados se resumen en la Tabla V. Se puede observar que las indicaciones son similares, que el tiempo quirúrgico no se incrementa en exceso y que no varía la morbimortalidad, aunque el número de casos hasta el momento actual es escaso
En los diez casos de nuestra serie se utilizó como vía de abordaje la lumbotomía con prolongación pararrectal hacía la espina iliaca anterosuperior intentando evitar, en todo momento la apertura de la cavidad peritoneal.
La extracción renal no difirió de la realizada para un donante vivo. Debe ser meticulosa sin manipulaciones traumáticas del riñón y su pedículo. La sobredisección puede provocar en estos casos la decapsulación renal y la devascularización del uréter.
Obtener una amplía pastilla de vena cava en el lado derecho y la mayor longitud posible de arteria renal izquierda facilitará la posterior implantación del órgano en la fosa iliaca.
Previo a la sección del pedículo vascular y de uréter, si fuese imprescindible interrumpir la vía urinaria, se debe realizar la disección de los vasos iliacos para disminuir el tiempo de isquemia al que se somete al riñón.
El tiempo de isquemia debe ser corto, siendo aconsejable que sea inferior a 60 minutos (42-89 minutos en nuestra serie), aunque en algunas circunstancias se puede requerir prolongar este tiempo por la necesidad de reconstrucción vascular del injerto durante la cirugía de banco. Esto además de permitir la reconstrucción vascular, posibilita la extirpación de neoplasias del parénquima y la reparación de lesiones ureterales. El injerto vascular más utilizado en nuestra serie fue la arteria hipogástrica que debido a su accesibilidad mediante esta vía y su tamaño es una buena elección para la reparación de la patología vascular renal.
La cirugía de banco permite la resolución ex vivo de patología del sistema pielocalicial. Así, en el caso de la estenosis ureteral secundaria a Enfermedad de Crohn inicialmente resuelta mediante stent ureteral, que posteriormente se obstruyó por incrustación litiásica, se observaba en la ecografía una litiasis única renal que se extrajo durante la cirugía de banco mediante ureteroscopio.
Debe evitarse en lo posible la interrupción de la vía urinaria, evitando el riesgo quirúrgico y las complicaciones derivadas de la ureteroneocistostomía posterior (fístulas, reflujo vesicoureteral, estenosis de la unión ureterovesical, ).
Para considerar el ATR efectivo no debe existir un deterioro de la función renal ni alteración de la tensión arterial en el seguimiento posterior de los pacientes. En nuestra serie con un tiempo medio de seguimiento de 72+-13 meses la función renal post-ATR fue buena con niveles medios de creatinina de 1,6 +- 0,4 mg/dl. Por otro lado el 70 % de ellos se encuentran normotensos sin necesidad de medicación hipotensora, siendo estos datos similares en los últimas series publicadas (1,3-5,10,11). (Figura 4)
Las complicaciones más importantes del ATR son básicamente de dos tipos: las que afectan a la función renal, cuya expresión máxima es la necrosis tubular aguda (NTA); y las de la técnica quirúrgica, de la cual la más importante es la trombosis vascular.
La principal repercusión sobre la función en los riñones autotrasplantados es la isquemia. Una isquemia caliente prolongada o hipotermia incorrecta son causas potenciales de NTA. Esto condiciona una lesión histológica en forma de edema y tumefacción de las células tubulares y como consecuencia la expansión del espacio intersticial que provoca una alteración biológica en forma de acidosis tisular con disminución de la actividad ATPasa y cese del funcionamiento de la bomba Na-K. Ambas alteraciones, tanto la histológica como la biológica, son reversibles sin alteración de la función de la unidad renal a largo plazo. En un solo caso de nuestra serie (10%) se presentó retrasándose la función el autoinjerto hasta el sexto día postoperatorio.
Para evitar estos factores que pueden llevar al daño renal, incluso a la perdida de la unidad renal, los riñones son perfundidos con una solución fría de preservación.
Existen varias soluciones de preservación, aunque todas ellas comparten características comunes: a) se emplean frías para disminuir la temperatura en el riñón y así disminuir las necesidades energéticas de las células, b) son hiperosmolares para minimizar el edema celular y c) son excelentes tampones de la acidosis que se produce durante la isquemia renal (21).
En el ATR dado que el tiempo de isquemia caliente es prácticamente inexistente se puede usar indistintamente las diferentes soluciones de preservación que existen, no siendo imprescindible utilizar soluciones de mayor precio como la de Wisconsin (22).
El riesgo más importante al que se someten estos pacientes es la perdida de la unidad renal siendo la causa más frecuente la trombosis vascular, tanto arterial como venosa. Suelen estar relacionados con la técnica quirúrgica realizada y en la mayoría de los procedimientos realizados, en manos experimentadas, condiciona las perdidas renales en aproximadamente el 8% de los casos (5) independientemente de la indicación que llevó a realizar el ATR.
La única pérdida de la unidad renal de nuestra serie (10%) correspondió al de la estenosis arterial secundaria a enfermedad de Takayasu. La causa de la pérdida del injerto fue la trombosis de la vena renal. Es imprescindible para el diagnóstico precoz de esta complicación la realización de ecografía doppler en el primer día postoperatorio, y la consecuencia suele ser invariablemente la transplantectomía (23).
La trombosis arterial, más frecuente que la venosa, está siempre relacionada con lesiones de la íntima del vaso, sea por traumatismo directo, elongación vascular con disrupción de la continuidad endotelial o defectos técnicos de la anastomosis, incrementándose este riesgo si se precisa de microcirugía vascular del pedículo renal.
Con el ATR se obtienen buenos resultados y es el tratamiento de elección para un determinado grupo de pacientes con lesiones de árbol vascular renal y lesiones del tracto urinario superior, pero debe ser considerado como una opción terapéutica excepcional. Entre estas indicaciones encontramos la cirugía conservadora del cáncer renal en pacientes con riñón único o insuficiencia renal con tumores no extirpables sin reconstrucción extracorpórea en banco, síndrome hematuria-dolor lumbar, traumatismos renales y litiasis ureterales complejas. Estas se resumen en la Tabla VI (1,3).
El resto de los casos publicados son casos aislados de indicaciones habituales como aneurisma de arteria renal aportados por Ysa y cols. (24) y Knobloch y cols. (25) en adultos, siendo éste último caso en un paciente monorreno, o los seis casos de estenosis de arteria renal bilateral en niños relatados por Ellis y cols. (26) en el años 2005. Murphy y cols. (27) publicaron la reparación mediante cirugía renal extracórporea de un caso de anomalía vascular en un paciente con riñón en herradura.
En relación con patología ureteral Lutter y cols. (28) aportaron un caso de reparación de lesión ureteral tras avulsión yatrógena postureteroscopia. Rios y cols. (13) y Trinchieri y cols. (29) aportan casos aislados de lesión ureteral tras discectomía lumbar.
Otras indicaciones excepcionales en las cuales es imprescindible considerar como opción de tratamiento el ATR son la cirugía conservadora del cáncer renal de gran tamaño o multifocal en pacientes monorrenos (6,7), síndrome hematuria-dolor lumbar (8,9), o traumatismos renales por arma de fuego (30).
En relación al trasplante renal, existen escasas referencias de autotrasplante renal de un injerto previo. Novick y cols. (3) en su serie aporta un caso de reparación mediante cirugía de banco de un aneurisma de arteria de injerto renal. Cassingal publico en el año 2005 un caso de ATR de injerto renal por oclusión arterial completa. Aunque no incluidos en esta serie por no ser propiamente ATR, si no reparación vascular de injertos renales con lesiones que requieren cirugía de banco, se han realizado en nuestro hospital 3 ATR de injertos renales en los que las causas fueron: estenosis extensa de la arteria del injerto no subsidiaria de angioplastia o revascularización in situ en 2 casos y por aneurisma de la anastomosis en 1 caso con resultados dispares.
Conclusiones
El ATR es una técnica compleja, aunque segura y efectiva que todavía en la actualidad se debe tener en cuenta para la resolución de casos complejos. Las indicaciones son excepcionales pero se debe plantear en casos seleccionados porque permite la reconstrucción vascular extracorpórea y rescata unidades renales no subsidiarias de tratamiento percutáneo.
Constituye una alternativa válida a la interposición de ileon en lesiones ureterales extensas y podría ser potencialmente útil en el tratamiento de otras patologías complejas como en tumores renales en monorrenos, o síndrome de hematuria- dolor lumbar.
Agradecimiento a Diego Burgos por su colaboración en la iconografía.
Bibliografía y lecturas recomendadas (*lectura de interés y ** lectura fundamental)
**1. WOTKOWICZ, C.; LIBERTINO, J.A.: Renal autotransplantation. BJU Int., 93: 253, 2004. [ Links ]
2. HARDY, J.D.: High ureteral injuries. Management by autotrasplantation of the kidney. JAMA, 84: 97, 1963. [ Links ]
*3. NOVICK, A.C.; STEWART, B.H.; STRAFFON, R.A.: Extracorporeal renal surgery and autotransplantation: indications, techniques and results. J. Urol., 123: 806, 1980. [ Links ]
4. CHICHE, L.; KIEFFER, E.; SABATIER, J. y cols.: Renal autotransplantation for vascular disease: late outcome according to etiology. J. Vasc. Surg., 37: 353, 2003. [ Links ]
5. BODIE, B.; NOVICK, A.C.; ROSE, M. y cols.: Long-term results with renal autotransplantation for ureteral replacement. J. Urol., 136: 1187, 1986. [ Links ]
6. KARDAR, A.H.; LINDSTEDT, E.M.; PERACHA, A. y cols.: Renal autotransplantation and pyelocystostomy for the treatment of urothelial tumors of the upper urinary tract. J. Urol., 159: 195, 1998. [ Links ]
7. BOUTEMY, F.; DEMAILLY, M.; PETIT, J.: Multifocal urothelial tumors and renal autotransplantation. Prog. Urol., 12: 1294, 2002. [ Links ]
8. CHIN, J.L.; KLOTH, D.; PAUTLER, S.E. y cols.: Renal autotransplantation for the loin pain-hematuria syndrome: long-term followup of 26 cases. J. Urol., 160: 1232, 1998. [ Links ]
9. KARVELAS, J.P.; RAMSEY, E.W.: Renal autotransplantation in patients with loin pain-hematuria syndrome. Can. J. Surg., 39: 121, 1996. [ Links ]
*10. WEBSTER, J.C.; LEMOINE, J.; SEIGNE, J. y cols.: Renal autotransplantation for managing a short upper ureter or after ex vivo complex renovascular reconstruction. BJU Int., 96: 871, 2005. [ Links ]
11. PLAS, E.; KRETSCHMER, G.; STACKL, W. y cols.: Experience in renal autotransplantation: analysis of a clinical series. Br. J. Urol., 77: 518, 1996. [ Links ]
12. BRAYMAN, K.: Ex vivo reconstruction of the renal artery for aneurysm and other abnormalities of renal vascular anatomy. Cann C ed. Modern Management of Renovascular Hypertension and Renal Salvage, 1st edn, Vol. I. Chapt 14. Baltimore: William and Wilkins, 269, 1996. [ Links ]
13. RIOS GONZÁLEZ, E.; RAMON DE FATA CHILLON, F.; TABERNERO GOMEZ, A. y cols.: Iatrogenic injury of the lumbar ureter and iliac vessels after lumbar discectomy: urologic treatment using kidney autotransplantation. Actas Urol. Esp., 26: 504, 2002. [ Links ]
14. BOXER, R.J.; FRITZSCHE, P.; SKINNER, D.G. y cols.: Replacement of the ureter by small intestine: clinical application and results of the ileal ureter in 89 patients. J. Urol., 121: 728, 1979. [ Links ]
15. MATTOS, R.M.; SMIMTH, J.J.: 3rd. Ileal ureter. Urol. Clin. North Am., 24: 813, 1997. [ Links ]
16. SERRALLACH MILA, N.; FRANCO MIRANDA, E.; RIERA CANALS, L.I. y cols.: Vasculo-renal disease. Actas Urol. Esp., 26: 600, 2002. [ Links ]
17. GILL INDERBIR, S.; UZZO, R.G.; HOBART, M.G. y cols.: Laparoscopic retroperitoneal live donor right nephrectomy for purposes of allotransplantation and autotransplantation. J. Urol., 164: 1500, 2000. [ Links ]
18. BLUEBOND-LANGNER, R.; RHA, K.H.; PINTO, P.A. y cols.: Laparoscopic-assisted renal autotransplantation. Urology, 63: 853, 2004. [ Links ]
19. MAXWELL, V.; MENG, C.E.; FREISE, y cols.: Expanded experience with laparoscopic nephrectomy and autotrasplantation for severe ureteral injury. J. Urol., 169: 1363, 2003. [ Links ]
20. TROXEL, S.A.; ROSS, G. Jr.; TEAGUE, J.L.: Hand-assisted laparoscopic approach to renal harvest for autotransplantation. J. Endourol., 19: 785, 2005. [ Links ]
21. COLLINS, G.M.; HALSZ, N.A.: Composition of intracellular flush solutions for hypotermic kidney storage. Lancet, 1: 220, 1975. [ Links ]
22. PLOEG, R.J.; VAN BOCKEL, J.H.; IANGENDIJK, P.T.: Effect of preservation solution on results of cadaveric kidney transplant. The European Multicenter Study Group. Lancet, 340: 129, 1992. [ Links ]
23. GIUSTACCHINI, P.; PISANTI, F.; CITTERIO, F. y cols.: Renal vein thrombosis after renal transplantation. An important cause of graft loss. Transplantation Proc., 34: 2126, 2002. [ Links ]
24. YSA-FIGUERAS, A.Y.; CLARÁ, A.; DE LA FUENTE´SÁNCHEZ, N. y cols.: Ex vivo surgery and autotrasplant in the treatment of renal artery aneurysms. Angiología, 55: 295, 2003. [ Links ]
25. KNOBLOCH, K.; WIEBE, K.; LICHTENBERG, A. y cols.: Ex vivo repair and renal autotransplantation for complex renal artery aneurysms in a solitary kidney. Ann Vasc. Surg., 19: 407, 2005. [ Links ]
26. ELLIS, D.; SHAPIRO, R.; SCANTLEBURY, V.P. y cols.: Evaluation and management of bilateral renal artery stenosis in children: a case series and review. Pediatr. Nephrol., 9: 259, 1995. [ Links ]
27. MURPHY, J.T.; BORMAN, K.R.; DAWIDSON, I.: Renal autotransplantation after horseshoe kidney injury: a case report and literature review. J. Trauma., 40: 840, 1996. [ Links ]
28. LUTTER, I.; MOLCAN, T.; PECHAN, J. y cols.: Renal autotransplantation in irreversible ureteral injury. Bratisl. Lek. Listy., 103: 437, 2002. [ Links ]
29. TRINCHIERI, A.; MONTANARI, E.; SALVINI, P. y cols.: Renal autotransplantation for complete ureteral avulsion following lumbar disk surgery. J. Urol., 165: 1210, 2001. [ Links ]
30. ANGELIS, M.; AUGENSTEIN, J.S.; CIANCIO, G. y cols.: Ex vivo repair and renal autotransplantation after penetrating trauma: is there an upper limit of ischemic/traumatic injury beyond which a kidney is unsalvageable?. J. Trauma., 54: 606, 2003 [ Links ]
31. CASINGAL, V.P.; ASOLATI, M.; HUNTER, D. y cols.: Emergent autotransplantation of a renal allograft. Clin. Transplant., 19: 563, 2005. [ Links ]
32. 1999 WORLD HEALTH ORGANIZATION-INTERNATIONAL SOCIETY OF HYPERTENSION GUIDELINES FOR THE MANAGEMENT OF HYPERTENSION. Guidelines Subcommittee. J. Hypertens. 17: 151, 1999. Comment in: J. Hypertens. 19:679, 2001. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Luis López-Fando Lavalle
Servicio de Urología
Hospital Ramón y Cajal
Ctra. de Colmenar Viejo km. 9.100
28034 Madrid. (España)
llfando@hotmail.com
Trabajo recibido: 10 de octubre de 2006