Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos Españoles de Urología (Ed. impresa)
versión impresa ISSN 0004-0614
Arch. Esp. Urol. vol.62 no.7 sep. 2009
Resultados del uso en cáncer de próstata del bloqueo androgenico completo en área de salud con Hospital de Referencia Tipo 2 (2a Parte). Calidad de Vida: Aplicación del instrumento EORTIC QLQ-PR25 y resultados globales. Supervivencia ajustada a la calidad de vida. Gasto farmaceútico y coste-utilidad
Outcomes of maximal androgen blockade in prostate cancer patients at a health area with type 2 reference hospital (2nd part). quality of life: application of EORTC QLQ-PR25 instrument and global results. Quality-of-life adjusted survival. Pharmaceutical expenses and cost-utility
Nicolás Alberto Cruz Guerra.
Complejo Asistencial de Zamora. Zamora. España.
Dirección para correspondencia
RESUMEN
Objetivo: Estudiar la calidad de vida en los pacientes diagnosticados entre los años 2000-2005 de adenocarcinoma de próstata en el área de salud de Zamora tratados con bloqueo androgénico completo (BAC). Repercusión farmacoeconómica.
Métodos: Aplicación basal, al mes 12, mes 24 y mes 36, del instrumento de medición de calidad de vida relacionada con la salud EORTC QLQ-PR25 a la muestra poblacional (n= 111) citada, así como a una muestra de sujetos control (n= 100). Estudio comparativo entre ambos grupos; entre las diferentes determinaciones temporales para los pacientes con BAC; e inter-categorías/ -intervalos de determinadas variables en pacientes con terapia de deprivación hormonal (tercer año de seguimiento). Análisis de los resultados globales de calidad de vida relacionada con la salud (QLQ-C30 + QLQ-PR25). Descripción del gasto farmacéutico en bloqueo androgénico. Análisis coste-utilidad a través del cálculo de los años de vida ajustados a la calidad (AVACs) obtenidos mediante el uso de los índices de ponderación preferencial correspondientes al instrumento EuroQol 5-D.
Resultados: Aparición de sofocos y deterioro de la esfera sexual como manifestaciones más significativas relacionadas con la hormonosupresión. Peor percepción subjetiva del estado general de salud y calidad de vida en pacientes tratados, frente a los sujetos no neoplásicos. La positividad gammagráfica, como factor de influencia negativa sobre la calidad de vida. La mayor parte de los pacientes sometidos a BAC presentan cifras de coste-utilidad menor de 5000 Euros/ AVAC.
Conclusiones: Repercusión negativa inicial del BAC sobre determinados aspectos calidad de vida, aunque matizable en función de cada esfera estudiada. Relativización del impacto económico de dicho tratamiento sobre el gasto farmacéutico total.
Palabras clave: Cáncer de próstata. Terapia hormonal. Calidad de vida. Economía de la salud.
SUMMARY
Objectives: To study quality of life in patients from the health area of Zamora diagnosed of prostate adenocarcinoma between 2000-2005 treated with maximal androgen blockade (MAB). To evaluate the pharmacoeconomics of the treatment.
Methods: Basal, 12-month, 24 -month and 36-month application of the health-related quality of life measurement instrument EORTC QLQ-C30 to the population sample (n= 111), as well as a control sample (n= 100). Comparative study of outcomes: between groups; between different time measurements in MAB patients; and inter-categories/-intervals of some variables in patients with hormonal deprivation therapy (third year of follow-up). Analysis of health-related quality of life global outcomes (QLQ-C30 + QLQ-PR25). Description of the pharmaceutical expenses in androgen blockade patients. Cost-utility analysis by means of quality-adjusted life years (QALYs) obtained using preference-based weighted index from the EUROQOL 5-D tool.
Results: Hot flushes and sexual field worsening as mean expressions related to hormonal suppression. Treated patients had worse subjective perception of health condition and quality of life, in opposition to non-tumoral individuals. Positive bone scan, was a negative-influence factor on quality of life. Most patients undergoing MAB needed cost-utility figures of less than 5000 Euros/ QALY.
Conclusions: There was a negative initial repercussion of MAB on quality of life, although tinged according to the different fields studied. The economic impact of this therapy on overall pharmaceutical expenses is relative.
Key words: Prostate cancer. Hormonal therapy. Quality of life. Health economics.
Resultados
CALIDAD DE VIDA RELACIONADA CON LA SALUD - CDVRS - (II).
A. Parámetros descriptivos correspondientes a los resultados de la aplicación del instrumento EORTC QLQ-PR25.
El resultado del ámbito miccional lo constituye la suma de los ítem 1 al 9 del QLQ-PR25. El ámbito de la sintomatología intestinal se obtiene de la suma de los ítem 10 al 13, y 17 al 18 del QLQ-PR25 del mismo instrumento. El valor de la puntuación del ítem 14 del QLQ-PR25 se corresponde con la presencia de sofocos.
Los valores obtenidos pertenecientes a la esfera sexual se han calculado mediante la suma de los ítem 19, 23, 24 y 25 del QLQ-PR25, a cuyo resultado se le ha restado la suma de los ítem 20 al 22, de escala interpretativa inversa. Los ítem 22 al 25 sólo son válidos en aquellos pacientes con actividad sexual en las últimas cuatro semanas, por tanto, no han sido incluidos los sujetos que no cumplen dicha premisa. En la determinación basal, un 37,84 % de los pacientes diagnosticados de neoplasia habían mantenido relaciones sexuales en las últimas cuatro semanas, frente al 36 % de sujetos sin cáncer. En las determinaciones correspondientes a los meses 12, 24 y 36 se obtuvieron unas cifras de 17,12; 16,22 y 16,22 %, respectivamente, para los pacientes con bloqueo androgénico completo; mientras que los valores para los sujetos sin neoplasia, por su parte, se mantuvieron constantes en las tres determinaciones - 37 % -.
La relación completa de los valores de la media, desviación típica y mediana para cada uno de los ámbitos de CDVRS mencionados, así como para la suma total del instrumento QLQ-C30 se reflejan en las Tablas I-IV.
B. Valores correspondientes a Calidad de Vida global.
El valor medio basal obtenido para la suma total de los instrumentos QLQ-C30 y QLQ-PR25, considerando los matices ya expuestos, fue de 52,2 puntos (desviación típica - DT - = 8) para los pacientes diagnosticados de adenocarcinoma de próstata, y de 53,9 puntos para los sujetos sin neoplasia (DT= 11,29). A los 12 meses de seguimiento se objetiva un valor medio de 57,4 puntos (DT= 10,18) para los pacientes tratados con bloqueo androgénico completo, frente a 54,2 puntos (DT= 11,51) en los sujetos sin neoplasia. A los 24 meses los resultados son de 57,2 puntos (DT= 10,95) en sujetos con cáncer, mientras que es de 55,2 puntos (DT= 12,31) para los que no lo padecen. Los valores a los 36 meses de seguimiento son de 55,2 (DT= 9,4) y 56,9 puntos (DT= 14,64), respectivamente.
La relación completa de los valores de la media, desviación típica y mediana para cada uno de los ámbitos de CDVRS mencionados, así como para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente se reflejan en las Tablas I-IV.
La relación completa de los valores de la media y desviación típica para los ítem 29 - autopercepción del estado general de salud - y 30 - autopercepción del grado de calidad de vida - del instrumento QLQ-C30 se reflejan en las Tablas V-VI.
C. Resultados de Calidad de Vida en función de las categorías/intervalos de determinadas variables (mes 36 de seguimiento).
La relación de los valores de la media, desviación típica y mediana - correspondientes a la determinación del mes 36 en pacientes sometidos a bloqueo androgénico completo - para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente en función de las diferentes categorías/ intervalos de las variables "nivel de estudios" y "ámbito del domicilio" se reflejan en la Tabla VII.
La relación de los valores de la media, desviación típica y mediana - correspondientes a la determinación del mes 36 en pacientes sometidos a bloqueo androgénico completo - para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente en función de las diferentes categorías/ intervalos de las variables "edad basal", "características prostáticas al tacto rectal", "cifra basal de PSA", "morfología prostática en la ecografía transrectal", "positividad uni- o bilateral de la biopsia transrectal prostática", "puntuación Gleason", "positividad de la gammagrafía ósea", y "tipo de bloqueo en función de antiandrógeno utilizado" se reflejan en las Tablas VIII-IX.
D. Parámetros descriptivos correspondientes a los resultados de la aplicación del sistema de ponderación preferencial del instrumento EuroQol 5-D.
El valor medio obtenido correspondiente a la supervivencia total ajustada a la calidad de vida calculado mediante la aplicación de ponderación preferencial con el instrumento EuroQol 5-D fue de 2,1 Años de Vida Ajustados a la Calidad (DT= 0,63) para los pacientes tratados con bloqueo androgénico completo, frente a 2,27 (DT = 0,34) para los sujetos sin cáncer de próstata (Tabla IV).
La relación de los valores de la media, desviación típica y mediana - correspondientes a la determinación del mes 36 en pacientes sometidos a bloqueo androgénico completo para la supervivencia total ajustada a la calidad de vida en función de las diferentes categorías/ intervalos de las variables "edad basal", "características prostáticas al tacto rectal", "cifra basal de PSA", "morfología prostática en la ecografía transrectal", "positividad uni- o bilateral de la biopsia transrectal prostática", "puntuación Gleason", "positividad de la gammagrafía ósea", y "tipo de bloqueo en función de antiandrógeno utilizado" se reflejan en las Tablas X-XI.
En la Figura 1 se recoge la distribución correspondiente a los resultados de supervivencia total ajustada a la calidad de vida, diferenciando a los pacientes con bloqueo androgénico completo con respecto a los sujetos sin neoplasia.
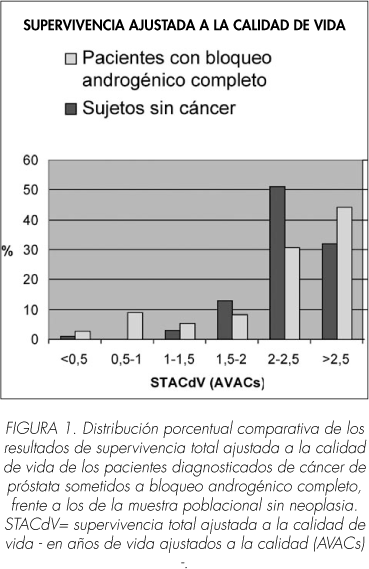
E. Estudio comparativo de los resultados de la aplicación del instrumento QLQ-PR25 y de las puntuaciones globales de calidad de vida.
1. Pacientes con bloqueo androgénico completo vs sujetos sin neoplasia.
Con respecto al ámbito miccional se encontraron diferencias significativas en la medición basal, así como en las correspondientes al mes 24 y 36. Los resultados fueron mejores en el grupo de sujetos sin cáncer de próstata.
La comparación de resultados en el ámbito de la sintomatología intestinal permitió objetivar diferencias significativas en las mediciones de los meses 12 y 24, perteneciendo los peores resultados al grupo de pacientes tratados con bloqueo androgénico.
El estudio comparativo de los resultados de las puntuaciones del ítem 14 del instrumento QLQ-PR25 - aparición de sofocos - permitió evidenciar diferencias significativas en todas las mediciones excepto en la basal, apreciándose los peores resultados para el grupo de pacientes sometidos a bloqueo androgénico completo frente a los sujetos no neoplásicos.
La comparación de los valores obtenidos en la esfera sexual deparó diferencias estadísticamente significativas en las mediciones de los meses 12, 24 y 36. Los peores resultados correspondieron al grupo de pacientes con cáncer de próstata. También se apreciaron diferencias significativas al comparar - para las determinaciones de los meses 12, 24 y 36 -los porcentajes de pacientes neoplásicos que habían mantenido relaciones sexuales en las últimas cuatro semanas, frente a las cifras correspondientes a los sujetos sin cáncer.
La comparación de las puntuaciones totales del QLQ-PR25, - con las consideraciones ya mencionadas con anterioridad -, permite evidenciar diferencias estadísticamente significativas en la medición correspondiente a los meses 12 y 24, obteniendo peores resultados el grupo de pacientes en tratamiento con deprivación hormonal.
Por su parte, al comparar la suma de las puntuaciones totales del instrumento QLQ-C30 más las del QLQ-PR25, se objetivan diferencias significativas en las mediciones de los meses 12 y 24, con peores resultados en los pacientes con cáncer de próstata tratado con bloqueo hormonal.
La comparación de los resultados correspondientes tanto al ítem 29 - autopercepción del estado general de salud - como al ítem 30 - autopercepción del grado de calidad de vida - del instrumento QLQ-C30 en los pacientes con neoplasia prostática frente a los de aquellos sujetos libres de enfermedad permitió evidenciar diferencias estadísticamente significativas para todas las mediciones temporales - basal, 12, 24 y 36 meses -. Dichas diferencias resultaron siempre favorables a los sujetos sin cáncer.
La relación completa - en cada determinación temporal - de los valores p obtenidos en el estudio comparativo de los pacientes con bloqueo androgénico completo frente a los sujetos sin neoplasia para cada uno de los ámbitos de CDVRS mencionados, para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente, así como para los ítem 29 y 30 del QLQ-C30 se reflejan en las Tablas I-VI.
2. Comparación inter-categorías/ -intervalos de determinadas variables en pacientes con bloqueo androgénico completo (mes 36 de seguimiento).
Se objetivaron diferencias significativas con respecto a la suma de valores de los instrumentos QLQ-C30 más QLQ-PR25 entre el subgrupo con estudios básicos o primarios frente a los que poseían estudios medios o superiores, con resultados más satisfactorios para estos últimos. El análisis de las diferencias no aportó significación estadística para el valor independiente obtenido con el instrumento QLQ-PR25.
Se obtuvieron asimismo diferencias estadísticamente significativas al comparar entre los subgrupos de pacientes con o sin gammagrafía ósea positiva los resultados de la suma de valores de los instrumentos QLQ-C30 más QLQ-PR25, así como al hacerlo con los del instrumento QLQ-PR25 de forma aislada.
La relación completa de los valores p obtenidos en el estudio comparativo de las diferentes categorías/ intervalos correspondientes a las variables mencionadas anteriormente para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente - en la determinación del mes 36, en pacientes con bloqueo androgénico completo - se reflejan en las Tablas VII-IX.
3. Comparaciones intertemporales (pacientes con bloqueo androgénico completo).
Sólo se objetivaron diferencias significativas dentro del ámbito miccional entre las mediciones basal y la correspondiente al mes 12.
Con respecto al ámbito intestinal, las diferencias resultaron significativas al comparar los valores de la medición basal con respecto a la del mes 12, y al hacerlo entre la primera y la del mes 36.
En lo que respecta a los valores del ítem 14 del instrumento QLQ-PR25 - aparición de sofocos -, se apreciaron diferencias significativas entre las determinaciones basal y las correspondientes a los meses 12 y 36.
La comparación de los valores de la puntuación total del instrumento QLQ-PR25 permitió objetivar diferencias significativas entre las determinaciones basal y del mes 12, así como entre la primera y la correspondiente al mes 36.
El análisis de las diferencias temporales entre los valores de la suma total del intrumento QLQ-C30 más la del QLQ-PR25 permitió apreciar significación estadística entre la determinación basal y del mes 12, entre ésta última y la del mes 24, así como entre la del mes 36 y la basal.
La comparación de los resultados temporales correspondientes tanto al ítem 29 - autopercepción del estado general de salud - como al ítem 30 - autopercepción del grado de calidad de vida - del instrumento QLQ-C30 permitió evidenciar diferencias estadísticamente significativas entre las determinaciones basal y del mes 12, entre éste y la del mes 24, así como la basal y la del mes 36.
No se apreciaron diferencias estadísticamente significativas al comparar las mediciones temporales en lo referente al ámbito sexual, a pesar de que sí se verifican peores resultados en el valor correspondiente al mes 12 con respecto al basal, debiendo recordarse asimismo que sólo se comparan los pacientes que han mantenido relaciones en las últimas cuatro semanas antes de cada aplicación temporal de los instrumentos de medición de CDVRS.
La relación completa de los valores p obtenidos en el estudio comparativo intertemporal de las mediciones para cada uno de los ámbitos de CDVRS mencionados, para las sumas totales de los instrumentos QLQ-PR25 de forma individual y QLQ-C30 más QLQ-PR25 conjuntamente, así como para los ítem 29 y 30 del QLQ-C30 se reflejan en las Tablas XII-XV.
F. Estudio comparativo de los resultados de la aplicación del sistema de pon-deración preferencial del instrumento EuroQol 5-D.
No se objetivaron diferencias significativas entre la supervivencia ajustada a la calidad de vida correspondiente a los sujetos con y sin neoplasia al mes 36 de seguimiento (Tabla IV).
La relación completa de los valores p obtenidos en el estudio comparativo de las diferentes ca-tegorías/intervalos correspondientes a las variables estudiadas, para la supervivencia total ajustada a la calidad de vida en la determinación del mes 36, en pacientes con bloqueo androgénico completo se reflejan en las Tablas X-XI. Para ninguna de ellas se obtuvo diferencia estadísticamente significativa.
GASTO FARMACÉUTICO. COSTE-UTILIDAD
A. Evolución temporal (años 2000-2005) del gasto farmacéutico total y relativo del bloqueo androgénico en el área de salud de Zamora.
Con respecto al gasto farmacéutico total de los fármacos empleados en la hormonoterapia del cáncer de próstata, se obtiene una cifra para el área de salud de Zamora de 1.348.820,04 Euros - € - en el año 2000, descendiendo un 3,85 % en el 2001, hasta situarse en 1.296.956,38 €. El ascenso en el 2002 es del 6,69 %, alcanzando una cifra de 1.383.779,87 €, reduciéndose nuevamente en 2003 un 1,23 % correspondiéndole un valor de 1.366.702,77 €. Para 2004 dicho gasto experimenta un incremento del 1,76 %, situándose en una cifra de 1.390.812,12 €, disminuyendo finalmente en el 2005 un discreto 0,27 %, equivalente a un gasto total de 1.386.988,5 €.
Si analizamos, por otra parte, la evolución del porcentaje relativo de gasto farmacéutico en bloqueo androgénico para el área de salud de Zamora con respecto al gasto farmacéutico total de la misma se obtiene un descenso progresivo en dichos valores entre los años 2000 y 2005, pasando de un 3,82 a un 2,63 % (Figura 2).

B. Resultados coste-utilidad.
Los datos obtenidos relacionando el coste del bloqueo androgénico completo y la supervivencia ajustada a la calidad de vida - en Euros/ año de vida ajustado a la calidad - se recogen en la Figura 3. El valor medio del gasto farmacéutico en bloqueo androgénico completo por AVAC ganado es de 4.768,52€ (DT= 3.509,86).

Discusión
SINTOMATOLOGÍA DEL TRACTO URINARIO INFERIOR
El efecto de la deprivación androgénica sobre la sintomatología del tracto urinario inferior - STUI - ha sido evaluado tanto en el contexto de hiperplasia benigna como en carcinoma prostético.
En estudios experimentales con ratas sometidas a castración se obtuvo un aumento en la densidad de receptores alfa-1 prostéticos, explicándose dicho resultado por el incremento relativo del componente estromal frente al epitelial durante la deprivación androgénica - reversible tras administración de suplementos de testosterona -, y no debido a fenómenos de autorregulación positiva (1).
En pacientes afectos de hiperplasia benigna prostática se ha objetivado una reducción del 29 % en el volumen prostático medido por ecografía tras 12 semanas de tratamiento con buserelina o acetato de ciproterona; acompañándose de un incremento en el flujo urinario máximo, y disminución en la frecuencia miccional diurna así como en los volúmenes de orina residual (2). Se apreció un cierto incremento en la capacidad contráctil del detrusor pero no se documentaron cambios en los valores de resistencia uretral. Tras el cese del tratamiento referido, se verificó un nuevo crecimiento del volumen prostático a partir de un periodo variable de 3-36 semanas, así como reversibilidad de los efectos clínicos y urodinámicos descritos.
En un estudio con 61 pacientes diagnosticados de adenocarcinoma de próstata localmente avanzado o metastático se analizaron de forma prospectiva y retrospectiva las diferencias obtenidas entre los resultados de aplicar el International Prostate Symptom Score - IPSS - y el Symptom Problem Index - SPI - a los tres y seis meses del comienzo del tratamiento con un análogo de la GnRH (3). Con el uso del método prospectivo se apreció mejoría estadísticamente significativa de 2,9 puntos en la primera medición al finalizar el primer trimestre, con un descenso no significativo de 0,9 puntos tras seis meses de seguimiento. Aplicando los test de forma retrospectiva - método del "then-test" -, el incremento en las puntuaciones a los tres meses fue de 4,2 puntos, mientras que en la determinación de los seis meses se objetivó una mejoría de 1,8 puntos. La mejoría obtenida en la calidad de vida a los tres meses y reflejada a través del SPI fue de 4 frente a 2,2 puntos, mediante el uso del método retrospectivo y prospectivo, repectivamente. A los seis meses de seguimiento se objetivó deterioro no significativo mediante medición prospectiva, mientras que con la retrospectiva se apreció mejoría de forma significativa.
Los resultados obtenidos con mediciones retrospectivas deben ser interpretados con precaución, debido a un potencial efecto de "cambio de respuesta" que explicara las diferencias con respecto a las mediciones realizadas a través del método "test/pretest", dado que los pacientes son susceptibles de cambiar sus estándares a la hora de juzgar los niveles de funcionamiento interno y por tanto sus síntomas/calidad de vida (4). Algunas publicaciones defienden que las variaciones en dichos estándares deben ser aceptados e incorporados a los resultados de los estudios de calidad de vida (5,6).
El hecho de que en nuestro estudio se aprecien con respecto al ámbito miccional diferencias significativas desfavorables para los varones sin neoplasia frente a los tratados con deprivación androgénica en la mayoría de determinaciones temporales, y considerando el rango etario de la muestra poblacional, puede vincularse a la mayor influencia sintomática que procesos como el crecimiento prostático benigno ejercen de forma aislada sobre dicha esfera de CDVRS. La estabilización de las puntuaciones tras un primer resultado desfavorable el mes 12 frente a la determinación basal se puede enmarcar dentro de un efecto terapéutico que el bloqueo ejercería con respecto a dicha sintomatología.
ALTERACIONES INTESTINALES
En el contexto del bloqueo androgénico completo, los antiandrógenos se asocian frecuentemente a efectos secundarios gastrointestinales tales como dolor abdominal, alteraciones en el hábito intestinal y anorexia. El mecanismo concreto se desconoce. Algunos estudios cifran la incidencia hasta en un 22% (7), apuntando la posibilidad de que no sólo la toxicidad local de la flutamida sea el único factor responsable. Es de destacar, en cualquier caso, que la sintomatología relacionada con el tracto intestinal se manifiesta con mayor frecuencia en pacientes sometidos a combinación de análogo de GnRH más antiandrógeno (8).
El uso de opiáceos condiciona la aparición de estreñimiento como principal efecto adverso de dicho tratamiento, al influir sobre el tracto gastrointestinal y determinadas vías medulares espinales, produciendo descenso en la capacidad secretora y peristáltica. Estas manifestaciones persisten en el tiempo, dada la lenta tolerancia que experimentan los pacientes, especialmente en el contexto de tratamientos habitualmente crónicos. El uso de laxantes y el incremento en la ingesta de fibra constituye el primer escalón terapéutico, debiendo asociarse catárticos osmóticos tipo lactulosa en casos refractarios (9).
Las diferencias significativas halladas en nuestro estudio con respecto a la sintomatología intestinal entre sujetos con y sin neoplasia en las determinaciones de los meses 12 y 24, desfavorables para los pacientes con bloqueo hormonal sintonizan con lo expuesto anteriormente, si bien el hecho de una estabilización de las puntuaciones a partir del mes 12 podría situarse en el contexto de mayor racionalización de la medicación complementaria - tipo opiáceos, por ejemplo -, junto a la adopción de medidas higiénico-dietéticas procedentes.
SOFOCOS
La influencia que sobre el bienestar físico ejerce la aparición de sofocos en el contexto de la deprivación androgénica para el cáncer de próstata ha sido objetivada en algunos estudios (10), mediante la aplicación del instrumento FACT de medición de CDVRS. Se demostró asimismo una relación significativa entre la evaluación clínica de dicha manifestación y el deseo de tratamiento expresado por parte de los pacientes. Los sofocos han sido descritos como síntoma "sumamente penoso" en el 27 % de sujetos en tratamiento hormonal (11).
La existencia de diferencias estadísticamente significativas entre los sujetos con y sin neoplasia de nuestro estudio, con respecto a la manifestación de sofocos, en todas las determinaciones temporales a partir del mes 12, es un hallazgo esperable. Lo son también las diferencias intertemporales halladas al comparar la determinación basal frente a las de los meses 12 y 36, así como la estabilización posterior de las cifras de objetivación de esta sintomatología a lo largo del periodo entre las dos últimas determinaciones mencionadas.
ÁMBITO SEXUAL
La sexualidad es un fenómeno complejo y multidimensional que incorpora aspectos biológicos, psicológicos, interpersonales y del comportamiento. Las variantes del comportamiento sexual normal vienen definidas por cada paciente y su pareja, siendo influenciadas por determinados factores como el género, la edad, las actitudes personales y los valores religiosos y culturales.
Los cálculos de incidencia de disfunción sexual después de tratamientos antineoplásicos varían entre un 40-100 % (12). Los problemas sexuales más comunes de estos pacientes en varones son la falta de apetito sexual y disfunción eréctil. Otras posibles manifestaciones son la aneyaculación, eyaculación retrógrada y anorgasmia - aunque con respecto a esta última, resulta más frecuente su retraso de origen farmacológico o secundario a cuadros de ansiedad (13) -.
A diferencia de muchos otros efectos secundarios fisiológicos del tratamiento del cáncer, los problemas sexuales no tienden a resolverse durante el primer o segundo año de supervivencia libre de enfermedad (14). Se ha observado que la calidad de vida post-tratamiento de las neoplasias prostáticas varía de forma significativa, incluso en aspectos como la calidad de la intimidad sexual, las relaciones cotidianas con el sexo opuesto, su capacidad de fantasear sexualmente, y la autopercepción de su masculinidad (15).
La disfunción sexual en el contexto oncológico tiene un origen multifactorial. Los factores físicos incluyen deterioro funcional, fatiga y dolor. El tratamiento analgésico con opioides puede dar lugar a reducción en la líbido, disfunción eréctil, e índice de testosterona bajo. Se cree que hay dos mecanismos que son responsables: inhibición de la producción de GnRH y producción de hiperprolactinemia, que causa retroalimentación negativa en la liberación de la LH y reduce la producción de testosterona (16). Se sabe que los opioides alteran la función normal del eje gonadal pituitario hipotalámico. Estos efectos suelen desaparecer después de haberse suspendido el opioide. Otros casos de pacientes que han recibido opioides para el tratamiento del dolor crónico, confirman estos hallazgos (17).
Los factores psicológicos pueden ser variados (13). Las creencias erróneas sobre el origen de la neoplasia y el posible sentimiento de culpabilidad relacionado con las mismas ejerce una influencia negativa significativa en el campo de la sexualidad; resultando frecuente la convicción de que alguna actividad sexual en el pasado, relación extramatrimonial, o enfermedad sexualmente transmitida haya podido causar su cáncer, o incluso de que la actividad sexual pueda fomentar una recurrencia de su tumor - especialmente en los individuos con neoplasias pélvicas o genitales -. La depresión coexistente - 15-25 % más prevalente en los pacientes con cáncer que en la población sana (18) -, los cambios en la imagen corporal y las tensiones en las relaciones interpersonales - a veces asociadas a miedo al rechazo - constituyen asimismo otros factores determinantes de una disfunción sexual de origen psicológico.
Los inhibidores selectivos de la recaptación de la serotonina - ISRSs - bloquean el mecanismo de realmacenamiento de dicho neurotransmisor en la vesícula sinaptosómica post-estímulo, dando como resultado una acumulación de serotonina en el espacio sináptico (19), ocasionando una infrarregulación de los receptores postsinápticos a nivel hipotálamico, lo cual origina a su vez una disminución en la liberación de neurotransmisores excitatorios de los centros erectógenos. La disfunción sexual debida a los ISRSs se estima que afecta a alrededor de un 8-20 % de todos los pacientes. Las tasas de disfunción sexual asociadas con cada uno de los ISRSs fueron las siguientes: sertralina - 16-56 % -, fluoxetina - 20-54 % -, paroxetina - 22-65 % -, fluvoxamina - 59 % -, y venlafaxina - 38 % -. Los síntomas sexuales más comunes eran orgasmo retrasado o anorgasmia, seguidos por la disminución de la líbido (20). La paroxetina produjo retardos significativamente mayores del orgasmo o de la eyaculación - 48 % -, y provocó disfunción eréctil más frecuentemente que la sertralina - 37 frente a 16 % -, la fluvoxamina - 31 frente a 10 % -, o la fluoxetina - 34 frente a 16 % -, respectivamente.
La edad no necesariamente se relaciona con disminución de la líbido, y así, en determinados estudios con varones de edad avanzada, estos coincidieron en que el sexo influye en su calidad de vida, que el rendimiento adecuado a la edad puede mantenerse aún y que los trastornos sexuales son preocupantes (21).
La deprivación androgénica en el tratamiento del cáncer de próstata supone una disminución paralela de la actuación de las hormonas sexuales masculinas en el cerebro para fomentar el deseo, y hasta un 80 % de pacientes refieren una profunda reducción del interés sexual, acompañada de disfunción eréctil y dificultad para alcanzar el orgasmo (22). Se ha estimado que concentraciones de testosterona sérica inferiores a 5-8 nmol/ L (23) se correlacionan con el declive en la función sexual, de tal forma que el descenso en los niveles de dicha hormona conllevarían una disminución en el efecto de retroalimentación positiva que ésta ejerce preferentemente sobre áreas corticales temporales (24).
El número creciente de hombres cada vez más jóvenes diagnosticados con cáncer prostático asintomático avanzado - unido al hecho de que éstos a veces pueden continuar gozando de una función sexual adecuada -, ha favorecido el otorgar cada vez más atención a la prevención de la morbilidad sexual del tratamiento, y en este sentido algunos autores han probado posponer la terapia hormonal hasta el comienzo de los síntomas (25), administrarla de manera intermitente (26) o utilizar una combinación de un inhibidor de la 5-alfa reductasa y un antiandrógeno en vez de los tratamientos bloqueantes hormonales completos (27) aunque no se haya terminado de evaluar la influencia que estas opciones tengan sobre la duración de la supervivencia.
Existen varios modelos de evaluación/ intervención sobre la esfera sexual, algunos de ellos específicamente diseñados para los pacientes neoplásicos (28). El modelo Kaplan facilita pautas de entrevista, concentrándose en la queja principal, el estado sexual, el estado psiquiátrico, la familia y los antecedentes psicosociales, procediendo posteriormente a la evaluación de las relaciones, el resumen del caso y las recomendaciones (29). El modelo PLISSIT - grado de permiso, información limitada, sugerencias específicas, y terapia intensiva -, es otro modelo de evaluación e intervención utilizado con regularidad como marco para la rehabilitación sexual en el cuidado oncológico (30).
Los factores generales que afectan el funcionamiento sexual y que precisan ser estimados en la evaluación son variados, y entre ellos podemos destacar:
• Funcionamiento sexual premórbido. El desarrollo sexual previo al diagnóstico de la enfermedad, así como sus preferencias y su experiencia son esenciales de cara a la evaluación del estado sexual. El grado de funcionamiento sexual, el interés en el sexo, la satisfacción y la importancia de la relación influyen en la posible angustia del paciente con respecto al momento de función sexual actual. Así, los individuos que ya han tenido dificultades sexuales pueden tener una vulnerabilidad acentuada a los efectos del tratamiento (31).
• Estado de la relación. Se debe tener en cuenta la duración, calidad y estabilidad de la relación antes del diagnóstico. Además, como muchos pacientes temen ser rehusados o abandonados, el clínico debe indagar sobre la respuesta de la pareja a la enfermedad y sobre las preocupaciones del paciente en cuanto a las consecuencias del tratamiento en aquélla (32). Las parejas comparten muchas reacciones con los pacientes ya que sus preocupaciones más importantes suelen relacionarse con la pérdida y el temor a la muerte.
• Estado psicológico. La ansiedad y la depresión son dos de las interrupciones afectivas comunes entre los pacientes con cáncer, debiendo ser evaluadas dada la ya vista repercusión en el ámbito sexual. Con frecuencia el papel social de la pareja cambia durante el tratamiento. La identidad de un individuo y su autoestima pueden verse amenazados cuando cambian estas funciones (28); y la participación del compañero en la atención física del paciente puede asimismo tener una potencial repercusión negativa en el sentimiento de sexualidad de éste.
La evaluación de la sexualidad se complementa desde un punto de vista médico con la aplicación de cuestionarios (33) como el International Index of Erectile Function - IIEF -, y el Brief Male Sexual Functioning Inventory - BMSFI -, escalas validadas que miden los aspectos de la función sexual y de la satisfacción sexual en el varón. Existe asimismo la posibilidad de utilizar escalas abreviadas, como el Sexual Health Inventory for Men - SHIM - .
Los ejercicios de "enfoque sensorial" del placer, sin coito (34), ofrecen una opción de expresión de sentimientos íntimos sin la presencia de la presión y/ o ansiedad que conlleva la obligación de intentar consumar el coito, constituyendo una alternativa no necesariamente excluyente con respecto al resto de enfoques terapéuticos - inhibidores de la 5-fosfodies-terasa, inyección intracavernosa de prostaglandina E-1, etc -, que actúan sobre el aspecto erectógeno de la dinámica sexual.
En un estudio (35) los pacientes sometidos a bloqueo androgénico intermitente presentaron diferencias significativas frente a la terapia continua en cuanto a actividad sexual, de tal forma que el 41 % de los primeros referían mantenerla a los nueve meses de tratamiento, un 40 % a los 15 meses, y el 35 % a los 21 meses.
Haciendo referencia específica a los resultados obtenidos en nuestro estudio, el hallazgo de diferencias significativas en la esfera sexual desfavorables a los pacientes con deprivación androgénica - así como la disminución del porcentaje de pacientes con actividad sexual en las últimas cuatro semanas - en todas las determinaciones temporales, excepto en la basal, se puede explicar por el negativo efecto ejercido en este ámbito por parte del bloqueo hormonal. La ausencia de diferencias intertemporales significativas en todos los pares de determinaciones comparados en pacientes con bloqueo androgénico es destacable; y si bien se objetivó una evolución hacia peores puntuaciones en los meses 12 y 24, la limitada cuantía de dichas diferencias puede apuntar a una adecuación relativemente precoz del comportamiento y hábitos sexuales de los pacientes a la nueva situación creada a partir de la instauración del tratamiento.
EVALUACIÓN GENERAL DE LA CDVRS TOTAL EN EL BLOQUE ANDROGÉNICO
La medición de la CDVRS total en pacientes con diagnóstico de adenocarcinoma prostático y sometidos a bloqueo androgénico ha sido reflejada en determinadas publicaciones. Así, se han objetivado en una serie de pacientes con enfermedad no metastática (36) mejores puntuaciones globales - tras 6 y 12 meses de seguimiento -, en aquellos a los que se les indicó una actitud expectante frente a los que se les inició de forma precoz el tratamiento hormonoterápico, apreciándose diferencias significativas en detrimento del segundo grupo tanto en los valores globales de CDVRS como en las subescalas de actividad física, fatiga, y disfunción sexual. El componente psicológico de angustia también resultó superior en aquellos pacientes a los que se administró bloqueo androgénico. Otros autores (37) han objetivado empeoramiento en la función sexual, así como deterioro en el desempeño de roles sociales y función cognitiva subjetiva, a pesar de apreciarse mejorías en las funciones física y urinaria.
Los resultados de un estudio randomizado con evaluaciones basadas en la administración de cuestionarios psicosociales - una semana antes del comienzo de terapia deprivativa androgénica en el grupo de pacientes con tratamiento activo -, no han logrado demostrar una clara ventaja de éste sobre la actitud expectante. Las oscilaciones - incrementos o descensos - en las puntuaciones globales de CDVRS - fueron menores en el grupo sometido a observación con respecto al tratado con hormonoterapia (38).
En una serie compuesta por 91 pacientes con diagnóstico histológico de cáncer de próstata con afectación adenopática (39) se objetivó una peor CDVRS global en el grupo de deprivación hormonal de instauración inmediata frente al de comienzo diferido, presentando asimismo el primero peores puntuaciones en las esferas sexual, emocional, y física, aparte de experimentar mayor frecuencia de sofocos. El tiempo hasta la progresión clínica fue significativamente más corto en el grupo de tratamiento diferido frente al de bloqueo hormonal inmediato - 33 vs 62 meses -, sin apreciarse diferencias significativas en cuanto a supervivencia total.
En un estudio basado en la aplicación del instrumento SF-36 a pacientes en tratamiento con deprivación androgénica durante menos de seis meses frente a un grupo tratado por un periodo superior de tiempo, y a otro sin tratamiento, en este último se apreciaron diferencias significativas en cuanto a mejor función física y puntuación global de CDVRS. No se objetivaron dichas diferencias en el campo de la función mental (40).
Otras publicaciones han aportado asimismo resultados de CDVRS desde un punto de vista global. Ejemplo de ello es la evaluación de 173 pacientes diagnosticados de cáncer de próstata metastático clínicamente asintomático (41) a los que se le dio la opción de tratamiento con asociación de leuprorelina más flutamida, un análogo de la GnRH como monoterapia, orquiectomía, dietilestilbestrol, flutamida, o abstención terapéutica. Los valores de CDVRS fueron significativamente mejores en los pacientes que se decantaron por la última opción. El bloqueo androgénico completo se asoció a una mayor fatiga y alteración emocional en comparación con las otras formas de deprivación androgénica, ejerciendo su influencia no sólo la disminución de los niveles de testosterona sérica, sino también el componente psicológico del recuerdo diario de la enfermedad que supone la administración del antiandrógeno.
En una publicación (22), derivada del Prostate Cancer Outcomes Study - PCOS -, se realizó un seguimiento de 661 pacientes, de cara a establecer una comparación entre terapia supresiva hormonal frente a abstención terapéutica. Se evaluaron cinco dominios - dolor, depresión/ansiedad, vitalidad, limitaciones físicas, y limitaciones secundarias al estado emocional -, así como un ítem global acerca del estado general de salud, obtenido del cuestionario genérico RAND SF-36. Se objetivó que aquellos pacientes sometidos a tratamiento farmacológico presentaban al año de seguimiento diferencias significativas en cuanto a pérdida de líbido, porcentaje de impotencia, e inactividad sexual con respecto al grupo de actitud expectante. La prevalencia de ginecomastia, así como la de sofocos - y la frecuencia semanal de aparición de estos - resultó también mayor en el grupo de hormonoterapia. Se apreciaron diferencias significativas en cuanto a disconfort físico en el subgrupo de pacientes con bajo riesgo de presentar enfermedad no organoconfinada y sometidos a tratamiento; sucediendo de igual forma en cuanto a limitación en la actividad diaria en el subgrupo de alto riesgo sometido a bloqueo hormonal, si bien en estos se obtuvieron diferencias significativas en lo referente a satisfacción con el tratamiento administrado.
En un estudio observacional de cohortes denominado Esfuerzo de Investigación Urológica Estratégica sobre Cáncer de Próstata - CaPSURE -, basado en un cuestionario que incluye el RAND 36 item Health Survey 1.0, el UCLA PCI, y otras cuestiones para la medición de la autoestima y el impacto general del cáncer de próstata en el sujeto y su familia, se ha objetivado una discreta mejoría en los dominios de la CDVRS durante el primer año de tratamiento hormonoterápico, exceptuando el referente a la función sexual y molestias derivadas (42, 43), mientras que los pacientes que eligieron una actitud expectante presentaron disminución de las puntuaciones obtenidas en las esferas de salud general, actividad física y relación social.
Krongrad, con el uso simultáneo del UCLAPCI y el RAND SF-36 señala que hasta un 41 % de las variaciones en los valores globales de CDVRS pueden ser atribuidos al componente no enfermedad-específico, mientras que a las esferas urinaria, sexual e intestinal les correspondería un porcentaje del 16, 15 y 14 %, respectivamente (44).
En un estudio sobre una muestra de 288 varones con adenocarcinoma de próstata, (45) se utilizó el cuestionario CARES para discriminar entre los diferentes estadíos clínicos de la enfermedad, demostrándose la utilidad de este instrumento para documentar cuantitativamente el progresivo empeoramiento de la CDVRS según progresa la neoplasia. Dichos hallazgos han sido también confirmados en otras publicaciones (46) mediante el uso de los instrumentos de la EORTC, analizando tanto a los pacientes como a sus parejas, demostrando que según avanza la enfermedad, el declive en la CDVRS de los primeros viene acompañado de un incremento paralelo en el estrés emocional de las segundas. En el mismo sentido cabe señalar los resultados de un estudio transversal (47), según el cual aquellos pacientes con enfermedad hormonosensible presentan mejores resultados frente a los hormonorresistentes en los dominios de CDVRS correspondientes a dolor, energía, interacción social y salud mental.
La mejora en la calidad de vida durante los periodos de descanso terapéutico en el bloqueo androgénico intermitente no ha sido confirmada - en la mayor parte de series - de forma estadísticamente significativa mediante cuestionarios validados (48), mientras que en las evaluadas con estos, los resultados no son coincidentes. Así, se ha publicado (49) una mejoría en los valores de bienestar general durante los periodos de pausa terapéutica. En otras publicaciones (50) se objetiva una mejoría del estado general en el 37,5 % de casos, de la astenia en el 42 %, del 62 % en la incidencia de sofocos y recuperación de la erección, y del 75 % en la recuperación de la líbido en los periodos de no tratamiento. Otros autores (51), utilizando el cuestionario EORTC QLQ-C30 sólo encuentran mejoría en los efectos adversos propios del tratamiento hormonal, pero no en las actividades sociales y ocupacionales, en el estado emocional ni en la función sexual. En un estudio aleatorio (52), se obtuvieron resultados preliminares observándose unos mejores resultados en calidad de vida en el grupo de intermitencia, pero sin mejora significativa en la actividad sexual. En otras publicaciones (53), utilizando el SF-36 y el PCI, se ha objetivado mejoría clínica significativa en los periodos sin tratamiento en astenia, función sexual, y líbido, frente a una menor mejoría en la función física y molestias urinarias.
A pesar de que la intervención psicosocial en el paciente diagnosticado de cáncer de próstata - defendida en algunas publicaciones (54) - no ha demostrado incrementos en la supervivencia, algunos autores hacen referencia al papel de los cuestionarios autoadministrados de CDVRS como un factor complementario a la hora de predecir dicho parámetro en términos temporales (55).
Para la realización del estudio que presentamos, se optó por la comunicación telefónica - debido a razones logísticas - para la evaluación de la CDVRS de los pacientes. El uso de este tipo de entrevista para la adquisición de datos acerca de CDVRS a través de instrumentos de medición del tipo cuestionario con valores en escala ha demostrado ser un método fiable (56) si se compara con la obtención de los mismos mediante una entrevista presencial con el sujeto, siendo las diferencias entre ambos métodos no significativas.
Con el objeto de facilitar la interpretación práctica de los resultados de los estudios de CDVRS debe obtenerse el mínimo número de mediciones que pueda ofrecer la mayor cantidad de información acerca de los cambios sucedidos. Los intervalos temporales deben ser lo más similares posibles entre los grupos en estudio y control, tomando como punto de referencia inicial los valores obtenidos en el momento del diagnóstico del proceso neoplásico - para el primer grupo mencionado -, dada la dificultad en disponer de datos basales - no retrospectivos -, previos a la confirmación del tumor.
No existen valores "umbral" que sean universalmente aceptados como puntos de corte que diferencien cambios significativos en la CDVRS, sin embargo, muchos autores consideran aceptable calificar como tales a aquellos que constituyan una variación del 5-10 % sobre la cifra previa.
Específicamente con respecto a las esferas física, emocional y social, así como en relación con la escala global de CDVRS del instrumento QLQ-C30 los propios pacientes sometidos al mismo estimaron que variaciones de entre 5-10, 10-20, ó > 20 puntos suponen cambios leves, moderados o importantes frente a la situación personal previa, respectivamente (57). Otros autores, sin embargo (58) consideran que la definición de "gran diferencia" con respecto al valor previo difiere según cada esfera - por ejemplo, 7 para la función emocional, 27 para la física, y 16 para la CDVRS global -. No faltan, asimismo, intentos de clasificación estandarizada de resultados de acuerdo a la edad y sexo (59).
Los hallazgos en nuestro estudio de una evolución hacia peores puntuaciones en las determinaciones temporales hasta el mes 24 para los valores totales del instrumento QLQ-C30 así como los de la suma QLQ-C30 más QLQ-PR25 en los pacientes sometidos a deprivación androgénica completa se sitúan en la línea de informaciones ya mencionadas acerca del deterioro de CDVRS tras la instauración de dicho tratamiento. Todo ello se ve reforzado con las diferencias significativas obtenidas en los meses 12 y 24 al comparar los valores totales del instrumento QLQ-PR25 así como los de la suma QLQ-C30 más QLQ-PR25 entre pacientes con bloqueo y sujetos sin neoplasia. Las particularidades de los resultados de dichos pacientes en el ámbito sexual son uno de los factores que condicionan en mayor medida la evolución de los valores totales del instrumento QLQ-PR25, presentando una estabilización más precoz que la verificada tanto para el otro instrumento utilizado en este estudio como para la suma de ambos.
Cabe mencionar el hallazgo - en la determinación temporal del mes 36 - de mejores puntuaciones totales del instrumento QLQ-C30, así como de la suma de éste más el QLQ-PR25 en pacientes sometidos a bloqueo androgénico con estudios medios/ superiores frente a los poseedores de estudios básicos o sin estudios. Podría atribuirse un cierto efecto que la comprensión de la multidimensionalidad de la CDVRS por parte del paciente con mayor formación ejerciera a la hora de éste contrarrestar la potencial influencia negativa de la neoplasia prostática y su tratamiento.
La objetivación, por su parte, de mejores puntuaciones totales de los instrumentos QLQ-C30 y QLQ-PR25, así como de la suma de ambos, en los pacientes con gammagrafía ósea positiva frente a los que presentaron resultado negativo se sitúa dentro del ámbito de lo esperable.
PERCEPCIÓN SUBJETIVA DEL PROPIO ESTADIO GLOBAL DE SALUD
Según los datos de la Encuesta Nacional de Salud de España (60) correspondiente al año 2003, el 73 % de los hombres y el 63,2 % de las mujeres de 16 y más años valoran su salud como buena o muy buena. Ello supone un 68 % de la población de dicho rango de edad, agrupando a ambos sexos; cifra discretamente inferior a la correspondiente a 1993 - 68,5 % -. España ocupa una posición intermedia entre los países de la UE respecto a esta percepción.
En nuestro estudio, las descripciones de los resultados correspondientes a la percepción del propio estado general de salud así como de la calidad de vida son coincidentes. Se objetiva que en todas las determinaciones temporales tras ambas mediciones resultan puntuaciones significativamente favorables para aquellos sujetos sin neoplasia, en sintonía con la existencia ya descrita de cifras satisfactorias en ausencia de enfermedad. Por otra parte, se aprecia un empeoramiento progresivo de dichas apreciaciones subjetivas en los varones sometidos a deprivación an-drogénica hasta la determinación del mes 24; y en este sentido, la relativa estabilización posterior de los valores objetivados pudiera estar en relación con una adaptación multidimensional de los pacientes a las situaciones emergentes que la entidad diagnosticada - y su tratamiento instaurado - van originando.
SUPERVIVENCIA AJUSTADA A LA CALIDAD DE VIDA
No existe evidencia acerca de la existencia de diferencias significativas en la supervivencia a los dos años al comparar pacientes con bloqueo androgénico completo frente a aquellos sometidos a castración aislada. A los cinco años, dicha diferencia es del 2,9 % - un 27,6 % frente al 24,7 % - favorable a la primera opción terapéutica. Los valores de supervivencia media se sitúan en 33,3 frente a 29,9 meses, objetivándose que la mencionada ventaja atribuida al bloqueo máximo se mantendría de forma independiente con respecto a los rangos etarios o estadíos de la enfermedad analizados (61). Otras publicaciones coinciden asimismo en aceptar el hecho de una mayor supervivencia en pacientes sometidos a bloqueo androgénico completo frente a castración como mo-noterapia (62), detectándose disminución del riesgo de mortalidad entre un 10-22 % a favor del primer tipo de tratamiento mencionado (63).
Las cifras de supervivencia resultantes son también similares cuando se comparan dos de los antiandrógenos no esteroideos - flutamida y nilutamida - que pueden usarse asociados al análogo de GnRH en el bloqueo hormonal completo. El análisis comparativo de aquellos con acetato de ciproterona permite objetivar supervivencias más cortas, con diferencias desfavorables para este último fármaco (61). Por otra parte, el ensayo correspondiente al estudio de bicalutamida vs flutamida - en asociación con análogo - detectó ciertas diferencias en la supervivencia media de los pacientes favorables a la primera, si bien carecieron de significación estadística (64). La ausencia en nuestro estudio de diferencias significativas al comparar los distintos antiandrógenos utilizados en el bloqueo hormonal está, por tanto, en consonancia con la literatura señalada.
Con el bloqueo máximo se obtiene incremento de la supervivencia cáncer-específica a los cinco años de seguimiento. La supervivencia libre de progresión experimenta mejoría significativa con el bloqueo androgénico completo hacia el final del primer año, pero no en los intervalos de seguimiento posteriores (62).
Algunos autores (65) han encontrado diferencias significativas en la supervivencia de los pacientes sometidos a deprivación androgénica completa en función de que ésta tenga una duración de cumplimiento mayor o menor de 120 días, con resultados más favorables para el primer supuesto.
El análisis de la CDVRS es uno de los puntos focales de nuestro estudio, y de ahí que se haya priorizado la evaluación de los resultados de supervivencia tras su ajuste mediante la aplicación de los valores de ponderación preferencial, y no desde un punto de vista neto, que supondría objeto de valoración por parte de otro tipo de trabajos, ejemplos de los cuales son las referencias bibliográficas referidas en los párrafos previos de este apartado. Partiendo de esta consideración, cabe señalarse la limitada mención que se ha dado hasta el momento en la literatura científica al ajuste de supervivencias en función de la calidad de vida. En este contexto de escasez se pueden, no obstante, referir determinadas consideraciones de interés; y así, por ejemplo, algunos autores señalan la falta de evidencia de la potencial asociación existente entre las características sociodemográficas de los pacientes - sexo, edad, estatus socioeconómico, estado civil, raza y religión - y los resultados de análisis de ponderación preferencial (66), y en este sentido se debe situar la ausencia de diferencias estadísticamente significativas obtenidas en nuestro estudio con respecto a la variable etaria analizada.
En relación al resto de variables evaluadas en nuestro estudio con respecto a la supervivencia ajustada a la calidad de vida, si bien se obtienen ciertas diferencias en los resultados, más o menos esperables "a priori" si nos refiriéramos a valores netos pre-ajuste, - tal y como sucede, por ejemplo al objetivarse mayor en pacientes que presentan cifras de PSA < 20 ng/ mL, morfología prostática ecográfica transrectal no sospechosa, positividad unilateral de la biopsia prostática y gammagrafía ósea negativa -, no logran ser de suficiente entidad. Ante la falta de disponibilidad de referencias bibliográficas específicas que ofrezcan reflexiones acerca de la relación de las variables mencionadas y valores ajustados de supervivencia, se apunta la conveniencia de realización de estudios multicéntricos para la eventual corroboración de ausencia de significación estadística no vinculada a una limitación en el número disponible de pacientes estudiados.
En nuestro estudio no se objetivaron diferencias significativas entre la supervivencia ajustada a la calidad de vida entre los sujetos con y sin neoplasia al mes 36 de seguimiento. Los resultados de análisis de ponderación preferencial suelen manifestar la tendencia a la asignación de mayor valoración de su estado de salud por parte de pacientes que han presentado o presentan algún grado de deterioro del mismo, con respecto a sujetos de la población general sin dicha experiencia (67).
La potencial influencia que este aspecto pudiera ejercer sobre la comparación de sujetos con y sin enfermedad en nuestro estudio, debe considerarse relativizada dado el uso de una base de datos de origen asistencial como fuente para la obtención de la muestra comparativa, tratándose por tanto de personas con algún grado de experiencia acerca de estados de afectación de la salud. Por ello, esta consideración permite mantener la validez de los resultados de supervivencia ajustada mencionados, haciéndose necesaria a la luz de los mismos la matización de la trascendencia que las alteraciones provocadas por el bloqueo androgénico completo en determinadas esferas o ámbitos de la CDVRS poseen a la hora de una valoración de ponderación preferencial por parte de los pacientes.
FARMACOECONOMÍA
A. Gasto farmacéutico
Los datos correspondientes al año 2003, sitúan el gasto sanitario público en España en 41.199,7 millones de Euros, lo que supone un 71,4% del gasto sanitario total del País, que asciende a 57.698,7 millones de Euros. El gasto sanitario total en España expresado como porcentaje del Producto Interior Bruto - PIB - es de un 7,7%, cifra discretamente inferior al promedio de la Unión Europea, situado en el 9%. El porcentaje sobre el PIB de gasto sanitario público es del 5,5% y el del gasto sanitario privado es el 2,2%. Según los datos publicados por el Ministerio de Sanidad y Consumo acerca de la composición del gasto, son los servicios hospitalarios y especializados los que representan un mayor porcentaje del mismo - 52 % -, seguidos por la prestación farmacéutica - 22,3% - y los servicios de Atención Primaria - 16 % -, (68).
La tasa de crecimiento anual del gasto farmacéutico público en España ha sido del 5,5% real desde 1980 y del 6,4% real en la década de los 90 (69). El crecimiento de dicho gasto es debido a tres fuentes potenciales principales:
- Niveles de precios. El precio de los medicamentos registrados en España ha crecido muy por debajo del Indice de Precios al Consumo - IPC -, máxime teniendo en cuenta que la mayoría de las novedades que se introducen en el mercado no están incluidas en este índice y que éstas suelen tener un precio más alto porque incorporan una prima por innovación. A su vez, los precios en España se encuentran entre los más bajos de Europa. La rebaja de márgenes farmacéuticos introducida en 1997, el sistema de precios de referencia implantado en diciembre de 2000, y la potenciación del uso de genéricos son las únicas medidas que han permitido una cierta contención del gasto.
- Consumo farmacéutico y coste medio por receta. El número medio de recetas por habitante no se ha incrementado significativamente - ha pasado de 12,2 a 14,4 recetas por habitante y año en los últimos 20 años -. La variable que más ha crecido en España ha sido el coste medio por receta, - un 5 % anual en la última década -, debido sobre todo al incremento de las prescripciones de productos de última generación que sustituyen a los ya existentes y que tienen un precio superior a estos. Este fenómeno sólo tendría repercusiones potencialmente positivas sobre el gasto sanitario total en caso de que dichas sustituciones se basaran en criterios de coste-efectividad.
- Envejecimiento de la población. El número de recetas de activos no ha crecido en los últimos 5 años, mientras que las recetas de pensionistas han crecido a una tasa media del 2,5% anual, crecimiento superior al del número de pensionistas, que lo ha hecho a una tasa del 1,4% anual. El envejecimiento conlleva un aumento del gasto farmacéutico, ya que las personas de más edad suelen ser los mayores consumidores de fármacos. Así, la fórmula del copago ha pasado de representar el 19% del consumo farmacéutico total en 1981, a un 11% en 1990, y hasta poco más del 7% en 2000. Por su parte, el gasto de los pensionistas constituyó un 58% del gasto farmacéutico en 1981, el 70% en 1990, y más de un 77 % en 2000.
El patrón actual de crecimiento del consumo farmacéutico en España es, por otra parte, similar al observado en el resto de la Unión Europea - si bien debe tenerse en cuenta que los valores netos per cápita en nuestro país resultan ser unos de los más bajos de la misma -. El gasto farmacéutico público español ha crecido un 5,22 % en 2007 - 5,19 % en Castilla y León -, sólo un punto por encima de la inflación registrada en dicho año, constituyendo esta última cifra por cuarto año consecutivo una cifra de crecimiento real de la industria farmacéutica inferior al incremento del PIB, manifestándose una tendencia decreciente del peso del gasto farmacéutico público, tanto sobre el gasto sanitario total como sobre el propio PIB (70) (71), habiendo sido favorecida desde un punto de vista institucional mediante la rebaja de precios de medicamentos impuesta por el Ministerio de Sanidad y Consumo en 2005 y 2006. El más reciente informe del National Economic Research Associates recoge una previsión de crecimiento del gasto farmacéutico en España para el año 2008 de un 5,37 % (72).
Las previsiones futuras de gasto farmacéutico global estarán condicionadas por la evolución del crecimiento de la población española en los próximos años, y sobre todo a su envejecimiento. Sin embargo, el descenso constante experimentado por la cuantía del coste de la asociación de fármacos utilizada en el bloqueo androgénico completo frente al gasto total del área de salud estudiada objetivado a partir del análisis de las cifras de la base de datos Concylia (73), debe hacernos pensar en la posibilidad de relativizar el peso económico atribuido a priori a esta opción terapéutica en particular.
B. Coste-utilidad del bloqueo androgénico completo.
El cáncer de próstata supuso un 5-6 % de los costes globales destinados a tratamiento tumoral, estimándose en 12.400 Dólares - $ - ya en la década de los años 90 el coste medio por paciente desde el diagnóstico de la neoplasia hasta su éxitus (74). Aproximadamente el 25 % del gasto total fue utilizado durante el primer año post-diagnóstico. Los costes hospitalarios constituyeron el 72 % del total, mientras que el gasto farmacéutico supuso un 15 %.
La proporción de pacientes diagnosticados "de novo" de cáncer de próstata subsidiarios de tratamiento hormonal a los que no se le ha administrado inicialmente el mismo ha ido progresivamente en descenso desde la segunda mitad de la década de los años 80 (75), contribuyendo al constante incremento en los costes generados por dicha patología. Si atendemos a los datos canadienses del Ontario Drug Benefit Program (76), los gastos farmacéuticos totales relacionados con el cáncer de próstata en varones de edad superior a 64 años se incrementaron de 0,2 a 15 millones de Dólares en el periodo 1985-1992 - un 7500% -, frente a un aumento del 305% en el gasto global de todos los fármacos. El coste anual estimado por paciente pasó de 77 a 1.838 $ - incremento del 2.387% -, frente al 240% para el global de grupos farmacológicos.
En Estados Unidos, los costes medios anuales generados por el tratamiento de un paciente con enfermedad metastática han sido estimados entre 1.807-2.225 $ (77,78). La mayoría de dichos costes - 80,5 % - se deberían a la terapia antiandrogénica. La combinación de nilutamida y goserelina resulta la opción farmacológica más cara - 41.400 $ como suma total durante el periodo de supervivencia -, aunque obtiene también la mejor cifra de AVAC - 5,13 -, frente a valores de 5,10 para orquiectomía sola, 4,68 para monoterapia con dietilestilbestrol, 4,89 con análogo de GnRH, y 4,61 con antiandrógeno no esteroideo, respectivamente (79). Los resultados del estudio coste-utilidad comparando antiandrógeno no esteroideo más orquiectomía frente a ésta sola fueron de 43.400-74.800 $/ AVAC ganado, mientras que dicha cifra fue de 110.900-196.700 $/ AVAC al comparar bloqueo androgénico completo con antiandrógeno no esteroideo frente a castración quirúrgica sola.
Recientemente en alguna publicación (80) se defiende el carácter de coste-utilidad del bloqueo androgénico completo con bicalutamida frente a monoterapia con análogo de la GnRH en pacientes con cáncer de próstata estadío D2 - a los cinco y diez años de seguimiento, los valores resultantes de ratio coste-utilidad incremental fueron de 33.677 y 20.053 $ por AVAC ganado, respectivamente -. Otros autores (81) publican asimismo resultados favorables en análisis coste-utilidad de bloqueo androgénico completo con bicalutamida frente a bloqueo completo con flutamida, obteniéndose un valor de ratio coste-utilidad incremental de 22.000 y 16.000 $ por AVAC ganado, respectivamente.
Alguna revisión (82) estima el coste anual del BAC en un rango de 8.717-12.209 $. Dicho estudio objetivó una tendencia creciente hacia su instauración precoz, de tal forma que en el año 1988 un 24,8% de los pacientes sometidos a dicha terapia presentaba metástasis en el momento del inicio del tratamiento, frente al 7,6% de los iniciados en 1996. Tras un seguimiento medio de 10 años (83), el gasto atribuido al bloqueo androgénico completo resultó 17,3-20,9 veces más caro que el de la realización de castración quirúrgica, resultando menos costoso con respecto a ésta sólo en aquellos pacientes - 5,2 % del total - en los que se verificaron supervivencias máximas de 2,7-3,4 meses.
Al comparar instauración precoz vs tardía de bloqueo androgénico completo, el menor número de AVACs - 5,9 - se obtienen al iniciar el tratamiento coincidiendo con el diagnóstico mientras que la mayor cifra se logra con un inicio diferido del mismo - 6,8 AVACs cuando el paciente está asintomático y 7 si presenta síntomas -. Los costes medios de la medicación son ligeramente superiores si se comienza a administrar cuando los pacientes están asintomáticos - 14.700 $ -, frente a los 12.200 $ si la terapia se inicia al detectarse metástasis a distancia asintomáticas. El inicio del bloqueo androgénico completo coincidiendo con la detección de metástasis sintomáticas a distancia presenta una ratio coste-utilidad de 14.300 $/ AVAC ganado. Otros autores (84) también publican resultados de análisis coste-utilidad favorables para la instauración del bloqueo androgénico completo en estadíos clínicamente avanzados de la enfermedad. Las estimaciones acerca del bloqueo completo apuntan a que para resultar con criterios de coste-utilidad, la combinación de agonista de GnRH más antiandrógeno debería incrementar la supervivencia en un 20 % comparada con la lograda por la orquiectomía sola (85).
El bloqueo androgénico completo es, por tanto, una opción terapéutica que puede considerarse cara, favorable en términos de coste-utilidad sólo en algunos supuestos; no obstante, el hecho de que en nuestro estudio un porcentaje notorio de pacientes sometidos a dicho tratamiento presenten unas cifras de gasto por AVAC situadas en los márgenes inferiores - < 5000 -, con respecto a un rango de valores por lo demás amplio, constituye otro elemento que hace procedente al menos una reflexión previa antes de anatematizar en el plano económico el uso conjunto de análogo de GnRH y antiandrógeno.
Conclusiones
La aparición de sofocos y los peores resultados en el ámbito sexual constituyen dos aspectos de diferenciación mantenida entre los pacientes en tratamiento con deprivación androgénica completa y los sujetos sin cáncer, en detrimento de los primeros; presentando asimismo la esfera intestinal diferencias relevantes de forma temporal puntual.
Se objetiva - expresada de forma constante en el tiempo - una peor valoración de la percepción subjetiva del estado general de salud así como de la calidad de vida por parte de los pacientes con cáncer tratados con bloqueo androgénico completo frente a sujetos no neoplásicos.
No se aprecia ninguna esfera o ámbito que mantenga un deterioro significativamente constante a lo largo del periodo de estudio en los pacientes sometidos a bloqueo completo, aunque en fases iniciales éste sí exista - en mayor o menor grado - para todos los aspectos a estudio, incluidos la valoración de la percepción subjetiva del estado general de salud así como de la calidad de vida. Se verifica recuperación en el ámbito miccional.
El menor nivel de estudios cursados por los pacientes en tratamiento con bloqueo androgénico completo persiste como factor de diferenciación negativa en los resultados de CDVRS obtenidos en esta parte del trabajo, ocurriendo de igual forma con la positividad gammagráfica ósea.
La supervivencia ajustada a la calidad de vida no se ve influenciada de forma sustancial por los aspectos estudiados.
Existen factores que permiten la relativización de la importancia tradicionalmente concedida al impacto económico ejercido por el BAC frente al gasto farmacéutico total del área de salud estudiada.
Agradecimientos
Al Dr. Juan Miguel Silva Abuín, Profesor Asociado de la Facultad de Medicina de la Universidad de Salamanca y Director de la Tesis Doctoral "Calidad de vida y farmacoeconomía en pacientes del área de salud de Zamora, diagnosticados de adenocarcinoma de próstata y sometidos a supresión androgénica farmacológica completa", de parte de la cual se ha derivado el presente artículo; y en general a todas las personas que contribuyeron de una u otra forma a que aquélla se hiciera realidad.
Bibliografía y lecturas recomendadas (*lectura de interés y **lectura fundamental)
1. Lacey JP, Donatucci CF, Price DT, et al. Effects of androgen deprivation on prostate alpha 1-adrenergic receptors. Urology 1996; 48: 335-41. [ Links ]
*2. Bosch RJ, Griffiths DJ, Blom JH, et al. Treatment of benign prostatic hyperplasia by androgen deprivation: effects on prostate size and urodynamic parameters. J Urol 1989; 141: 68-72. [ Links ]
3. Rees J, Waldron D, O'Boyle C, et al. Prospective vs retrospective assessment of lower urinary tract symptoms in patients with advanced prostate cancer: the effect of 'response shift'. BJU Int 2003; 92: 703-6. [ Links ]
4. Sprangers MA. Response shift bias: a challenge to the assessment of patients' quality of life in cancer clinical trials. Cancer Treat Rev 1996; 22 (Suppl A): 55-62. [ Links ]
5. Breetvelt IS, Van Dam FS. Underreporting by cancer patients: the case of response shift. Soc Sci Med 1991; 32: 981-7. [ Links ]
6. Schwartz CE, Sprangers MA. Methodological approaches for assessing response shift in longitudinal health-related quality-of-life research. Soc Sci Med 1999; 48: 1531-48. [ Links ]
7. Langenstroer P, Porter HJ 2nd, McLeod DG, et al. Direct gastrointestinal toxicity of flutamide: comparison of irradiated and nonirradiated cases. J Urol 2004; 171(2 Pt 1): 684-6. [ Links ]
8. Kumar RJ, Barqawi A, Crawford ED. Adverse events associated with hormonal therapy for prostate cancer. Rev Urol 2005; 7(Suppl 5): S37-S43. [ Links ]
9. Portenoy RK. Constipation in the cancer patient: causes and management. Med Clin North Am 1987; 71: 303-11. [ Links ]
*10. Nishiyama T, Kanazawa S, Watanabe R, et al. Influence of hot flashes on quality of life in patients with prostate cancer treated with androgen deprivation therapy. Int J Urol 2004; 11: 735-41. [ Links ]
11. Karling P, Hammar M, Varenhorst E. Prevalence and duration of hot flushes after surgical or medical castration in men with prostatic carcinoma. J Urol 1994; 152: 1170-3. [ Links ]
12. Derogatis LR, Kourlesis SM. An approach to evaluation of sexual problems in the cancer patient. CA Cancer J Clin 1981; 31: 46-50. [ Links ]
13. Schover LR, Montague DK, Lakin MM. Sexual problems. En: DeVita VT Jr, Hellman S, Rosenberg SA, editores.: Cancer: principles and practice of Oncology. 5th ed. p. 2857-72. Lippincott-Raven Publishers. Philadelphia; 1997. [ Links ]
14. Helgason AR, Adolfsson J, Dickman P, et al. Factors associated with waning sexual function among elderly men and prostate cancer patients. J Urol 1997; 158: 155-9. [ Links ]
*15. Bokhour BG, Clark JA, Inui TS, et al. Sexuality after treatment for early prostate cancer: exploring the meanings of "erectile dysfunction". J Gen Intern Med 2001; 16: 649-55. [ Links ]
16. Gulliford SM: Opioid-induced sexual dysfunction. J Pharm Care Pain Symptom Control 1998; 6: 67-74. [ Links ]
17. Rajagopal A, Vassilopoulou-Sellin R, Palmer JL, et al. Symptomatic hypogonadism in male survivors of cancer with chronic exposure to opioids. Cancer 2004; 100: 851-8. [ Links ]
18. Massie MJ, Popkin MK. Depressive disorders. En: Holland JC, Breitbart W, Jacobsen PB, Lederberg M, Loscalzo M, Massie MJ et al., editores. Psycho-oncology. p. 518-40. Oxford University Press. New York; 1998. [ Links ]
19. Matsumoto AM: Endocrine and reproductive diseases. En: Bennett JC, Plum F, editores.: Cecil Textbook of Medicine. 20th ed. p. 1328-9. WB Saunders. Philadelphia; 1996. [ Links ]
20. Keller Ashton A, Hamer R, Rosen RC. Serotonin reuptake inhibitor-induced sexual dysfunction and its treatment: a large-scale retrospective study of 596 psychiatric outpatients. J Sex Marital Ther 1997; 23: 165-75. [ Links ]
21. Helgason AR, Adolfsson J, Dickman P, et al. Sexual desire, erection, orgasm and ejaculatory functions and their importance to elderly Swedish men: a population-based study. Age Ageing 1996; 25: 285-91. [ Links ]
**22. Potosky AL, Reeve BB, Clegg LX, et al. Quality of life following localized prostate cancer treated initially with androgen deprivation therapy or no therapy. J Natl Cancer Inst 2002; 94: 430-7. [ Links ]
23. Gooren LJ. Androgen levels and sex functions in testosterone-treated hypogonadal men. Arch Sex Behav 1987; 16: 463-73. [ Links ]
24. Stoleru S, Gregoire MC, Gerard D, et al. Neuroanatomical correlates of visually evoked sexual arousal in human males. Arch Sex Behav 1999; 28: 1-21. [ Links ]
25. Klein EA. Hormone therapy for prostate cancer: a topical perspective. Urology 1996; 47(1A Suppl):3-12. [ Links ]
26. Trachtenberg J. Innovative approaches to the hormonal treatment of advanced prostate cancer. Eur Urol 1997; 32 (Suppl 3): 78-80. [ Links ]
27. Brufsky A, Fontaine-Rothe P, Berlane K, et al. Finasteride and flutamide as potency-sparing androgen-ablative therapy for advanced adenocarcinoma of the prostate. Urology 1997; 49: 913-20. [ Links ]
28. Schover LR. Sexuality and Fertility After Cancer. John Wiley and Sons. New York; 1997. [ Links ]
29. Kaplan HS. The Evaluation of Sexual Disorders: Psychological and Medical Aspects. Brunner/Mazel Inc. New York; 1983. [ Links ]
30. Gallo-Silver L. The sexual rehabilitation of persons with cancer. Cancer Pract 2000; 8: 10-5. [ Links ]
31. Talcott JA, Manola J, Clark JA, et al. Time course and predictors of symptoms after primary prostate cancer therapy. J Clin Oncol 2003; 21: 3979-86. [ Links ]
32. McNeff EA. Issues for the partner of the person with a disability. En: Sipski ML, Alexander CJ, editores. Sexual Function in People With Disability and Chronic Illness. p. 595-616. Aspen Publishers, Inc. Gaithersburg; 1997. [ Links ]
33. Rosen RC. Evaluation of the patient with erectile dysfunction: history, questionnaires, and physical examination. Endocrine 2004; 23: 107-11. [ Links ]
34. Kaplan HS: The New Sex Therapy: active treatment of sexual dysfunctions. Brunner/ Mazel. New York; 1974. [ Links ]
35. Calais da Silva FM, Calais da Silva F, Bono A, et al. Phase III intermittent MAB vs continuous MAB. J Clin Oncol (Meeting Abstracts) 2006; 24: 4513. [ Links ]
36. Herr HW, O'Sullivan M. Quality of life of asymptomatic men with nonmetastatic prostate cancer on androgen deprivation therapy. J Urol 2000; 163: 1743-6. [ Links ]
37. Green HJ, Pakenham KI, Headley BC, et al. Coping and health-related quality of life in men with prostate cancer randomly assigned to hormonal medication or close monitoring. Psychooncology 2002; 11: 401-14. [ Links ]
*38. Green HJ, Pakenham KI, Headley BC, et al. Quality of life compared during pharmacological treatments and clinical monitoring for non-localized prostate cancer: a randomized controlled trial. BJU Int 2004 ; 93: 975-9. [ Links ]
39. van Andel G, Kurth KH. The impact of androgen deprivation therapy on health related quality of life in asymptomatic men with lymph node positive prostate cancer. Eur Urol 2003; 44: 209-14. [ Links ]
40. Dacal K, Sereika SM, Greenspan SL. Quality of life in prostate cancer patients taking androgen deprivation therapy. J Am Geriatr Soc 2006; 54:85-90. [ Links ]
41. Herr HW, Kornblith AB, Ofman U. A comparison of the quality of life of patients with metastatic prostate cancer who received or did not receive hormonal therapy. Cancer 1993; 71 (3 Suppl): 1143-50. [ Links ]
*42. Lubeck DP, Litwin MS, Henning JM, et al. Measurement of health-related quality of life in men with prostate cancer: the CaPSURE database. Qual Life Res 1997; 6: 385-92. [ Links ]
**43. Lubeck DP, Litwin MS, Henning JM, et al. Changes in health-related quality of life in the first year after treatment for prostate cancer: results from CaPSURE. Urology 1999; 53: 180-6. [ Links ]
*44. Krongrad A, Litwin MS, Lai H, et al. Dimensions of Quality of Life in prostate cancer. J Urol 1998; 160: 807-10. [ Links ]
45. Ganz PA, Schag CA, Lee JJ, et al. The CARES: a generic measure of health-related quality of life for patients with cancer. Qual Life Res 1992; 1:19-29. [ Links ]
46. Kornblith AB, Herr HW, Ofman US, et al. Quality of life of patients with prostate cancer and their spouses. The value of a data base in clinical care. Cancer 1994; 73: 2791-802. [ Links ]
*47. Albertsen PC, Aaronson NK, Muller MJ, et al. Health-related quality of life among patients with metastatic prostate cancer. Urology 1997; 49: 207-16. [ Links ]
48. Zerbib M, Conquy S, Gerbaud PF, et al. Efficacy and effect on quality of life (QOL) of intermittent androgen deprivation for prostate cancer treatment. Eur Urol 1998; 33 Suppl: A354. [ Links ]
49. Goldenberg SL, Bruchovsky N, Gleave ME, et al. Intermittent androgen suppression in the treatment of prostate cancer: a preliminary report. Urology 1995; 45: 839-44. [ Links ]
50. Bales GT, Sinner MD, Kim JH, et al. Impact of intermittent androgen blockage on quality of life. J Urol 1996; 155 Suppl 578A: A1069. [ Links ]
51. Bouchot O, Lenormand L, Karam G, et al. Intermittent androgen suppression in the treatment of metastatic prostate cancer. Eur Urol 2000; 38: 543-9. [ Links ]
52. Calais da Silva F, Bono A, Whelan P, et al. Phase III study of intermittent MAB versus continous MAB international cooperative study. Eur Urol 2002; 41 Suppl: A531. [ Links ]
53. Grossfeld GD, Small EJ, Lubeck DP, et al. Androgen deprivation therapy for patients with clinically localized (stages T1 to T3) prostate cancer and for patients with biochemical recurrence after radical prostatectomy. Urology 2001; 58 (2 Suppl 1): 56-64. [ Links ]
54. Spiegel D. Psychosocial intervention in cancer. J Natl Cancer Inst 1993; 85: 1198-205. [ Links ]
55. Herr HW. Quality of life in prostate cancer patients. CA Cancer J Clin 1997; 47: 207-17. [ Links ]
56. Kattan MW, Fearn PA, Cantor SB, et al. Telephone interviews vs. workstation sessions for acquiring quality of life data. Proc AMIA Symp 1999: 296-300. [ Links ]
57. Osoba D, Rodrigues G, Myles J, et al. Interpreting the significance of changes in health-related quality-of-life scores. J Clin Oncol 1998; 16: 139-44. [ Links ]
58. King CR. Overview of quality of life and controversial issues. En: King CR, Hinds PS (editores). Quality of life from nursing and patient perspectives. p. 23-34. Jones & Bartlett. Boston; 1998. [ Links ]
59. Hjermstad MJ, Fayers PM, Bjordal K, et al. Using reference data on quality of life--the importance of adjusting for age and gender, exemplified by the EORTC QLQ-C30 (+3). Eur J Cancer 1998; 34: 1381-9. [ Links ]
60. M.S.C. Datos relevantes sobre la salud de los españoles. En: Sistema Nacional de Salud. p. 6576. Ministerio de Sanidad y Consumo. Madrid; 2006. [ Links ]
61. P.C.T.C.G. Maximum androgen blockade in advanced prostate cancer: an overview of the randomised trials. Prostate Cancer Trialists' Collaborative Group. Lancet 2000; 355: 1491-8. [ Links ]
**62. Schmitt B, Bennett C, Seidenfeld J, et al. Maximal androgen blockade for advanced prostate cancer. The Cochrane Database of Systematic Reviews 1999; Issue 2. Art. No.: CD001526. DOI: 10.1002/ 14651858. CD001526. [ Links ]
**63. Bennett CL, Tosteson TD, Schmitt B, et al. Maximum androgen-blockade with medical or surgical castration in advanced prostate cancer: a meta-analysis of nine published randomized controlled trials and 4128 patients using flutamide. Prostate Cancer Prostatic Dis 1999; 2: 4-8. [ Links ]
64. Schellhammer PF, Sharifi R, Block NL, et al. Clinical benefits of bicalutamide compared with flutamide in combined androgen blockade for patients with advanced prostatic carcinoma: final report of a double-blind, randomized, multicenter trial. Casodex Combination Study Group. Urology 1997; 50: 330-6. [ Links ]
*65. Sarosdy MF, Schellhammer PF, Johnson R, et al. Does prolonged combined androgen blockade have survival benefits over short-term combined androgen blockade therapy? Urology 2000; 55:391-5. [ Links ]
66. Weeks JC. Preferences of older cancer patients: Can you judge a book by its cover?. J Natl Cancer Inst 1994; 86: 1743-44. [ Links ]
67. Stiggelbout AM, de Haes JC. Patient preference for cancer therapy: an overview of measurement approaches. J Clin Oncol 2001; 19: 220-30. [ Links ]
68. M.S.C. Recursos económicos y gasto sanitario público. En: Sistema Nacional de Salud. p. 5560. Ministerio de Sanidad y Consumo. Madrid; 2006. [ Links ]
69. NERA. Diagnóstico y perspectivas del gasto farmacéutico en España. Farmaindustria. Madrid; 2001. [ Links ]
70. Farmaindustria. El mercado del medicamento en España. Boletín de Coyuntura no 33. Enero 2008. [ Links ]
71. Ministerio de Sanidad y Consumo. [sede Web]. [Acceso 1 de febrero de 2008]. Gasto farmacéutico a través de receta oficial del Sistema Nacional de Salud. Disponible en: http://www.msc.es/pro-fesionales/farmacia/datos/diciembre2007.htm [ Links ]
72. NERA. Perspectivas del gasto farmacéutico en España. Farmaindustria. Madrid; 2006. [ Links ]
73. Concylia. Consumo de Castilla y León. Sistema de Información de Farmacia. [base de datos]. Valladolid: Gerencia Regional de Salud de Castilla y León. Sanidad de Castilla y León [acceso 15 de septiembre de 2006]. [ Links ]
74. Koopmanschap MA, Roijen LV, Bonneux L, et al. Current and future costs of cancer. Eur J Cancer 1994; 30A: 60-5. [ Links ]
75. Jones GW, Mettlin C, Murphy GP. Patterns of care for carcinoma of the prostate gland: results of a national survey of 1984 and 1990. J Am Coll Surg 1995; 180: 545-54. [ Links ]
76. To T, Iscoe N, Klotz L, et al. Orchiectomy and hormonal therapy of prostate cancer. Can J Urol 1995; 2: 109-15. [ Links ]
77. Krahn MD, Mahoney JE, Eckman MH, et al. Screening for prostate cancer. A decision analytic view. J A M A 1994; 272: 773-80. [ Links ]
78. Taplin SH, Barlow W, Urban N, et al. Stage, age, comorbidity, and direct cost of colon, prostate, and breast cancer care. J Natl Cancer Inst 1995; 87: 417-26. [ Links ]
**79. Seidenfeld J, Samson DJ, Aronson N, et al. Relative effectiveness and cost-effectiveness of methods of androgen suppression in the treatment of advanced prostate cancer. Evid Rep Technol Assess (Summ) 1999; (4): i-x, 1-246, I1-36, passim. [ Links ]
*80. Penson DF, Ramsey S, Veenstra D, et al. The cost-effectiveness of combined androgen blockade with bicalutamide and luteinizing hormone releasing hormone agonist in men with metastatic prostate cancer. J Urol 2005; 174: 547-52. [ Links ]
*81. Ramsey S, Veenstra D, Clarke L, et al. Is combined androgen blockade with bicalutamide cost-effective compared with combined androgen blockade with flutamide? Urology 2005; 66: 835-9. [ Links ]
*82. Mariani AJ. Terapia de supresión androgénica en el cáncer de próstata: un ejercicio de gestión de recursos. En: Resel Estévez L, Ruiz de la Roja JC, Sánchez Sánchez E, editores. AUA Update Series. Actualización en Urología. (ed. española 2003). p. 25-32. Medical Trends. Barcelona; 2002. [ Links ]
*83. Mariani AJ, Glover M, Arita S. Medical versus surgical androgen suppression therapy for prostate cancer: 10-year longitudinal cost study. J Urol 2001; 165: 104-7. [ Links ]
**84. Bayoumi AM, Brown AD, Garber AM. Cost-effectiveness of androgen suppression therapies in advanced prostate cancer. J Natl Cancer Inst 2000; 92: 1731-9. [ Links ]
85. Hellerstedt BA, Pienta KJ. The current state of hormonal therapy for prostate cancer. CA Cancer J Clin 2002; 52: 154-79. [ Links ]
 Dirección para correspondencia:
Dirección para correspondencia:
Nicolás Alberto Cruz Guerra
Av. de los Reyes Católicos, 5, bajo izda
49021 Zamora. (España)
ncruz_g@hotmail.com
Trabajo recibido: 15 de diciembre 2008.











 texto en
texto en 


