My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actas Urológicas Españolas
Print version ISSN 0210-4806
Actas Urol Esp vol.34 n.8 Sep. 2010
Más allá del diagnóstico fotodinámico: buscando la excelencia en el diagnóstico del cáncer vesical no músculo-invasivo
Beyond the photodynamic diagnosis: Searching for excellence in the diagnosis of non-muscle-invasive bladder cancer
J. Oliva Encina, A. Marco Valdenebro, J. Pelegrí Gabarró y C. Rioja Sanz
Servicio de Urología, Hospital Royo Villanova, Zaragoza, España
Dirección para correspondencia
RESUMEN
La cistoscopia es el método de elección en el diagnóstico positivo del cáncer vesical no músculo-invasivo. La tasa de tumores que pasan inadvertidos durante la cistoscopia puede llegar al 30%; esto es debido a factores como la existencia de formas tumorales planas, de pequeño tamaño o de difícil visualización. El diagnóstico fotodinámico ha conseguido disminuir la tasa de tumores que pasan inadvertidos, y ha conseguido mejorar el diagnóstico de lesiones planas; con el consiguiente aumento del tiempo libre de recidiva y disminuyendo el número de actuaciones endoscópicas iterativas; pero a costa de una tasa de falsos positivos elevada. En los últimos años se han desarrollado una serie de sistemas ópticos que pretenden; sólos o asociados; mejorar la sensibilidad diagnóstica de la cistoscopia sin menoscabo de su especificidad. Entre estos sistemas debemos destacar algúnos como Narrow Band Imaging, la Tomografía de Coherencia Óptica y la Endomicroscopía Láser Confocal.
Palabras clave: Cáncer de vejiga. Narrow band imaging. Tomografía de coherencia óptica. Endomicroscopía láser confocal.
ABSTRACT
Cystoscopy is gold-standard method in non muscule invasive bladder cancer diagnosis. In the cistoscopic exploratión 30% of tumors could be overlookeed: it is due to a flat forms, litle size tumours or difficult visualization. Photodynamic diagnosis reduces overlooked tumours rate, and has improved diagnosis on flat forms, with the consequence of increasing lap time to recurrence and decrasing the number of iterative cistoscopy; nevertheless the false positive rate is high. In the last years developed new optical devices who try to improve alone or asociated diagnostic sensibility in cistoscopy whithout reduction of specificity. Among new devices we must emphasize some like Narow Band Imaging, Optical Coherence Tomography or Laser Confocal Endomicroscopy.
Key words: Bladder cancer. Narrow band imaging. Optical coherence tomography. Laser confocal endomicroscopy.
Introducción
El cáncer vesical no músculo-invasivo (NMIBC), es la segunda neoplasia urológica más frecuente y una de las de mayor prevalencia en el mundo occidental1. Su historia natural, caracterizada por un curso crónico, que discurre por un camino de eventos quirúrgicos, es una carrera que reta al urólogo a enfrentarse pronto a la recidiva y a llegar antes que la progresión.
En la práctica urológica diaria sabemos que la resección del NMBIC ha de ser en todo momento lo más completa posible. La calidad en la resección va a determinar a corto y medio plazo una disminución de la tasa de recidivas y de la tasa de progresión; con el consiguiente descenso en el número de resecciones por paciente, y disminución del gasto por paciente. Esto se demuestra en estudios clásicos como el de Brausi2, donde se evidencia la existencia de una amplia variabilidad en la tasa de recidiva dependiendo del centro y del cirujano; así aprecia tasas de recidiva en casos de tumores únicos del 3,4% al 20,6% anuales, y en el caso de tumores multifocales del 7,4% al 45,6% anuales; hecho que no puede explicarse por medio de la variabilidad en la conducta biológica del tumor.
Ante lo anteriormente expuesto; el urólogo ha buscado la excelencia en la identificación y posterior resección del NMIBC; siendo su principal objetivo la localización de la lesión plana, y la localización del mayor número de lesiones neoplásicas y preneoplásicas, que son recidivas en potencia, y que representan el embrión de la futura recidiva precoz. Para alcanzar este objetivo, el urólogo ha desarrollado una serie de técnicas que evidencian la presencia de neoplasia vesical, entre ellas el diagnóstico fotodinámico (PDD) ya sea con ácido 5 amnolevulínico (5-ALA) o con hexaminolevulinato (HAL). El empleo de PDD ha demostrado superioridad sobre el diagnóstico cistoscópico convencional (WL), pero presenta sus limitaciones; implica un sobrecoste a medio y corto plazo. El objeto de este artículo es analizar las nuevas técnicas de imagen que permiten junto a PDD, o de modo aislado, mejorar la capacidad diagnóstica del urólogo ante el NMIBC.
Diagnóstico fotodinámico
El diagnóstico fotodinámico es una técnica diagnóstica cistoscópica que mejora la visualización de lesiones neoplásicas vesicales. Está basada en la fluorescencia emitida por los tejidos neoplásicos al ser iluminados con una luz de cierta longitud de onda; previamente habremos administrado una sustancia intravesical; que puede ser 5-ALA o HAL, la cual es captada con avidez por el tejido neoplásico. Los tejidos embebidos en la sustancia fotosensibilizante, al ser iluminados por un haz de luz de determinada longitud de onda emiten una típica fluorescencia roja.
Los estudios clásicos con PDD empleando HAL, sobre un volumen de 553 pacientes, evidencian una tasa de sobredetección de PDD sobre WL del 29%. Si desglosamos esta tasa de sobredetección según el tipo de lesión, PDD diagnostica un 89% más de displasias que WL, un 59% más de CIS que WL, un 17% más de tumores en estadio Ta que WL y un 12% más de tumores en estadio T1 que WL, arrojando una tasa de falsos positivos del 30%3-8.
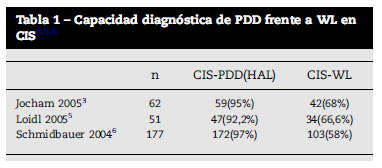
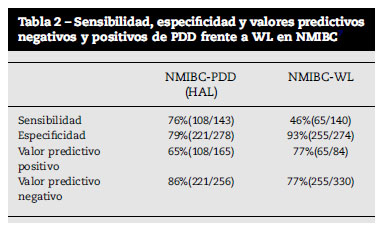
El diagnóstico fotodinámico ha demostrado su excelencia en la detección del carcinoma in situ (CIS), donde en la serie de Hungerhuber9, llega a obtenerse una sensibilidad en la detección del CIS del 92% empleando 5-ALA. Este mismo autor, comunica una incidencia del 17% de CIS en su serie de tumores, cuando la incidencia habitual es del 3% de los NMIBC. Otros autores más recientemente, comunican detecciones del 97%6. Este hecho hace que actualmente el empleo de PDD sea una de las herramientas claves en el diagnóstico de CIS. Las Guías Clínicas de la Asociación Europea de Urología indican el empleo de PDD con un grado de recomendación B y un nivel de evidencia Ilb10,11. Por otro lado la Asociación Austriaca de Urología recomienda en sus guias clínicas el uso de PDD en casos de citologías positivas y ausencia e hallazgos cistoscópicos, así como en el seguimiento de los tumores de alto riesgo10,11. Ahondando en el tema de las indicaciones del diagnóstico fotodinámico remito al lector a un artículo recientemente publicado por nuestro grupo donde defendemos y justificamos su empleo universal (tablas 1 y 2)12.
No existen estudios a largo plazo de PDD con empleo de HAL, pero PDD empleando 5-ALA nos oferta estudios de seguimiento a medio y largo plazo; en concreto la serie de Denzinguer13,14 nos presenta el seguimiento de un grupo sometido a resección de NMIBC con PDD (5-ALA), y otro sometido a resección convencional WL, a los 8 años la tasa de supervivencia libre de recidiva es del 71% con PDD y del 45% con WL. Esta diferencia entre ambos brazos es debida a la mejor resección efectuada con PDD que condiciona un menor número de tumores pasados por alto (overlooked), y que a medio y corto plazo condicionaran una recidiva. Estos hechos también son avalados por series como la de Filbeck15,16, que comunica una reducción de la tasa de recidivas del 59%, y Daniltchenko17, que aprecia un incremento de la supervivencia libre de enfermedad del 67% (tabla 3) (figura 1).
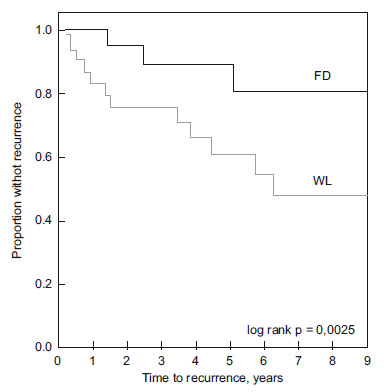
Figura 1. Tomada de13. En ordenadas proporción libre de recurrencia,
en abscisas tiempo a la recurrencia. (WL) Cistoscopia convencional.
(FD) Diagnóstico fotdinámico.
Limitaciones actuales del diagnóstico fotodinámico
Las limitaciones del diagnóstico fotodinámico actualmente son dos: la elevada tasa de falsos positivos y el elevado coste del agente fotosensibilizante que determina una aumento del gasto sanitario a corto plazo con una rentabilidad a medio y largo plazo.
La tasa de falsos positivos de PDD oscila entre el 30-40%, mientras que la de WL se encuentra entre el 21-31%8, si analizamos la tasa de falsos positivos en el contexto de una instilación de BCG previa, esta se eleva al 47%, teniendo en cuenta que la mayoría de los pacientes a los que se aplica PDD está en tratamiento con BCG, el elevado número de falsos positivos será una constante18.
Recientemente se ha realizado un riguroso análisis estadístico que identifica los factores pronósticos del falso positivo con el empleo de PDD. Sobre 306 pacientes sometidos a cistoscopia con PDD (5-ALA) realizandose 1.874 biopsias en 552 procedimientos endoscópicos, se concluyó que existia una mayor tasa de falsos positivos en mujeres, en pacientes sometidos a reseciones recientes, y en instilaciones previas de BCG, siendo las dos primeras variables predictoras de falso positivo pero independientes y recomiendan emplear PDD entre 9-12 semanas tras la última resección o instilación de BCG19.
Respecto al coste, la sustancia fotosensibilizante tiene, un precio en torno a los 420 . Este hecho va a condicionar que el empleo de PDD vaya a aumentar el coste del tratamiento de los pacientes con NMIBC, pero los estudios coste beneficio realizados hasta la fecha demuestran la disminución del gasto en recursos sanitarios, ya que el hecho de aumentar el tiempo a la recidiva y a la progresión, y disminuir la tasa de tumores residuales, determina un menor número de cistoscopias y un menor número de resecciones iterartivas, lo que compensaría sobradamente el gasto en sustancia fotosensibilizadora17. Debemos reseñar a la vez que en pacientes de alto riesgo de progresión, disminuye la tasa de esta, pero incrementa el número de cistoscopias, ya que retrasa o evita la cistectomía en un número elevado de pacientes, y aumenta el diagnóstico precoz de pacientes con lesiones planas de alto grado (CIS), pacientes que permaneceran en el conjunto de NMIBC de alto riesgo, precisando estos, controles cistoscópicos más frecuentes. Remito al lector a una revisión sobre coste beneficio en el empleo de PDD publicada por nuestro grupo12.
De este modo podemos identificar los dos puntos débiles que cuestionarían el empleo de PDD, primero la moderada o elevada tasa de falsos positivos o su discreta inespecifiidad, y segundo el precio de la sustancia sensibilizante que originaria un aumento del coste a corto plazo, pero una disminución de éste a medio y largo plazo. Estos dos motivos nos han llevado a revisar las nuevas técnicas diagnósticas en NMIBC que pudiesen complementar al diagnóstico fotodinámico.
Narrow band imaging
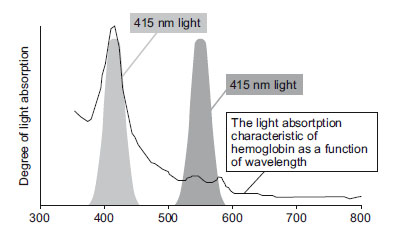
Narrow band imaging (NBI), es un sistema óptico de refuerzo de la imagen. Se fundamenta en el empleo de dos haces de luz de longitud de onda corta de 415 y 540nm. La luz de estos haces atraviesa los tejidos superficiales y es absorbida con avidez por la hemoglobina. La capacidad de penetración es mayor cuanto mayor es la longitud de onda, así podremos apreciar la trama vascular vesical que aparecerá de aspecto oscuro, contrastada con la claridad y semitransparencia del epitelio vesical. Pretende de este modo poner de manifiesto la estructura vascular subyacente al epitelio transicional, esta estructura adquiere una distribución característica y se altera adquiriendo especial conformación en torno a las neoplasias de urotelio suprayacentes20-22 (figura 2 y 3).
Figura 2. Características físicas del doble haz de luz de NBI.
En ordenadas grado de absorción del haz de luz por la hemoglobina,
y en abscisas longitud de onda del haz de luz en nm. Tomado de23.
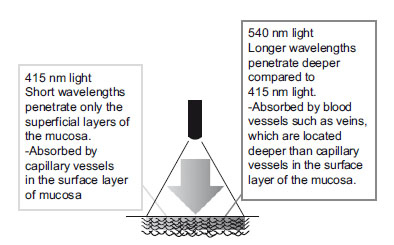
Figura 3. Diferente comportamiento de las diferentes longitudes
de onda que componen el haz de kuz de NBI la luz de longitud de
onda menor penetra sólo en los estratos superficiales del muro vesical,
la luz de mayor longitud de onda penetra de modo más profundo; ambas
son absorbidas con avidez por la hemoglobina que discurre en los capilares.
Tomado de23.
Subjetivamente NBI ofrece una visión nítida de los capilares suprficiales, apareciendo estos con un aspecto azulado y tornándose de color verdoso a medida que discurren de modo más profundo. Las lesiones tumorales aparecen con un vasculatura subyacente de aspecto verde oscuro, casi negro y las papilas muestran un punteado marrón oscuro que se corresponde con la visión transversal de los ejes vasculares de las papilas (figuras 4-6).
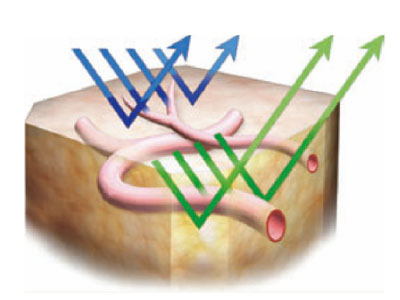
Figura 4. Diferente capacidad de penetración en función de
la longitus de onda del haz incidente. Tomado de23.
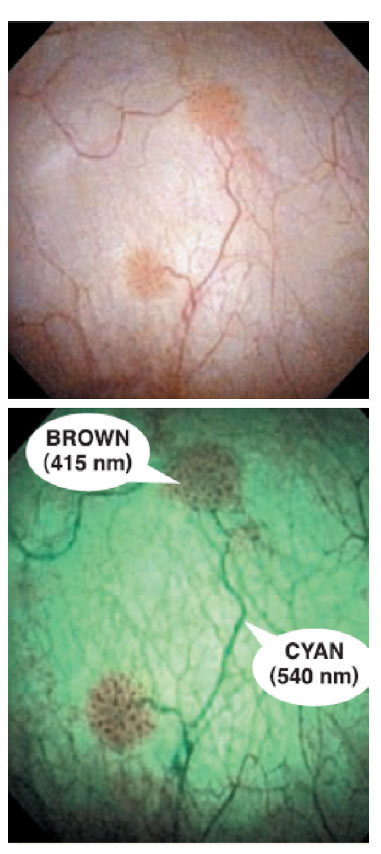
Figura 5. Imagen de un NMIBC con WL y con NBI. Tomado de23.
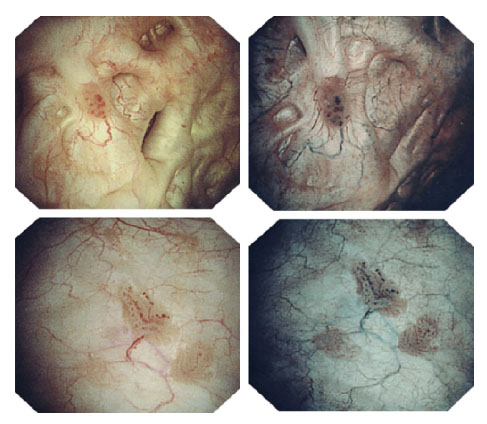
Figura 6. Imagen de varios NMIBC con WL y con NBI. Tomado de23.
La capacidad diagnóstica de NBI ha sido comunicada ya por algunos autores; en concreto son cuatro las series publicadas, la primera es la de Bryan23, este autor somete a 29 pacientes con antecedente de NMBIC en estadio pTa G1,G2, a una cistocopia con luz blanca convencional (WL), seguida de una cistoscopia con NBI. WL identificó 64 lesiones neoplásicas con una media de 2,21 lesiones por paciente (0-6), mientras que NBI identificó 79 lesiones, con una media de 2.72 lesiones por paciente, (1-7). Las 15 lesiones adicionales puestas en evidencia por NBI fueron detectadas en 12 de los 29 pacientes, y se repartieron del siguiente modo; en 10 pacientes se identificó una lesión adicional, y en otros 2 pacientes 2 y 3 lesiones adicionales respectivamente.
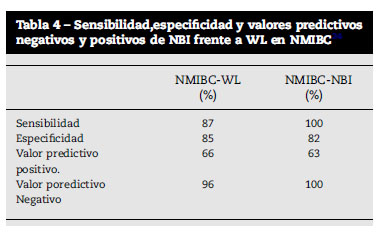
Una de las series más amplias es la de Herr24, en esta, a un total de 427 pacientes con antecedentes de NMIBC, se les sometió a cistoscopia con WL y NBI, se halló recidiva en 103 de los 427 pacientes, de estos, el 79% presentaba recidiva múltiple y un 67% presentaban CIS. WL identificó la recidiva en el 87% de los casos y NBI en el 100%, es decir que en un 13% de los casos el diagnóstico de la recidiva se debió a NBI en exclusividad. Todas las lesiones detectadas por WL eran visibles con NBI. El número de lesiones detectadas por WL fue de 231 lesiones con una media de 2,3 lesiones por paciente (0-11), mientras que NBI detectó 334 lesiones con una media por paciente de 3,4 lesiones (1-15). NBI identificó lesiones peritumorales en 58 casos, lo que representa el 56% del total de casos, éstas fueron 33 CIS, 25 pTa y 3 pT1. NBI fue capaz de descubrir una lesion tumoral más en el 28% de los pacientes, 2 o más en el 22%, 3 o más en el 6% y 4 o más en el 3%. Todo ello obliga a pagar un precio en forma de falsos positivos de del 36% para un total de 162 biopsias, tasa que no difiere mucho de la de WL que resultó ser del 33% para un total de 136 biopsias (tabla 4 y 5).
Similares resultados presentan otros centros, un grupo japonés comunica la realización de 147 biopsias sobre 82 pacientes. El 71% de las lesiones eran visibles con WL y NBI. Se diagnosticó neoplasia en 58 pacientes, de los cuales el 83% tenían alguna lesion solo evidenciables por medio de NBI, y el 34% de los pacientes tenían unicamente lesiones detectables por medio de NBI. Comunican una sensibilidad del 94% y una especificidad del 60,2%25.
Otros autores han comunicado experiencias con NBI en el reestadiaje de tumor vesical de alto grado tras resección primaria. Sobre 35 pacientes, se realizaron 235 biopsias con WL y 54 con NBI. WL detectó neoplasia en 6 pacientes y NBI en 13 pacientes, WL identificó neoplasia de alto grado en 5 casos y NBI en 13 casos26.
Tomografía de coherencia óptica
La Tomografía de Coherencia Óptica (OCT), es un nuevo sistema de cistoscopia, que permite la visión en tiempo real de la microarquitectura de la pared vesical. Nos ofrece imágenes transversales del muro vesical. Se presenta como un complemento a la visión cistoscópica convencional.
El principio físico de esta técnica es el análogo de la ecografía en modo B, pero empleando luz de longitud de onda próxima a la infraroja en lugar de sonido. La imagen que se obtiene se basa en la diferencia existente entre las longitudes de onda de luz incidente y la dispersión de ésta en el tejido incidido, (Scattering). Dependiendo de la profundidad y el estado del tejido la luz reflejada presentará una determinada longitud de onda.
Los diferentes patrones tisulares se traducirán en una escala de grises, ofertando una imagen similar a la histopatológica, con una resolución de 10μm en el eje lateral y de 3μm en el eje axial, así como un alcance en profundidad de 1-2mm20-22.
Los primeros estudios publicados se han realizado sobre piezas quirúrgicas, y de este modo se han obtenido patrones de imagen de OCT que se han correlacionado con el corte histopatológico y la posterior visión microscópica del tejido, identificando así los patrones de OCT que se corresponderían con tejido sano y los que se corresponderán con tejido neoplásico27.
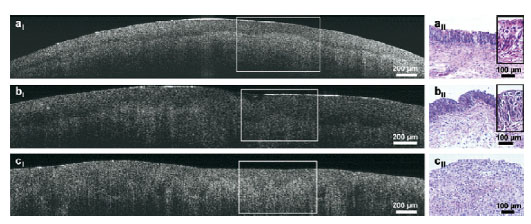
Sobre 142 piezas histopatológicas, 105 sin patología, 35 carcinomas, y 2 CIS procedentes de resección vesical, prostatectomías y cistectomías, se aplica OCT. Se correlaciona la imagen de OCT con los hallazgos histopatológicos, teniendo en cuenta las alteraciones que puede generar en OCT la fijación, deshiratación, congelación y tinción del especimen27 (figura 7).
aI-aII: PARED SANA: el urotelio aparece como una formación delgada con poca dispersión, algo más oscuro que el tejido subepitelial. La membrana basal aparece como un delgado estrato con mínima señal de intensidad y discreta dispersión.La mayor dispersión de la imagen se halla en la lámina própia.
bI-bII: CIS: la membrana basal aparece integra, con aspecto normal, y el urotelio no aparece homogeneo, se aprecia una alteración importante del tejido subpitelial respecto al tejido sano.
cI-cII: CÁNCER MUSCULO-INFILTRANTE: el tumor aparece sin diferenciaciones en los estratos, la membrana basal desaparece siendo un continuo entre el urotelio lámina propia y múscular.Toma el patrón de grano grueso.
Se identificaron correctamente 82 de los 105 especimenes sanos, con una especificidad del 78%; la tasa de falsos positivos fue del 5,7%, y fueron considerados como neoplásicos 6 especímenes sanos, ninguno fue catalogado como CIS y un 16,2% de los casos fue inclasificable. De los 35 casos neoplásicos 29 fueron correctamente estadiados (82,9%) pero ningún caso neoplásico fue etiquetado como no neoplásico. La sensibilidad global para el tumor vesical fue del 83%27.
La serie más representativa hasta la fecha realizada en humano "in vivo" es la de Goh y cols28. Emplea OCT de 10-20μm de resolución con una penetración de 2mm y con un tiempo de escaneo por imagen de 1,5 segundos. Realiza OCT sobre 32 pacientes: 24 con antecedente de tumor vesical superficial, 6 con diagnóstico cistoscópico inicial de tumor vesical, 1 con cáncer prostático y una hematuria sin hallazgos cistoscópicos ni ecográficos. Se obtienen 94 imágenes de zonas sospechosas, y se biopsian 38 de las 94 lesiones y establece la capacidad diagnóstica de OCT para la detección de tumores sin afectación de lámina propia, con afectación de ésta, y con afectación de la muscular, así como los diferentes patrones de imagen que presentan (tabla 6).
Retomando el problema de la relativa baja especificidad de PDD debemos citar un estudio que combina la aplicaión de PDD con hexaminolevulinato y el empleo de OCT. Demostrada la utilidad de diagnóstico fotodinámico en la búsqueda de lesiones planas se pretende disminuir la tasa de falsos positivos implementando el estudio fotodinámico (PDD) con la aplicación de OCT. En esta serie 66 pacientes con diagnóstico o sospecha de NMIBC son sometidos a cistoscopia con luz blanca (WL), cistoscopia con hexaminolevulinato (PDD), y por último se aplica OCT. Resultaron 232 lesiones sospechosas biopsiadas; 118 papilares y 114 planas; y 132 áreas de apariencia normal biopsiadas, lo que da un total de 364 muestras29.
PDD diagnosticó 12 lesiones papilares adicionales no visibles con WL (13,2%) y 19 CIS adicionales no visibles con WL (48,7%). En 6 pacientes con cistoscopia WL negativa se halló tumor vesical con PDD. Se diagnosticaron 96 lesiones papilares, 79 (86,8%) diagnosticadas con WL, todas excepto una visibles con PDD. La tasa de falsos positivos con WL fue del 11% mientras que con PDD fue del 36,8% (42 muestras).
OCT identificó como no neoplásicas 36 lesiones de las 42 falso positivas identificadas por PDD (85,7%). Sobre las 132 biopsias sobre tejido normal según las 3 técnicas, la histología demostró la existencia de 3 CIS y 1 papiloma de potencial malignos incierto (PUNLMP).
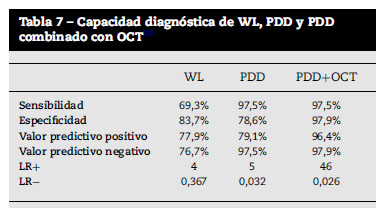
Analizando la tasa de detección por paciente, WL detectó tumor en 52 pacientes, lo que supuso la detección del 89.7% de los casos, mientras que PDD y PDD+OCT diagnosticaron el 100%. La especificidad de PDD fue del 62,5%, y al combinar PDD con OCT ésta ascendió al 87,5%; hecho que confirma nuestra tesis de que OCT puede ser una gran herramienta en la disminución del falsos positivos en el empleo de PDD (tabla 7) (figuras 8-12).

Figura 8. A) Pared sana: Estrato urotelial nítido. Se conserva
la estructura estratificada. Lámina propia patente y brillante,
seguida de muscular propia continuada por el estrato muscular.
(U) Uroltelio. (LP) Lámina propia. (MP) Muscular propia. Tomado de29.
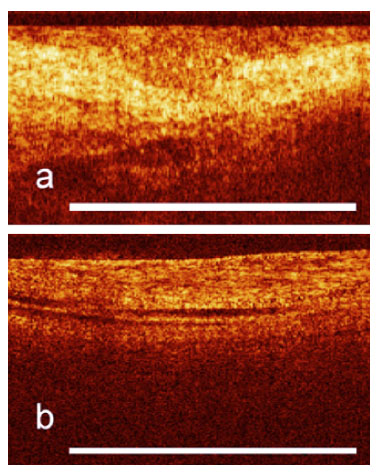
Figura 9. A) Displasia: Alto contraste entre estratos. Acusado límte entre uroltelio
y lámina propia. El urotelio permanece uniforme. Tomado de29. B) CIS: No clara
separación entre urotelio y lámina propia. Aparece como estrato único con aumento
de brillo. Muscular propia aparece independiente. Tomado de29.

Figura 10. Ta: Patrón top: Presenta bajo contraste sin
estratificación. Lámina propia intacta. Tomado de29.
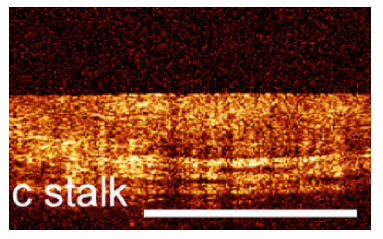
Figura 11. Ta: Patrón stalk: Presenta alto contraste con
estratificación. Lámina propia intacta. Tomado de29.

Figura 12. D) pT1: Se intuyen estratos, no se distingue urotelio
ni se define bien la lámina propia. Tomado de29. E)
pT2: Ausencia absoluta de estratificación. Tomado de29.
Espectroscopia de raman
Raman Spectroscopy (RS), es un sistema capaz de medir los componentes del tejido de un modo cuantitativo y cualitativo. Se basa en un efecto óptico descrito en 1928 por Sir C.V. Raman, efecto Raman o dispersión inelástica. Se da cuando los fotones de un haz incidente interactúan con las moléculas del tejido incidido, produciéndose un cambio en el estado vibracional de las moléculas del tejido, ello condiciona la liberación de un fotón de una determinada longitud de onda, fruto de la dispersión del haz de luz en el tejido. Cada molécula tiene un nivel vibracional específico, con su correspondiente longitud de onda. El espectro resultado, de la liberación energética secundaria a la actuación de un haz incidente de cada una de las moléculas del tejido, forma el espectro de raman. Este espectro en la pared vesical puede cambiar atendiendo a alteraciones neoplásicas o inflamatorias, y de este modo analizar la existencia o no de tejido neoplásico o inflamatorio20,21 (figura 13).
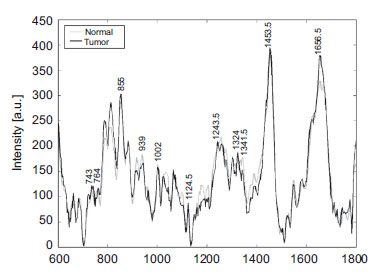
Figura 13. Comparación del espectro de raman de tejido
normal y de tejido tumoral. Tomado de20.
Los primeros resultados comunicados se han realizado ex-vivo, y anuncian sobre 15 muestras de de tejido, una sensibilidad el del 92% y una especificidad del 94% en la diferenciación entre tejido sano o neoplásico30.
Una serie de mayor tamaño sobre 75 muestras de tejido diferencia entre neoplásico, benigno e inflamatorio, con una sensibilidad del 90-95% y una especificidad del 95-98%. En la discriminación entre pT1-2 y pT3 sensibilidades y especificidades son superiores al 93%31.
Endomicroscopia láser confocal
La endomicroscopía láser confocal (ELC) es un sistema óptico que permite la visualización de la pared vesical en tiempo real. En los últimos años la miniaturización de los sistemas de edomicroscopía láser confocal han permitido su aplicación en el terreno de la gastroenterología y han comenzado a aplicarse ex-vivo. ELC permite obtener información de la microarquitectura del tejido urotelial sano y del neoplásico, previa infusión de fluoresceina intravenosa o su instilación intravesical32.
Hasta la fecha solo se ha comunicado un estudio in-vivo33. Este estudio emplea una fibra de 2,6mm por la que discurre un manojo de 30.000 fibras de láser asociadas a una fuente de láser de 480nm. Esto consigue una capacidad de penetración en la pared vesical de 60μm, un límite de resolución en el eje lateral de 1μm y una amplitud de campo de 240μm de diámetro. La incidencia de la luz láser sobre el tejido impregnado en fluoresceína origina la emisión de una fluorescencia que es recogida por las mismas fibras que emiten la luz láser a una velocidad de 8-12 imágenes por segundo. Previamente a la exploración se instila una solución de 300-500c.c. de fluoresceína al 0,1% 5min antes y/o 5ml intravenosos de fluoresceína al al 10%.
Se realizó el procedimiento sobre 27 pacientes con sospecha o diagnóstico de NMIBC. Inicialmente se procedió a describir el patrón de imagen del tejido urotelial sano, a medida que presionamos la fibra del láser sobre la pared vesical podemos apreciar un estrato más profundo. El estrato más suprficial es el llamado de células grandes donde las células del urotelio se hacen patentes debido a la distribución de la fluoresceína en el intersticio celular; a medida que nos adentramos en profundidad, los perfiles celulares se hacen más pequeños, es la parte más profunda del urotelio, y en un tercer estrato aparece el plano vascular originado por la fluorescencia en el seno del torrente vascular, pudiéndose ver en ocasiones los eritrocitos circulando por los capilares. Se apreció como el estrato vascular era menos patente en aquellos casos donde la aplicación de fluoresceína había sido solamente intravesical.
Respecto a los hallazgos en tejido tumoral, el autor comunica que de los 27 pacientes, 9 no presentaron neoplasia, del resto, 9 presentaron neoplasia de bajo grado y 9 de alto grado, incluyendo un carcinoma in situ. En los pacientes con halllazgo tumoral histopatológico ELC evidenció diferencias estructurales entre el tejido sano y los tumores de bajo y de alto grado, en los tumores de bajo grado se aprecia mayor densidad celular, pero sin perder la estructura tisular, apareciendo las céluas de modo uniforme. Los tumores de alto grado se presentan con una clara alteración de la estructura y una gran variabilidad en el tamaño celular. No puede obtenerse información sobre el aspecto de los núcleos, pues la fluoresceína no penetra a nivel intracelular. Con profundidades de penetración de 60μm no se ha podido discriminar la afectación o no de la capa muscular (figuras 14 y 15).
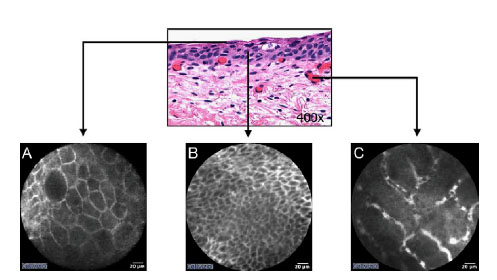
Figura 14. Comparación entre el corte de urotelio sano teñido con hematoxilina-eosina
con las diferentes estratos visibles con ELC. (A) Estrato superficial con células de gran
tamaño, células en paraguas. (B) Estrato más profundo con la porción estrecha de las
células en paraguas del epitelio transicional. (C) Estrato vascular evidenciando los
eritrocitos circulando en los capilares. Tomado de33.
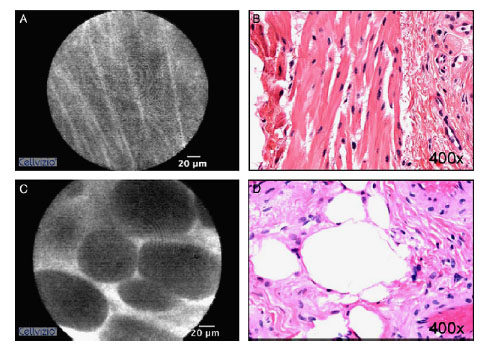
Figura 15. (A)(B) Imagen endomicrosóopica de Lecho de resección de NMIBC
y su correspondiente visión micróscópica teñida con hematoxilina-eosina apreciando
células el estrato muscular. (C)(D) Imagen endomicroscopicade lecho de resección de Tomado de33.
Endocytoscopy
Es un sistema desarrolllado por Olympus Medical Systems, su empleo no está generalizado, y consiste en la aplicación por medio de cistoscopia de una varilla de 3,5mm de diámetro en íntimo contacto con la pared vesical; la vejiga habrá sido bañada previamente en una solución de azul de metileno; el sistema consigue la magnificación del area de contacto de la varilla de hasta 450 veces, de este modo la magnificación nos ofrece imágenes comparables con visiones microscópicas34.
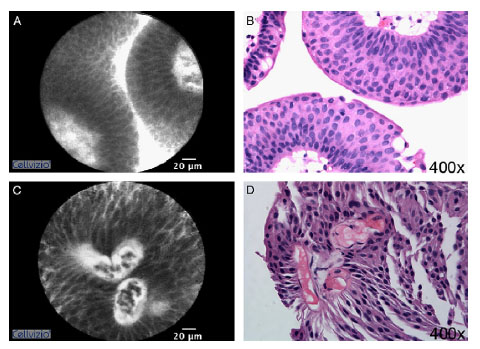
Figura 16. (A)(B) Imagen endomicroscopicadeLecho de resección de NMIBC
papilar de bajo grado y su correspondiente visión microscópica con tinción con
hematoxilina-eosina. (C)(D) Imagen endomicroscopicadeLecho de resección de
NMIBC papilar de alto grado y su correspondiente visión microscópica con
tinción de hematoxilina-eosina. Tomado de33.
Cápsula intravesical
El empleo de cápsulas dotadas de una microcámara que transmite imágenes al exterior es una técnica que lleva empleándose en los últimos 10 años en gastroenterología de modo generalizado. Actualmente se intenta reproducir esta técnica en el ámbito urológico. Se ha conunicaddo su emepleo de modo experimental en modelos porcinos. Esta cápsula transmite 4 imágenes por segundo, la cámara es movilizada de modo pasivo por los movimientos del animal y de modo activo por medio de placas magnéticas desde el exterior. Se ha conseguido visualizar la totalidad de la mucosa vesical35 (figura 17).

Figura 17. Wireless Capsule Endoscop (WCE). En su extremo
derecho presenta el sistema óptico, y en el extremo izquierdo
el sistema magnético para su guiado. Tomado de35.
Conclusiones
Todas las técnicas descritas, exceptuando PDD, necesitan mayor investigación para demostrar su verdadera utilidad clínica y evaluar la sistematización de su empleo. Por otro lado no puede cuestionarse la indicación universalmente aceptada del empleo de PDD en la detección de CIS en el caso de la existencia de citologías positivas y ausencia de hallazgos cistoscópicos. No admite ninguna discusión que el uso de PDD nos brinda una resección más completa, con disminución de la tasa de tumor residual y disminución de la tasa de recidivas. Asimismo se admite que su utilización origina un aumento considerable del coste, con disminución de éste a medio y largo plazo plazo debido al ahorro en cistocopias y en resecciones iterativas; y por último debemos de asumir la alta tasa de falsos positivos en el empleo de PDD, que se sitúa entre el 30-40%.
Respecto a NBI tenemos que decir que es aplicable en cualquier momento y a cualquier paciente sin precisar instilación previa de sustancia algúna, que no presenta contraindicaciones sistémicas, y que apenas supone sobrecoste; puede emplearse junto a PDD disminuyendo la tasa de falsos positivos, o de modo aislado. Aún está sin evaluar su implicación pronóstica a medio y largo plazo (tabla 8).
OCT y RS ofrecen información en tiempo real en extensión y en características histopatológicas del tumor. Pueden adyuvar a la vez a PDD disminuyendo también la tasa de falsos positivos. No puede obtenerse un cribado completo de la vejiga; tampoco está evaluada la capacidad de llevar a cabo una resección mas completa con OCT y RS; la posible presentación de artefactos artefactos con OCT en zonas límite de reseción condicionarían su empleo. OCT y RS podrían emplearse en la identificación de lesiones neoplásicas planas en tracto urinario superior. El resto de técnicas como ELC, endocytoscopy y la cápsula intravesical se encuentran aún en fases muy tempranas de su desarrollo.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
El autor agradece epecialmente a la editorial Elsevier y al consejo editorial de British Journal of Urology, por permitir la reproducción las figura 1-17; así como a los autores reseñados en los pies de cada figura y en la secuencia de referencias bibliográficas.
Bibliografía
1. American Cancer Society. Cancer Facts and Figures 2009. Atlanta, Ga: American Cancer Society; 2009. [ Links ]
2. Brausi M., Collette L., Kurth K., van der Meijden A.P., Oosterlinck W., Witjes J.A., et al, EORTC Genito-Urinary Tract Cancer Collaborative Group. Variability in the recurrence rate at first follow-up cystoscopy after TUR in stage Ta T1 transitional cell carcinoma of the bladder: a combined analysis of seven EORTC studies. Eur Urol. 2002; 41:523-31. [ Links ]
3. Jocham D., Witjes F., Wagner S., Zeylemaker B., van Moorselaar J., Grimm M.O., et al. Improved detection and treatment of bladder cancer using hexaminolevulinate imaging: a prospective, phase III multicenter study. J Urol. 2005; 174:862-6. [ Links ]
4. Witjes J.A., Moonen P.M., van der Heijden A.G. Comparison of hexaminolevulinate based flexible and rigid fluorescence cystoscopy with rigid white light cystoscopy in bladder cancer: results of a prospective Phase II study. Eur Urol. 2005; 47:319-22. [ Links ]
5. Loidl W., Schmidbauer J., Susani M., Marberger M. Flexible cystoscopy assisted by hexaminolevulinate induced fluorescen a new approach for bladder cancer detection and surveillance?. Eur Urol. 2005; 47:323-6. [ Links ]
6. Schmidbauer J., Witjes F., Schmeller N., Donat R., Susani M., Marberger M. Improved detection of urothelial carcinoma in situ with hexaminolevulinate (HAL) fluorescence cystoscopy. J Urol. 2004; 171:135-8. [ Links ]
7. Jichlinski P., Guillou L., Karlsen S.J., Malmström P.U., Jocham D., Brennhovd B., et al. Hexylaminolevulinate fluorescence cystoscopy: new diagnostic tool for photodiagnosis of superficial bladder cancer-a multicenter study. J Urol. 2003; 170:226-9. [ Links ]
8. Durek C., Wagner S., Zeylemaker B., Van Moorselaar J., Witjes F., Grimm M.O., et al. The significance of hexyl 5-aminolevulinate hydrochloride based fluorescence cystoscopy in treatment decisions-Results of a prospective phase 3 multicenter study. Eur Urol Suppl. 2004; 3:95. [ Links ]
9. Hungerhuber E., Stepp H., Kriegmair M., Stief C., Hofstetter A., Hartmann A., et al. Seven years' experience with 5-Aminolevulinic acid in detection of transitional cell carcinoma of the bladder. Urol. 2007; 69:260-4. [ Links ]
10. Babjuk M., Oosterlinck W., Sylvester R., Kaasinen E., Böhle A., Palou J. EAU Guidelines on Non-Muscle-Invasive Urothelial Carcinoma of the Bladder. Eur Urol. 2008; 54:303-14. [ Links ]
11. Jocham D., Stepp H., Waidelich R. Photodynamic diagnosis in urology: state-of-the-art. Eur Urol Suppl. 2008; 53:1138-48. [ Links ]
12. Oliva Encina J., Rioja Sanz C. Photodinamic diagnosis (PDD) in non-muscle-invasive bladder cancer (NMIBC), bibliographic review. Actas Urol Esp. 2009; 33:965-75. [ Links ]
13. Denzinger S., Wieland W.F., Otto W., Filbeck T., Knuechel R., Burger M. Does photodynamic transurethral resection of bladder tumour improve the outcome of initial T1 high-grade bladder cancer? A long-term follow-up of a randomized study. BJU Int. 2008; 101:566-9. [ Links ]
14. Denzinger S., Burger M., Walter B., Knuechel R., Roessler W., Wieland W.F., et al. Clinically relevant reduction in risk of recurrence of superficial bladder cancer using 5-aminolevulinic acid-Induced fluorescence diagnosis: 8-year results of prospective randomized study. Eur Urol Suppl. 2007; 51:1320-5. [ Links ]
15. Filbeck T., Pichlmeier U., Knuechel R., Wieland W.F., Roessler W. Clinically relevant Improvement of recurrence-free survival with 5-Aminolevulinic acid induced fluorescence diagnosis in patients with superficial bladder tumors. J Urol. 2002; 168:67-71. [ Links ]
16. Filbeck T., Pichlmeier U., Knuechel R., Wieland W., Roessler W. 5aminolevulinic acid induced fluorescence endoscopy decreases recurrence rate of superficial bladder carcinoma. Eur Urol Suppl. 2002; 1:121. [ Links ]
17. Daniltchenko D., Riedl C., Sachs M.D., Kurosch F.K., Pflueger D.H., loaning S., et al. Long-term benefit of 5-aminolevulinic acid fluorescence assisted transurethral resection of superficial bladder cancer: 5-year results of a prospective randomized study. J Urol. 2005; 174:2129-33. [ Links ]
18. Brausi M.A. Arguments against the Use of Fluorescence for the Diagnosis of Non-Muscle-invasive bladder tumours (NMIBT). Eur Urol Suppl. 2008; 7:430-3. [ Links ]
19. Draga R.O., Grimbergen M.C., Kok E.T., Jonges T.N., Bosch J.L. Predictors of false positives in 5-aminolevulinic acid-induced photodynamic diagnosis of bladder carcinoma: identification of patient groups that may benefit most from highly specific optical diagnostics. Urology. 2009; 74:851-6. [Epub 2009 Aug 15]. [ Links ]
20. Cauberg E.C., de Bruin D.M., Faber D.J., van Leeuwen T.G., de la Rosette J.J., de Reijke T.M. A new generation of optical diagnostics for bladder cancer: technology, diagnostic accuracy, and future applications. Eur Urol. 2009; 56:287-96. [Epub 2009 Mar 6]. [ Links ]
21. Goh A.C., Lerner S.P. Application of new technology in bladder cancer diagnosis and treatment. World J Urol. 2009; 27:301-7. [Epub 2009 Feb 22]. [ Links ]
22. Lee C.S., Yoon C.Y., Witjes J.A. The past, present and future of cystoscopy: the fusion of cystoscopy and novel imaging technology. BJU Int. 2008; 102(9 PtB):1228-33. [ Links ]
23. Bryan RT, Billingham LJ, Wallace DM. Narrow-band imaging flexible cystoscopy in the detection of recurrent urothelial cancer of the bladder. BJU Int 2008;101:702-5; discussion 705-6. [Epub 2007 Nov 13]. [ Links ]
24. Herr H.W., Donat S.M. A comparison of white-light cystoscopy and narrow-band imaging cystoscopy to detect bladder tumour recurrences. BJU Int. 2008; 102:1111-4. [Epub 2008 Sep 3]. [ Links ]
25. Tatsugami K., Kamoto T., Nishiyama H., Nishiyama A., Ishikawa S., Shinohara N., et al. Detection of bladder cancer with narrow-band-imaging. J Urol. 2009; 112:. Suppl, 414. [ Links ]
26. Naselli A., Introini C., Bertolotto F., Spina B., Puppo P. Narrow band imaging for detecting residual/recurrent cancerous tissue during second transurethral resection of newly diagnosed non-muscle-invasive high-grade bladder cancer. BJU Int. 2009. [Epub ahead of print]. [ Links ]
27. Hermes B., Spöler F., Naami A., Bornemann J., Först M., Grosse J., et al. Visualization of the basement membrane zone of the bladder by optical coherence tomography: feasibility of noninvasive evaluation of tumor invasion. Urology. 2008; 72:677-81. [Epub 2008 May 2]. [ Links ]
28. Goh A.C., Tresser N.J., Shen S.S., Lerner S.P. Optical coherence tomography as an adjunct to white light cystoscopy for intravesical real-time imaging and staging of bladder cancer. Urology. 2008; 72:133-7. [ Links ]
29. Schmidbauer J., Remzi M., Klatte T., Waldert M., Mauermann J., Susani M., et al. Fluorescence Cystoscopy with High-Resolution Optical Coherence Tomography Imaging as an Adjunct Reduces False-Positive Findings in the Diagnosis of Urothelial Carcinoma of the Bladder. Eur Urol. 2009. [Epub ahead of print]. [ Links ]
30. De Jong B.W., Schut T.C., Maquelin K., van der Kwast T., Bangma C.H., Kok D.J., et al. Discrimination between nontumor bladder tissue and tumor by Raman spectroscopy. Anal Chem. 2006; 78:7761-9. [ Links ]
31. Crow P., Uff J.S., Farmer J.A., Wright M.P., Stone N. The use of Raman spectroscopy to identify and characterize transitional cellcarcinoma in vitro. BJU Int. 2004; 93:1232-6. [ Links ]
32. Sonn G.A., Mach K.E., Jensen K., Hsiung P.L., Jones S.N., Contag C.H., et al. Fibered confocal microscopy of bladder tumors: an ex vivo study. J Endourol. 2009; 23:197-201. [ Links ]
33. Sonn G.A., Jones S.N., Tarin T.V., Du C.B., Mach K.E., Jensen K.C., et al. Optical biopsy of human bladder neoplasia with in vivo confocal laser endomicroscopy. J Urol. 2009; 182:1299-305. Epub 2009 Aug 14. [ Links ]
34. Ohigashi T., Kozakai N., Mizuno R., Miyajima A., Murai M. Endocyto-scopy: novel endoscopic imaging technology for in-situ observation of bladder cancer cells. J Endourol. 2006; 20:698-701. [ Links ]
35. Gettman M.T., Swain P. Initial experimental evaluation of wireless capsule endoscopes in the bladder: implications for capsule cystoscopy. Eur Urol. 2009; 55:1207-12. [Epub 2009 Feb 4]. [ Links ]
 Dirección para correspondencia:
Dirección para correspondencia:
jolivaencina@ono.com
(J. Oliva Encina)
Recibido 15 Marzo 2010
Aceptado 27 Marzo 2010