Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Medicina Intensiva
versión impresa ISSN 0210-5691
Med. Intensiva vol.32 no.2 mar. 2008
REVISIÓN
Monitorización de la presión tisular de oxígeno (PtiO2) en la hipoxia cerebral: aproximación diagnóstica y terapéutica
Monitoring of tissue oxygen pressure (PtiO2) in cerebral hypoxia: diagnostic and therapeutic approach
A.J. Marín-Caballos, F. Murillo-Cabezas, J.M. Domínguez-Roldan, S.R. Leal-Noval, M.D. Rincón-Ferrari, M.Á. Muñoz-Sánchez
Servicio de Cuidados Críticos y Urgencias. Hospitales Universitarios Virgen del Rocío. Sevilla. España.
Dirección para correspondencia
RESUMEN
Una de las causas principales de lesión cerebral secundaria es la hipoxia cerebral, fundamentalmente de origen isquémico. No obstante, la oxigenación tisular cerebral depende de múltiples variables fisiológicas y la hipoxia cerebral puede ser originada por una alteración de cualquiera de ellas.
Aunque han sido desarrollados varios métodos de monitorización continua de la oxigenación cerebral en pacientes neurocríticos, la medición directa y continua de la presión de oxígeno en el tejido cerebral (PtiO2) es una realidad en el manejo de pacientes neurocríticos desde los últimos años. Esta técnica destaca por su fiabilidad y valor de la información que proporciona.
En el presente artículo se expone una revisión de los aspectos más relevantes de la monitorización de la PtiO2 y se propone un protocolo para su interpretación. Este algoritmo pretende facilitar la identificación de diferentes tipos de hipoxia cerebral y la correcta elección terapéutica en el complejo proceso de toma de decisiones en pacientes neurológicos críticos en riesgo de hipoxia cerebral.
Palabras clave: hipoxia cerebral, presión tisular cerebral de oxígeno, presión de extracción de oxígeno, presión de saturación de oxígeno del 50%, neuromonitorización, pacientes neurocríticos, traumatismo craneoencefálico grave.
ABSTRACT
One of the main causes of secondary cerebral injury is cerebral hypoxia, basically of ischemic origin. However, cerebral tissue oxygenation depends on multiple physiological variables and cerebral hypoxia may be caused by an alteration of any one of them.
Although several methods of continuous cerebral oxygenation monitoring of neurocritical patients have been developed, direct and continuous measurement of the oxygen pressure in the cerebral tissue (PtiO2) has been a reality in the handling of the neurocritical patients over recent years. This technique is highlighted by its reliability and value of the information that it provides.
This present article presents a review of the most outstanding aspects of the PtiO2 monitoring and proposes a protocol for the interpretation of this monitoring technique. This algorithm attempts to facilitate the identification of the different types of different cerebral hypoxia and of the correct therapeutic choice in the complex decision making process in neurocritical patients at risk of cerebral hypoxia.
Keywords: cerebral hypoxia, cerebral tissue oxygen pressure, oxygen extraction pressure, 50% oxygen saturation pressure, neuromonitoring, neurocritical patients, severe head injury.
Introducción
Una de las causas principales de lesión cerebral secundaria, reconocida ampliamente desde hace unos treinta años, es la hipoxia cerebral, fundamentalmente de origen isquémico1. El manejo actual de la patología neurocrítica requiere el uso creciente de la denominada monitorización cerebral multiparamétrica. Este enfoque en la monitorización cerebral está destinado fundamentalmente a conocer los diversos eventos fisiopatológicos implicados en la génesis de la lesión cerebral secundaria2.
Diversos elementos participan en el estado de oxigenación del tejido cerebral. Entre los más relevantes se hallan la presión parcial de oxígeno (pO2), la concentración de hemoglobina (Hb) en sangre, la afinidad de la Hb por el oxígeno, la presión de perfusión cerebral (PPC), el estado de la microcirculación cerebral, el gradiente de difusión del oxígeno desde el capilar a la mitocondria y el grado de consumo metabólico cerebral de oxígeno (CMRO2). Las alteraciones producidas en cualquiera de los elementos participantes en esta cadena de la oxigenación tisular cerebral conllevará la posibilidad de originar hipoxia cerebral3. Dado que la monitorización continua y directa del CMRO2 no está disponible en la práctica clínica rutinaria, las técnicas que exploran la oxigenación cerebral han derivado en intentar conocer la disponibilidad de O2 en el citado órgano, la cual esencialmente resulta del balance entre transporte y consumo cerebral de oxígeno2.
Entre los métodos que exploran la hipoxia cerebral, los más accesibles para la práctica clínica son, actualmente, la saturación de la Hb en el bulbo de la vena yugular interna (SjvO2), la saturación regional de O2 (rSO2) mediante haces de luz cercanos a los infrarrojos (NIRS) y la presión tisular de oxígeno cerebral (PtiO2). Este último método, aun con las limitaciones que posteriormente se discutirán, va desplazando a los anteriores por la superior exactitud en la medida4, mayor duración de tiempo de monitorización con resultados fiables5, facilidad de inserción y mantenimiento6 y ausencia de complicaciones destacables7,8.
Uno de los inconvenientes atribuidos a la monitorización de la PtiO2, y que en cierta medida ha lastrado su desarrollo, es la necesidad de familiarizarse con la interpretación de sus resultados y, sobre todo, con la toma de decisiones terapéuticas que su información conlleva. En el presente artículo mostramos un protocolo o algoritmo para la interpretación y el manejo de la monitorización de la PtiO2.
Descripción de los tipos de hipoxia tisular
Tipos de hipoxia tisular cerebral (clasificación de Siggaard-Andersen)
Siguiendo a Siggaard-Andersen, se han caracterizado hasta 7 causas y tipos principales de hipoxia tisular3:
1. Hipoxia isquémica, por descenso del flujo sanguíneo cerebral.
2. Hipoxia por baja extracción o extractibilidad, cuya causa es la disminución de la capacidad de extracción de O2 de sangre capilar, que a su vez puede ser debida a las siguientes razones: una pO2 insuficiente (hipoxia hipoxémica); una concentración de Hb baja (hipoxia anémica); una alta afinidad de la Hb por el oxígeno (hipoxia por alta afinidad) debida a factores que desplazan la curva de disociación de la Hb a la izquierda: hipocapnia, alcalosis, hipotermia o descenso del 2-3 difosfoglicerato (2-3DPG) por hipofosforemia entre otros.
3. Hipoxia por shunt, o cortocircuito arteriovenoso.
4. Hipoxia por disperfusión, o alteración de la difusión del O2 desde el capilar a la mitocondria.
5. Hipoxia histotóxica, por tóxicos que bloquean la cadena respiratoria mitocondrial.
6. Hipoxia por desacoplamiento, por agentes que desacoplan la reducción del O2 mitocondrial de la síntesis de ATP.
7. Hipoxia hipermetabólica, por aumento del metabolismo celular.
En la práctica clínica habitual las dos causas más frecuentes de hipoxia son la hipoxia por baja extracción secundaria a hipocapnia por hiperventilación, que a su vez provoca vasoconstricción cerebral y aumento de la afinidad de la Hb por el O2, y la hipoxia isquémica debida a descenso de la PPC bien por hipertensión intracraneal, hipotensión sistémica, causas locales (vasoespasmo arterial, cono de presión intracraneal, etc.) o la suma de estas circunstancias9.
La presión de extracción de oxígeno y la presión de saturación de oxígeno del 50%
Para identificar situaciones de hipoxia por baja extracción disponemos de un índice útil que nos informa del estado de oxigenación de la sangre: la presión de extracción de oxígeno (Px)3. Este parámetro hace referencia al oxígeno extraíble de la sangre arterial que puede ser transferido a los tejidos, que depende a su vez y a efectos prácticos de la pO2, la concentración de Hb efectiva y la afinidad de la Hb por el O2. La Px se define como la presión parcial de oxígeno después de la extracción de 2,3 mmol/l de oxígeno en sangre arterial a un pH y una presión parcial de dióxido de carbono arterial (pCO2) constantes, y refleja por tanto la pO2 al final del capilar asumiendo condiciones estándar. El oxígeno extraíble en sangre arterial se considera insuficiente cuando la Px es menor de 32 mmHg, lo que puede condicionar una hipoxia por baja extracción.
La afinidad de la Hb por el O2, a su vez, puede ser cuantificada por otro índice con el que está inversamente relacionada, la presión de saturación del 50% (p50). La pO2 a la que se satura de oxígeno el 50% de la Hb define la p50. Se considera que la afinidad de la Hb por el O2 está aumentada cuando la p50 es menor de 24 mmHg.
La Px y la p50 son parámetros disponibles en algunos sistemas de oximetría o analizadores de gas, por ejemplo la serie Radiometer (Radiometer Medical® ApS, Brønshøj, Dinamarca), pero también puede calcularse conociendo los resultados de laboratorio de una analítica básica (gasometría arterial y hemograma) mediante software, desarrollado por O. Siggaard Andersen (OSA), el cual es de libre acceso en la web (www.osa.suite.dk).
Revisión de la monitorización de la presión de oxígeno tisular cerebral
Técnicas de monitorización de la oxigenación cerebral
El manejo diagnóstico y terapéutico del paciente neurocrítico ha evolucionado ampliamente en las últimas décadas. Históricamente, este manejo se focalizó en la monitorización de la presión intracraneal (PIC). La doctrina de Monro-Kellie establecía que el cráneo es un compartimento rígido con tres componentes no compresibles: tejido cerebral, volumen sanguíneo cerebral y líquido cefalorraquídeo, y que un incremento de la PIC puede originar un descenso de la PPC, lo cual conlleva isquemia cerebral y un peor pronóstico10.
Sin embargo, diversos estudios han puesto de manifiesto que la monitorización de la PIC y la PPC no es suficiente para garantizar una adecuada oxigenación cerebral11, con lo que se han desarrollado diversos modos de monitorizar la oxigenación cerebral: la SjvO2, la rSO2 por espectroscopia de infrarrojos (near-infrared spectroscopy), la PtiO2 y la microdiálisis (MD) cerebral2,8.
En la actualidad la monitorización de la PtiO2 se ha convertido en el método más útil y directo de monitorización de la oxigenación cerebral y existe alguna limitada evidencia que sugiere que el uso de una terapia basada en la monitorización de la PIC y la PtiO2 podría asociarse con mejores resultados pronósticos en pacientes con traumatismo craneoencefálico (TCE) grave12. Así pues, dado que la monitorización de la PIC y la PPC sólo nos infiere la presencia de hipoxia isquémica, y no es suficiente para diagnosticar otros tipos de hipoxia cerebral, la asociación de la PtiO2 a los sistemas de monitorización tradicionales (PIC, SjvO2) incrementa la capacidad diagnóstica en la detección de la hipoxia cerebral.
Origen de la monitorización de la presión tisular de oxígeno
La cuantificación directa de la presión de oxígeno a nivel tisular y de forma continua es posible, desde la década pasada, mediante métodos fiables y seguros de monitorización13. Aunque se han desarrollado dos sistemas de monitorización de PtiO2 comercialmente disponibles: Licox® (Integra Neuroscience, Plainsboro, NJ, EE. UU.) y Neurotrend® (Diametrics Medical, St. Paul, MN, EE. UU.), en adelante nos referiremos al primero por estar más ampliamente extendido y porque la mayoría de los estudios de PtiO2 se han realizado con este sistema.
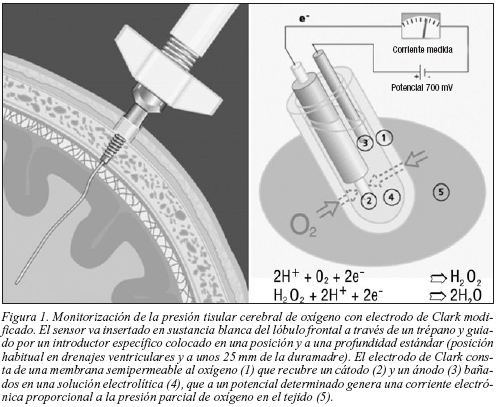
La monitorización de PtiO2 con sistema Licox® se basa en el electrodo de Clark, que fue descrito en los años cincuenta14 y que permite por el método polarográfico cuantificar la presión de oxígeno en un medio. Este electrodo consta de una membrana semipermeable al oxígeno que recubre un cátodo y un ánodo bañados en una solución electrolítica, y que puede óxido-reducir el oxígeno disuelto generando una corriente eléctrica que es proporcional a la pO2 en el medio y que se puede cuantificar (fig. 1).
A finales de los años ochenta en Alemania Fleckenstein et al desarrollan la monitorización de presión de oxígeno en parénquima cerebral en modelos experimentales animales con un electrodo de Clark modificado15.
A principios de los años noventa Meixensberger et al iniciaron la monitorización de la PtiO2 en humanos, sugiriendo que esta podría ayudar a prevenir eventos hipóxicos en pacientes neurocríticos y mejorar su pronóstico13.
Consideraciones técnicas de la monitorización de la PtiO2 con sistema Licox®
La medición de la PtiO2 en la sustancia blanca profunda se ha considerado de mayor interés porque el consumo y la PtiO2 es más estable en esta área16, así como por ser esta más sensible a la hipoxia8. Por convenio, la ubicación estándar del catéter es la misma que la del sensor de PIC, en la sustancia blanca frontal, a través de un trépano situado a 2 cm de la línea media y frente de la sutura coronal6, es decir, en territorio frontera entre la arteria cerebral anterior y media. El catéter debe ser posicionado en el área de interés: en tejido no lesionado o en área de penumbra próxima a la lesión encefálica17, evitando áreas contundidas y hemorrágicas en la tomografía axial computarizada (TAC) craneal18, ya que la medición en estas sería artefactualmente baja. La inserción del catéter se realiza a través de un trépano guiada por un introductor específico que se mantiene fijado al cráneo, hasta una profundidad predeterminada de unos 34 mm. Así pues, es necesario realizar una TAC craneal de control tras la implantación del catéter para objetivar la posición correcta del mismo y descartar posibles complicaciones relacionadas con su inserción (hematomas post-inserción)18.
También se producen mediciones artefactualmente bajas en los primeros momentos tras la inserción del catéter debido a que esta provoca un microtraumatismo con áreas de edema y microhemorragias en la interfase tejido-sensor, alrededor del canal de inserción del catéter19. Por ello, hay que esperar un periodo de tiempo de adaptación (run-in time o adaptation time)6 hasta que los cambios histológicos en la interfase tejido-sensor se autolimiten y la medición se estabilice. Este periodo de tiempo en la mayoría de las ocasiones es inferior a 120 minutos. No obstante, en un discreto porcentaje de casos puede prolongarse hasta 6 o incluso 24 horas20.
Hoy día la calibración del catéter Licox® es automática y nos viene suministrada por una tarjeta electrónica que acompaña a cada catéter y que proporciona información al sistema sobre su precalibración realizada en fábrica. Además, la introducción de la temperatura central es necesaria para que la medición de la PtiO2 sea corregida acorde al coeficiente de temperatura a razón de 4,5% por cada grado centígrado6. Así pues, la temperatura debe ser introducida, bien manualmente con ritmo horario o bien continuamente mediante un sensor de temperatura cerebral conectado al monitor Licox®.
Validez clínica de la monitorización de la PtiO2 y umbrales de hipoxia tisular
La monitorización de la pO2 a nivel tisular local ha sido validada en pacientes con TCE grave comparándola con otros métodos establecidos de monitorización de la oxigenación cerebral, como la SjvO2, donde un 50% de saturación de oxígeno es indicativo de hipoxia cerebral inminente y se corresponde con un umbral medio de PtiO2 de 8,5 mmHg4. Otros estudios clínicos muestran que son indicadores de mal pronóstico cualquier periodo de PtiO2 menor de 10 mmHg durante las primeras 24 h tras el TCE21,22, así como cualquier periodo menor de 10 mmHg durante más de 30 minutos23. Por otro lado, otros artículos han puesto de manifiesto que la probabilidad de muerte aumenta con la duración del tiempo de hipoxia tisular con una PtiO2 ≤ 15 mmHg7, y con la existencia de cualquier episodio de PtiO2 ≤ 6 mmHg24. Estudios clínicos usando tomografía por emisión de positrones (PET)15 y monitorización de la PtiO2 han confirmado que el umbral de oxigenación tisular a partir del cual aumenta la fracción de extracción de oxígeno (OEF) se sitúa por debajo de 14 mmHg25. Por tanto, en la actualidad se considera 15 mmHg el umbral de hipoxia tisular leve-moderada, 10 mmHg el de hipoxia tisular grave y 5 mmHg el de hipoxia tisular crítica.
Según las guías de práctica clínica actuales, la monitorización de la PtiO2 se considera una opción para el manejo del TCE grave y sólo la monitorización de la PIC alcanza el nivel de recomendación tipo II de las «guidelines»26.
Parámetros fisiológicos que influencian la PtiO2 y su aplicación clínica
La monitorización de la PtiO2 ha sido aplicada fundamentalmente en el manejo del TCE grave y de la hemorragia subaracnoidea espontánea de pobre grado clínico27. Otros usos han incluido la monitorización de la PtiO2 en neurocirugía de aneurismas, malformaciones arteriovenosas y resección de tumores cerebrales, en el estudio del efecto de maniobras terapéuticas tales como el aumento de la PPC, la hiperventilación, la hiperoxia normobárica, la hipotermia, la craneotomía descompresiva, el tratamiento hiperosmolar con manitol, el uso de agentes anestésicos, etc.27
Varios estudios han encontrado que la PtiO2 se puede correlacionar positivamente con una amplia gama de parámetros fisiológicos que incluyen la PPC y la presión arterial media25,28-32, el flujo sanguíneo cerebral (CBF)33, la presión parcial arterial del oxígeno (PaO2) o la fracción inspiratoria de oxígeno (FiO2)25,31,34,35, la concentración de la Hb36,37 y el comienzo de la fiebre38. Otros estudios han encontrado correlaciones inversas de la PtiO2 con la OEF25 determinada en estudios de PET, con el tiempo de tránsito medio39 del contraste a través del tejido cerebral en estudios de tomografía computarizada de perfusión, con la hiperventilación o hipocapnia40-42, y más dudosamente con la hipotermia terapéutica43,44, ya que algún estudio ha mostrado una relación directa con esta última45.
Como sugieren estos estudios, realizados entre otros por nuestro grupo, la monitorización de la PtiO2 podría ser útil en la determinación del umbral de la PPC necesario para evitar la hipoxia isquémica, ya que el riesgo de hipoxia tisular se incrementa con umbrales de PPC por debajo de 60 y 70 mmHg32 (fig. 2), así como en la decisión de transfundir concentrados de hematíes a pacientes anémicos ya que la oxigenación cerebral se incrementa de forma prolongada tras la transfusión de concentrados de hematíes en pacientes con TCE grave, con hipoxia cerebral y anemia37 (fig. 3). También podría auxiliar en la determinación del nivel de hiperventilación tolerable para el manejo de la hipertensión intracraneal.
El uso terapéutico de la hiperoxia normobárica para contrarrestar el efecto de la hipoxia cerebral está recibiendo cada vez más atención en el manejo del TCE grave. Aunque los diversos estudios coinciden en que la PtiO2 se incrementa con esta maniobra y que ello tiene ciertos efectos bioquímicos como la disminución del lactato medida en el espacio extracelular cerebral medido con MD, sin embargo existe controversia sobre si la entrega de oxígeno es mejorada sustancialmente por la hiperoxia normobárica. Puesto que el cociente lactato/piruvato, un mejor indicador del estado redox celular que el lactato solo, no se modifica con la hiperoxia en estudios de MD cerebral46, y aunque puede ser cierta la hipótesis de que el metabolismo celular mejore con la hiperoxia en situación de isquemia, diversos autores consideran que hasta la fecha no existe suficiente evidencia que soporte el beneficio clínico de la hiperoxia en pacientes con TCE grave y su uso continúa siendo controvertido47.
Limitaciones de la monitorización de la PtiO2
La monitorización de la PtiO2 tiene algunas limitaciones que deben ser tenidas en consideración:
1. La monitorización de la PtiO2, aunque se aproxima al patrón oro de la monitorización de la hipoxia cerebral a pie de cama, no es una medida absoluta de la misma. Así, por ejemplo, aunque en condiciones metabólicas normales (CMRO2 estable) un decremento de la PtiO2 por debajo de un cierto umbral es sinónimo de hipoxia cerebral, es discutible si ese mismo umbral de PtiO2 crítica es válido en condiciones metabólicas anómalas de hiper o hipometabolismo cerebral en las que el CBF acoplado al CMRO2 se modifica aunque la OEF se mantenga estable48,49. Asimismo, estaría por determinar si la hipoxia celular de origen citotóxica o por desacoplamiento provocaría un descenso de la presión de oxígeno en el intersticio tisular detectable por la monitorización de la PtiO2.
2. La medición de PtiO2 es local y solo un pequeño volumen de tejido es monitorizado (la superficie del sensor mide unos 14 mm2). La posición del sensor constituye una cuestión de vital importancia en la interpretación de la medición. Cuando se coloca en tejido en riesgo de hipoxia o área de penumbra la información que proporciona debe ser considerada puramente regional, pero cuando es posicionado en áreas aparentemente normales o con supuesta lesión difusa, la lectura de la la PtiO2 puede ser considerada un indicador de la oxigenación global27,49,50. Por ello, algunos autores preconizan colocar el sensor en el área de penumbra de una lesión focal para conocer la oxigenación tisular a este nivel y simultanear su registro con una medida de la oxigenación cerebral global como la SjvO2. Sin embargo, otros muchos utilizan en la actualidad la monitorización de la PtiO2 en tejido sano como exponente del efecto que las distintas causas de hipoxia tisular pueden tener sobre la globalidad del encéfalo27,49,50.
3. Aunque existe evidencia que sugiere mejores resultados en el manejo del TCE grave utilizando la monitorización de la PtiO2, esta es limitada por tratarse de un único estudio con un reducido número de pacientes en el que obtienen menor mortalidad en un grupo con tratamiento de TCE grave protocolizado para mantener una PtiO2 > 25 mmHg con respecto a un grupo control histórico12. Hasta la fecha no se han realizado estudios de alto nivel de evidencia, randomizados controlados, que demuestren el beneficio clínico de la terapia guiada por PtiO2 en TCE grave ni otra patología neurocrítica.
4. Es una técnica de monitorización invasiva que precisa de la intervención de Neurocirugía para la inserción del catéter de PtiO2 junto con el de PIC, lo cual limita su aplicabilidad en situaciones de coagulopatía, por ejemplo, y tiene un coste económico relativamente superior cuando se ha comparado con un sistema de monitorización de PIC acoplado a fluido intraventricular, pero no si se la compara con cualquier sensor de PIC de fibra óptica intraparenquimatoso.
Protocolo de actuación ante una PtiO2 baja
Ante una medición de PtiO2 inicial baja (PtiO2 ≤ 15 mmHg)7,24 tras la inserción del sensor, debemos plantearnos una serie de cuestiones (fig. 4):
¿Es la medición de PtiO2 inicial real o artefactual?
Aunque una medida de PtiO2 inicial puede ser baja debido a la existencia de una fase de hipoperfusión cerebral en las primeras horas tras el TCE grave51, es preciso descartar que la medición de la PtiO2 sea artefactualmente baja tras la inserción del sensor de PtiO2 (fig. 4). Para ello debemos verificar lo siguiente:
¿Es la ubicación del catéter de PtiO2 correcta?
El sensor de PtiO2, a pesar de su pequeño diámetro (0,5 mm), es visible en la TAC craneal. La ubicación del catéter se considera correcta cuando es similar a la del drenaje ventricular6,8: en la sustancia blanca del lóbulo frontal en territorio frontera entre la arteria cerebral media y la cerebral anterior en tejido sano, evitando focos contusivos18 (hipodensos/hiperdensos en la TAC de cráneo). En un discreto porcentaje de casos (≈ 2%) puede producirse un pequeño hematoma (< 2 cc de volumen) alrededor del sensor, que es visible en la TAC craneal7,8,18 y que no tiene relevancia clínica, aunque sí artefactúa la medida de PtiO2.
¿Se ha completado el periodo de adaptación?
Es preciso esperar el tiempo suficiente hasta que la medición de PtiO2 se estabilice y sea mayor de 10 mmHg, pues tras la inserción del catéter se produce un microtraumatismo en la interfase entre el sensor y el tejido19 que provoca una medida inicial artefactualmente baja, que se resuelve con el tiempo en cuestión de horas, periodo que se conoce como «run-in time». Habitualmente es suficiente con esperar unas 2 h6, aunque a veces se precisan hasta 12-24 h20.
¿Existe malfunción del sensor de PtiO2?
Si a pesar de lo expuesto la medición de PtiO2 continúa baja, es preciso descartar malfunción del sensor realizando una prueba de hiperoxia18: al administrar una FiO2 del 100% con el respirador debe producirse un incremento rápido y notable de la PtiO2. Si ello no ocurre habrá que pensar en un malfuncionamiento del sensor, debido a su rotura o a la existencia de un microhematoma en la interfase sensor-tejido, no visible en la TAC, que artefactúe la medida, lo que ocurre en un mínimo porcentaje de casos (< 1%).
¿Se trata de una hipoxia por baja extracción de oxígeno?
El siguiente paso es verificar el estado de oxigenación de la sangre extrayendo una muestra de sangre arterial y determinar la Px. Si la Px es insuficiente (Px < 32 mmHg) estaremos ante una hipoxia por baja extracción o extractibilidad7,8, que puede ser corregida mejorando el estado de oxigenación de la sangre. Para ello habrá que determinar la causa que la origina, que puede ser triple (fig. 4):
¿Hipoxia hipoxémica?
Si PaO2 < 75 mmHg (hipoxemia), optimizar la oxigenación mediante estrategias ventilatorias (↑ FiO2, reclutamiento alveolar si procede, etc.).
¿Hipoxia por alta afinidad?
Cuando la afinidad de la Hb por el O2 es excesiva, la p50 está disminuida (p50 < 24 mmHg), entonces es preciso verificar variables que desplazan la curva de disociación de la Hb a la izquierda:
1. Si hipocapnia (pCO2 < 35 mmHg) o alcalosis respiratoria: normalizar los parámetros de ventilación mecánica (normoventilar).
2. Si alcalosis metabólica (pH > 7,45): tratar la causa subyacente (pérdidas intestinales, abuso de diuréticos, deshidratación, exceso de bicarbonato secundario a aumento de reabsorción por hipocaliemia o a ingesta de alcalinos) y realizar expansión de volumen con ClNa y ClK.
3. Si hipofosforemia (fósforo < 2,5 mEq/l): administrar fosfato en perfusión para evitar déficit de 2-3 DPG.
4. Si hipotermia no terapéutica (Tª < 36,5 ºC): inducir normotermia con medidas físicas.
¿Hipoxia anémica?
En pacientes neurocríticos con hipoxia y anemia, la transfusión de concentrados de hematíes puede incrementar de forma prolongada la oxigenación tisular cerebral (fig. 3)28. Si Hb < 9-10 g/dl o hematocrito < 30%: transfundir concentrados de hematíes.
¿Se trata de una hipoxia tisular de tipo isquémico?
A continuación, si la Px indica un aceptable estado de oxigenación de la sangre (Px > 32 mmHg) la causa más frecuente de hipoxia es la isquémica. Para ello valorar las diferentes causas de hipoxia isquémica3,8 (fig. 4).
¿Hipertensión intracraneal?
Si la PIC es inapropiada (> 20 mmHg): realizar medidas para controlar la hipertensión intracraneal según protocolos de la Brain Trauma Foundation26.
¿Presión de perfusión cerebral insuficiente?
Si la PPC es menor de 60-70 mmHg, considerar que puede ser insuficiente (fig. 2)32 y que al aumentar la PPC puede incrementarse la PtiO2.
¿Flujo sanguíneo cerebral comprometido?
Mediante sonografía doppler transcraneal (DTC) se puede estimar el flujo sanguíneo en las principales arterias cerebrales según el patrón de velocidades que sigue52. Si el patrón DTC es de alta resistencia o vasoespasmo de arteria tributaria del territorio que monitorizamos: valorar medidas para mejorar la perfusión cerebral (hipervolemia, hipertensión inducida, angioplastia, etc.).
¿Se trata de una hipoxia tisular de otro origen?
Por último, en ausencia de hipoxia isquémica e hipoxia por baja extractibilidad, considerar que aunque menos frecuentes y de más difícil confirmación diagnóstica, pueden existir otras posibles causas de hipoxia3,8 (fig. 4):
¿Hipoxia por shunt arteriovenoso?
Se sospechará shunt arteriovenoso en situación de síndrome de respuesta inflamatoria sistémica (SIRS) secundario al propio traumatismo, situaciones de sepsis, etc.: realizar tratamiento específico y control del SIRS.
¿Hipoxia por disperfusión?
El gradiente de difusión del O2 se verá afectado en situación de edema cerebral al incrementarse la distancia entre el capilar sanguíneo y la mitocondria: evitar causas de edema vasogénico y citotóxico.
¿Hipoxia hipermetabólica?
Ocurre cuando se produce un incremento de las necesidades metabólicas, por ejemplo crisis epilépticas o fiebre: profilaxis y tratamiento de la epilepsia y control de hipertermia.
Y considerar si podría ocurrir hipoxia celular con PtiO2 en rango de normoxia está por determinar, aunque estas causas de hipoxia son muy raras.
¿Hipoxia histotóxica?
Se produce inhibición de la cadena respiratoria mitocondrial tras afectación de citocromos por tóxicos.
¿Hipoxia por desacoplamiento?
Sucede por desacoplamiento entre la reducción de O2 y la síntesis de ATP mitocondrial.
La monitorización de la PtiO2 ha representado un hito en el desarrollo de la neuromonitorización, ya que permite conocer el estado de la oxigenación tisular cerebral de forma continua, en tiempo real y a la cabecera del enfermo. Como cualquier método de monitorización presenta ventajas, inconvenientes y limitaciones. Entre las ventajas destacaríamos:
1. Fácil manejo y mantenimiento de la técnica6.
2. Ausencia de complicaciones relevantes relacionadas con la inserción7,8.
3. Exactitud y fiabilidad de la medida en el transcurso de los días4,5.
4. Capacidad para detectar todos los tipos de hipoxia tisular cerebral (con teórica excepción de las causadas por agentes que bloquean o desacoplan la cadena respiratoria mitocondrial)3,8.
5. Quizá pueda mejorar el pronóstico funcional de los pacientes neurocríticos12.
Una medida de la PtiO2 baja no es sinónimo de isquemia y requiere interpretación de la misma en un contexto de monitorización multiparamétrica (mediante TAC craneales seriadas, monitorización de PIC/PPC, de velocidad de flujo sanguíneo cerebral con DTC, y variables fisiológicas que influyen en la capacidad de transporte de oxígeno de la sangre a los tejidos) para su correcto enfoque terapéutico. Así pues, es necesario el conocimiento de la causa fisiopatológica que origina una situación de hipoxia tisular detectada mediante monitorización de PtiO2 para su apropiada corrección.
Teniendo en cuenta que la fisiopatología de la hipoxia cerebral puede ser múltiple y de cierta complejidad, consideramos que el algoritmo que se propone puede ser una herramienta útil para el diagnóstico y tratamiento de la hipoxia tisular cerebral en la práctica asistencial cotidiana. A nuestro juicio, el algoritmo tiene el interés de integrar todos los elementos que intervienen en la cinética de la oxigenación cerebral, tanto los que dependen de la dinámica intracraneal como los de origen sistémico, y examina paso a paso el estado de cada uno de los factores que pueden alterar la oxigenación cerebral, según su importancia y frecuencia de aparición. Ello facilita tomar la decisión terapéutica más correcta y ajustada al estado de oxigenación cerebral del paciente.
Aunque la Px es un concepto probablemente poco conocido y que ha sido escasamente utilizado en la literatura médica, consideramos que tiene interés para el diagnóstico de la hipoxia tisular cerebral por baja extracción de oxígeno, que es una de las causas más frecuentes de hipoxia. El propósito de la Px es conocer si un cierto grado de hipoxemia, anemia o de alta afinidad de la Hb por el oxígeno sería tolerable sin que se comprometa una entrega estándar de oxígeno a los tejidos, sabiendo que un decremento de cualquiera de estas tres variables, pO2, Hb efectiva o afinidad de la Hb por el O2, podría estar compensada por un aumento de cualquiera de las otras dos. Así, por ejemplo, en un supuesto de PtiO2 baja con Px normal y con un cierto grado de anemia no sería necesario transfundir porque la disminución de la Hb efectiva estaría compensada por una pO2 y una afinidad de la Hb adecuadas, por lo que la cesión de oxígeno de la sangre a los tejidos no estaría comprometida y la causa de la hipoxia tisular sería otra. Una vez descartadas la hipoxia isquémica y de baja extractibilidad, que son relativamente factibles de corregir, debemos considerar que existen otras causas de hipoxia que si bien no podemos diagnosticar con certeza, sí podemos sospecharlas por la situación clínica.
Puede imputársele a este algoritmo cierta dificultad de aplicación dada la necesidad de calcular la Px y de disponer de DTC para el diagnóstico de hipoperfusión cerebral o vasoespasmo. No obstante, la Px es suministrada por muchos gasómetros existentes en Unidades de Cuidados Intensivos (UCI) o puede calcularse fácilmente a partir de una analítica básica mediante un programa informático de dominio público en la red (www.osa.suite.dk), como previamente se ha referido. Igualmente, el DTC es una tecnología de amplia difusión, y que probablemente haya sido incorporada con anterioridad a la introducción de la monitorización de la PtiO2 en la mayoría de las Unidades de Cuidados Neurocríticos.
El algoritmo de actuación que se propone ante una PtiO2 baja está basado en la bibliografía referenciada y es el que se emplea desde hace años como protocolo clínico en la UCI de Neurocríticos de nuestro centro para el manejo de pacientes con monitorización multiparamétrica.
En conclusión, consideramos que el presente algoritmo de actuación para el manejo diagnóstico y terapéutico de la hipoxia cerebral puede servir de guía para facilitar la interpretación de la monitorización de la PtiO2 y su corrección cuando los valores se aparten de la normalidad.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Bibliografía
1. Graham DI, Adams JH, Doyle D. Ischaemic brain damage in fatal non missile head injuries. J Neurol Sci. 1978;39:213-34. [ Links ]
2. Kett-Whitte R, Hutchinson PJ, Czosnyka M, Boniface S, Pickard JD, Kirkpatrick PJ. Multimodal monitoring of acute brain injury. Adv Tech Stand Neurosurg. 2002;27:87-134. [ Links ]
3. Siggaard-Andersen O, Gothgen IH, Fogh-Andersen N, Larsen LH. Oxygen status of arterial and mixed venous blood. Crit Care Med. 1995;23:1284-93. [ Links ]
4. Kiening KL, Unterberg AW, Bardt TF, Schneider GH, Lanksch WR. Monitoring of cerebral oxygenation in patients with severe head injuries: brain tissue pO2 versus jugular vein oxygen saturation. J Neurosurg. 1996;85:751-7. [ Links ]
5. Sarrafzadeh AS, Unterberg AW, Kiening KL, Bardt TF, Schneider GH, Lanksch WR. Monitoring of cerebral oxygenation in traumatic brain injured patients. En: Bauer BL, Kuhn TJ, editors. Severe head injuries. Berlin: Springer Verlag; 1997. p. 109-20. [ Links ]
6. Dings J, Meixensberger J, Roosen K. Brain tissue pO2-monitoring: catheter stability and complications. J Neurological Res. 1997;19:241-5. [ Links ]
7. Van den Brink WA, van Santbrink H, Steyerberg EW, Avezaat CJ, Suazo JA, Hogesteeger C, et al. Brain oxygen tension in severe head injury. Neurosurgery. 2000,46:868-78. [ Links ]
8. Poca MA, Sahuquillo J, Mena MP, Vilalta A, Riveiro M. Actualizaciones en los métodos de monitorización cerebral regional en los pacientes neurocríticos: presión tisular de oxígeno, microdiálisis cerebral y técnicas de espectroscopia por infrarrojos. Neurocirugía. 2005;16:385-410. [ Links ]
9. Kiening KL, Härtl R, Unterberg AW, Schneider GH, Bardt T, Lanksch WR. Brain tissue pO2-monitoring in comatose patients: implications for therapy. J Neurological Res. 1997;19:233-40. [ Links ]
10. Miller JD. Head injury and brain ischemia--implications for therapy. Br J Anaesth. 1985;57:120-30. [ Links ]
11. Cruz J, Jaggi JL, Hofftad OJ. The first decade of continuous monitoring of jugular bulb oxyhemoglobin saturation: management strategies and clinical outcome. Crit Care Med. 1998;26: 344-51. [ Links ]
12. Stiefel MJ, Spiotta AJ, Gracias VH, Garruffe AM, Guillamondegui O, Maloney-Wilensky E, et al. Reduced mortality rate in patients with severe traumatic brain injury treated with brain tissue oxygen monitoring. J Neurosurg. 2005;103:805-11. [ Links ]
13. Meixensberger J, Dings J, Kuhnigk H, Roosen K. Studies of tissue pO2 in normal and pathological human brain cortex. Acta Neurochir Suppl (Wien). 1993;59:58-63. [ Links ]
14. Clark LC. Monitor and control of blood and tissue oxygen tensions. Trans Am Soc Artif Int Org. 1956;2:41-5. [ Links ]
15. Fleckenstein W, Nowak G, Kehler U, Maas AER, Dellbrügge HJ, Yong DAD, et al. Oxygen pressure measurements in cerebrospinal fluid. Medizintechnik. 1990;110:44-53. [ Links ]
16. Maas AIR, Fleckenstein W, de Jong DA, van Santbrink H. Monitoring cerebral oxygenation: experimental studies and preliminary results of continuous monitoring of cerebrospinal fluid and brain tissue oxygen tension. Acta Neurochir Suppl (Wien). 1993;59:50-7. [ Links ]
17. Sarrafzadeh AS, Kiening KL, Bardt TF, Schneider GH, Unterberg AW, Lanksch WR. Cerebral oxygenation in contusioned vs. nonlesioned brain tissue: monitoring of PtiO2 with LICOX and Paratrend. Acta Neurochir Suppl 1998;71:186-9. [ Links ]
18. Dings J, Meixensberger J, Jäger A, Roosen K. Clinical experience with 118 brain tissue oxygen partial pressure catheter probes. Neurosurgery. 1998;43:1082-95. [ Links ]
19. Van den Brink WA. Brain parenchyma-pbrO2 catheter interface, a histopathological study in the rat. En: van den Brink WA, editor. Head injury, from man to model. Delft, NL: Eburon Publishers; 2000. p. 125-43. [ Links ]
20. Gopinath SP, Valadka AB, Uzura M, Robertson CS. Comparison of jugular venous oxygen saturation and brain tissue pO2 as monitors of cerebral ischemia after head injury. Crit Care Med. 1999;27:2337-45. [ Links ]
21. Van Santbrink H, Maas AIR, Avezaat CJ. Continuous monitoring of partial pressure of brain tissue oxygen in patients with severe head injury. Neurosurgery. 1996;38:21-31. [ Links ]
22. Dings J, Jäger A, Meixensberger J, Roosen K. Brain tissue pO2 and outcome after severe head injury. Neurological Res. 1998;20:71-5. [ Links ]
23. Bardt TF, Unterberg AW, Härtl R, Kiening KL, Schneider G-H, Lanksch WR. Monitoring of brain tissue pO2 in traumatic brain injury: effect of cerebral hypoxia on outcome. Acta Neurochir. 1998;Suppl 71:153-6. [ Links ]
24. Valadka AB, Gopinath SP, Contant ChF, Uzura M, Robertson CS. Relationship of brain tissue pO2 to outcome after severe head injury. Crit Care Med. 1998;26:1576-81. [ Links ]
25. Johnston AJ, Steiner LA, Coles JP, Chatfield DA, Fryer TD, Smielewski P, et al. Effect of cerebral perfusion pressure augmentation on regional oxygenation and metabolism after head injury. Crit Care Med. 2005;33:189-95. [ Links ]
26. The Brain Trauma Foundation, The American Association of Neurological Surgeons, The Joint Section on Neurotrauma and Critical Care. Guidelines for the Management of Severe Traumatic Brain Injury. 3rd edition. J Neurotrauma. 2007;24:S1-S106. [ Links ]
27. Nortje J, Gupta AK. The role of tissue oxygen monitoring in patients with acute brain injury. Br J Anaesth. 2006;97:95-106. [ Links ]
28. Johnston AJ, Steiner LA, Chatfield DA, Coles JP, Hutchinson PJ, Al-Rawi PG, et al. Effect of cerebral perfusion pressure augmentation with dopamine and norepinephrine on global and focal brain oxygenation after traumatic brain injury. Intensive Care Med. 2004;30:791-7. [ Links ]
29. Lang EW, Czosnyka M, Mehdorn HM. Tissue oxygen reactivity and cerebral autoregulation after severe traumatic brain injury. Crit Care Med. 2003;31:267-71. [ Links ]
30. Menzel M, Soukup J, Henze D, Clausen T, Marx T, Hillman A, et al. Brain tissue oxygen monitoring for assessment of autoregulation: preliminary results suggest a new hypothesis. J Neurosurg Anesthesiol. 2003;15:33-41. [ Links ]
31. Reinert M, Barth A, Rothen HU, Schaller B, Takala J, Seiler RW. Effects of cerebral perfusion pressure and increased fraction of inspired oxygen on brain tissue oxygen, lactate, and glucose in patients with severe head injury. Acta Neurochir (Wien). 2003; 145:341-9. [ Links ]
32. Marín-Caballos AJ, Murillo-Cabezas F, Cayuela-Domínguez A, Domínguez-Roldán JM, Rincon-Ferrari MD, Valencia-Anguita J, et al. Cerebral perfusion pressure and risk of brain hypoxia in severe head injury: a prospective observational study. Crit Care. 2005;9:R670-6. [ Links ]
33. Jaeger M, Soehle M, Schuhmann MU, Winkler D, Meixensberger J. Correlation of continuously monitored regional cerebral blood flow and brain tissue oxygen. Acta Neurochir (Wien). 2005; 147:51-6. [ Links ]
34. McLeod AD, Igielman F, Elwell C, Cope M, Smith M. Measuring cerebral oxygenation during normobaric hyperoxia: a comparison of tissue microprobes, near-infrared spectroscopy, and jugular venous oximetry in head injury. Anesth Analg. 2003;97: 851-6. [ Links ]
35. Reinprecht A, Greher M, Wolfsberger S, Dietrich W, Illievich UM, Gruber A. Prone position in subarachnoid hemorrhage patients with acute respiratory distress syndrome: effects on cerebral tissue oxygenation and intracranial pressure. Crit Care Med. 2003;31:1831-8. [ Links ]
36. Smith MJ, Stiefel MF, Magge S, Frangos S, Bloom S, Gracias V, et al. Packed red blood cell transfusion increases local cerebral oxygenation. Crit Care Med. 2005;33:1104-8. [ Links ]
37. Leal-Noval SR, Rincon-Ferrari MD, Marín-Niebla A, Cayuela A, Arellano-Orden V, Marin-Caballos A, et al. Transfusion of erythrocyte concentrates produces a variable increment on cerebral oxygenation in patients with severe traumatic brain injury: A preliminary study. Intensive Care Med. 2006;32: 1733-40. [ Links ]
38. Stocchetti N, Protti A, Lattuada M, Magnoni S, Longhi L, Ghisoni L, et al. Impact of pyrexia on neurochemistry and cerebral oxygenation after acute brain injury. J Neurol Neurosurg Psychiatry. 2005;76:1135-9. [ Links ]
39. Hemphill JC, Smith WS, Sonne DC, Morabito D, Manley GT. Relationship between brain tissue oxygen tension and CT perfusion: feasibility and initial results. AJNR Am J Neuroradiol. 2005;26:1095-100. [ Links ]
40. Carmona Suazo JA, Maas AI, van den Brink WA, van Santbrink H, Steyerberg EW, Avezaat CJ. CO2 reactivity and brain oxygen pressure monitoring in severe head injury. Crit Care Med. 2000;28:3268-74. [ Links ]
41. Clausen T, Scharf A, Menzel M, Soukup J, Holz C, Rieger A, et al. Influence of moderate and profound hyperventilation on cerebral blood flow, oxygenation and metabolism. Brain Res. 2004;1019:113-23. [ Links ]
42. Hemphill JC, Knudson MM, Derugin N, Morabito D, Manley GT. Carbon dioxide reactivity and pressure autoregulation of brain tissue oxygen. Neurosurgery. 2001;48:377-83. [ Links ]
43. Soukup J, Zauner A, Doppenberg EM, Menzel M, Gilman C, Bullock R, et al. Relationship between brain temperature, brain chemistry and oxygen delivery after severe human head injury: the effect of mild hypothermia. Neurol Res. 2002;24:161-8. [ Links ]
44. Gupta AK, Al-Rawi PG, Hutchinson PJ, Kirkpatrick PJ. Effect of hypothermia on brain tissue oxygenation in patients with severe head injury. Br J Anaesth. 2002;88:188-92. [ Links ]
45. Zhi D, Zhang S, Lin X. Study on therapeutic mechanism and clinical effect of mild hypothermia in patients with severe head injury. Surg Neurol. 2003;59:381-5. [ Links ]
46. Magnoni S, Ghisoni L, Locatelli M, Caimi M, Colombo A, Valeriani V, et al. Lack of improvement in cerebral metabolism after hyperoxia in severe head injury: a microdialysis study. J Neurosurg. 2003;98:952-8. [ Links ]
47. Longhi L, Stocchetti N. Hyperoxia in head injury: therapeutic tool? Curr Opin Crit Care. 2004;10:105-9. [ Links ]
48. Coles JP. Regional ischemia after head injury. Curr Opin Crit Care. 2004;10:120-5. [ Links ]
49. Rosea JC, Neill TA, Hemphill JC. Continuous monitoring of the microcirculation in neurocritical care: an update on brain tissue oxygenation. Curr Opin Crit Care. 2006;12:97-102. [ Links ]
50. Sarrafzadeh AS, Kiening KL, Unterberg AW. Neuromonitoring: brain oxygenation and microdialysis. Curr Neurol Neurosci Rep. 2003;3:517-23. [ Links ]
51. Martín NA, Patwardhan RV, Alexander MJ, Africk CZ, Lee JH, Shalmon E, et al. Characterization of cerebral hemodynamic phases following severe head trauma: Hypoperfusion, hyperemia and vasospam. J Neurosurg. 1997;87:9-19. [ Links ]
52. Murillo-Cabezas F, Arteta-Arteta D, Flores Cordero JC, Muñoz-Sánchez MA, Rincón Ferrari MD, Rivera Fernández MV, et al. Utilidad del Doppler transcraneal en la fase aguda del traumatismo craneoencefálico. Neurocirugía (Astur). 2002;13:196-208. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dr. A.J. Marín-Caballos.
C/ Burdeos, 34.
41012 Sevilla. España.
Correo electrónico: antmarin@terra.es
Manuscrito aceptado el 8-VI-2007.