Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Medicina Intensiva
versión impresa ISSN 0210-5691
Med. Intensiva vol.35 no.9 dic. 2011
Escalas predictivas de transfusión masiva en trauma. Experiencia de un registro de transfusiones
Massive transfusion predictive scores in trauma. Experience of a transfusion registry
M. Chico-Fernández, C. García-Fuentes, M.A. Alonso-Fernández, D. Toral-Vázquez, S. Bermejo-Aznarez y E. Alted-López
Unidad de Cuidados Intensivos de Trauma y Emergencias, Servicio de Medicina Intensiva, Hospital Universitario 12 de Octubre, Madrid, España
Dirección para correspondencia
RESUMEN
Objetivo: Valorar la utilidad de diferentes escalas previamente descritas, en la predicción de transfusión masiva (TM) con un registro de transfusiones en trauma grave.
Diseño: Estudio retrospectivo de cohortes.
Ámbito: Unidad de Cuidados Intensivos de Trauma de un hospital terciario.
Pacientes: Se incluyeron pacientes adultos con trauma grave (Injury Severity Score >15), admitidos desde octubre de 2006 hasta julio de 2009.
Intervención: Ninguna.
Variables: Se evaluaron las siguientes escalas y puntos de corte (PC): Trauma Associated Severe Haemorrhage (TASH) PC: >16 y >18; Assessment Blood Consumption (ABC) PC: >2 y Emergency Transfusion Score (ETS) PC: >3, >4 y >6. TM fue definida como la transfusión de 10 o más unidades de concentrados de hematíes (CH) en las primeras 24 horas del ingreso. Estudiamos la sensibilidad (S), especificidad (E), valor predictivo positivo y negativo (VPP y VPN), razones de verosimilitud positiva y negativa (RVP y RVN) y las curvas receiver-operating characteristics (ROC) y el área bajo las mismas (AUROC).
Resultados: Se estudiaron 568 pacientes, el 77,6% hombres, con una edad media de 41,16±18 años e ISS de 30±13. El 93,8% con trauma cerrado. La frecuencia global de TM fue del 18,8%. La mejor S se obtuvo para el ETS>3 y la mejor especificidad con el TASH>18. El AUROC para los diferentes escalas fue: ABC: 0,779, ETS: 0,784 y el TASH: 0,889.
Conclusiones: Estas escalas pueden ser útiles para caracterizar la población con TM, la exclusión de población de bajo riesgo, intentar ser objetivos en la resucitación con control de daños y apoyar las decisiones clínicas, con pocos datos y fáciles de obtener.
Palabras clave: Transfusión masiva. Trauma. Lesión. Escalas. Unidad de Cuidados Intensivos.
ABSTRACT
Objectives: Our purpose is to validate previously described massive transfusion (MT) scoring in our Transfusion Trauma Registry.
Design: A retrospective cohort of adult trauma patients.
Setting: Trauma and Emergency Intensive Care Unit of a tertiary hospital.
Patients: Patients with severe trauma (injury severity score>15) admitted from October 2006 to July 2009.
Interventions: None.
Variables: The following MT scoring and cutoff points (CP) were evaluated: Trauma-Associated Severe Hemorrhage (TASH) CP: >16 and >18; Assessment Blood Consumption (ABC) CP: >2 and Emergency Transfusion Score (ETS) CP: >3, >4, >6. MT was defined as the transfusion of 10 units or more of packed red blood cells in the first 24hours. We studied the sensivity (S), specifity (SP), and positive and negative predictive values (PPV, NPV), the positive and negative likehood ratios (LHR +, LHR-) and area under the receiver operating characteristic curve (ROC).
Results: A total of 568 patients were available for analysis; 77.6% were men, with a mean age of 41.16±18 years and an ISS of 30±13. 93.8% with blunt trauma. The overall MT rate was 18.8%. The best S was obtained with ETS >3 and best SP was obtained with TASH >18. ROC for different scores was: ABC: 0.779, ETS: 0. 784, TASH: 0.889.
Conclusion: These scales can be useful for characterizing the TM population, for excluding low-risk populations, and for attempting to be objective in hematological damage control and in supporting clinical decisions, based on fe1w and easily obtainable data.
Key words: Massive transfusion. Trauma. Injury. Scores. Intensive Care Unit.
Introducción
El trauma es una importante causa de muerte en la población con edades comprendidas entre 1 y 44 años1 y contribuye hasta en el 10% a la mortalidad global2. La hemorragia en el trauma grave causada por una combinación de sangrado quirúrgico y coagulopático, es la causa más frecuente de mortalidad precoz3 y la segunda causa global de muerte en trauma4. Los nuevos conocimientos en la fisiopatología de la coagulopatía asociada al trauma y las experiencias militares en escenarios internacionales5 han generado un cambio estratégico en la resucitación del paciente traumatizado, denominado resucitación con control de daños que requiere la administración precoz y agresiva de hemoderivados (concentrados de hematíes, plasma fresco congelado, plaquetas y fibrinógeno)6.
Dentro de esta estrategia global se encuentra el desarrollo de protocolos de transfusión masiva (PTM). Para la logística y desarrollo de los PTM, uno de los puntos de mayor dificultad y controversia reside en los criterios de activación de los mismos, y a pesar de la proliferación de estos, muy pocos tienen una política de inicio estandarizada7. El retraso en el tratamiento y error en el juicio en la toma de decisiones son causas de mortalidad durante la atención inicial8. De manera especial para la identificación de aquellos pacientes que necesitan transfusión masiva (TM) y esto ha sido reconocido hace tiempo en la medicina militar9-13. Para este fin se han desarrollado diferentes escalas que combinan un amplia gama de variables en diferentes ámbitos (civil, militar, etc.)14. Nos proponemos evaluar diferentes escalas de activación de TM en una UCI de Trauma y Emergencias de un hospital terciario.
Pacientes y métodos
Se planteó la realización de un estudio retrospectivo de cohortes para la validación de 3 escalas predictoras de TM, basado en nuestro registro de trauma y en el registro de transfusión de la unidad. Estos registros cumplen los criterios de confidencialidad exigidos en nuestro hospital, son anónimos y se encuentran encriptados. En este último se registran de manera prospectiva todas las transfusiones de hemoderivados, los resultados analíticos antes y después de cada indicación de transfusión, una aproximación a los costes, complicaciones y el uso de fármacos relacionados con la hemostasia.
En el estudio se incluyeron los pacientes mayores de 15 años con trauma grave definido como Injury Severity Score (ISS) >1515, ingresados en nuestra UCI de Trauma y Emergencias de 9 camas de un hospital terciario que atiende población traumática grave del medio urbano y rural, entre octubre de 2006 y julio de 2009. Fueron excluidos los enfermos que fueron considerados cadáver al ingreso y aquellos que rechazaron la transfusión de hemoderivados. La atención inicial al trauma se realiza por un equipo de atención especializado en la atención inicial al trauma, constituido por dos médicos intensivistas (adjunto y residente), 2 enfermeras asistenciales más una tercera de registro, auxiliares, celadores e integrando las diferentes especialidades consultoras relacionadas con la asistencia a estos enfermos y siguiendo esquemas de atención de aceptación internacional como el Advanced Trauma Life Support (ATLS®).
El hospital dispone de un PTM aprobado por la Comisión de Transfusiones y la dirección del hospital y que puede ser consultado en la página web del hospital (www.h12o.es).
Se decidió utilizar como escalas de predicción de TM por su posibilidad de aplicación en nuestro ámbito las siguientes escalas:
1) Assessment of Blood Consumption (ABC)16,17, que maneja asignando un valor de 0 o 1 a la presencia de trauma penetrante, eco abdominal dirigido a la valoración del trauma positivo (FAST), tensión arterial sistólica (TAS) <90mm Hg y frecuencia cardíaca (FC) >120 lpm (estos dos últimos a la llegada).
2) El Emergency Transfusion Score (ETS)18,19 que maneja TAS <90mm Hg, FAST positivo, inestabilidad clínica de la pelvis, edad, admisión desde la escena, mecanismo de lesión (accidente de tráfico o caída de más de 3 metros).
3) El Trauma Associated Severe Haemorrhage (TASH) valora siete variables independientes correlacionadas con un aumento de probabilidad para TM y con diferente ponderación: TAS, hemoglobina (hgb), presencia de fluido intraabdominal, fracturas de huesos largos o pélvicas complejas, FC, exceso de base <10 o género varón20-23.
Para cada escala concreta se valoraron diferentes puntos de corte (PC):
Se definió como TM la administración de > 10 de concentrados de hematíes (CH) en las primeras 24 horas tras el trauma, como es habitual en la literatura que compara estas escalas16-23.
Se calcularon para cada escala y diferente PC la sensibilidad (S), especificidad (E), valor predictivo positivo (VPP), valor predictivo negativo (VPN), razón de verosimilitud positiva (RVP) y razón de verosimilitud negativa (RVN). El uso de herramientas como el normograma de Fagan permite, mediante la combinación de la probabilidad pre-test y la RVP+, el cálculo para un determinado punto de corte estimar la probabilidad post-test de requerir TM.
Se utilizó la probabilidad pre-test (incidencia en la serie) y la RVP para el cálculo de la probabilidad post-test en el normograma de Fagan para las escalas y PC que podían ser de mayor utilidad, con el objetivo de su posible aplicación a un paciente en concreto, siguiendo las posibles combinaciones para buscar el PC más bajo que fuera capaz de predecir la TM24.
Asimismo se obtuvieron las curvas ROC (como representación gráfica de la capacidad discriminativa de una determinada escala a partir de todos sus puntos de corte) y se calcularon las áreas bajo la curva receiver-operating characteristics (AUROC) para las escalas y PC que podían ser de mayor utilidad con intervalos de confianza al 95%25,26.
Se realizó estadística inferencial de comparación de estas áreas con el test de la Chi-cuadrado con nivel de significación estadística (p<0,05), Se utilizó el paquete estadístico SSPS 15.0®.
Resultados
Se estudiaron 568 pacientes con una edad media de 41±18 años. Hubo un predominio del sexo masculino (77,6% hombres) y del trauma cerrado (93,8%). La serie tuvo un ISS elevado con una media: 30±13. Requirieron algún tipo de hemoderivado el 52,9% de los pacientes y TM un 18,8% de los enfermos. El volumen medio de CH transfundidos fue de 2.692±2.793 cc en la población completa y de 4.925±3.055 cc en los pacientes con TM.
Las cifras de S, E, VPP, VPN, RVP y RVN para cada escala y PC se resumen en la Tabla 1. Las curvas ROC y las AUROC se resumen en la Figura 1. Se realizó una comparación con el test de la Chi-cuadrado entre las escalas ABC y ETS sin que se encontraran diferencias significativas. Sí que se encontraron diferencias muy significativas entre la escala TASH frente a los otros dos (ABC y ETS) (p<0,00001).
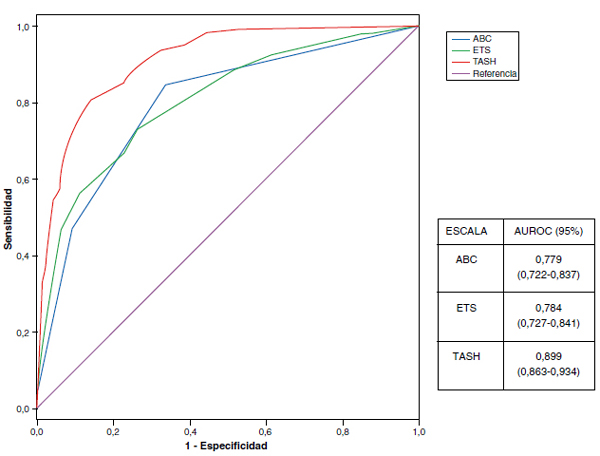
Figura 1. Curvas ROC y AUROC para las diferentes escalas.
ABC: Assessment Blood Consumption; ETS: Emergency
Transfusion Score; TASH: Trauma Associated
Severe Haemorrhage.
Para el cálculo de las probabilidades post-test y tener una representación gráfica de las mismas se utilizó el normograma de Fagan27 para las escalas y PC más útiles (TASH>18, TASH>16y ETS>6) encontrándose probabilidades post-test en torno al 70-78% tras la aplicación de dichas escalas (fig. 2).
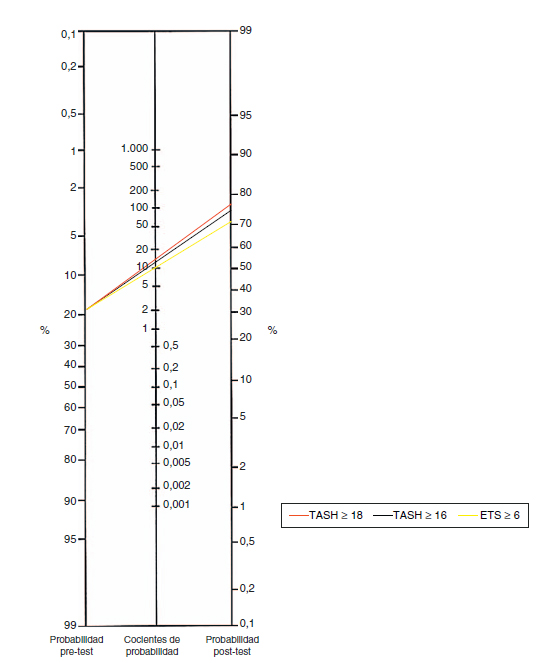
Figura 2. Normograma de Fagan para el TASH PC > 18, TAHS > 16, ETS > 6.ETS:
Emergency Transfusion Score; TASH: Trauma Associated Severe Haemorrhage.
Discusión
La TM es un procedimiento que se produce en una cantidad muy pequeña de enfermos, pero con una elevada mortalidad (40-60%) y consume hasta el 70% de todos los hemoderivados en este tipo de población28.
La predicción precoz de la necesidad de TM es muy difícil y su detección precoz probablemente pueda mejorar el desarrollo de los PTM, sobre todo en relación con la preparación precoz de su logística y disponibilidad de plasma fresco congelado y la adquisición de ratios de hemoderivados adecuados11. El porcentaje de enfermos que requieren TM en nuestra serie respecto a otras publicadas es mucho mayor (18% frente al 3-5% en población civil y 8-10% en población militar)29,30. Estas diferencias se pueden explicar porque en nuestro caso se trata de una población seleccionada con ISS elevado y se encontrarían excluidos muchos enfermos que cumplirían los requerimientos de definición de TM, pero que tendrían un trauma que afectaría a menos regiones anatómicas (por ejemplo, trauma ortopédico grave con necesidad de cirugía).
Además existen otras escalas de predicción TM que no han sido valoradas en este estudio31,32. Otras son específicas para determinados tipos de trauma como el penetrante en torso11. En ocasiones se ha utilizado la estimación visual para la valoración de las pérdidas sanguíneas33,34, las cifras de calcio iónico al ingreso35, parámetros hemodinámicos secundarios derivados36.
La decisión de aplicar los estudiados se basó en su posibilidad de cálculo y en las recomendaciones de sociedades científicas internacionales14 y su adecuación al tipo de población, civil en nuestro caso.
El TASH con PC elevados (16-18) se mostró como mejor predictiva de TM probablemente por la similitud entre la población estudiada y nuestra serie, aunque a la hora de su aplicación en la práctica asistencial esta escala muestra la dificultad de manejar una gran cantidad de variables frente a la ABC. Especialmente son útiles para descartar población con bajo riesgo de TM como demuestran los altos VPN de las diferentes escalas y para los diferentes PC.
Nuestro estudio tiene varias limitaciones. Alguna de ellas no están resueltas en su planteamiento, como son la definición de TM con un concepto temporal a posteriori en lugar de ser apriorístico (con capacidad para determinar hemorragia masiva)37, el tipo de política institucional en cuanto al manejo del trauma grave y de terapia de transfusiones.
Además se trata de un estudio en el cual se aplican escalas predictivas de una manera retrospectiva, aunque hasta el conocimiento de los autores no existen estudios de naturaleza prospectiva, la variabilidad interoperador de determinadas técnicas (FAST) y la ambigüedad en la definición de algunas variables de las escalas que puede comprometer su reproducibilidad.
Finalmente, los hallazgos han sido de utilidad en la renovación de nuestro protocolo institucional de TM.
Conclusiones
Las escalas predictivas de TM pueden ser útiles para caracterizar la población con TM, excluir población de bajo riesgo, y sirven para intentar ser objetivos en el desarrollo de la reanimación con control de daños, diseñar y auditar los PTM, aunque en el momento actual probablemente no puedan sustituir el juicio clínico y la reevaluación continua durante el dinámico proceso de la atención inicial al trauma. La elección de uno u otro debe basarse no solo en sus capacidades predictivas sino también en su posibilidad de aplicación de una manera sencilla, rápida e incluso desde el medio prehospitalario. Para la validación clínica se requieren estudios prospectivos y multicéntricos38 adaptados al medio de aplicación, con las herramientas estadísticas más útiles e incluso la contribución de cada componente39.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
A todo el personal de la UCI de Trauma y Emergencias del Hospital Universitario 12 de Octubre y a la Comisión de Transfusiones y el grupo de Transfusión Masiva de dicho hospital.
Bibliografía
1. Krug EG, Sharma GK, Lozano R. The global burden of injuries. Am J Public Health. 2000; 90:523-6. [ Links ]
2. Murray CJ, López AD. Mortality by cause for eight regions of the world: global burden of disease study. Lancet. 1997; 349:1269-76. [ Links ]
3. Sauaia A, Moore FA, Moore EE, Moser KS, Brennan R, Read RA, et al. Epidemiology of trauma deaths: a reassement. J Trauma. 1995; 38:185-93. [ Links ]
4. Kauvar DS, Lefering R, Wade CE. Impact of hemorrhage on trauma outcome: an overview of epidemiology, clinical presentations, and therapeutic considerations. J Trauma. 2006; 60:s3-s11. [ Links ]
5. Shaz BH, Winkler AM, James AB, Hillyer CD, Macleod JB. Pathophysiology of early trauma - induced coagulopathy: emerging evidence hemodilution and coagulation factor deplection. J Trauma. 2011; 70:1401-7. [ Links ]
6. Duchesne JC, McSwain NE, Cotton BA, Hunt JP, Dellavolpe J, Lafaro K, et al. Damage control resuscitation: the new face of damage control. J Trauma. 2010; 69:976-90. [ Links ]
7. Malone DL, Hess JR, Fingerhut A. Massive transfusion practices around the globe and a suggestion for a common massive transfusion protocol. J Trauma. 2006; 60:s91-6. [ Links ]
8. Teixeira PG, Inaba K, Salim A, Rhee P, Brown C, Browder T, et al. Preventable morbidity at a mature trauma center. Arch Surg. 2009; 144:536-41. [ Links ]
9. McLaughlin DF, NIles SE, Salinas J, Perkins JG, Cox ED, Wade CE, et al. A predictive model for massive transfusion in combat casualty patients. J Trauma. 2008; 64:s57-63. [ Links ]
10. Schreiber MA, Perkins J, Kiraly L, Underwood S, Wade C, Holcomb JB. Early predictors of massive of massive transfusion in combat casualties. J Am Coll Surg. 2007; 205:541-5. [ Links ]
11. Dente CJ, Shaz BH, Nicholas JM, Harris RS, Wyrzykowky AD, Ficke BW, et al. Early predictors of massive transfusion in patients sustaining torso gunshot wounds in a civilian level I trauma center. J Trauma. 2010; 68:298-304. [ Links ]
12. Spinella PC, Holcomb JB. Resuscitation and transfusión principles for traumatic hemorrhagic shock. Blood Rev. 2009; 23:231-40. [ Links ]
13. Marshall WB. Resuscitation of combat casualties. AACN Advanced Critical Care. 2010; 21:279-87. [ Links ]
14. DeLoughery TG. Logistic of Massive Transfussions. Hematology Am Soc Hematol Educ Program. 2010; 470-3. [ Links ]
15. Baker SP, O'Neill B, Haddon W, Long WB. The injury severity scores a method for describing patients with multiple injuries and evaluating emergency care. J Trauma. 1974; 14:187-96. [ Links ]
16. Nunez TC, Voskrsensky IV, Dossett LA, Shinall R, Dutton WD, Cotton BA. Early prediction of massive transfusion in trauma: simple as ABC (assessement of blood consumption)?. J Trauma. 2009; 66:346-52. [ Links ]
17. Cotton BA, Dossett LA, Haut ER, Shafi S, Nunez TC, Au BK, et al. Multicenter validation of a simplified score to predict massive transfusion in trauma. J Trauma. 2010; 69:s33-9. [ Links ]
18. Ruchholtz S, Pehle B, Lewran U, Lefering R, Muller N, Oberbeck R, et al. The emergency room transfusion score (ETS): prediction of blood transfusion requirement in initial resuscitation after severe trauma. Transf Med. 2006; 16:49-56. [ Links ]
19. Kuhne CA, Zettl RP, Fischbacher M, Lefering R, Ruchholtz S. Emergency Transfusion Score (ETS): a useful instrument for prediction of blood transfusion requirement in severely injured patients. World J Surg. 2008; 32:1183-8. [ Links ]
20. Yucel N, Lefering R, Maegele M, Vorweg M, Tjardes T, Ruchholtz S, et al. Trauma Associated Severe Hemorrhage (TASH) - Score: probability of mass transfusion as surrogate for life threating hemorrhage after multiple trauma. J Trauma. 2006; 60:1228-36. [ Links ]
21. Maegele M. Frecuency, risk stratification and therapeutic management of acute post-traumatic coagulopathy. Vox Sang. 2009; 97:39-49. [ Links ]
22. Maegele M, Lefering R, Wafaisade A, Theodoru P, Wutzler S, Fischer P, et al. Revalidation and update of the TASH-Score: a scoring system to predict the probability for massive transfusion as a surrogate for life-threatening haemorrhage after severe injury. Vox Sang. 2011; 100:231-8. [ Links ]
23. Borgman MA, Spinella PC, Holcomb JB, Blackbourne LH, Wade CE, Lefering R, et al. The effect of FFP:RBC ratio on morbidity and mortality in trauma patients based on transfusion prediction score. Vox Sang. 2011; 101:44-54. [ Links ]
24. Whiting PF, Sterne JAC, Westwood ME, Bachmann LM, Harbord R, Egger M, et al. Graphical presentation of diagnostic information. BMC Med Res Methodol. 2008; 8:20. [ Links ]
25. Leeflang MM, Deeks JJ, Gatsonis C, Bossuyt PM. Systematics reviews of diagnostic test accuracy. Ann Intern Med. 2008; 149:889-97. [ Links ]
26. Thompson ML. Assessing the diagnostic accuracy of a sequence of tests. Biostatics. 2003; 4:341-51. [ Links ]
27. Akobenq AK. Understanding diagnostic tests 2: likehoods ratios, pre- and post- test probabilities and their uses in clinical practice. Acta Pediatr. 2007; 96:487-91. [ Links ]
28. Hoyt DB, Bulger EM, Knudson MM, Morris J, Ieardi R, Sugerman HJ, et al. Death in the operating room: an analisys of a multi-center experience. J Trauma. 1994; 37:426-32. [ Links ]
29. Como JJ, Dutton RP, Scalea TM, Edelman BB, Hess JR. Blood transfusion rates in the care of acute trauma. Transfusion. 2004; 44:809-13. [ Links ]
30. Holcomb JB. Damage control resuscitation. J Trauma. 2007; 62:S36-7. [ Links ]
31. McLaughlin DF, Niles SE, Salinas J, Perkins JG, Cox ED, Wade CE, et al. A predictive model for massive transfusion in combat casualty patients. J Trauma. 2008; 64:s57-63. [ Links ]
32. Rainer TH, Ho AM, Yeung JH, Cheung NK, Wong RS, Tang N, et al. Early risk stratification of patients with major trauma requiring massive blood transfusion. Resuscitation. 2011; 82:724-9. [ Links ]
33. Frank M, Schumucker U, Stengel D, Fischer L, Lange J, Grossjohann R, et al. Proper estimation of blood loss on scene of trauma: tool or tale?. J Trauma. 2011; 69:1191-5. [ Links ]
34. Cancio LC, Wade CE, West SA, Holcomb JB. Prediction of mortality and of the need for massive transfusion in casualties arriving at combat support hospitals in Iraq. J Trauma. 2008; 64:s51-5. [ Links ]
35. Magnotti LJ, Bradburn EH, Webb DL, Berry SD, Fischer PE, Zarzaur BL, et al. Admission ionized calcium levels predict the need for multiple transfusions: a prospective study of 591 critically ill trauma patients. J Trauma. 2011; 70:391-5. [ Links ]
36. Vandrome MJ, Griffin RL, Kirbin JD, McGwin G, Rue LW. Identifying risk for massive transfusion in the relatively normotensive patient: utility of the prehospital shock index. J Trauma. 2011; 70:384-90. [ Links ]
37. Stanworth SJ, Morris TP, Gaarder C, Gosling JC, Maegele M, Cohen MJ, et al. Reappraising the concept of massive transfusion in trauma. Critical Care. 2010; 14:R39. [ Links ]
38. Vandrome MJ, Grifin RL, McGwin GJ, Weinberg JA, Rue LW, Kerby JD. Prospective identification of patients at risk for massive transfussion: an mprecise endeavor. Am Surg. 2011; 77:155-61. [ Links ]
39. Callcut RA, Johannigman JA, Kadon KS, Hanseman DJ, Robinson BR. All massive transfusion criteria are not created equal: defining the predictive value of individual transfusion triggers to better determine who benefits from blood. J Trauma. 2011; 70:794-801. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: murgchico@yahoo.es
(M. Chico-Fernández)
Recibido el 17 de mayo de 2011
Aceptado el 27 de junio de 2011














