Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Medicina Intensiva
versión impresa ISSN 0210-5691
Med. Intensiva vol.36 no.5 jun./jul. 2012
Relación entre el gradiente alveolo-arterial de oxígeno y la PaO2/FiO2 introduciendo la PEEP en el modelo
Relationship between the alveolar-arterial oxygen gradientand PaO2/FiO2-introducing peep into the model
M. Sánchez Casadoa, M. Quintana Díazb, D. Palaciosa, V. Hortigüelaa, C. Marco Schulkea, J. Garcíac, A. Canabala, M.J. Pérez Pedreroa, A. Velasco Ramosa y M.A. Arresea
aUnidad de Cuidados Intensivos, Complejo Hospitalario de Toledo, Toledo, España
bHospital Universitario La Paz, Madrid, España
cServicio de Neumología, Hospital Nuestra Señora del Prado, Talavera de la Reina, Toledo, España
Dirección para correspondencia
RESUMEN
Objetivo: Valorar si el gradiente alveolo-arterial de oxígeno (Grad[A-a]O2) ayuda a confirmar la influencia de la PEEP en la PaFi (PaO2/FiO2).
Diseño: Estudio observacional; usamos una regresión lineal para realizar un estudio multivariable y mejorar la fórmula de la PaFi teniendo en cuenta la PEEP.
Ámbito: Hospital terciario.
Pacientes: Todos los pacientes de cuidados intensivos, con o sin daño pulmonar.
Variables de interés principal: Registramos los antecedentes personales, juicio clínico, datos durante ingreso en UCI, puntuaciones de severidad en el primer día y durante evolución; dos variables calculadas: PaFi and Grad(A-a)O2.
Resultados: Un total de 956 patientes incluidos; 63,9% hombres; edad mediana 68 años. Primer día, 31,8% no tienen ventilación mecánica (VM), 13,1% tienen VM no invasiva y 55,1% VM invasiva. PaFi: 32,9% 0-200, 32,2% 201-300, y 34,8% >300. PEEP: 0-5 69,8%, 6-10 27,5% y >10 2,6%. Observamos una correlación (Pearson) entre el Grad(A-a)O2 y la PaFi de -0,84 (p<0,001). Realizamos una regresión múltiple (variable dependiente: Grad(A-a)O2Grad[A-a]O2); variables incluidas en el modelo: PaFi, PEEP, APACHE IV y SOFA; coeficiente de determinación (R2) de 0,62 sin PEEP y 0,72 con PEEP. Cambiamos la fórmula de la PaFi, denominándola PaFip (PaFi más PEEP): Ln (PaFi/[PEEP+12]). El índice de correlación entre PaFip y Grad(A-a)O2: -0,9 (p<0,001). Realizamos una regresión lineal (variable dependiente: Grad[A-a]O2) y utilizamos PaFip en vez de la PaFi. Solo la PaFi permanece en el modelo, y es discretamente complementada por APACHE IV; R2 0,8.
Conclusiones: Añadiendo la PEEP a la PaFi, creamos una variable (PaFip) que mejora el modelo, demostrando mayor capacidad de bondad de ajuste.
Palabras clave: Gradiente alveolo-arterial de oxígeno. PaFi. PaO2/FiO2. Daño pulmonar.
ABSTRACT
Objectives To determine whether the alveolar-arterial oxygen gradient (Grad[A-a]O2) helps confirm the influence of PEEP on PaFi (PaO2/FiO2).
Design: Observational study; we used linear regression to perform a multivariate study to improve the PaFi formula by taking PEEP into account.
Setting: Tertiary hospital.
Patients: We included all patients who were admitted to the intensive care unit, regardless of pulmonary damage.
Variables: We recorded personal history, clinical judgment, intensive care data, severity scores on the first day and progression. Two calculated variables: PaFi and Grad(A-a)O2.
Results: A total of 956 patients were included: 63.9% men; median age 68 years. On the first day, 31.8% did not have mechanical ventilation (MV), 13.1% had non-invasive MV and 55.1% had invasive MV. PaFi values: 32.9% 0-200, 32.2% 201-300, and 34.8% >300. PEEP values: 0-5 69.8%, 6-10 27.5% and >10 2.6%. We observed a correlation (Pearson) between Grad(A-a)O2 and PaFi of -0.84 (p<0.001). On performing multiple regression (dependent variable: Grad[A-a]O2), the following variables were included in the model: PaFi, PEEP, APACHE IV and SOFA; coefficient of determination (R2) of 0.62 without PEEP and 0.72 with PEEP. We changed the PaFi formula, referring to it as PaFip (PaFi plus PEEP): Ln (PaFi/[PEEP+12]). Correlation index between PaFip and Grad(A-a)O2: -0.9 (p<0.001). We performed linear regression (dependent variable: Grad[A-a]O2) and used PaFip instead of PaFi. Only PaFi remained in the model, and was discretely complemented by APACHE IV; R2=0.8.
Conclusions: By adding PEEP to the PaFi model (PaFip), we clearly improve the latter, as reflected by a better goodness of fit.
Key words: Alveolar-arterial oxygen gradient. PaFi. PaO2/FiO2. Lung damage.
Introducción
A partir de la introducción de los conceptos de lesión pulmonar aguda (ALI) y de síndrome respiratorio agudo (SDRA) en la conferencia de consenso de 1994, el concepto de PaFi (PaO2/FiO2) se universaliza como una forma de cuantificar la intensidad del daño pulmonar en el paciente crítico1. La PaFi homogeneiza con independencia de la utilización o no de ventilación mecánica, y si la PEEP es o no utilizada. Pero cuando trabajamos en la clínica con pacientes críticos en ventilación mecánica observamos que la PaFi muchas veces podría no reflejar la intensidad del daño pulmonar. Así una PaO2 de 80, con una FiO2 de 0,5 marcaría una PaFi de 160, pero parecería lo mismo tener una PEEP de 5, una de 10 o una de 15.
El gradiente alveolo-arterial de oxígeno (Grad[A-a]O2) es una forma sencilla de medir la alteración entre el alveolo y el capilar, utilizado últimamente en el estudio de diferentes dolencias críticas (EPOC, TEP, etc.)2-4.
Nuestro objetivo es valorar si la utilización del Grad(A-a)O2 puede ayudarnos a confirmar la influencia de la PEEP sobre la PaFi e intentar mejorar la fórmula de la PaFi si tenemos en cuenta la PEEP.
Material y método
Durante dos años (2008 y 2009) hemos incluido todos los enfermos ingresados en la unidad de cuidados intensivos (UCI), presentasen o no daño pulmonar. La UCI donde se ha llevado a cabo el estudio es una UCI de adultos, del H. Virgen de la Salud, Toledo, España. Es una unidad que consta de 23 camas de atención al paciente crítico y 3 camas de atención al postoperatorio de especial riesgo o que requiere monitorización especial durante las primeras horas (ejemplo de ello es la cirugía no complicada de tumores craneales y otros procedimientos neuroquirúrgicos, maxilofaciales, vasculares, otorrinolaringológicos, etc.).
Las variables registradas se relacionan con los datos de filiación (año ingreso, sexo, edad), antecedentes personales (fumador, obesidad, bronquitis crónica, EPOC, asma, insuficiencia respiratoria restrictiva, traqueostomizado, ventilación domiciliaria), juicio clínico, situación basal, grupo diagnóstico (médico, quirúrgico), tipo de deterioro antes del ingreso UCI, procedencia), datos y puntuaciones en UCI durante el primer día (intubación orotraqueal, tipo ventilación mecánica en el primer día, radiografía de tórax, PaO2, FiO2, PEEP, APACHE II, APACHE IV, SOFA, SAPS II y SAPS III).
En los pacientes que tenían ventilación mecánica, se esperaba a que el médico responsable del enfermo estableciera los mejores parámetros de reclutamiento, y entonces se registraban. En todos los pacientes se recogía la gasometría, durante el primer día de ingreso, una vez el paciente presentaba varias horas de estabilización hemodinámica (con o sin fármacos) y respiratoria (no variaba la saturación ni la tensión arterial sistémica en las últimas 2 horas): se determinaban PaO2, FiO2, y PEEP. De ellas se obtenían dos variables calculadas: la PaFi (PaO2/FiO2) y el Grad(A-a)O2 según la fórmula5:
![]()
Análisis estadístico
Las variables categóricas se expresarán mediante el valor del recuento y el porcentaje. Las variables cuantitativas se expresan mediante la media±desviación; cuando se consideraba adecuado se expresaba mediante la mediana (intervalo). Para comparar variables categóricas utilizamos la prueba de chi cuadrado; si interesaran las variables cuantitativas (Grad[A-a]O2, PaFi, PEEP, etc.) se codificarán en intervalos de medidas y serán consideradas variables categóricas. Para estudiar la relación entre una variable categórica y una cuantitativa utilizamos la prueba t de student cuando son dos variables y cuando son más de dos, utilizamos la prueba de análisis de la variancia.
Cuando estudiamos la correlación entre dos variables cuantitativas utilizamos el coeficiente de correlación de Pearson. También hemos realizado los diagramas de dispersión ajustando la línea que mejor explica su relación. Hemos empleado la regresión lineal para realizar un estudio multivariante cuando la variable dependiente es cuantitativa (PaFi, Grad[A-a]O2). Para el análisis multivariante se utilizan las variables que han salido significativas en el análisis bivariable y todas aquellas que se consideran de interés por su importancia (sexo, edad, PEEP, tipo de ventilación mecánica).
Se considera significativo todo valor de p<0,05.
Resultados
Han sido incluidos 956 pacientes. El 63,9% son hombres, y los pacientes tienen una edad mediana de 68 años (15-91 años). La mediana de las puntuaciones fue: APACHE II 17; APACHE IV 58; SAPS II 43; SAPS III 63 y SOFA 7. El 33,6% de los enfermos eran quirúrgicos; el 36,9% procede de planta de hospitalización y el 32,5% de urgencias.
Las causas más frecuentes de ingreso en UCI fueron insuficiencia cardiaca congestiva (9,8%), neumonía comunitaria (8,9%), peritonitis secundaria (6,3%), sepsis urológica (5,5%), parada cardiorrespiratoria (5,4%), shock cardiogénico (4,8%), neumonía nosocomial (4,5%), EPOC agudizado (3,5%), shock hemorrágico postoperatorio (3,2%), pancreatitis aguda (3,1%), infección de partes blandas (2,6%) y sepsis de origen desconocido (2,5%).
El 64,5% de los pacientes fueron intubados. El primer día el 31,8% no tenían ventilación mecánica, el 13,1% ventilación mecánica no invasiva y el 55,1% ventilación mecánica invasiva. El 32,9% tenían una PaFi entre 0 y 200, el 32,2% entre 201 y 300; el 34,8% tenían una PaFi mayor de 300. El 69,8% de los pacientes tenían una PEEP entre 0 y 5; el 27,5% entre 6 y 10; y el 2,6% una PEEP mayor de 10 durante el primer día. El Grad(A-a)O2 mediano era 128.
En la Tabla 1 se muestran las variables con las que está relacionado el Grad(A-a)O2. Vemos que existe más Grad(A-a)O2 cuando existe patología pulmonar, sea primaria o secundaria, cuando es el sexo varón, cuando los pacientes no tienen antecedentes de asma o son fumadores; los pacientes médicos tienen más Grad(A-a)O2 que los quirúrgicos y también los procedentes de planta de hospitalización convencional. Los pacientes intubados orotraquealmente, los ventilados mecánicamente (sobre todo con ventilación invasiva), aquellos con alteraciones radiológicas pulmonares, y los que presentan las puntuaciones pronósticas más altas durante el primer día, junto con los que fallecían, presentan un Grad(A-a)O2 mayor.
Si observamos la relación entre el Grad(A-a)O2 y la PaFi (Figura 1), vemos que existe una correlación (índice de correlación de Pearson) entre las dos variables de -0,84 (p<0,001). En el grupo de PaFi entre 0-200 el Grad(A-a)O2 es 290±127 (intervalo: 48-610); los pacientes con PaFi entre 201-300 tienen un Grad(A-a)O2 de 136±60 (intervalo: 31-449); los pacientes con PaFi >300 tienen un Grad(A-a)O2 de 60±41 (intervalo: 0-222); las diferencias en el Grad(A-a)O2 según el nivel de PaFi son significativas (p<0,001). En la Figura 2 mostramos el diagrama de dispersión con la línea de mejor ajuste al modelo.

Figura 1. La relación entre el Grad(A-a)O2 y la PaFi durante el primer día.
PaFi es codificada de acuerdo con la Conferencia Consenso.o y *: valores atípicos.

Figura 2. Diagrama de dispersión entre el Grad(A-a)O2 y PaFi,
con la línea que mejor se adapta al modelo. R2 0,62.
Si realizamos una regresión múltiple, siendo la variable dependiente el Grad(A-a)O2, observamos que las variables que entran en el modelo son la PaFi, la PEEP, el APACHE IV y el SOFA (Tabla 2). Destacamos que la edad, el SAPS II, SAPS III y APACHE II no entran en el modelo. En el modelo de regresión la introducción de la PEEP mejora claramente el modelo, pasando de un coeficiente de determinación (R2) de 0,62 del modelo sin PEEP a uno de 0,72 del modelo con PEEP, con independencia de las otras variables.
Ante la confirmación matemática de un hecho que pensábamos claro (que la PEEP tenía importancia en cuantificar el grado de deterioro respiratorio), intentamos cambiar la fórmula de la PaFi, introduciendo la PEEP, con el fin de mejorar el ajuste. Después de algunas tentativas, la fórmula planteada, que se denominó PaFip (PaFi añadiendo la PEEP) que mejor ajuste produce, es la siguiente:
![]()
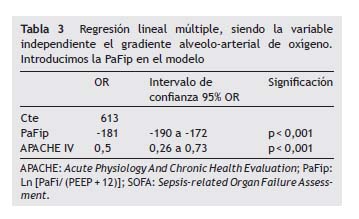
En fórmula cuando la PEEP sea 0 se pone el valor de 1. En el resto de valores (>1) se pone el valor que corresponda. Esta fórmula la hemos determinado en pacientes con o sin ventilación mecánica. Con esta fórmula obteníamos un índice de correlación de Pearson entre la PaFip y el Grad(A-a)O2 de -0,9 (p<0,001). Cuando realizamos el ajuste a la recta, observamos que el ajuste en el diagrama de dispersión mejora ostensiblemente (Figura 3). La PaFip tiene, en el total de pacientes, una mediana de 2,8, con media 2,8±0,6 (intervalo 0,9-3,9). Si realizamos una regresión lineal, siendo la variable dependiente el Grad(A-a)O2, e introduciendo en vez de la PaFi, la PaFip, los resultados son los reseñados en la Tabla 3. Como vemos, en el modelo solo queda la PaFi, complementada discretamente por el APACHE IV, que mejora poco el modelo; el resto de variables no intervendrían. La R2 (coeficiente de determinación) en el modelo de PaFip es de 0,8 (el 80% de los datos se explicarían en este caso, y mejorando un 18% la explicación de los datos solo por la PaFi). La PaFi y la PaFip tienen una correlación de 0,92 (p<0,001).
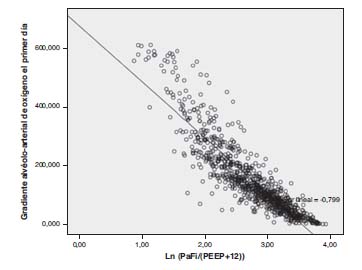
Figura 3. Diagrama de dispersión entre el Grad(A-a)O2 y
PaFip, con la línea que mejor se adapta al modelo. R2 0,8.
Cuando observamos la correlación entre los valores del Grad(A-a)O2 y la PaFi codificada por intervalos según la conferencia de consenso, encontramos que en el intervalo 0-200 es de -0,76; en el intervalo 201-300 es de -0,43; y en el intervalo >300 de PaFi, es de -0,63. Si hacemos lo mismo con la PaFip, es decir, la correlación entre el Grad(A-a)O2 y los nuevos intervalos hallados, encontramos que entre 1 y 1,99 la correlación es de -0,7; entre 2 y 2,99 es de -0,7; y entre 3 y 4 la correlación con el Grad(A-a)O2 es de -0,73. En todos los casos, PaFi y PaFip, las correlaciones son significativas (p<0,001).
Discusión
Tras los primeros trabajos de 1910 en que se demuestra que el intercambio gaseoso es un producto de los fenómenos de difusión, se ha hablado mucho sobre su caracterización en la clínica práctica6. A raíz de los trabajos realizados durante la segunda guerra mundial por Fenn, Rahn y Riley se conocen de forma profusa conceptos asimilados hoy en día sobre la fisiología del oxígeno en general y sobre el Grad(A-a)O2 en particular7-10.
La PaFi (PaO2/FiO2) es un índice muy extendido para evaluar el intercambio de oxígeno debido a su facilidad de cálculo y poder realizarlo «a pie de cama». Su importancia se potencia al formar parte de las definiciones de SDRA y ALI, en la Conferencia de Consenso Americano-Europea1 y el Lung Injury Score10. Así se puede hablar de ALI en presencia de infiltrados pulmonares bilaterales, descartando causa cardiogénica (presión de enclavamiento pulmonar menor de 18mmHg) y una PaFi entre 201 y 300; se considera SDRA cuando tiene los mismos condicionantes radiográficos y hemodinámicos y la PaFi se sitúa en valores iguales o inferiores a 200. Su gran ventaja es la sencillez de cálculo. Sus principales problemas son:
- Los cambios en la FiO2 ejercen una influencia sobre la fracción del shunt intrapulmonar observado11. Al incrementar la FiO2 a 1 los efectos de las alteraciones de la relación ventilación/perfusión pueden ser enmascarados, pudiéndose subestimar el shunt intrapulmonar, sobre todo en situaciones en las que existe una disminución de la relación ventilación/perfusión (EPOC, asma, etc.) Además, con FiO2 elevadas suelen producirse atelectasias, que incrementan el shunt12.
- La relación entre la PaFi y la FiO2 no es lineal. Debido a la compleja relación entre la curva de disociación de la hemoglobina, el Grad(A-a)O2, la presión arterial de CO2 y los niveles de hemoglobina, la relación entre la PaFi y la FiO2 es compleja13: no es constante ni lineal, ni siquiera en situaciones en las que el shunt permanece constante. Por ello, la PaFi puede mostrar distintos comportamientos para una mayor o menor FiO2 en función de la fracción de shunt presente14.
- La PEEP modifica la PaFi, de forma que un mismo valor de PaFi puede ser obtenido en condiciones respiratorias muy distintas con PEEP muy diferentes15. Dichos problemas se han intentado solventar mediante índices de PaFi modificados por la PEEP, como el oxygenation index [PaO2/(FiO2 × presión media respiratoria)]; se realizó en una muestra de paciente en postoperatorio de cirugía cardiaca y actualmente parece tener utilidad en el ámbito pediátrico, no habiéndose extendido a los adultos16.
El cálculo del Grad(A-a)O2 permite valorar la desigualdad de la ventilación-perfusión. Por ello, lo hemos utilizado para ver si la PaFi puede ser mejorada mediante una fórmula que contenga la PEEP en la explicación de las alteraciones difusión. Todos los intensivistas observamos en la práctica clínica el valor de la PEEP, una vez realizado el ajuste adecuado, como índice de gravedad de la afección pulmonar. Por ello se utilizan con frecuencia escalas en donde esta es un componente fundamental de la valoración, junto con la PaFi10.
En nuestro estudio obtenemos que, en el análisis multivariable, la PaFi sola explica el ajuste del 62% de los datos mostrados por el Grad(A-a)O2. Si introducimos la PEEP, se explicaría el 72% de estos mismos datos. Es claro que la PEEP debe ser introducida en el modelo, en el denominador junto a la FiO2, dada su mutua contribución a la oxigenación, pero no lo podemos hacer de una forma aritmética simple. Así, de los modelos probados, al final hemos tenido que utilizar una fórmula en la que se realice un logaritmo neperiano, que hace más lineal el modelo matemático. Con esta ecuación, denominada PaFip, hemos obtenido un ajuste muchísimo mejor. Esta bondad de ajuste alcanza el 80% de los datos del Grad(A-a)O2 explicados por el modelo de regresión de la PaFip. Con esto no haríamos sino justificar matemáticamente algo que vemos en la clínica habitual todos los días.
El Grad(A-a)O2 se utiliza con frecuencia en la valoración de enfermedades pulmonares. Somos conscientes de que presenta algunas limitaciones importantes:
- Está condicionado por la FiO2. Así, un Grad(A-a)O2 elevado con FiO2 alta puede ocurrir en sujetos sanos. Esto se intentaría mitigar ajustando de forma previa a su determinación la FiO2 mínima que necesite el paciente.
- Es solo un reflejo fiable de las alteraciones en el shunt fisiológico cuando existe estabilidad cardiovascular, FiO2 constante y PaO2 elevada. En nuestro estudio se obtenían las muestras cuando el paciente presentaba estabilidad cardiovascular, y la FiO2 era constante durante varias horas.
Esto hace que pacientes con EPOC e hipoventilación alveolar puedan mostrar cifras normales en presencia de alteraciones importantes de la relación ventilación/perfusión, o incluso ser normal en pacientes con embolismo pulmonar3,17. De todas formas, se sigue utilizando como elemento de referencia en muchas ocasiones en la actualidad4,17-23 por lo que nos ha parecido de interés cotejarlo como «elemento de referencia» del empeoramiento respiratorio.
A raíz de la conferencia de consenso, se ha categorizado la PaFi en varios grupos, que definen en sus extremos el ALI y SDRA, en conjunción con un entorno clínico apropiado1,10. Llama la atención el gran solapamiento que se produce en los valores de Grad(A-a)O2 en cada intervalo, en una gran extensión de los mismos (Figura 1). Se suele indicar que el valor del Grad(A-a)O2 no debe exceder los 20mmHg en situaciones de estabilidad hemodinámica y FiO2 de 0,21. En nuestros enfermos, en el grupo de PaFi >300, la media del mismo es de 60. Por tanto es difícil en pacientes críticos definir los puntos de corte del Grad(A-a)O2 que permitan delimitar contextos de mayor empeoramiento respiratorio; para esto no está diseñado nuestro estudio. Pero lo que sí observamos es la correlación entre los valores de PaFi en cada intervalo y los valores del Grad(A-a)O2. Observamos que existe una adecuada correlación (-0,76) en el intervalo de PaFi 0-200, una menor correlación en el intervalo PaFi>300 (-0,63), con una más que deficiente correlación en el intervalo de PaFi de 201-300 (-0,43). Esto nos indicaría una zona de penumbra en este último intervalo, y sobre todo, la mejor caracterización de los pacientes con PaFi más baja, y por tanto, con Grad(A-a)O2 más alto. Si añadimos la PEEP al modelo, y utilizamos la PaFip, hemos establecido 3 nuevos puntos de corte, similares a los anteriores, que, en general, presentan una correlación mucho mejor (> -0,7 en cada intervalo de PaFip).
En nuestro estudio hemos introducido pacientes con o sin ventilación mecánica y/o PEEP, con una muestra muy heterogénea en los pacientes. Esta falta de homogeneidad resta fuerza a los resultados, pero les da valor a las conclusiones, pues queremos que esta aproximación que realizamos se aplique a todos los pacientes que vemos en el entorno de la UCI (ganando validación externa).
Como conclusión podemos establecer que al añadir la PEEP en el modelo de PaFi, utilizando la PaFip (Ln (PaFi/(PEEP+12)) mejoramos de forma ostensible el modelo, con una mejor bondad de ajuste, y lo acercamos más a la clínica habitual, introduciendo de forma fácil un parámetro tan importante como la PEEP. Esto conllevaría la utilización de nuevos puntos de corte.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Bernard GR, Artigas A, Brigham KL, Carlet J, Falke K, Hudson L, et al. The American European Consensus Conference on ARDS. Definitions, mechanisms, relevant outcomes, and clinical trial coordination. Am J Respir Crit Care Med. 1994; 149:818-24. [ Links ]
2. Santamaría Herrero SA. Alveolar-arterial gradient of oxygen in COPD patients. An Med Interna. 2001; 18:115-6. [ Links ]
3. Stein PD, Goldhaber SZ, Henry JW. Alveolar-arterial oxygen gradient in the assessment of acute pulmonary embolism. Chest. 1995; 107:139-43. [ Links ]
4. Donoso H, Katz R, Velasco M. Study of the alveolar-arterial gradient of oxygen in liver cirrhosis. Rev Med Chil. 1960; 88:466-71. [ Links ]
5. http://www.mecriticalcare.net/medical_calculators/respiratory_calculators.php%23anchor1. [ Links ]
6. Severinghaus JW, Astrup P, Muray JF. Blood gas analysis and critical care medicine. Am J Respir Crit Care Med. 1998; 157:S114-22. [ Links ]
7. Fenn WO, Rahn H, Otis AB. A theoretical study of the composition of the alveolar air at altitude. Am J Physiol. 1946; 146:637-53. [ Links ]
8. Rahn H. A concept of mean alveolar air and the ventilation-bloodflow relationships during pulmonary gas exchange. Am J Physiol. 1949; 158:21-30. [ Links ]
9. Riley RL, Cournand A. "Ideal" alveolar air and the analysis of ventilation-perfusion relationships in the lungs. J Appl Physiol. 1949; 1:825-47. [ Links ]
10. Murray J, Matthay MA, Luce J, Flick M. An expanded definition of the adult respiratory distress syndrome. Am Rev Respir Dis. 1998; 138:720-3. [ Links ]
11. Santos C, Ferrer M, Roca J, Torres A, Hernández C, Rodríguez, et al. Pulmonary gas exchange response to oxygen breathing in acute lung injury. Am J Respir Crit Care Med. 2000; 161:26-31. [ Links ]
12. Bartter TC, Pratter MR, Abouzheib WB, Irwin RS. Respiratory Failure Part I: A physiologic approach to respiratory failure. En: Irwin R.S., Rippe J.M., editors. Intensive Care Medicine. 6a ed. Philadelphia: Lippincott Williams & Wilkins; 2008. 491-8. [ Links ]
13. Karbing DS, Kjaergaard S, Smith BW, Espersen K, Allerod C, Andreassen S, et al. Variation in the PaO2/FiO2 ratio with FiO2: mathematical and experimental description, and clinical relevance. Crit Care. 2007; 11:R118. [ Links ]
14. Aboab J, Lous B, Jonson B, Brochard L. Relation between PaO2/FiO2 ratio and FiO2: a mathematical description. Int Care Med. 2006; 32:1494-7. [ Links ]
15. Marini JJ, Wheeler AP. Respiratory monitoring. En: Marini J.J., Wheeler A.P., editors. Critical Care Medicine. The Essentials. 4a ed. Philadelphia: Lippincott Williams & Wilkins; 2010. 81-113. [ Links ]
16. El-Khatib M, Jamaleddine G. A new oxygenation index for reflecting intrapulmonary shunting in patients undergoing open-heart surgery. Chest. 2004; 125:592-6. [ Links ]
17. Carrión Valero F, Martínez Francés M, Perpiñá Torderá M, Pascual Izuel JM, Marín Pardo J. Alveolar-arterial gradient of O2 in COPD with hypercapnia. An Med Interna. 2001; 18:117-20. [ Links ]
18. Cancio LC, Galvez E, Turner CE, Kypreos NG, Parker A, Holcomb JB. Base deficit and alveolar-arterial gradient during resuscitation contribute independently but modestly to the prediction of mortality after burn injury. J Burn Care Res. 2006; 27:289-96. [ Links ]
19. McLaughlin GE. Use of alveolar-arterial gradient as predictor of outcome in respiratory failure. J Pediatr. 1992; 121:330. [ Links ]
20. Moler FW, Custer JR. Use of alveolar-arterial gradient as predictor of outcome in respiratory failure. J Pediatr. 1992; 121:330-1. [ Links ]
21. Fernández Bonetti P, Martínez Guerra ML, Lupi Herrera E. Factors involved in the alveolar-arterial gradient of oxygen, during rest and respiration of environmental air. Arch Inst Cardiol Mex. 1979; 49:1066-72. [ Links ]
22. Kreuzer F. Temporary changes of the alveolar-arterial gradient of oxygen by physiological agents. J Physiol (Paris). 1962; 54:358-9. [ Links ]
23. Saunders KB. Alveolar-arterial gradient for oxygen in heart-failure. Lancet. 1965; 1:160-2. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
marcel55@terra.es
(M. Sánchez Casado)
Recibido 22 Junio 2011
Aceptado 15 Octubre 2011