Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO  Similares em Google
Similares em Google
Compartilhar
Nutrición Hospitalaria
versão On-line ISSN 1699-5198versão impressa ISSN 0212-1611
Nutr. Hosp. vol.20 no.4 Madrid Jul./Ago. 2005
Original
Estudio multicéntrico de incidencia de las complicaciones de la nutrición enteral total
en el paciente grave. Estudio ICOMEP 2ª parte
T. Grau*, A. Bonet** y el Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva Critica y Unidades Coronarias
*Servicio de Medicina Intensiva. Hospital Doce de Octubre. Madrid. **Servicio de Medicina Intensiva. Hospital Josep Trueta. Girona. España.
| Resumen Objetivo: Valorar la incidencia de complicaciones de la nutrición enteral en una cohorte prospectiva de enfermos ingresados en UCI. (Nutr Hosp 2005, 20:278-285) Palabras clave: Nutrición enteral. Enfermo grave. Complicaciones intestinales. Infección nosocomial. | MULTICENTER STUDY ON INCIDENCE OF TOTAL PARENTERAL NUTRITION COMPLICATIONS IN THE CRITICALLY-ILL PATIENT. ICOMEP STUDY. PART II. Abstract Objective: To assess enteral nutrition complications in a prospective cohort of patients admitted to the ICU. (Nutr Hosp 2005, 20:278-285) Key words: Enteral nutrition. Critically ill patient. Intestinal complications. Nosocomial infection. |
Correspondencia: Dr. Teodoro Grau
Servicio de Medicina Intensiva. Unidad Polivalente, 2ª planta.
Hospital Doce de Octubre.
Av. De Córdoba s/n. 28041 Madrid.
E-mail: tgrau@grupobbva.net
Recibido: 12-I-2005.
Aceptado: 23-III-2005.
Introducción
La nutrición enteral (NE) parece ser el método de elección para nutrir a los pacientes graves. La NE es un método seguro de alimentar a estos enfermos incluso en situaciones complejas. Aunque se desconoce cuánto tiempo puede estar un enfermo grave sin nutrición, el catabolismo acelerado y el ayuno pueden ser deletéreos y la recomendación más frecuente es la de empezar la nutrición enteral cuando se prevea un periodo de ayuno entre 5 y 10 días1. Un metaanálisis que comparaba el efecto de la NE respecto a los cuidados estándares en una población pacientes con cirugía gastrointestinal demostró únicamente una incidencia menor de complicaciones en el grupo tratado, si los pacientes estaban desnutridos en el momento de iniciar la nutrición, y no había cambios en la mortalidad2. Diferentes estudios clínicos han demostrado que la nutrición enteral disminuye la incidencia de infecciones nosocomiales en estos enfermos aunque no la mortalidad, salvo en grupos concretos de pacientes, especialmente en enfermos quirúrgicos3-8. El mayor inconveniente de la nutrición enteral es su intolerancia digestiva y el abordaje transpilórico, necesario cuando se produce gastroparesia8-11. También existen dudas de su eficacia cuando el enfermo está en situación de isquemia tisular12. Para acentuar la eficacia de este método nutricional se ha propuesto utilizar la nutrición enteral de forma precoz, en las primeras 48 horas tras el ingreso en UCI4, 13-14. Esta técnica no está exenta de dificultades pues el riesgo de intolerancia es mayor y existe la duda de que incremente la incidencia de neumonía asociada a ventilación mecánica15-17. El objetivo de este estudio ha sido obtener la incidencia de complicaciones de la administración como las infecciones nosocomiales de una cohorte de enfermos tratados con NE en centros con investigadores con amplia experiencia, utilizando un protocolo de uso de la misma, unas definiciones homogéneas de las diferentes complicaciones basadas en criterios clínicos y en datos de laboratorio, así como un programa de recogida de datos y seguimiento de los casos reclutados en un periodo de tiempo definido. Asimismo, se pretende ver la incidencia de complicaciones gastrointestinales cuando se administra la NE de forma precoz, en las primeras 24 horas de ingreso.
Pacientes y métodos
Este estudio multicéntrico prospectivo de la incidencia de las complicaciones relacionadas con la NE, en pacientes de cuidados intensivos que recibían soporte nutricional, se realizó durante 45 días (1 febrero hasta 15 de marzo del año 2000) en 40 Unidades de Cuidados Intensivos españolas. Antes de iniciar el estudio se realizaron reuniones con los investigadores para conseguir un acuerdo sobre la técnica de administración de la NE, las definiciones de las complicaciones relacionadas con la NE, así como el seguimiento y recogida de las mismas. Todos los pacientes incluidos en el estudio fueron seguidos durante 28 días o hasta el alta hospitalaria. De acuerdo con la legislación española vigente, no fue necesario solicitar consentimiento informado para la participación del estudio.
Pacientes. Todos los enfermos candidatos se reclutaron de forma consecutiva. Sólo se excluyeron los pacientes terminales. Los enfermos eran reclutados cuando tenían indicación de recibir NE o estaban con nutrición parenteral total (NPT) y podía hacerse la transición a NE, a criterio de cada investigador.
Protocolo de administración de la NE. El aporte calórico calculado se estableció en 25 Kcal. por Kg. de peso y día. Cada investigador era libre de indicar el tipo de NE que administraba a sus pacientes y la composición de la misma así como el tipo de acceso al tracto gastrointestinal. Se realizó una radiografía del abdomen para confirmar la posición adecuada de la sonda entérica antes de hincar la NE. Se recomendó que los pacientes permanecieran en una posición semi-sentada a 30º. La nutrición se administró siguiendo un protocolo previamente establecido11. La dieta se infundió de forma continua durante las 24 horas del día, a velocidad constante, con bomba de infusión y los sistemas y contenedores se cambiaban cada día. Las dietas se administraban sin diluir y se iniciaban a 42 ml/h el primer día y se progresaban en incrementos en 20 ml/h cada 12 horas, hasta alcanzar los requerimientos calóricos calculados. Se definió NE precoz aquella que se iniciaba en las primeras 24 horas de ingreso en la UCI.
Definición de las complicaciones gastrointestinales. Las complicaciones gastrointestinales de la NE que se analizaron fueron la distensión abdominal, el aumento del residuo gástrico, los vómitos y la regurgitación, la diarrea asociada a la NE (DANE), el estreñimiento y la broncoaspiración de la dieta. Estas definiciones ya han sido utilizadas por nuestro grupo y se muestran en la tabla I18.
Definición de las complicaciones infecciosas: La complicaciones infecciosas se definieron siguiendo los criterios del CDC19, 20. La infección por catéter se definió de varias formas. Catéter colonizado: Cultivo semi-cuantitativo < 15 ufc en punta con cultivo positivo de la piel o de la conexión; catéter con infección local: signos clínicos de infección (aspecto punto punción), más cultivo positivo del frotis de la piel y algún segmento del catéter con cultivo semicuantitativo con > 15 ufc/ml y hemocultivos negativos. Catéter infectado: signos clínicos con desaparición de la fiebre tras la retirada, cultivos semicuantitativos de la punta del catéter con > 15 ufc/ml., en ausencia de otro foco, respuesta al tratamiento sin retirada del catéter y algún cultivo positivo de la piel, la conexión o hemocultivos (debe cumplirse los tres primeros y uno de los tres segundos). Sepsis por catéter: Signos clínicos de infección, desaparición fiebre tras la retirada del catéter, ausencia de otros focos, cultivos semicuantitativos de la punta del catéter > 15 ufc/ml y hemocultivos positivos al mismo germen (de certeza si cumple todos los criterios y sospecha si sólo los hemocultivos son positivos). Neumonía. se definió separadamente de otras infecciones del tracto respiratorio inferior. Los criterios de neumonía fueron cualquiera de los siguientes: 1) Crepitantes o matidez a la percusión del tórax más uno de los siguientes: a) expectoración purulenta o cambio en las características del esputo; b) aislamiento de gérmenes en el hemocultivo; c) aislamiento del gérmen en muestras obtenidas por aspiración transtraqueal, cepillado bronquial o biopsia. 2) El examen radiológico del tórax muestra un infiltrado nuevo o progresivo, consolidación, cavitación o derrame pleural más uno de los siguientes: a) Expectoración purulenta o cambio en las características del esputo; b) aislamiento de gérmenes en el hemocultivo; c) aislamiento del germen en muestras obtenidas por aspiración transtraqueal, cepillado bronquial o biopsia. Infección de la herida quirúrgica. La infección de la herida quirúrgica (HQ) se divide en incisional (HQI) y de órgano-espacio (absceso intraabdominal). La HQI puede afectar a la piel y tejido subcutáneo (superficial, HQIS) o a los tejidos profundos, fascia y planos musculares (HQIP). Las HQ comprenden cualquier parte de la anatomía abierta y manipulada durante el acto quirúrgico diferente de la incisión. HQ incisional superficial (HQIS). Se define como la infección que ocurre en los 30 días siguientes a la cirugía y afecta sólo a la piel y tejido subcutáneo de la incisión quirúrgica junto con al menos uno de los siguientes: 1) Drenaje purulento a través de la incisión. 2) Cultivos positivos de líquidos o tejidos de la incisión obtenidos asépticamente. 3) Por lo menos uno de los siguientes signos y síntomas: dolor, edema localizado, eritema o calor y la herida es abierta deliberadamente por el cirujano salvo que el cultivo sea negativo. 4) Diagnóstico de HQIS hecho por el cirujano. No se considera HQIS: a) mínima inflamación o drenaje de los puntos de sutura, b) infección de la quemadura, c) HQIS que se extiende a fascia y capas musculares. HQ incisional profunda (HQIP). Se define como la infección que ocurre en los 30 días siguientes a la cirugía y afecta a la piel, tejido subcutáneo, fascia y planos musculares y la infección parece relacionada con el acto quirúrgico junto con al menos uno de los siguientes: 1) Drenaje purulento a través de la incisión profunda pero no de un órgano o espacio. 2) Dehiscencia espontánea de la profundidad de la incisión o incisión abierta por los cirujanos cuando el paciente presenta por lo menos uno de los siguientes: fiebre > 38oC o dolor salvo que el cultivo sea negativo. 3) Se halla un absceso o cualquier otra evidencia de infección que afecta a la incisión profunda al realizar un examen directo, durante la reoperación o mediante examen radiológico o histopatológico. 4) Diagnóstico de HQIP hecho por el cirujano. Si la infección afecta tanto a la incisión superficial como a la profunda se clasifica como profunda. Absceso intraabdominal y peritonitis. Comprende cualquier parte de la anatomía (órgano o espacio), distinta de la incisión, que ha sido abierta o manipulada durante el procedimiento quirúrgico. Debe de cumplir los siguientes criterios: la infección aparece en los 30 días siguientes al acto quirúrgico, parece relacionada con el mismo y comprende cualquier parte de la anatomía distinta de la incisión, manipulada o abierta durante la cirugía, junto con uno de los siguientes: 1) Drenaje purulento colocado en dicho órgano o espacio. 2) Cultivos positivos de líquidos o tejidos del órgano o tejido obtenidos asépticamente. 3) Un absceso u otra evidencia de infección en el órgano o espacio hallados en el examen directo, durante la reoperación o por examen radiológico o histopatológico. 4) Diagnóstico de absceso intraabdominal hecho por el cirujano. Infección del tracto urinario. Cualquiera de los dos criterios siguientes: fiebre > 38ºC, tenesmo, disuria, dolor abdominal y urocultivo positivo con más de 105 colonias/ml de orina con 2 o menos gérmenes distintos, o fiebre > 38ºC, tenesmo, disuria, dolor abdominal y uno de los siguientes: a) urocultivo positivo con más de 102 colonias/ml de orina de gérmenes uropatógenos; b) Urocultivo positivo con menos de 105 colonias/ml de orina de un solo germen uropatógeno en un paciente tratado adecuadamente; c) diagnóstico y/o tratamiento instaurado por su médico.
Recogida de datos: Se registraron los siguientes datos: Hospital, número de historia clínica, sexo, edad, peso, fecha de ingreso en el hospital y en el Servicio de Medicina Intensiva (SMI), fecha alta del SMI y del hospital, destino a los 28 días, diagnóstico principal, Apache II, índice de FMO, tipo de enfermo, la presencia de sepsis y shock séptico, la necesidad de ventilación mecánica y días de la misma y uso de la sonda urinaria. Se registró el índice subjetivo de estado nutricional al ingreso, el índice de riesgo nutricional21, los requerimientos energéticos al ingreso, uso de la NE, vía de administración, su duración y las causas que condicionaron su supresión definitiva. Para cada grupo de complicaciones se debía especificar la fecha de la complicación, el tipo, si precisó de alguna intervención terapéutica, y si fue motivo de supresión de la NE. Se recogieron los aportes calóricos prescritos y administrados los días 1, 3 y 7,14 y 28. Cada 6 horas se determinó la glucemia o glucosuria y cada 24 horas la urea, creatinina e ionograma en sangre y semanalmente colesterol, triglicéridos, fósforo, calcio, magnesio, osmolaridad y pruebas de función hepática (bilirrubina total, GOT, GPT, FA, Gama GT y tiempo de protrombina). Se practicaron hemocultivos y cultivos específicos cuando se sospechó infección.
Base de datos y análisis estadístico. Cada complicación fue considerada como un episodio y se registró en una base de datos construida en MS Access. A cada investigador se le proporciono un manual de instrucciones, un CD con la hoja de recogida de datos y un sistema de ayuda para la instalación del programa. Al final del período de estudio, las base de datos se cerró y el análisis fue hecho por un grupo independiente de investigadores. Cualquier diferencia respecto al protocolo fue discutida con cada investigador y la decisión final la tomaron los investigadores principales. Los investigadores desconocían el número de total de casos y sus características clínicas hasta el final del período de estudio. No se conoció en ningún momento la identidad de los pacientes incluidos en el estudio. Para cada complicación se calculó la tasa de incidencia ( número de episodios por 100 enfermos) y la densidad de incidencia ( número de episodios por 100 partido días de NE). Las variables cuantitativas con distribución normal se analizaron con la t de Sudent y, en caso contrario con pruebas no paramétricas. Las variables cualitativas se analizaron con la prueba de Chi-cuadrado sin corrección de Fisher. Se calculó la razón de probabilidad (odds ratio) con su intervalo de confianza al 95%. Los datos cuantitativos se expresan como mediana y rango intercuartil y los cualitativos en número absoluto y porcentaje.
Resultados
Datos generales. 544 pacientes fueron tratados con NE, de un total de 725 enfermos tratados con nutrición artificial (tabla II). De ellos, 374 (69%) eran hombres y con una mediana de edad de 63 años. 303 enfermos ingresaron por patología médica, 149 tenían patología quirúrgica y 92 eran traumáticos. 138 enfermos presentaban sepsis al ingreso y la mediana de APACHE II fue de 18 (13-23) y el índice MOF 5 (3-7). 495 enfermos recibieron ventilación mecánica durante 10 días (5-17). 99 pacientes presentaban desnutrición moderada o severa y la mediana del índice re riesgo nutricional era 69,7. La NE se administró durante 9 días (5-17) y la nutrición parenteral asociada durante 1 día (0-4). Se contabilizaron un total de 6.210 días de NE. Otros datos demográficos y nutricionales se reseñan en la tabla III y el diagnóstico al ingreso se muestra en la tabla IV.
Complicaciones gastrointestinales de la NE: El 86% de los pacientes presentó uno o más de los 469 episodios que se registraron, con una incidencia de 7,6 complicaciones por 100 días de NE (tabla V). La complicación más frecuente fue el aumento del residuo gástrico que afectó al 35% de los enfermos con una densidad de incidencia de 3,03 episodios por 100 días de NE. Le siguió la DANE con 16% de pacientes afectados y una incidencia de 1,4 episodios por 100 días de NE. En 89 ocasiones estas complicaciones provocaron la suspensión definitiva de la dieta y 67 enfermos fueron tratados con NPT a consecuencia de las mismas. La broncoaspiración de la dieta fue una complicación muy infrecuente con una densidad de incidencia de 0,03 episodios por 100 días de NE. Para tratar estas alteraciones se utilizaron diversas medidas terapéuticas, siendo la más frecuente la retirada transitoria de la NE durante menos de 24 horas, en 140 ocasiones. También se utilizaron profusamente los procinéticos en 115 ocasiones y la aspiración gástrica en 48 ocasiones (tabla VI).
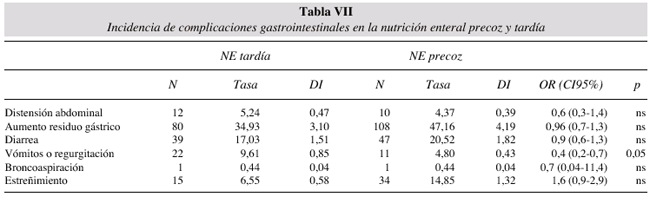
Complicaciones gastrointestinales y nutrición enteral precoz. 315 enfermos (58%) recibieron nutrición enteral en las primeras 24 horas de ingreso. La incidencia de complicaciones gastrointestinales fueron similares en el grupo tratado precozmente y en el grupo que recibió NE tardía. La complicación más frecuente era en ambos casos el aumento del residuo del gástrico con incidencia de 4,2 episodios en el grupo de NE precoz respecto a 3,1 episodios por 100 días de NE en el grupo tratado de forma tardía (O.R. 0,96; IC95% 0,7-1,3). La única complicación que apareció de forma más frecuente en el grupo de NE tardía fueron los vómitos con una incidencia de 9,6 episodios respecto a 4,8 episodios en el grupo de NE precoz (O.R. 0,4; IC 95% 0,2-0,7). La incidencia de las demás complicaciones fue similar en ambos grupos (tabla VII). La persistencia de estas complicaciones hizo que la mediana del aporte calórico al tercer y séptimo día de ingreso fueran inferiores a los requerimientos energéticos calculados al ingreso.
Complicaciones infecciosas. Con un total de 241 catéteres colocados (incluyendo centrales y PICC), y 3.200 catéter-día, se produjeron 55 episodios de infección del catéter en el 29% de los enfermos, con una DI de infección de 1,8 episodios por cien días de catéter. Los resultados pormenorizados aparecen en la tabla VIII. Se produjeron 20 aislamientos de gérmenes grampositivos, 1 aislamiento de SAMR, 6 aislamientos de bacilos gramnegativos y 1 aislamientos de Cándida. Las infecciones nosocomiales más habituales en esta serie de pacientes tienen origen pulmonar (35%) con una incidencia de 3,1 episodios por 100 días de nutrición , seguidas de las ITU (7,2%) con una densidad de incidencia de 0,63 episodios por 100 días de nutrición. El 51% de los enfermos presentó alguna infección no relacionada con el catéter con una densidad de incidencia de 4,5 episodios por 100 días de nutrición (tabla VIII). Se produjeron 35 aislamientos de Pseudomonas, 32 de Acinetobacter, 32 aislamientos de de Estafilocos y 23 de Cándidas.
Discusión
Este estudio prospectivo de incidencia de las complicaciones relacionadas con el uso de la NE describe de forma amplia y sistemática todas aquellas que tienen relevancia clínica y pretende servir de referencia para la realización de estudios más complejos sobre este tema. El 21,3% los pacientes ingresados en UCI, incluyendo las unidades coronarias recibieron algún tipo de nutrición, de los cuales el 75% recibió nutrición enteral, sola (50%) o en combinación con NPT (25%). En 1995, se realizó un estudio en nuestro país basado en cuestionarios que mostraba una incidencia similar (59%) del uso de NE22, siendo los enfermos médicos los más susceptibles de recibir este tratamiento. Una encuesta europea más reciente revela unas tasas de uso del 58% de NE sola y del 19% combinada con NE23.
Otros estudios prospectivos demuestran que el uso de NE está entre el 76% y 85% de los pacientes ingresados en UCI24-25. Nuestros datos son similares a los publicados y llama la atención el hecho de que sean más próximos a los estudios citados que los presentados por la encuesta antes citada y correspondientes a nuestro país23. Para conocer la incidencia exacta del uso de nutrición artificial es preciso que se consideren poblaciones homogéneas y, en nuestro caso, la inclusión de enfermos procedentes de unidades coronarios hace bajar la frecuencia de utilización del soporte nutricional.
Un aspecto relevante es el uso precoz de la nutrición enteral precoz en esta serie de enfermos pues se utilizó en 315 casos (43,4%) en las primeras veinticuatro horas de ingreso. Hay evidencia suficiente para afirmar que, la nutrición enteral precoz, definida como aquélla que se inicia en las primeras 48 horas tras la agresión, tiene ventajas sobre cualquier otro método nutricional en los pacientes graves4, 7, 8, 26, 27, y un estudio español realizado por nuestro grupo, realizado en un grupo heterogéneo de pacientes que recibió nutrición enteral precoz, presentaba una mortalidad menor que la predicha por el APACHE II, independientemente del tipo de dieta utilizada14.
La mayor preocupación del uso de la nutrición enteral, ya sea precoz o no, está en la aparición de complicaciones gastrointestinales y del aumento de la incidencia de infecciones nosocomiales, en especial de la neumonía asociada a ventilación mecánica. Cerca del 70% de los pacientes de este estudio presentaron alguna complicación gastrointestinal relacionada con la NE, una frecuencia incluso superior a la publicada por nuestro grupo hace años, del 63%11. Ello se podría explicar por el elevado número de enfermos que recibieron nutrición enteral precoz pero nuestro análisis no lo corrobora ya que la incidencia de residuos gástricos aumentados es menor que en el estudio citado, 35% y 39% respectivamente. Un aumento del aspirado gástrico es la causa de retirada de la dieta y origina un menor aporte calórico. Por ello, algunos autores han cuestionado el uso rutinario del volumen gástrico como medidor de la intolerancia a la nutrición enteral28. El protocolo utilizado por nosotros ha utilizado el aspirado gástrico como indicador y ello explicaría la intolerancia a la dieta que dio lugar a la suspensión de la dieta en 89 pacientes (16%). Los vómitos aparecen más frecuentemente en el grupo que recibió nutrición enteral tardía. Ello podría explicarse por los intentos repetidos de iniciar nutrición enteral en el grupo de pacientes tratado inicialmente con nutrición parenteral, grupo que no es analizado en el estudio previo de nuestro grupo. Sin embargo, la incidencia de complicaciones por día de nutrición es escasa, de 6 episodios por cada 100 días de nutrición. Para prevenir estas complicaciones se ha propuesto la elección de nutrición nasoentérica más allá del píloro que ha sido motivo de numerosos estudios, con resultados poco significativos4. Sólo el 8,8% de los pacientes de esta serie recibieron una sonda transpilórica. Por el contrario, sí se utilizaron de forma profusa todos los métodos reconocidos para prevenir las complicaciones gastrointestinales como los procinéticos29 y la fibra30, aunque la suspensión transitoria de la dieta fue el recurso más utilizado, lo que puede dar lugar a un menor aporte calórico.
Las complicaciones sépticas relacionadas con la nutrición artificial han sido motivo de preocupación, sobre todo con la nutrición parenteral, y se ha postulado que la nutrición enteral es más beneficiosa que la primera31-32. En nuestro trabajo se clasificaron las complicaciones infecciosas en dos grupos, las relacionadas con la vía venosa central y las relacionadas con las infecciones nosocomiales según las definiciones del CDC. Las relacionadas con los catéteres demostraron que las tasas de colonización y de infección local fueron del 4,98% y 1,24% del total de catéteres colocados con una densidad de incidencia de 0,4 y 0,1 por 100 días de catéter. Respecto a la sepsis relacionada con el catéter la tasa fue de 7,47% de los enfermos con una densidad de incidencia de 0,6 bacteriemias por 100 días de catéter. Cuando se comparan estos datos con los del estudio ENVIN nos encontramos que son muy similares. Según este estudio de vigilancia de la infección nosocomial en la unidades de cuidados intensivos españolas, la incidencia de bacteriemia relacionada con el catéter es de 6,5 bacteriemias por 100 enfermos y 0,45 bacteriemias por cada 100 días de catéter vascular33. Durante el tiempo del estudio el cuidado de las vías centrales se realizo de manera protocolizada siguiendo las recomendaciones vigentes34. En una serie reciente de bacteriemias relacionadas con catéter en la que comparaban dos grupos de enfermos, unos con llaves de 3 pasos y otros con sistema de conexiones desinfectables y sin agujas, la tasa de bacteriemias fue del 2,9%35.
Las infecciones nosocomiales de nuestra serie se recogieron durante la estancia en la UCI. Su incidencia global fue del 51,47%, con 0,6 episodios por enfermo y una densidad de incidencia se situó en 4,5 episodios por 100 días de NE. En el informe ENVIN del año 2002 la incidencia de infección nosocomial en una población de enfermos de UCI fue de 1,4 infecciones por enfermo estudiado33. En un estudio muy similar al nuestro en el que se analizaban las complicaciones sépticas de enfermos tratados con nutrición enteral o parenteral no se encontraron diferencias entre ambas36.
Tomando los datos de los tratados con nutrición enteral observamos que la frecuencia de complicaciones sépticas fue el 35,1% de los enfermos con un número de complicaciones por enfermo de 0,45 episodios, similar a nuestros resultados (0,5 episodios por enfermo). Una consideración aparte merecen las neumonías nosocomiales. El 35% de los enfermos de este estudio presentaron neumonía con una incidencia de broncoaspiración muy baja. Nuestra incidencia de 3,1 episodios por 100 días de nutrición enteral es sustancialmente inferior a los datos publicados por el ENVIN33 y superiores a los publicados en otro trabajo ya citado36. Una razón importante que puede justificar esta heterogeneidad en la cifras se debe a la ausencia de criterios diagnósticos homogéneos de neumonía. Un interés especial es la baja tasa de broncoaspiración e incluso de aspiración y vómitos que ofrecen nuestros resultados de menos del 7%, en contraposición con tasas muchos más altas publicadas en la literatura, del orden del 50% o superiores37.
Como conclusiones, señalaremos que el estudio pormenorizado de las complicaciones gastrointestinales relacionadas con la nutrición enteral el enfermo grave afectan a un porcentaje elevado de enfermos pero su densidad de incidencia durante el tiempo de uso es baja. Sin embargo, un porcentaje significativo de enfermos (16%) dejan de ser alimentados por esta vía. Tal como se ha demostrado recientemente, el uso de protocolos y guías de practica clínica y un correcto entrenamiento hacen que estas tengan poca relevancia clínica, que comporten pocas actuaciones terapéuticas y no sean causa de supresión definitiva de la nutrición enteral. Una incidencia baja de infecciones nosocomiales de otros grupos de nuestro país habla a favor de la eficacia del uso de protocolos de administración y tratamiento. En todo caso, la nutrición enteral es el mejor método para nutrir a los enfermos graves por la persistencia de malnutrición en los mismos y por su mayor eficacia respecto a la nutrición parenteral.
Agradecimientos
Los autores desean agradecer a los Dres. Albert Santacreu, Carlos Requena y a la empresa B. Braun, su inestimable colaboración para la realización de este estudio.
Miembros del Grupo de Trabajo de Metabolismo y Nutrición participantes en el estudio
Zabarte M (Hospital Nª Sra de Aranzazu, San Sebastián), Bonet Sarís A. (Hospital Joseph Trueta, Girona) Farré Viladrich M, Salvadó Salvat J (Hospital Universitari de La Vall D´Hebron, Barcelona), Acosta Escribano JA (Hospital Universitario de Alicante, Alicante), Blesa Malpica A (Hospital Clinico San Carlos, Madrid), Montejo González JC (Med-Surg ICU, Hospital 12 De Octubre, Madrid), Jiménez Jiménez J, Ortiz Leyba C (Hospital Virgen Del Rocio, Sevilla), Cuñat J, Arguedas J (Hospital Universitario La Fe, Valencia), Abella A, Blanco J (Hospital Universitario de Getafe, Madrid), Sanchez-Izquierdo Riera JA (Trauma ICU, Hospital 12 de Octubre, Madrid), Iturralde Yánez J (Hospital de Navarra), Ruiz Santana S, Peña Morant V (Hospital Universitario Dr Negrín, Las Palmas de Gran Canaria), Morán García V (Hospital de León, León), Albert Bonamusa I (Hospital Del Mar, Barcelona), García de Lorenzo y Mateos A (Hospital Universitario La Paz, Madrid), Mesejo Arizmendi A. (Hospital Clínico Universitario de Valencia, Valencia), Lander Azcona A (Hospital Virgen del Camino, Pamplona), Sanchez Miralles A (Hospital Universitario De San Juan, Alicante), López Martínez J (Hospital Severo Ochoa, Madrid), Rodríguez A, Serviá L (Hospital Universitari Arnau De Vilanova, Lleida), Tejada Artigas A (Trauma ICU, Hospital Miguel Server, Zaragoza), Martínez García P (Hospital Universitario De Puerto Real, Cadiz), Palacios Rubio V (Hospital Miguel Server, Zaragoza), Jara Clemente F (Hospital Mutua de Terrassa), De La Fuente O'connor E (Hospital Principe de Asturias, Madrid), Masdeu Eixarch G (Hospital Verge De La Cinta, Tortosa), Fernandez Ortega JF (Hospital Universitario Carlos Haya, Málaga), Casanovas Taltavull M (Hospital General de Igualada, Igualada), Domínguez LA (Hospital Universitario Río Ortega, Valladolid), Rey G (Hospital San Agustin, Aviles), González Ramos T (Hospital Virgen De La Vega, Salamanca), Martín Velasco M (Hospital Universitario La Candelaria, Tenerife), Arteta Arteta D (Clínica Asisa Santa Isabel, Sevilla), Macías S (Hospital General de Segovia, Segovia), Ortells Huerta X (Hospital Marina Alta, Alicante), Herrera Morillas F (Hospital Naval San Carlos, Cadiz), Gómez Tello V (Clinica Moncloa, Madrid), Serón Arbeola C (Hospital San Jorge, Huesca), Añón Elizalde JM (Hospital Virgen De La Luz, Cuenca), Fajardo López-Cuervo JJ (Hospital Militar Vigil De Quiñones, Se-villa), Zubillaga S (C.M. ICE, Madrid).
Referencias
1. ASPEN Board of Directors and The Clinical Guidelines Task Force. Guidelines for the use of parenteral and enteral nutrition in adult and pediatric patients. Moniotring for complications. JPEN 2002; 26 (suppl 1):39SA-41SA. [ Links ]
2. Lewis SJ, Egger M, Sylvester PA et al.: Early enteral feeding versus "nil by mouth" after gastrointestinal surgery: systematic review and meta-analysis of controlled studies. Br Med J 2001; 323:1-5. [ Links ]
3. Moore FA, Feliciano DV, Andrassy RJ et al.: Early enteral feeding, compared with parenteral, reduces postoperative septic complications. The results of a meta-analysis. Ann Surg 1992; 216:172-183. [ Links ]
4. Heyland KD, Dhaliwal R, Drower JW, Gramlich L, Dodk P, and the Canadian Critical Care Practice Guidelines Committee: Canadian Clinical Practice Guidelines for nutritional support in mechanically ventilated critically ill patients. JPEN 2003; 27:355-373. [ Links ]
5. Beale RJ, Bryg DJ, Bihary DJ: Immunonutrition in the critically ill: A systematic review of clinical outcome. Crit Care Med 1999; 27:2799-2805. [ Links ]
6. Heys SD, Walker LG, Smith I et al.: Enteral nutrition supplementation with key nutrients in patients with critical illness. A meta-analysis of randomized controlled clinical trials. Ann Surg 1999; 229:467-477. [ Links ]
7. Heyland DK, Novak F, Drover JW et al.: Should immunonutrition become routine in critically ill patients? A systematic review of the evidence. JAMA 2001; 286:944-953. [ Links ]
8. Montejo JC, Zarazaga A, López-Martínez J: Immunonutrition in the Intensive Care Unit. A Systematic Review and Consensus Statement. Clin Nutr 2003; 22:221-233. [ Links ]
9. Hervé Mentec, Hervé Dupont, Maria Bocchetti, Pascale Cani et al.: Upper digestive intolerance during enteral nutrition in critically ill patients:frecuency, risk factors and complications. Crit Care Med 2001; 29:1955-1961. [ Links ]
10. Stephen A. McClave, Harvy Sneider: Clinical use of gastric residual volumes as a monitor for patients on enteral tube feeding. JPEN 2002; 26:S43-S50. [ Links ]
11. Montejo JC, Grau T, Acosta J: Multicenter, prospective, randomized, single blind study comparing the efficacy and gastrointestinal complications of early jejunal feeding with early gastric feeding in critically ill patients. Crit Care Med 2002; 30:796-800. [ Links ]
12. Griensven M, Stalp M, Seekamp A: Ischemia-reperfusion directly increases pulmonary endothelial permeability in vitro. Shock 1999; 11:259-263 [ Links ]
13. Kompan L, Kremzar b, Gadzijev E et al.: Effects of early enteral nutrition on intestinal permeability and the development of multiple organ failure after multiple injury. Intensive Care Med 1999; 25: 157-161 [ Links ]
14. Caparros T, Lopez J, Grau T: Early enteral nutrition in critically ill patients with a high-protein diet enriched with arginine, fiber, and antioxidants compared with a standard high-protein diet. The effect on nosocomial infections and outcome. JPEN 2001; 25:299-308. [ Links ]
15. Torres A, Aznar R, Gatell JM et al.: Incidence, risk and prognosis factors for nosocomial pneumonia in mechanically ventilated patients. Am Rev Respir Dis 1990; 142:523-528. [ Links ]
16. Tejada A, Bello S, Chacón E et al.: Risk factors for nosocomial pneumonia in critically ill trauma. Crit Care Med 2001; 29:304-309. [ Links ]
17. Ibrahim EH, Mehringer L, Prentice D et al.: Early versus late enteral feeding of mechanically ventilated patients: results of a clinical trial. JPEN 2002; 26:174-181. [ Links ]
18. Montejo JC and the Nutritional and Metabolic Working Group of the Spanish Society of Intensive Care Medicine and Coronary Units (SEMICYUC): Enteral nutrition-related gastrointestinal complications in critically ill patients. A multicenter study. Crit Care Med 1999; 27:1447-1453. [ Links ]
19. Garner JS, Jarvis WR, Emoerl TG et al.: CDC definitions for nosocomial infections. Am J Infect Control 1988; 16:128-140. [ Links ]
20. Garner JS, Jarvis WR, Emoerl TG et al.: CDC definitions of nosocomial surgical site infections. A modification of CDC definitions of surgical wound infections. Am J Infect Control 1992; 21:606-608. [ Links ]
21. Veterans Affairs Total Parenetral Nutrition Cooperative Group: Perioperative total parenteral nutrition in surgical patients. N Eng J Med 1991; 325:525-532. [ Links ]
22. Planas M: Artificial nutrition support in intensive care units in Spain. The Nutrition and Metabolism Working Group of the Spanish Society of Intensive Care and Coronary Units (SEMYUC). Intens Care Med 1995; 21:842-846. [ Links ]
23. Preiser JC, Berre J, Carpentier Y et al.: Management of nutrition in European intensive care units: Results of a questionnaire. Intens Care Med 1999; 25:95-101. [ Links ]
24. Heyland DK, Schrotter-Noppe D, Drover JW et al.: Nutrition support in critical care setting: Current practice in Canadian ICUs. Opportunities for improvement? JPEN 2003; 27:74-83. [ Links ]
25. Iapichino G, Rossi C, Radrizan D, Simini B, Albicini M, Ferla L et al.: Nutrition given to critically ill patients during high level/complex care (on Italian ICUs). Clin Nutr 2004; 23:409-416. [ Links ]
26. Marik PE, Zaloga GP: Early enteral nutrition in acutelly ill patients: A systematic review. Crit Care Med 2001; 29:2264-2270. [ Links ]
27. Spain DA: When is the serious patient ready to be feed? JPEN 2002; 26:S62-S68. [ Links ]
28. McClave SA, Snider HL: Clinical use of gastric residual volume as a monitor for patients on enteral tube feeding. JPEN 2002; 26:S43-S50. [ Links ]
29. Booth CM, Heyland DK, Paterson WG: Gastrointestinal promotility drugs in the critical care setting: A systematic review of the evidence. Crit Care Med 2002; 28:1408-1411. [ Links ]
30. Green CJ: Fibra para la nutrición enteral. ¿Una nueva era? Nutr Hosp 2002; 27 (supl 2):1-6. [ Links ]
31. Marik PE, Pinsky M: Death by parenteral nutrition. Intensive Care Med 2003; 29:867-869. [ Links ]
32. Varga P, Griffiths R, Chiolero R et al.: Is parenteral nutrition guilty. Intensive Care Med 2003; 29:1861-1864. [ Links ]
33. Alvarez Lerma F, Palomar Martinez M, Olaechea Astigarraga P y Grupo de Estudio de Vigilancia de Infección Nosocomial en UCI: Estudio nacional de vigilancia de infección en Unidades de Cuidados Intensivos del año 2002. Med Intensiva 2005; 29:1-12. [ Links ]
34. O'Grady NP, Alexander M, Dellinger EP et al.: Guidelines for the prevention of intravacular catheter-related infections. Infect Control Hosp Epidemiol 2002; 23:759-769. [ Links ]
35. Yebenes JC, Vidaur L, Serra-Prats M et al.: Prevention of chatheter-related bloodstream infection in critically ill patients using a disinfectable, needle-free connector: A randomized controlled trial. Am J Infect Control 2004; 32:291-295. [ Links ]
36. Woodcock NP, Ziegler D, Palmer MD et al.: Enteral versus parenteral nutrition: a pragmatic study. Nutrition 2001;17:1-12. [ Links ]
37. DeLeege MH: Aspiration pneumonia: Incidence, mortality and at-risk populations. JPEN 2002; 26:S19-S25. [ Links ]