Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.22 no.3 Madrid may./jun. 2007
Cirugía gástrica como factor de riesgo nutricional
Gastric surgery as a nutritional risk factor
C. Cuerda*, M. Camblor*, I. Bretón*, C. Velasco*, L. Parón*, E. Hervás*, A. Muñoz-Calero** y P. García-Peris*
*Unidad de Nutrición.
**Servicio de Cirugía General. Hospital General Universitario Gregorio Marañón, Madrid. España.
Dirección para correspondencia
RESUMEN
Objetivo: El estómago tiene un papel importante en la digestión y absorción de nutrientes, por lo que los pacientes con resección gástrica están en riesgo nutricional. El objetivo del estudio fue evaluar el estado nutricional de pacientes gastrectomizados seguidos en una consulta externa de Nutrición de un Hospital General Universitario.
Material y métodos: Estudiamos de manera retrospectiva 54 pacientes (27 V, 27 M) con un tiempo mínimo de evolución desde la gastrectomía de 12 meses. La edad media fue 61 ± 14 años y la media de seguimiento 35 meses. La valoración nutricional incluyó antropometría, datos bioquímicos y valoración de la densidad mineralósea mediante DEXA. El estudio estadístico se realizó con pruebas no paramétricas.
Resultados: La indicación principal de la cirugía fue oncológica (85%). El 63% de los pacientes presentaban gastrectomía total. Los pacientes recibieron suplementos de hierro (43%), vitamina B12 (87%), calcio (18%) y vitamina D (17%). El 13% de los pacientes tenían bajo peso (IMC < 18,5). La incidencia de deficiencia de 25 OH vitamina D y de hiperparatiroidismo secundario fue de 45% y 76%, respectivamente. La incidencia de osteoporosis en columna fue del 46%. Comparadas con personas de su misma edad y sexo, los pacientes mantenían el 85,6% de la densidad mineral ósea.
Conclusiones: La pérdida de peso y la enfermedad metabólica ósea fueron las complicaciones más prevalentes en nuestros pacientes gastrectomizados. Por ello, creemos que es importante realizar un seguimiento nutricional en los pacientes gastrectomizados.
Palabras clave: Cirugía gástrica. Gastrectomía. Riesgo nutricional. Enfermedad metabólica ósea.
ABSTRACT
Background: The stomach has a role in the digestion and absorption of nutrients, so patients are in nutritional risk after gastric resection. The aim of this work was to study the nutritional status of postgastrectomy outpatients followed in our hospital.
Methods: We retrospectively studied 54 patients (27 M, 27 F) followed more than 12 months postgastrectomy. Mean age was 61 ± 14 yr and median follow-up was 35 months. The nutritional assessment included anthropometry, biochemical data and measurement of bone mineral density by dual-energy X-ray absorptiometry. The statistical analysis was performed by non-parametric tests.
Results: Malignancy was the most frequent indication (85%), 63% of patients had total gastrectomy. Patients were supplemented with iron (43%), B12 (87%), calcium (18%) and vitamin D (17%). 13% of patients had a BMI< 18.5. The incidence of 25 OH vitamin D deficiency and secondary hyperparathyroidism was 45% and 76%, respectively. The incidence of osteoporosis at lumbar spine was 46%. Matched with same age-sex people patients had 85.6% of bone mineral density.
Conclusions: The loss of weight and the metabolic bone disease were the most prevalent impairments after gastric resection. These impairments point to the importance of a nutritional surveillance of patients after gastric resection.
Key words: Gastric surgery. Postgastrectomy. Nutritional risk. Metabolic bone disease.
Introducción
El estómago, a través de sus procesos mecánicos y químicos, tiene un papel importante en la digestión y absorción de los diferentes nutrientes. Primero prepara la comida ingerida para la digestión y la absorción en el intestino delgado separándola en pequeñas porciones y regulando el flujo hacia el duodeno.
A pesar de que el intestino es el órgano principal en la digestión y absorción, una parte apreciable de la digestión de carbohidratos, grasas y proteínas ocurre en el estómago1. La mucosa del cuerpo y del fundus del estómago contiene las células principales que secretan pepsinógeno y lipasa gástrica. Las pepsinas rompen entre el 10-15% de las uniones de los péptidos de las proteínas de la dieta. El estómago contribuye a la digestión de la grasa emulsionando las grasas de la dieta para prepararlas para la digestión mediante las lipasas en el intestino y por la propia lipasa gástrica. Bajo condiciones normales, la lipasa gástrica digiere el 20-30% del total de grasas ingeridas en la dieta.
Las células parietales del cuerpo y fundus gástrico secretan HC1 y factor intrínseco, necesarios para la solubilización de las sales férricas y para la absorción de la vitamina B12 en el íleon.
Sin embargo, el principal problema de los pacientes gastrectomizados no es la ausencia del estómago como órgano digestivo, sino como reservorio de comida y regulador del flujo de la comida hacia el intestino delgado1.
La pérdida de peso y la anemia debida a la deficiencia de hierro, vitamina B12 y de folato ha sido descrita en pacientes con gastrectomía parcial y total2. Estas son las complicaciones más frecuentes en estos pacientes a corto y a largo plazo3. También se ha descrito como complicación a largo plazo la enfermedad metabólica ósea con características de osteomalacia, osteoporosis o ambas4,5. Varios estudios sugieren una reducción en la densidad mineral ósea después de gastrectomías parciales o totales y un aumento de la prevalencia de fracturas y deformidades vertebrales. Sin embargo, los estudios disponibles son contradictorios6,7.
El objetivo del estudio fue evaluar el estado nutricional y el metabolismo óseo de los pacientes gastrectomizados seguidos en una consulta externa de Nutrición y relacionarlo con el tipo de cirugía, la indicación, el tiempo de seguimiento y los cuidados nutricionales recibidos.
Material y métodos
Realizamos un estudio retrospectivo de corte trasversal que incluyó 54 pacientes gastrectomizados (27 V, 27M) con una edad media 61 ± 14 años (m ± SD) (rango 33-86), seguidos en nuestra consulta de Nutrición. Todos fueron operados al menos 12 meses antes (mediana 36 meses, rango 13-480). Debido a su influencia en el metabolismo óseo, los pacientes con insuficiencia renal o hiperparatiroidismo primario fueron excluidos del estudio. En el momento del estudio no hubo evidencia de recidiva del tumor en los pacientes oncológicos.
En la última revisión en la consulta se evaluó el estado nutricional mediante antropometría y parámetros bioquímicos (hemograma, colesterol, triglicéridos, proteínas totales, albúmina, transferrina, prealbúmina, calcio, fósforo, magnesio, zinc, hierro, ferritina, vitamina B12, ácido fólico, vitamina A, vitamina E, 25 OH vitamina D, y PTH).
La vitamina A y la E fueron determinadas mediante cromatografía líquida de alta resolución (HPLC) (Bio-rad, GmbH, Postfach, München, Germany). Los coeficientes de variación intra e inter-ensayo fueron < 5% para la vitamina A y < 10% para la vitamina E, respectivamente. La 25 OH vitamina D se determinó mediante RIA (DiaSorin, Stillwater, Minnesota, USA). El coeficiente de variación intra e inter-ensayo fue < 10%. La PTH intacta fue medida por quimioluminiscencia tras un enzimoinmunoanálisis en fase sólida (Immulite 2000, DPC). El coeficiente de variación intra e inter-ensayo fue < 5% y < 10%, respectivamente.
Las deficiencias nutricionales se establecieron de acuerdo a los límites normales de nuestro laboratorio. Para la medición del peso y de la talla se utilizó una balanza y un tallímetro (Seca) de precisión 0,2 kg y 0,1 cm respectivamente. El índice de masa corporal (IMC) se calculó dividiendo el peso (kg) de los pacientes entre su talla al cuadrado (m2). Se consideró bajo peso la presencia de un IMC menor de 18,5. El porcentaje de pérdida de peso se calculó con la diferencia entre el peso previo a la cirugía, referido por el paciente, y el peso en la revisión.
La densidad mineral ósea (DMO) se midió en 24 pacientes en columna (L1 - L4) y cuello femoral mediante DEXA (Lunar DPX-IQ, Lunar Radiation Corporation, Madison, WI, USA) con un coeficiente de variación de 1,04%. Se utilizó el T score para describir la desviación standard de la DMO en relación con el pico máximo de DMO en adultos jóvenes. De acuerdo con los criterios de la OMS, se consideró osteoporosis si el T score fue menor de -2,5 DE y osteopenia si el T score estaba entre -2,5 DE y -1 DE. Se utilizó el Z score para comparar la DMO en nuestros pacientes con personas de su misma edad y sexo y se expresó como porcentaje.
Los resultados están presentados como media ± DE, mediana y rango, y medidas de frecuencia (valores absolutos y porcentaje). El estudio estadístico se realizó con pruebas no paramétricas. Se consideró significativo un valor de p < 0,05.
Resultados
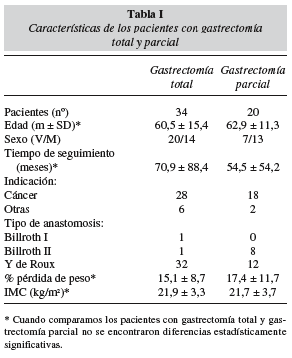
Las características de los pacientes se muestran en la tabla I. La mayoría de los pacientes habían sido intervenidos de gastrectomía total (63%). Los tipos de anastomosis fueron: Y de Roux (n = 44), Billroth II (n = 9), Billroth I (n = 1). La indicación más frecuente de la gastrectomía fue el cáncer gástrico (85%).
En el momento del estudio, el 41% de los pacientes estaban tratados con suplementos nutricionales orales, 43% con hierro (oral 87%, intramuscular 13%), 87% con vitamina B12 intramuscular, 46% recibía multivitamínicos orales, 18% calcio, 17% vitamina D y 11% enzimas pancreáticas.
Los pacientes habían perdido una media de 16 ± 10% (m ± SD) de su peso previo. El 70% de los pacientes habían perdido más del 10% del peso previo y el 24% más del 20%. Los pacientes presentaron un IMC de 21,8 ± 3,4, y en el 13% de los casos éste fue menor de 18,5. El porcentaje de pérdida de peso fue mayor en las mujeres, si bien la diferencia no fue estadísticamente significativa (19,1 ± 1,3 vs 13,2 ± 9,8, p = 0,07). Tampoco encontramos ninguna diferencia en el porcentaje de pérdida de peso con respecto al tipo de gastrectomía (tabla I), indicación (pacientes oncológicos 15,6 ± 9,2 vs pacientes no oncológicos 18,0 ± 13,5; ns), ni en el tiempo de evolución desde la gastrectomía (r = - 0,1; ns).
Los datos bioquímicos en el global del grupo y en los diferentes subgrupos (paciente oncológico vs no oncológico, gastrectomía total vs parcial) se muestran en la tabla II.
El 24% de los pacientes presentaba anemia microcítica (sin diferencia entre sexos) y el 29% linfopenia. El 16% de los pacientes presentaba hipoproteinemia y el 6% hipoalbuminemia. Sólo el 13% de los pacientes presentaba bajos niveles de hierro y el 15% presentaba valores de ferritina por debajo del rango normal del laboratorio. Aunque las mujeres presentaban niveles más bajos de ferritina, la diferencia no fue estadísticamente significativa (p = 0,09). Las deficiencias de vitamina B12, folato, zinc, cobre, magnesio, calcio, fósforo y vitamina A se encontraron en menos del 10% de los pacientes.
Las mujeres mostraron valores más altos de cobre (127,4 ± 39,9 vs 101,0 ± 24,8; p < 0,05), ácido fólico (8,8 ± 3,9 vs 6,2 ± 3,6; p < 0,05) y vitamina E (1.399,6± 431,8 vs 1.032,4 ± 278,8; p < 0,05), y niveles más bajos de hemoglobina (12,7 ± 1,3 vs 13,7 ± 1,2; p < 0,01). Cuando comparamos los parámetros bioquímicos entre los pacientes con gastrectomía total y gastrectomía parcial solo encontramos diferencias estadísticamente significativas en los niveles de lípidos y en el número de linfocitos (tabla II). Los parámetros bioquímicos fueron similares en los pacientes oncológicos y los no oncológicos, exceptuando la vitamina E, que fue más baja en los pacientes oncológicos (tabla II).
A pesar del tratamiento, el 45% de los pacientes tenían niveles bajos de 25-OH vitamina D, y el 76% presentaban hiperparatiroidismo secundario. Ambos resultados no se correlacionan con la edad (r = 0,27, ns; r = 0,26, ns), el sexo (p = 0,4; p = 0,6), el tipo de gastrectomía (tabla II), indicación (tabla II) ni con el tiempo de seguimiento (r = -0,04, p = 0,6; r = 0,04, p = 0,8).
Los datos de la DMO se muestran en la tabla III. La incidencia de osteoporosis en la columna lumbar fue del 46% (58% mujeres, 33% hombres) y la de osteopenia fue del 30% (33% mujeres, 25% hombres). Comparados con personas de su misma edad y sexo (Z score) los pacientes conservaban el 85,6% de la DMO (86% mujeres, 85% hombres). La incidencia de osteoporosis en cuello femoral fue del 33% (25% mujeres, 42% hombres) y la de osteopenia fue del 58% (66% mujeres, 50% hombres). Los pacientes tenían un 83,6% (87% mujeres, 79% hombres) de la DMO comparado con personas de su misma edad y sexo (Z score).
Los hombres presentaron mayor DMO (p < 0,05) estando esta correlacionada negativamente con la edad (r: -0,58; p < 0,01) y con la pérdida de peso (r: - 0,53; p < 0,01). No se encontró correlación con el tipo de gastrectomía (p = 0,9), indicación (p = 0,5), tiempo de seguimiento (r = -0,003, p = 0,9), o los niveles plasmáticos de vitamina D (r = -0,23, p = 0,3) y PTH (r = 0,20, p = 0,4).
Discusión
A pesar del descenso en la indicación de cirugía gástrica en el tratamiento de la enfermedad péptica, la gastrectomía continúa siendo la primera opción en el tratamiento del cáncer gástrico. Además el uso de esta técnica está aumentando en los últimos años para el tratamiento de la obesidad mórbida. Estos pacientes están en riesgo de desarrollar las complicaciones metabólicas ya descritas en pacientes gastrectomizados por enfermedad péptica3.
La pérdida de peso es muy frecuente después de la cirugía gástrica8. Como ha sido descrito anteriormente por otros autores3, hemos observado que las mujeres pierden más peso aunque, debido al número de pacientes, esta diferencia no fue estadísticamente significativa. Sin embargo, a diferencia de otros autores no hemos encontrado ninguna diferencia entre la gastrectomía total y parcial9.
Probablemente, la principal causa de la pérdida de peso sea el descenso en la ingesta dietética. Este descenso en la ingesta se produce como consecuencia de la saciedad precoz, dispepsia, síndrome de dumping y de factores emocionales3. Está descrito en el estudio de Braga y cols., que la ingesta dietética media un mes después de la cirugía era de 1.458 kcal/día, aumentando hasta 2.118 kcal/día seis meses después10.
Además, estos pacientes presentan cierto grado de malabsorción debido a diferentes mecanismos: sobrecrecimiento bacteriano11, disminución del tiempo de tránsito intestinal12, pérdida de la superficie de absorción en el duodeno13 y disminución de la secreción pancreática exocrina14.
Como consecuencia de la malabsorción de hierro, vitamina B12 y ácido fólico se produce anemia en más del 50% de los pacientes gastrectomizados8. En nuestro estudio, la incidencia de anemia fue menor en los pacientes que seguían las revisiones en la consulta regularmente. La deficiencia de hierro es común en estos pacientes3 debido a la disminución en la secreción de ácido que empeora la solubilidad de los iones férricos y disminuye la conversión a iones ferroso15 y a que el duodeno es el lugar más importante para su absorción15. Por eso, en mujeres premenopáusicas con cirugía reconstructiva en Y de Roux algunos autores recomiendan el uso de suplementos orales de hierro para prevenir el desarrollo de anemia16. La suplementación oral es la forma más usual, pero en algunos pacientes debe administrarse de forma parenteral (intramuscular o intravenoso) debido a malabsorción e intolerancia digestiva17.
Después de la gastrectomía total y en algunos casos de gastrectomía parcial, la cobalamina (vitamina B12) ingerida en la dieta no se absorbe. Los mecanismos implicados son: deficiencia del factor intrínseco1, aumento del pH gástrico después de la gastrectomía parcial1, sobrecrecimiento bacteriano11. Los grandes depósitos de esta vitamina en el hígado evitan el desarrollo de manifestaciones clínicas de la deficiencia de cobalamina a corto plazo3. A pesar de que el tratamiento más usual es la administración de vitamina B12intramuscular después de la gastrectomía, algunos autores sugieren que la administración oral puede ser suficiente en algunos pacientes16,18.
La incidencia de la deficiencia de folato es menor que la del hierro y la vitamina B12. Se produce como consecuencia de la exclusión duodenal y puede prevenirse con multivitamínicos por vía oral16.
Se ha descrito la aparición de osteomalacia, descenso en la DMO y un aumento del riesgo de fracturas después de resecciones gástricas por úlceras pépticas4,5. Nosotros hemos observado una alta prevalencia de deficiencia de 25 OH vitamina D y de hiperparatiroidismo secundario en nuestra serie, que no está relacionada con el sexo, el tipo de gastrectomía, la indicación o el tiempo de evolución desde la cirugía. A pesar de que la edad media en nuestros pacientes era alta y la deficiencia de vitamina D en personas mayores puede alcanzar el 30-50% de los casos19, no creemos que ésta sea la principal razón de nuestros resultados ya que no hemos encontrado ninguna correlación entre los niveles de vitamina D y la edad de los pacientes.
Otros autores también han descrito bajos niveles de vitamina D e hiperparatiroidismo secundario en pacientes gastrectomizados9. Bisballe y cols., realizaron biopsias óseas en 68 pacientes gastrectomizados. En su estudio, el 62% de los pacientes tenían aumento de la superficie del osteoide, el 56% aumento del grosor del osteoide, el 24% presentaron retraso en el tiempo de mineralización y el 18% cumplían criterios diagnósticos de osteomalacia20.
Por otra parte, Liedman y cols., encontraron niveles altos de PTH con valores normales de calcitriol en suero en sólo algunos de sus pacientes gastrectomizados6. En su artículo consideran varias explicaciones a las divergencias con otros autores9: todos sus pacientes habían recibido consejo dietético por dietistas después de la cirugía y algunos de ellos estaban tomando suplementos extra de calcio (1.000 mg al día), y vitamina D (400 UI al día), además, la población sueca ingiere diariamente productos fortificados con vitamina D, por lo que, probablemente, sus resultados no son extrapolables a otras poblaciones.
Nosotros encontramos un alto porcentaje de osteopenia y osteoporosis en nuestro estudio, coincidiendo con estudios previos9,21. A pesar de que podría deberse a la edad de los pacientes, cuando comparamos con personas de la misma edad (Z-score) también encontramos un descenso en la densidad mineral ósea. La pérdida de DMO fue mayor en mujeres y en pacientes con mayor pérdida de peso.
Otros autores han encontrado resultados similares7,22. En el estudio de Adachi y cols., también se evaluó la DMO mediante DEXA en columna lumbar en 59 pacientes gastrectomizados encontrando un 37% de osteoporosis (18% en hombres y 71% en mujeres), y un 85,9% de DMO con respecto a personas de la misma edad y sexo. La pérdida de DMO fue asociada a la edad y al sexo, pero no al tipo de gastrectomía o al tiempo de evolución después de la cirugía7. Inoue y cols., observaron que esta pérdida ocurría en los 5 primeros años después de la resección gástrica23.
Sin embargo, Liedman y cols., no encontraron ninguna diferencia cuando compararon la DMO de sus pacientes con personas de la misma edad y sexo6.
La Asociación Americana de Gastroenterología publicó recientemente un documento basado en la evidencia sobre la EMO en pacientes gastrectomizados (tabla IV)24.
La etiología de las alteraciones del metabolismoóseo después de la gastrectomía es multifactorial. Estos pacientes tienen una ingesta reducida (debido a una intolerancia a productos lácteos) y/o una malabsorción de calcio y vitamina D (debido a la exclusión duodenal, al rápido tránsito intestinal, a la malabsorción grasa)4,5. En pacientes astrectomizados, el descenso de la acidez gástrica puede estar implicado en la peor absorción del calcio. Adachi y cols., estudiaron la DMO en pacientes tratados durante más de 2 años con antagonistas de los receptores H2. Ellos concluyen que estos tratamientos tienen poca influencia en la DMO, y sugieren que el aumento del pH gástrico no siempre está asociado con la osteoporosis después de la gastrectomía25.
Gertner y cols., observaron que en pacientes gastrectomizados con osteomalacia, la absorción oral de 25 OH vitamina D era normal26. Davies y cols., encontraron resultados similares en pacientes con gastrectomía parcial27. No está claro por qué estos pacientes tienen niveles bajos de vitamina D, especialmente cuando la dieta no es la principal fuente de dicha vitamina. En estudios posteriores, estos autores observaron un aumento del catabolismo de la 25 OH vitamina D, y encontraron que el tratamiento con calcio oral podría prevenir el hiperparatiroidismo secundario que presentan estos pacientes28. Como se ha observado en ratas29, la explicación podría estar en que la baja ingesta y/o la malabsorción de calcio produciría hiperparatiroidismo secundario y elevación de la 1.25 OH vitamina D asociado con aumento del aclaramiento de su precursor (25 OH vitamina D). Si esto fuera cierto, la administración oral de sales de calcio sería suficiente para descender los niveles de PTH en estos pacientes. Por el contrario, en el estudio de Ichikawa y cols., sólo aquellos pacientes que recibieron suplementos orales de calcio y vitamina D tuvieron un descenso en los niveles de PTH comparado con los pacientes que sólo recibieron suplementos de calcio30. Por otra parte, la estimación de la absorción de calcio mediante métodos isotópicos ha mostrado concentraciones normales o bajas de 47Ca después de la gastrectomía31,32.
Otro mecanismo implicado en la enfermedad mineralósea en pacientes gastrectomizados podría ser la falta de gastrina ya que el eje gastrina - calcitonina parece jugar un papel importante en la homeostasis del calcio33. En ratas, se ha descrito recientemente que la pérdida de DMO tras la gastrectomía se correlaciona con la resección del fundus gástrico, siendo necesario mantener entre el 10-30% de la mucosa del fundus para preservar la masa ósea34. Estos autores concluyen que podría explicarse por la deficiencia de diferentes hormonas (grelina, pancreastatina...) que son producidas por las células de la mucosa del fundus.
Hay poca información sobre la utilidad de los bifosfonatos en el tratamiento de la osteoporosis en pacientes gastrectomizados. Aunque algunos autores apoyaban que estos pacientes serían más resistentes a este tratamiento que las mujeres posmenopáusicas35, recientemente Suzuki y cols., observaron mejoría en la DMO de la columna lumbar en 13 pacientes con gastrectomía o bypass gástrico con osteopenia Vitamina D-resistentes tratados con Alendronato y Vitamina D durante 2 años36.
Como conclusión, aunque los pacientes con gastrectomía están en riesgo de desarrollar enfermedad metabólica ósea, con los datos actuales no es posible establecer si el tratamiento con calcio y/o vitamina D es efectivo para su prevención y tratamiento. Desconocemos la correcta dosificación de estos micronutrientes en este grupo de pacientes, aunque intuimos que pueden existir diferencias entre distintas poblaciones. Respecto a la utilización de otras terapias en el tratamiento de la osteoporosis (bifosfonatos, PTH,...) existen pocos estudios que avalen su utilidad en estos pacientes.
Agradecimientos
Agracedemos a la Dra. Lola Vigil del Servicio de Medicina Preventiva su colaboración en la revisión del manuscrito.
Referencias
1. Stenson WF. The esophagus and stomach. En: Shils ME, Olson JA, Shike M, Ross AC, Eds. Modern Nutrition in Health and Disease, 9th edn. Baltimore: Williams & Wilkins, 1999: 1125-1133. [ Links ] 2. Grant JP, Chapman G, Russell MK. Malabsorption associated with surgical procedures and its treatment. Nutrition in Clinical Practice 1996; 11:43-52. [ Links ] 3. Tovey FI, Godfrey JE, Lewin MR. A gastrectomy population: 25-30 years on. Postgrad Med J 1990; 66(776):450-456. [ Links ] 4. Thompson GR, Lewis B, Booth CC. Vitamin D absorption after partial gastrectomy. Lancet 1966; 1:457-458. [ Links ] 5. Deller DJ, Edwards RG, Addison M. Calcium metabolism and the bones after partial gastrectomy. The nature and cause of the bone disorder. Aust Ann Med 1963; 12:295-309. [ Links ] 6. Liedman B, Henningsson A, Mellström D, Lundell L. Changes in bone metabolism and body composition after total gastrectomy. Results of a longitudinal study. Digestive Diseases and Sciences 2000; 45:819-824. [ Links ] 7. Adachi Y, Shiota E, Matsumata T, Iso Y, Yoh R, Kitano S. Osteoporosis after gastrectomy: bone mineral density of lumbar spine assessed by dual-energy X-ray absorptiometry. Calcif Tissue Int 2000; 66:119-122. [ Links ] 8. Harju E. Metabolic problems after gastric surgery. Int Surg 1990; 75:27-35. [ Links ] 9. Zittel TT, Zeeb B, Maier GW, Kaiser GW, Zwirner M, Liebich H, Starlinger M, Becker HD. High prevalence of bone disorders after gastrectomy. Am J Surg 1997; 174:431-438. [ Links ] 10. Braga M, Zuliani W, Foppa L, Di Carlo V, Cristallo M. Food intake and nutritional status after total gastrectomy: results of a nutritional follow-up. Br J Surg 1988; 75:477-480. [ Links ] 11. Broido PW, Gorbach SL, Nyhus LM y cols.: Microflora of the gastrointestinal tract and surgical malabsorption syndromes. Surg Gynecol Obstet 1972; 135:449-460. [ Links ] 12. Lundh G. Intestinal digestión and absorption after gastrectomy. Acta Chir Scand 1958; 1:231-236. [ Links ] 13. MacGregor I, Parent J, Meyer JH. Gastric emptying of liquid meals and pancreatic and biliary secretion after subtotal gastrectomy or truncal vagotomy and pyloroplasty in man. Gastroenterology 1977; 72:195-205. [ Links ] 14. Friess H, Böhm J, Müller MW, Glasbrenner B, Riepl RL, Malfertheiner P, Büchler MW. Maldigestion after total gastrectomy is associated with pancreatic insufficiency. Am J Gastroenterol 1996; 91:341-347. [ Links ] 15. Lloyd DA, Valberg LS. Serum ferritin and body iron ferritin after gastric operations. Am J Dig Dis 1977; 22:598-604. [ Links ] 16. Brolin RE, Gorman JH, Gorman RC, Petschenik AJ, Bradley LJ, Kenler HA, Cody RP. Are vitamin B12 and folate deficiency clinically important after roux-en-Y gastric bypass? J Gastrointest Surg 1998; 2:436-442. [ Links ] 17. Kumpf VJ. Update on parenteral iron therapy. NCP 2003; 18:318-326. [ Links ] 18. Adachi S, Kawamoto T, Otsuka M, Todoroki T, Fukao K. Enteral vitamin B12 supplements reverse postgastrectomy B12 deficiency. Ann Surg 2000; 232(2):199-201. [ Links ] 19. Mowe M, Böhmer T, Haug E. Serum calcidiol and calcitriol concentrations in elderly people: variations with age, sex, season and diseases. Clin Nutr 1996; 15:201-6. [ Links ] 20. Bisballe S, Eriksen EF, Melsen F, Mosekilde L, Sorensen OH, Hessov I. Osteopenia and osteomalacia after gastrectomy: interrelations between biochemical markers of bone remodelling, vitamin D metabolites, and bone histomorphometry. Gut 1991; 32:1303-1307. [ Links ] 21. Mellstrom D, Johansson C, Johnell O, Lindstedt G, Lundberg PA, Obrant K, Schöön IM, Toss G, Ytterberg BO. Osteoporosis, metabolic aberrations, and increased risk for vertebral fractures after partial gastrectomy. Calcif Tissue Int 1993; 53:370-377. [ Links ] 22. Heiskanen JT, Kröger H, Pääkkönen M, Parviainen MT, Lamberg-Allardt C, Alhava E. Bone mineral metabolism after total gastrectomy. Bone 2001; 28:123-127. [ Links ] 23. Inoue K, Shiomi K, Higashide S, Kan N, Nio Y, Tobe T, Shigeno C, Konishi J, Okumura H, Yamamuro T, Fukunaga M. Metabolic bone disease following gastrectomy: assessment by dual-energy X-ray absorptiometry. Br J Surg 1992; 78:321-324 [ Links ] 24. Bernstein CN, Leslie WD, Leboff MS. AGA technical review on osteoporosis in gastrointestinal diseases. Gastroenterology 2003; 124 (3):795-841. [ Links ] 25. Adachi Y, Shiota E, Matsumata T, Iso Y, Yoh R, Kitano S. Bone mineral density in patients taking H2-receptor antagonist. Calcif Tissue Int 1998; 62:283-5. [ Links ] 26. Gertner JM, Lilburn M, Domenech M. 25-Hydroxycholecalciferol absorption in steatorrhoea and postgastrectomy osteomalacia. Br Med J 1977; 1(6072):1310-1312. [ Links ] 27. Davies M, Mawer EB, Krawitt EI. Comparative absoption of vitamin D3 and 25-hydroxyvitamin D3 in intestinal disease. Gut 1980; 21:287-292. [ Links ] 28. Davies M, Heys SE, Selby PL, Berry JL, Mawer EB. Increased catabolism of 25-Hydroxyvitamin D in patients with partial gastrectomy and elevated 1,25-Dihydroxyvitamin D levels. Implications for metabolic bone disease. J Clin Endocrinol Metab 1997; 82(1):209-212. [ Links ] 29. Clements MR, Johnson L, Fraser DR. A new mechanism for induced vitamin D deficiency in calcium deprivation. Nature 1987; 325:62-65. [ Links ] 30. Ichikawa C, Takiguchi N, Koda K, Oda K, Suzuki H, Miyazaki M. Early phase metabolic disorders after gastrectomy: influence of active vitamin D treatment. Dig Dis Sci 2002; 47(8):1886-1890. [ Links ] 31. Nilas L, Christiansen C, Christiansen J. Regulation of vitamin D and calcium metabolism after gastrectomy. Gut 1985; 26:252-257. [ Links ] 32. Gregory DH, Van Uelft R. Calcium absoption following gastric resection. Am J Gastroenterol 1972; 57:34-40. [ Links ] 33. Filipponi P, Gregorio F, Cristallini S, Mannarelli C, Blass A, Scarponi AM, Vespasiani G. Partial gastrectomy and mineral metabolism effects on gastrin-calcitonin release. Bone Miner 1990; 11:199-208. [ Links ] 34. Lehto-Axtelius D, Chen D, Surve VV, Hakanson R. Post-gastrectomy osteopenia in the rat. Scand J Gastroenterol 2002; 4:437-443. [ Links ] 35. Tovey FI, Hall ML, Ell PJ, Hobsley M. Cyclical etidronate therapy and postgastrectomy osteoporosis. Br J Surg 1994; 81:1168-1169. [ Links ] 36. Suzuki Y, Ishibasi Y, Omura N, Kawasaki H, Yanaga K, Abo M, Usashima M. Alendronato improve Vitamina D-Resistant osteopenia triggered by gastrectomy in patients with gastric cancer followed long term. J Gastrointest Surg 2005; 9(7):955-60. [ Links ] ![]() Dirección para correspondencia:
Dirección para correspondencia:
Cristina de la Cuerda Compés.
Unidad de Nutrición.
Hospital General Universitario Gregorio Marañón.
Doctor Esquerdo, 36
28007 Madrid
E-mail: mcuerda.hgugm@salud.madrid.org
Recibido: 19-I-2007.
Aceptado: 5-III-2007.