Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.25 no.6 Madrid nov./dic. 2010
Estudio transversal sobre la prevalencia de la Enfermedad Metabólica Ósea (EMO) y Nutrición Parenteral Domiciliaria (NPD) en España: datos del Grupo NADYA
Transversal study on the prevalence of Metabolic Bone Disease (MBD) and Home Parenteral Nutrition (HPN) in Spain: data from NADYA group
C. Martínez1, N. Virgili2, C. Cuerda3, L. Chicharro4, P. Gómez1, J. M. Moreno5, J. Álvarez6, E. Martí7, P. Matía8, M. A. Penacho9, C. Garde10, D. De Luis11, M. Gonzalo12, G. Lobo13 y Grupo NADYA-SENPE
1Hospital Universitario Central de Asturias. Oviedo.
2Hospital de Bellvitge. Hospitalet de Llobregat. Barcelona.
3Hospital Gregorio Marañón. Madrid.
4Hospital Vall d´Hebrón. Barcelona.
5Hospital 12 de Octubre. Madrid.
6Hospital Príncipe de Asturias. Alcalá de Henares. Madrid.
7Hospital General de Valencia.
8Hospital Clínico de Madrid.
9Hospital del Bierzo. León.
10Hospital de Donostia.
11Hospital Universitario Río Ortega. Valladolid.
12Hospital Universitario Carlos Haya. Málaga.
13Hospital Universitario Virgen de las Nieves. Granada. España.
Dirección para correspondencia
RESUMEN
Los pacientes con insuficiencia intestinal que reciben NPD presentan un elevado riesgo de presentar EMO. El origen de esta afectación ósea es multifactorial y depende en gran parte de la enfermedad de base que origina la necesidad del soporte. En nuestro medio no disponemos de datos acerca de la prevalencia de esta enfermedad, por lo que el grupo NADYA-SENPE ha patrocinado este estudio transversal para intentar conocer la prevalencia de la EMO.
Material y métodos: Se han recogido datos retrospectivos de 51 pacientes pertenecientes a 13 hospitales. La encuesta realizada incluía datos demográficos y los datos clínicos más relevantes que pudieran influir en la aparición de EMO. También se han registrados los datos analíticos más significativos para este proceso (calciuria, PTH, 25 OH vitamina D) y los resultados de la primera y la última densitometría realizadas.
Resultados: Solamente 21 pacientes tenían realizada una densitometría en el momento de iniciar la NPD. La calidad del hueso está alterada al inicio de la NPD en un porcentaje significativo de casos (52%) Tras un seguimiento medio de 6 años ese porcentaje se eleva hasta el 81%. Dado el carácter retrospectivo del estudio y el escaso número de sujetos no es posible determinar el papel que juega la NPD en la etiología de la EMO. Sólo un 35% de los pacientes presentan niveles de vitamina D por encima de los niveles recomendados y la mayoría de ellos no recibe suplementación específica.
Conclusiones: La NPD se asocia a un riesgo muy elevado de presentar EMO, por tanto es necesario disponer de protocolos de actuación que permitan detectar precozmente este problema y orientar el seguimiento y tratamiento de estos pacientes.
Palabras clave: Nutrición parenteral domiciliaria. Osteoporosis.
ABSTRACT
Patients with intestinal failure who receive HPN are at high risk of developing MBD. The origin of this bone alteration is multifactorial and depends greatly on the underlying disease for which the nutritional support is required. Data on the prevalence of this disease in our environment is lacking, so NADYA-SEMPE group has sponsored this transversal study with the aim of knowing the actual MBD prevalence.
Material and methods: Retrospective data from 51 patients from 13 hospitals were collected. The questionnaire included demographic data as well as the most clinically relevant for MBD data. Laboratory data (calciuria, PTH, 25 -OH -vitamin D) and the results from the first and last bone densitometry were also registered.
Results: Bone mineral density had only been assessed by densitometry in 21 patients at the moment HPN was started. Bone quality is already altered before HPN in a significant percentage of cases (52%). After a mean follow up of 6 years, this percentage increases up to 81%. Due to retrospective nature of the study and the low number of subjects included it has not been possible to determine the role that HPN plays in MBD etiology. Only 35% of patients have vitamin D levels above the recommended limits and the majority of them is not on specific supplementation.
Conclusions: HPN is associated with very high risk of MBD, therefore, management protocols that can lead to early detection of the problem as well as guiding for follow up and treatment of these patients are needed.
Key words: Home parenteral nutrition. Osteoporosis.
Introducción
La prevalencia real de la enfermedad metabólica ósea (EMO) en los pacientes que reciben nutrición parenteral domiciliaria (NPD) no se conoce en nuestro medio. Datos de estudios previos parecen indicar que, en este grupo de pacientes, un elevado porcentaje de casos presenta alteración de la calidad del hueso, porcentaje que, según algunas series, puede llegar hasta el 100%1,2,3. Tampoco está claro el papel que juega la NPD en la pérdida de masa ósea y cada vez existe más consenso en reconocer que la EMO tiene un origen multifactorial dependiendo en gran medida de la enfermedad subyacente que origina la insuficiencia intestinal4.
Además de los factores de riesgo tradicionales para la aparición de osteoporosis (sexo femenino, menopausia, edad avanzada, bajo peso, consumo de tabaco o alcohol, inactividad física y ciertos fármacos)5 se pueden añadir otros relacionados con la NPD por posible aporte insuficiente de nutrientes esenciales para el metabolismo óseo (calcio, fosfato, vitamina D), o por efecto tóxico de algunos compuestos de la NP, como es la contaminación por aluminio (Al) o por la propia vitamina D. El Al, que disminuye los niveles de PTH y por tanto de 1-25 OH vitamina D, ha sido una de las causas que, hasta hace unos años, más se han relacionado con la afectación ósea; no obstante, desde que se dejaron de usar los hidrolizados de caseína apenas existe contaminación de la fórmula por ese metal, aunque sigue estando presente, en pequeñas cantidades, en las sales de calcio y de fosfato así como en los preparados de vitaminas y de elementos traza6-8. La propia vitamina D administrada parenteralmente en algunos casos parece que puede tener un efecto negativo en la formación de hueso9. La hipercalciuria inducida por la perfusión de los nutrientes también podría jugar un papel relevante, al haberse observado una correlación positiva entre la cantidad administrada de aminoácidos, glucosa, sodio y calcio y la eliminación urinaria de este último10.
Existe otra serie de factores asociados a la enfermedad de base que favorecen la pérdida de masa ósea como la acidosis metabólica que altera el metabolismo de la vitamina D y el empleo de glucocorticoides que, como es conocido, disminuyen la actividad de los osteoblastos y pueden aumentar la de los osteoclastos, además de inhibir la absorción de calcio intestinal y de frenar la producción de hormonas sexuales11.
El grupo NADYA-SENPE ha impulsado el pasado año la publicación de un protocolo para el diagnóstico y tratamiento de la EMO en pacientes en programa de NPD4, planteándose además realizar un estudio transversal para conocer la situación actual en nuestro país que pueda servir de base para futuros estudios prospectivos y así valorar la influencia de los distintos factores relacionados con la NPD en el desarrollo y evolución de la EMO.
Métodos
Hemos recogido datos retrospectivos de 51 pacientes (35 mujeres, 16 varones) pertenecientes a 13 hospitales de 7 comunidades autónomas. Se han incluido todos los pacientes que recibían NPD en noviembre de 2007 en los hospitales participantes, excluyéndose únicamente aquellos que, en el momento de iniciar el soporte domiciliario, tenían pocas expectativas de supervivencia a corto plazo (procesos oncológicos avanzados).
La encuesta remitida a los hospitales participantes incluía la recogida de datos demográficos (edad, sexo, menopausia), el diagnóstico que motivó el soporte nutricional, la fecha de inicio de la NPD, si habían recibido tratamiento con esteroides y/o bifosfonatos y el resultado de la primera y última densitometría realizada. También se recogieron datos clínicos y analíticos que podrían ser de interés a la hora de relacionar la NPD con la alteración ósea: índice de masa corporal (IMC), número de bolsas que se aportaban a la semana, si recibían tratamiento con suplementos orales de calcio y/o vitamina D, además de determinación de calciuria, de PTH y de 25 OH vitamina D.
A la hora de valorar los resultados de la densitometría ósea, se ha optado por recoger el t- score (puntuación que expresa la densidad mineral ósea comparada con adultos sanos jóvenes) ya que era más accesible en todos los hospitales que el valor z-score (que expresa la densidad mineral ósea ajustada por edad y sexo), aunque hoy en día se reconoce que para mujeres premenopáusicas y varones este segundo parámetro es más fiable. Hemos aplicado los criterios de la OMS a la hora de definir osteopenia (t-score entre -1 y -2,5 desviaciones estándar) y osteoporosis (t-score inferior a -2,5 desviaciones estándar).
El densitómetro utilizado en este estudio fue distinto en cada hospital y no existió una calibración entre centros, lo cual puede alterar la interpretación de los resultados.
Todos los análisis estadísticos se realizaron mediante SPSS 12.0 (SPSS, Chicago, Illinois, Estados Unidos). Los valores referidos de p están basados en test de dos colas con límite de significación estadística en p < 0,05. Las comparaciones transversales entre grupos para variables cuantitativas se realizaron mediante análisis de la varianza (ANOVA). Para la comparación de proporciones se usó la prueba de la χ2.
Resultados
La edad media al iniciar NPD era 43,98 ± 16,41 años (15-74). En la figura 1 se aprecia la distribución por décadas de la edad al comienzo de la NPD.
La principal indicación que motivó la NPD fue el síndrome de intestino corto postquirúrgico en relación con diversos procesos (47%) seguido por las lesiones intestinales ocasionadas por la radioterapia (17,6%). En tercer lugar figuran distintas enfermedades que cursan con alteración de la motilidad intestinal (15,6%) y otros procesos como tumores, SIDA, enfermedad inflamatoria intestinal, etc agrupan el resto de indicaciones (19,8%)
De las 35 mujeres incluidas en el estudio 16 eran postmenopáusicas con un tiempo medio transcurrido desde la desaparición de los ciclos menstruales de 6,5 ± 2,1 años (1-24).
La duración media de la NPD era de 60,54 ± 64,4 meses (1-273). El número de bolsas semanales que recibía cada paciente oscilaba entre 1 y 7, con una media de 5,6 ± 1,6, destacando que el 86% (44 enfermos) necesitaba, al menos, 4 bolsas a la semana y de ellos 24 (el 47% del total) dependía diariamente de la NP.
El IMC medio en el momento de la recogida de datos era de 20,33 ±3,08 kg/m2 (15,6-28,9); en 11 casos (21,5%) era inferior a 18 y solo 4 (7,8%) presentaban discreto sobrepeso.
Respecto a la administración de corticoides, 5 pacientes (10%) habían recibido tratamiento esteroideo en algún momento durante la evolución de la enfermedad.
Los niveles de 25 OH vitamina D están recogidos en 39 de los 51 pacientes. Se aprecia un déficit severo en 3 de ellos (7,6%) al presentar cifras inferiores a 10 ng/ml, recibiendo 2 de ellos suplementos orales de vitamina D; otros 12 (31%), presentaban una carencia moderada, con valores entre 10 y 20 ng/ml y de los cuales solo en 2 casos se informa de que reciben tratamiento oral complementario. En los 24 casos restantes, las cifras eran superiores a 20 ng/ml. Si se aceptan las últimas recomendaciones respecto a los niveles aconsejables de 25 OH vitamina D (> 30 ng/ml), solo 14 de los 39 pacientes (35,8%) cumplían este criterio, destacando que 6 de ellos estaban tratados con dosis orales complementarias.
La calciuria solo consta en 16 sujetos, estando elevada por encima de 300 mg/24 horas en 3 casos (18,7%) y por debajo de 100 mg/24 horas en otros 6 (37,5%).
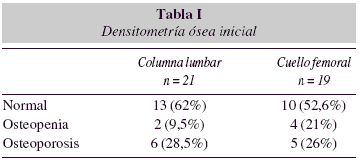
Al inicio de la NPD únicamente 21 pacientes (41%) tenían realizada una densitometría ósea en un plazo de 6 meses anterior o posterior al comienzo del soporte nutricional, con un T-score medio de -1,35 ± 1,72 desviaciones standard a nivel lumbar y -1,24 ± 1,47 a nivel de cuello femoral, resultados que se muestran en la tabla I. Solo 10 de los pacientes (48%) tenían valores normales en los 2 sectores estudiados.
Hemos tratado de determinar qué datos demográficos podrían estar relacionados con la densidad mineral ósea en el momento de iniciar el soporte nutricional por vía parenteral, encontrando únicamente correlación (p 0,076) con el antecedente de menopausia, que no es significativa dado el escaso número de pacientes. No hemos encontrado diferencias en cuanto a edad, sexo ni diagnóstico.
Entre los pacientes estudiados, 6 sujetos (11,7%) han presentado fracturas (2 anteriores al inicio de la NPD, una a los 3 meses y otras 3 después de varios años de tratamiento), quedando reflejados en la tabla 2 los datos más relevantes. Solo hemos encontrado correlación significativa entre la existencia de fracturas y el antecedente de tratamiento con esteroides (p 0,009) así como con el valor de T-score lumbar al inicio (p 0,002) y al final del seguimiento (p 0,0023).
De los 21 pacientes que disponían de densitometría al inicio de la NPD sólo 13 tienen realizada una segunda determinación de masa ósea que muestra una pérdida de masa ósea (t-score) a nivel lumbar de 0,54 ± 1,12 desviaciones Standard y de 0,62 ± 0,92 a nivel de cuello femoral con un plazo medio de seguimiento de 37 meses. A nivel lumbar, esta diferencia se correlaciona estadísticamente con la duración del soporte nutricional (p 0,004).
Por otro lado, tras un seguimiento medio de 70,97 ± 67,09 meses (7-273), se ha realizado una densitometría ósea a 34 sujetos, de los cuales no se dispone de densitometría al inicio del soporte nutricional en 21 casos. A nivel lumbar, la densidad mineral ósea media es de - 1,96 ± 1,46 y a nivel femoral de -1,95 ± 1,3, quedando recogidos en la tabla 3 los resultados en categorías diagnósticas. Tan solo 5 pacientes (14,7%) presentan valores normales en los dos sectores estudiados. No hemos encontrado correlación estadística entre los resultados de la densitometría realizada en este momento evolutivo con ninguno de los parámetros estudiados: sexo, IMC, antecedente de menopausia, diagnóstico, tiempo de evolución de la NPD, niveles de calcidiol, calciuria o de PTH ni administración de suplementos de vitamina D o de calcio).
De los 36 sujetos que tienen realizada una densitometría en los últimos 2 años (en algunos casos, se trata de la previa a iniciar el soporte nutricional) 16 presentaban datos compatibles con osteoporosis en alguno de los sectores y sólo 5 (31,25%) recibían tratamiento específico con bifosfonatos.
Discusión
Este estudio nos aproxima al problema de la EMO en nuestro medio mostrando una elevada prevalencia de EMO (52%) en el momento del inicio de la NPD que se dispara a prácticamente el 85% tras un seguimiento medio de más de 70 meses. Estos datos son similares a los de otros estudios como el de Raman14 que, en 25 pacientes, detecta un 77% de alteración de la calidad del hueso, con un elevado porcentaje de fracturas (24%) a los 113 meses de seguimiento y a los de Pironi15 publicados en 2002, que encuentra un porcentaje de EMO del 84% (43% osteopenia, 41% con osteoporosis, 10% con fracturas patológicas) tras un seguimiento de 61 meses
El diseño retrospectivo de nuestro estudio, junto con el bajo número de pacientes reclutados, impide extraer conclusiones acerca de las causas que predisponen a desarrollar EMO en los enfermos que reciben NPD, ya que ni siquiera hemos encontrado relaciones significativas entre la alteración de la calidad del hueso y los factores de riesgo de osteoporosis tradicionalmente reconocidos (edad, sexo, IMC). La pérdida de masa ósea a nivel lumbar que en nuestra serie se correlaciona significativamente con la duración de la NPD, pero no difiere mucho de la esperada en población general (< 1% al año en varones y mujeres premenopáusicas y 5% anual tras la menopausia). Por tanto no podemos aportar nuevos datos al debate sobre si la NPD en sí misma induce un riesgo mayor de presentar EMO como indica 14 al describir una relación significativa entre el tiempo de tratamiento y la pérdida de masa ósea o, por el contrario, como parecen indicar todos los estudios longitudinales realizados hasta la fecha se trata de una consecuencia de la enfermedad subyacente, de la insuficiencia intestinal y de los tratamientos asociados, sin que la NPD juegue ningún papel relevante. Como apunta Pironi al describir incluso una ganancia de masa ósea en columna lumbar tras 18 meses de seguimiento16, en los casos en los que se aprecia pérdida de masa ósea el análisis de regresión múltiple únicamente encontró relación con el sexo femenino y la edad avanzada en el momento de iniciar la NPD. También Cohen-Solal17 en un estudio longitudinal no sólo no observa ningún efecto negativo del soporte parenteral a nivel óseo sino que evidencia un aumento de densidad ósea trabecular en pacientes que inician la NPD después de los 21 años. Verhage en 1995 refiere también un discreto aumento en la densidad ósea a nivel lumbar durante el seguimiento de un grupo de pacientes con NPD18
Es necesario disponer de más estudios prospectivos con el suficiente número de casos para poder aportar más luz sobre esta cuestión.
Destaca el elevado número de sujetos que presenta deficiencia de vitamina D a pesar de recibir aporte parenteral en las bolsas de NP por lo que es interesante plantear estudios posteriores para revisar las cantidades de esta vitamina que se deben administrar en pacientes con NPD. Actualmente las guías clínicas desarrolladas por la Sociedad Europea de Nutrición Enteral y Parenteral (ESPEN)19 y por el grupo NADYA20 recomiendan un aporte diario de 200 UI de vitamina D.
Llama la atención el escaso porcentaje de pacientes que tienen realizada densitometría ósea en los momentos cercanos al inicio del soporte nutricional sobretodo teniendo en cuenta la elevada prevalencia de EMO que se detecta en esa fase. Recordemos que en las guías clínicas desarrolladas por la ESPEN19 y por el grupo NADYA21 se recomienda la realización de una densitometría ósea al inicio de la NPD y posteriormente con carácter anual.
Durante el seguimiento un número significativo de pacientes desarrolla osteoporosis sin que conste en la recogida de datos que hayan recibido el tratamiento más adecuado.
Se hace necesario el desarrollo y uso de protocolos de actuación que permitan identificar precozmente este problema y que pueda servir de guía en el seguimiento y tratamiento de estos pacientes ajustando el aporte de nutrientes en la NP, incidiendo en cambios saludables en el estilo de vida o aportando tratamientos específicos.
Referencias
1. BuchmannAL, Moukarzal A. Metabolic bone diseaseassociated with total parenteral nutrition. Clin Nutr 2000; 19 (4): 217-31. [ Links ]
2. Saitta JC, Ott SM, Sherrard D et al. Metabolic bone disease in adults receiving long-term parenteral nutrition: longitudinal study with regional densitometry and bone biopsy. JPEN 1993; 17: 214-219. [ Links ]
3. Haderslev KV, TjllensenL Halderslev PH et al. Assessment of the longitudinal changes in bone mineral density in patients receiving home parenteral nutrition. JPEN 2004; 28: 289-94. [ Links ]
4. Gómez Enterría P, Laborda González L, Martínez Faedo C. Protocolo para el diagnóstico y tratamiento de la osteopatía metabólica en el enfermo con nutrición parenteral domiciliaria. Nutr Hosp 2007; 22 (3): 351-7. [ Links ]
5. Guañabens N. Osteoporosis 2003. Med Clin (Barc) 2003; 121: 625-230. [ Links ]
6. Charney P. ASPEN Statement on aluminium parenteral nutrition solutions. NCP 2004; 19: 416-7. [ Links ]
7. Gura KM, Puder M. Recent developments in aluminium contamination of products used in parenteral nutrition. Cur Opin Clin Nut Metab Care 2006; 9: 239-46. [ Links ]
8. Advenier E, Landry C, Colomb V et al. Aluminium contamination of parenteral nutrition and aluminium loading in children on long-term parenteral nutrition. Journal of Pediatrics Gastroenterology and Nutrition 2003; 36: 448-53 [ Links ]
9. Jeejeebhoy KN. Metabolic bone disease and total parenteral nutrition: a progress report. Am J Clin Nutr 1998; 67: 186. [ Links ]
10. Wood RJ, Bengoa JM, Sitrin MD, Rosemberg IM. Calciuretic effect of cyclic versus continous total parenteral nutrition. Am J Clin Nutr 1985; 41: 614-913. [ Links ]
11. ShackerJ, Lukert B. Osteoporotsis associated with excess glucocorticoids. Endocrinol Metab Clin N Am 2005; 34: 341-53. [ Links ]
12. Leslie WD, AdlerRA, El-Hajj FuleihanG et al. Application of the 1994 WHO Classification to populations other than postmenopausial caucasian women: the ISCD Official Possitions. J Clin Densitom 2006; 9 (1): 22-30. [ Links ]
13. WHO Assessment of osteoporotic fracture risk and its role in screening for postmenopausal osteoporosis. WHO Technical Reports series 843, 1994. [ Links ]
14. Raman M, Aghdassi E, Baun M et al. Metabolic bone disease in patients receiving home parenteral nutrition: a canadian study and review. JPEN 2006; 30: 492-496. [ Links ]
15. Pironi L, Morselli Labate A, Pertkiewiwicz M y cols: Prevalence of bone disease in patients on home parenteral nutrition. Clin Nutr 2002; 21: 289-296. [ Links ]
16. Pironi L, Tjellensen L, Francesco A et al. Bone mineral density in patients on home parenteral nutrition: a follow-up study. Clin Nutr 2004; 23: 1288-302. [ Links ]
17. Cohen-Solal M, Baudoin C, Joly F et al. Osteoporosis in patients on long term home parenteral nutrition: a longitudinal study. J Bone Miner Res 2003; 18: 1989-1994 [ Links ]
18. Verhage AH, Cheong WK, Allard JP et al. Increase in lumbar spine bone mineral content in patients on long-term parenteral nutrition without vitamin D supplementation. JPEN 1995; 19: 431-436. [ Links ]
19. Staun M, Pironi L, Bozzetti F et al. ESPEN Guidelines on Parenteral Nutrition: Home Parenteral Nutrition in adult patients. Clin Nutr 2009; 28: 467-479. [ Links ]
20. Villares JM. Composición de las bolsas de nutrición parenteral. Nutr Hosp 2009; suppl. 2 (1): 8-12. [ Links ]
21. Gómez Enterría P, Laborda L. Preparación, métodos y pautas de administración de la nutrición parenteral domiciliaria. Seguimiento de los pacientes. Educación a pacientes y a cuidadores. Nutr Hosp 2009; suppl. 2 (1): 18-24. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Ceferino Martínez Faedo.
Hospital Universitario Central de Asturias.
C/ Julián Clavería, s/n. 33006 Asturias. España.
E-mail: ceferinofaedo@yahoo.es
Recibido: 27-IX-2009.
1a Revisión: 31-XII-2009.
Aceptado: 6-I-2010.