Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.27 no.4 Madrid jul./ago. 2012
https://dx.doi.org/10.3305/nh.2012.27.4.5855
ORIGINAL
Bypass gástrico en Y de Roux para el tratamiento de pacientes con diabetes mellitus tipo II con IMC de 30 a 35 kg/m2
Roux-en-Y gastric bypass for treatment of patients with DM type 2 and BMI of 30 to 35 Kg/m2
S. Navarrete Aulestia1, J. Leyba1, S. Navarrete LL.2, M. García Caballero3, N. Sánchez4, V. Pulgar5 y A. Vivas6
1Profesores de la Facultad de Medicina. UCV. Caracas. Venezuela
2Cirujano Bariátrico. Clínica Santa Sofía. Caracas. Venezuela
3Acreditado Catedrático Profesor de la Universidad de Málaga
4Cirujano General. Valencia. Venezuela
5Nutrólogo Clínico. Grupo Médico SMT. Caracas
6Estudiante Facultad de Medicina. UCV. Caracas. Venezuela
Dirección para correspondencia
RESUMEN
La incidencia de obesidad y una de sus comorbilidades más temida la diabetes mellitus tipo II está en aumento y no pareciera haber tratamiento médico que ayude a controlar estas pandemias. Existe una técnica quirúrgica bariátrica, el Bypass Gástrico en Y de Roux (BGYR) que es segura y no sólo ayuda a controlar el exceso de peso sino también produce resultados alentadores en el control y remisión de la diabetes.
Métodos: Se presentan 15 pacientes con IMC entre 30 y 35 kg/mt2 diabéticos tipo II seleccionados sometidos a BGYR por laparoscopia con seguimiento de un año.
Resultados: Se operaron 14 mujeres y un hombre con los siguientes valores promedios: Edad: 37 años, Peso: 88,3 kg, IMC: 32,8 kg/mt2, Glicemia: 120 ± 38,8 mg%, HbA1c: 7,6% ± 0,73. 40% de hipertensión arterial y 33,3% dislipidémicos. El tiempo quirúrgico promedio fue de 75 minutos, dos días de hospitalización bajo índice de complicaciones y sin mortalidad. Se logró una remisión de la diabetes en el 93%, de los casos, con descensos de la glicemia y HbA1c significativos (p ≤ 0,05 y p ≤ 0,001 respectivamente) con un control de la dislipidemia del 100% y 83,3% de la HTA.
Conclusiones: El BGYR en obesos tipo I diabéticos seleccionados es una técnica segura y eficaz en el control metabólico y de la obesidad.
Palabras clave: Diabetes mellitus. Obesidad. BGYR. Laparoscopia.
ABSTRACT
Background: The incidence of obesity and its most feared comorbidity, diabetes mellitus type 2, is increasing and there would not seem to be any medical treatment to help control these pandemics. However, there is a bariatric surgery technique, the Roux-en-Y Gastric Bypass (RYGB), which is safe and not only helps control excess weight, but produces encouraging results in the control and remission of diabetes.
Methods: We present 15 selected patients with a BMI between 30 and 35 kg/mt2 and diabetes type 2 who underwent a laparoscopic RYGB with of one-year follow-up.
Results: A total of 14 women and one man were operated with the following average values: age: 37 years, weight: 88.3 kg, BMI: 32.8 kg/mt2, blood glucose: 120 ± 38.8 mg%, HbA1c: 7.6 ± 0.73. Forty percent (40%) suffered from high blood pressure and 33.3% were dyslipidemic. Average surgical time was 75 minutes, hospital length of stay was two days, and there was a low rate of complications and no mortality. Diabetes remission was achieved in 93% of cases with significant drops in blood glucose and HbA1c (p ≤ 0.05 and p ≤ 0.001 respectively), dyslipidemia was 100% controlled and hypertension was 83.3% controlled.
Conclusions: RYGB in selected patients with obesity type 1 and diabetes mellitus type 2 is a safe and effective technique for metabolic control and obesity control.
Key words: Diabetes mellitus. Obesity. RYGB. Laparoscopy.
Introducción
La obesidad ha aumentado de tal manera en los últimos años que en el año 2008 se estimaban alrededor de 250 millones de obesos en el mundo y fue declarado como un problema epidémico por la OMS1.
El incremento de la adiposidad como es bien sabido predispone al aumento de la diabetes mellitus tipo II y su incremento corre paralelo a ella haciéndola una enfermedad de proporciones epidémicas aumentando el riesgo cardiovascular 200-400%2 y se estima que afectará aproximadamente a 300 millones de personas en todo el mundo para el año 20253. Su tratamiento que se ha basado fundamentalmente en una combinación de dieta, cambios de conducta en relación al estilo de vida y medicación, es siempre paliativo con una brecha importante entre los resultados clínicos y lo esperado3,4.
El desarrollo de técnicas quirúrgicas como formas de tratamiento de esta enfermedad se ha logrado gracias a los resultados clínicos obtenidos con cirugía bariátrica en pacientes obesos con IMC ≥ 35 kg/mt2 y representa una nueva alternativa con posibilidades sólidas de remisión como ha sido reportado por numerosos estudios5-8.
Sin embargo existen pocas publicaciones9-15 para el tratamiento quirúrgico de esta entidad clínica en pacientes con IMC ≤ 34,9 kg/mt2 por lo que hemos decidido realizar un estudio prospectivo en quince pacientes con obesidad tipo I diabéticos tipo II con consentimiento informado realizándoles un BGYR con un reservorio gástrico de mayor capacidad (50 cc) y asas tanto alimentaria como bilio-pancreática más cortas (100 y 50 cm respectivamente) para evaluar la eficacia y seguridad de esta técnica en este grupo de pacientes.
Métodos
Desde enero del año 2007 hasta diciembre del año 2010, quince pacientes con diagnóstico de Diabetes Mellitus Tipo II16 con IMC entre 30 y 34,9 kg/mt2 fueron seleccionados para el estudio y operados en la Clinica Santa Sofía y el Hospital Universitario de Caracas. Con los siguientes criterios de inclusión: enfermedad de menos de 10 años de evolución, ausencia de enfermedad vascular o nefropatía diabética y con uso de insulina menor a 6 años. Pacientes con cirugía gástrica previa, enfermedad siquiátrica mayor, historia de abuso de alcohol o drogas y un IMC < 30 kg/mt2 ( por ser parte estos últimos de otro protocolo de estudio) fueron excluídos. El protocolo fue aprobado por el Comité de Bioética asi como el consentimiento informado en cada paciente. Los valores pre y posoperatorios de glicemia en ayunas y Hb A1c fueron obtenidos y analizados con la Prueba t de Student para muestras pareadas, considerando como significativo una p < 0,05.
Técnica quirúrgica
Con la técnica estándar utilizada por nosotros17 de 6 puertos, con el paciente en decúbito dorsal, el cirujano a la derecha al igual que el asistente de cámara y un ayudante del lado izquierdo, se comienza la confección del reservorio gástrico en el tercer vaso de la curvatura menor con la sección y engrapado a esa altura del estómago (carga azul de 45 mm), con lo cual al ir a la parte vertical del estómago utilizamos siempre tres cargas azules de 60 mm lográndose de esta manera un reservorio gástrico de mayor capacidad( 50 cc aprox.). Posterior a la sección del epiplón mayor buscamos el asa fija en el ángulo de Treitz y a 50 cms de la misma realizamos la Y de Roux completándose el bypass con un asa alimentaria de un metro, antegástrica, antecólica, que es anastomosada al reservorio con engrapado quirúrgico lográndose una boca de 15 mm aproximadamente. Las brechas fueron cerradas con sutura continua no reabsorbible.
Todos los pacientes recibieron terapia antimicrobiana profiláctica con Sultamicilina 1,5 g IV sin uso de algún tipo de heparina.
Posoperatorio
Se inició la tolerancia oral con líquidos claros sin azúcar al segundo día de operados siendo egresados ese mismo día si la glicemia capilar era inferior a 200 mg% y había buena tolerancia a la vía oral. Esta dieta fue continuada en casa hasta el quinto día cuando progresivamente fue pasado por 4 etapas durante 6 semanas (líquidos, licuados, puré y sólidos) y al final de ellas el paciente tomaba tres comidas principales antidiabéticas pequeñas y dos meriendas.
Se realizaron controles de glicemia al mes, y cada 6 meses hasta el primer año. En cada control se tomó el peso e IMC. Se consideró el siguiente esquema para hablar de los resultados del control metabólico18:
- Remisión: sin medicación ni insulina, Hb A1c < 7%.
- Control: menos medicación/ sin insulina Hb A1c < 7%.
- Mejoría: menos medicación, con menos insulina Hb A1c basal.
- Sin Respuesta: igual o empeoramiento de la enfermedad.
Resultados
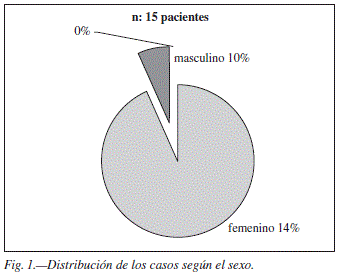
Entre enero 2007 y diciembre 2010 fueron operados 15 pacientes obesos tipo I con Diabetes Mellitus tipo II, catorce del sexo femenino y uno masculino con esta técnica (fig. 1). Los promedios de edad y talla, medias de IMC y peso preoperatorios fueron los siguientes: 37 años (15-52), 1,62 (1,49-1,76), 32,8 kg/mt2 ± 1,37 (3034,7) y 88,3 kg ± 7,79 (79,2-105,4) respectivamente.
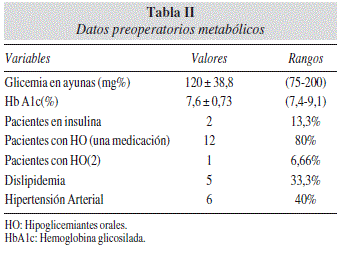
La glicemia preoperatoria en ayunas tuvo una media de 120 mg% ± 38,8 (75-200) HbA1c media preoperatoria: 7,6% ± 0,73 (7,4-9,1). Con un promedio de duración de la enfermedad de 5, 5 años (1 a 9 años) (tabla I).
Trece pacientes recibían algún tipo de hipoglicemiante oral y dos recibían insulina: uno de ellos más de 50 uds diarias de LANTUS®. Habían 5 pacientes con dislipidemia mixta y 6 con hipertensión arterial (tabla II).
Todos los casos fueron operados por laparoscopia. No hubo conversión.
De la cirugía
Los quince pacientes pudieron ser operados por laparoscopia. No se presentaron complicaciones intra-operatorias, con un tiempo promedio de 75 minutos. El promedio de hospitalización fue de dos días. Cabe resaltar que hubo una complicación antes de los treinta días que fue una estenosis de la anastomosis, que respondió a una dilatación con balón neumático y esa misma paciente hizo una úlcera en la gastroyeyunostomía a los dos meses asi como también una litiasis vesicular con hernia interna. Esta paciente es portadora de un Lupus Eritematoso Sistémico (LES) (tabla III).
No hubo mortalidad en la serie.
Antropométricos y metabólicos
Luego de un año de seguimiento los pacientes habían logrado bajar el 103% del sobrepeso con una pérdida promedio de 24 kg (p ≤ 0,001) y el IMC más bajo alcanzado fue de 21,5 kg/mt2 (media de IMC posoperatorio: 24,2 kg/mt2) con una media de pérdida de 8,2 kg/mt2 (p ≤ 0,001). El porcentaje de IMC perdido fue de 26,7%, y de 107% del exceso de IMC17. La glicemia se redujo 28% y descendió a 86,35 mg% ± 8,84 y la Hb A1c descendió hasta 5,53% ± 0,64 (tabla IV), siendo ambos estadísticamente significativos (p ≤ 0,05 y p ≤ 0,001 respectivamente). Considerando los criterios antes descritos logramos una remisión de la Diabetes en 93% de nuestros pacientes, quiere decir 14 pacientes sin medicación alguna, glicemia en ayuna normal y Hb A1c por debajo de 6% y sólo uno quedó con inhibidores de la DPP4 (Janumet®) una tableta dos veces al día. Cabe resaltar que este paciente era el que tenía una dosis de insulina LANTUS muy elevada con mal control de su diabetes(Hb A1c de 9,1%), de mayor edad y con más tiempo de evolución de la enfermedad. Actualmente tiene una glicemia en ayunas de 105 mg% con una HB A1c de 6,3% (fig. 2).
Discusión
La edad promedio de nuestros pacientes fue de 37 años bastante menor que la de las otras series similares, Huang 47 años20, Boza 4814, Shah 4512, Curvelo 5013 pero similar a la de Cohen 34 años9 y a la de Lee 3921. Debe destacarse que el primero20 concluye que la menor edad es un factor predictivo positivo pudiendo ser este un factor de ayuda en lograr los resultados que obtuvimos como discutiremos más adelante. Predomina en nuestra serie el sexo femenino (92%) como en la serie de Huang (91%) Cohen, 83%9 y Lee 81%21 ya que en las otras series hay una distribución diferente Curvelo 74%13, Boza 56%14 y Shah 46%12. Es interesante que el peso promedio inicial es similar en las series latinoamericanas media de IMC de nuestra serie que fue de 32,8 kg/mt2 es bastante similar a los otros grupos Cohen 32,5 kg/mt29, Curvelo 33,513, Boza 33,714 y debe recalcarse porque son series latinoamericanas cuyos resultados deben ser analizados diferentes a las series asiáticas: Shah 28,9 kg/mt212, Lee 31,721 o Huang 30,81 kg/mt220 porque como sabemos tienen problemas con la diabetes mucho más severos porque ésta se aprecia de manera prevalente con IMC más bajos22. Sólo existen publicados datos en series latinoamericanas y asiáticas con estas características de población. Luego de un año de operados nuestros pacientes alcanzan media de IMC de 24,2 kg/mt2 y peso de 64,3 kg similar a Curvelo 25/6813, Boza 23,9/64,414 o Cohen 27,6 kg/mt29 y en las asiáticas los siguientes: Shah 23/ 62,712, Huang 23,720 y Lee 23,1 kg/mt221. Es importante destacar que estos valores son alcanzados con una técnica quirúrgica bastante similar con reservorios pequeños que van desde 15 cc (Boza14, Huang y Lee 30 cc20,21 hasta el de 50 cc como el nuestro y el de Curvelo13 y asas bastante similares en longitudes que van desde 50 cm la biliopancreática como la nuestra y la de Shah12, hasta un metro Curvelo13 y Boza14 y el asa alimentaria entre un metro y 150 cm12,13,14. Lee en el minigastric Bypass mide 1,20 desde el ángulo de Treitz21. Por lo que podemos interpretar nuestros resultados metabólicos desde la restricción y las modificaciones en el tubo digestivo de manera similar, como lo haremos más adelante; pareciera no tener mucha influencia estas longitudes de las asas en los resultados metabólicos26. El tiempo quirúrgico promedio nuestro fue de 75 minutos bastante similar en todas la series y van desde 7121 min, 7214,20 hasta 90 minutos12. Es necesario resaltar que la morbilidad temprana y tardía, 2%20 4,5%21 puede llegar al 16%14 pero son complicaciones que se resuelven apreciándose una mortalidad de 0%9,12,14,20,21 en todas las series, aun en las que hubo que convertir algún caso13 lo cual la convierte en una técnica bastante segura. Queremos comentar que tuvimos 20% de complicaciones tardías (3 complicaciones) pero se presentaron como dijimos antes en la misma paciente y la colelitiasis fue resuelta junto con la hernia interna por laparoscopia en el mismo acto quirúrgico.
En relación con los datos metabólicos preoperatorios cabe resaltar que nuestros pacientes parecieran tener una enfermedad menos severa porque teníamos una glicemia media inicial de 120 mg% y HbA1c de 7,6%, 86% de los pacientes controlados con hipoglicemiantes orales y sólo 2 pacientes con control insulínico (13,3%). Boza14 en su trabajo tiene 97% de pacientes controlados con HO y sólo un caso (3,3%) usando insulina. No hicimos mediciones periódicas de glicemias, Hb A1c ni de peso por cuanto en los diferentes trabajos publicados se conoce que la glicemia se corrige en los primeros 6 días después de la cirugía23,24 por lo que lo consideramos innecesario sobretodo teniendo en cuenta las dificultades socioeconómicas de nuestro país. . El resultado final al año de la cirugía 93,3% de remisión se aproxima a lo publicado por Cohen9 donde reporta hasta un 100% al igual que Shah12, independientemente de algunos factores que pudieran ser pre-dictivos negativos25 como pudiera ser el hecho de tener HbA1c preoperatoria muy elevada de 10,112, el uso de insulina7 o el tiempo de evolución de la enfermedad25. Otros autores reportan índices de remisión menores para este tipo de pacientes, 63%20 en estudios asiáticos, 74%15 y 83%14 en estudios latinoamericanos. Es de hacer notar que la media de glicemia en ayunas de nuestros pacientes luego de un año de cirugía es de 90,69 mg% al igual que en todos estos estudios está por debajo de 110 mg%. 8021, 889, 8912, 10320, 10914. Lo mismo puede decirse de la hemoglobina glicosilada de 5,53% como puede apreciarse en esos trabajos: < 6%9, 5,6%21, 5,920, 5,97%13, 6,1%12 y 6,5%14. El control de la dislipidemia es del 100% y de la hipertensión del 83% (5 de los 6 pacientes) como se aprecia con algunas diferencias en los otros trabajos12,20,21 y en sujetos con IMC mayor que 35 kg/mt227. Estos resultados son alentadores para este grupo de pacientes28 con esta técnica, que es bastante segura con baja morbilidad y mortalidad sobretodo si tomamos en cuenta que en países asiáticos como Japón y la India, Kasama29 y Praveen30 plantean el uso de una técnica muy buena como es la Gastrectomía Vertical (GV) asociada al Bypass Duodenoyeyunal (BDY) para el tratamiento de la obesidad asociada o no a diabetes mellitus, debido a la alta incidencia de cáncer gástrico en esos países. En el trabajo de Praveen30 se comparan las dos técnicas: el Bypass gástrico en Y de Roux con la GV asociada al BDY con asas de igual longitud, para el tratamiento de la obesidad mórbida en grupos similares con IMC similares (alrededor de 46 kg/mt2) y con buenos resultados para el control de la diabetes mellitus en esos pacientes, llegando a alcanzar una remisión con ambas técnicas mayor al 80%, sin embargo Kasama reporta una remisión del 92% con IMC superior a 40 kg/mt2. Esta técnica es más compleja, más costosa y lleva más tiempo quirúrgico18,29,30 y pareciera que en nuestros países donde la incidencia del cáncer gástrico es menor pudiera reservarse para pacientes superobesos31,32 o diabéticos no obesos18, sin embargo debemos recordar que con menos peso (no obesos) cualquier técnica no tiene los mismos resultados en el control de la diabetes mellitus11,18,25,33. Herron and Tong34, Dixon35 y Cumming36 han resumido cuidadosamente las diferentes teorías de los mecanismos involucrados en la pérdida de peso y control de la diabetes que se logra con la cirugía en pacientes obesos, ellas incluyen la pérdida de peso, disminución de las calorías, cambios hormonales y malabsortivos, arreglos en la anatomía del intestino (hipótesis del intestino anterior y posterior) sin olvidar también la hipótesis de Troy37 de la neoglucogénesis intestinal. La respuesta diferente en pacientes no obesos es distinta lo cual supone un reto para los investigadores y abre nuevos horizontes a estudiar.
Conclusiones
A la luz de nuestro trabajo y otros de estas características nos parece que el BGYR en pacientes obesos no mórbidos (o tipo I) con diabetes mellitus tipo II es una técnica segura y con buenos resultados para el control de esta enfermedad en pacientes seleccionados.
Referencias
1. James WP. WHO recognition of the global obesity epidemic. Int J Obes (Lond) 2008; 32 (Suppl. 7): S120-6. [ Links ]
2. Gu K, Cowie CC, Harris MI. Mortality in adults with and without diabetes in a national cohort of the U.S. population, 1971-1993. Diabetes Care 1998; 21: 1138-45. [ Links ]
3. Zimmet P, Alberti K, Shaw J. Global and societal implications of the diabetes epidemic. Nature 2001; 414: 782-7. [ Links ]
4. Eliasson B, Eeg-Olofsson K, Cederholm J et al. Antihyper-glycemic treatment of type 2 diabetes: results from a national diabetes register. Diab Metab 2007; 33: 269-76. [ Links ]
5. Buchwald H, Avidor Y, Braunwald E et al. Bariatric surgery: a systematic review and meta-analysis. JAMA 2004; 292: 1724-37. [ Links ]
6. Pories WJ, Swanson MS, Kg McDonald et al. Who would have thought it? An operation proves to be the most effective therapy for adult-onset diabetes mellitus. Ann Surg 1995; 222: 339-50. [ Links ]
7. Schauer PR, Burguera B, Ikramuddin S et al. Effect of laparoscopic Roux-en Y gastric bypass on type 2 diabetes mellitus. Ann Surg 2003; 238: 467-85. [ Links ]
8. Greenway SE, Frank L, Greenway III et al. Effects of obesity surgery on non-insulin-dependent diabetes mellitus. Arch Surg 2002; 137: 1109-17. [ Links ]
9. Cohen R, Pinheiro JS, Correa JL et al. Laparoscopic Roux-en-Y gastric bypass for BMI < 35 kg/m2: a tailored approach. Surg Obes Relat Dis 2006; 2: 401-4. [ Links ]
10. Cohen RV, Schiavon CA, Pinheiro JS et al. Duodenal-jejunal bypass for the treatment of type 2 diabetes in patients with body mass index of 22-34 kg/m2: a report of 2 cases. Surg Obes Relat Dis 2007; 3: 195-7. [ Links ]
11. De Paula AL, Macedo AL, Rassi N et al. Laparoscopic treatment of type 2 diabetes mellitus for patients with a body mass index less than 35. Surg Endosc 2008; 22: 706-16. [ Links ]
12. Shah SS, Todkar JS, Shah PS, et al. Diabetes remission and reduced cardiovascular risk after gastric bypass in Asian Indians with body mass index < 35 kg/m2. Surg Obes Relat Dis 2010; 6: 332-8. [ Links ]
13. Curvelo Tavares V, Ferraz A, Campos J et al. Gastric Bypass in the Treatment of Type 2 Diabetes in Patients with a BMI of 30 to 35 kg/mt2. Obes Surg 2011; 21: 283-287. [ Links ]
14. Boza C, Muñoz R, Salinas J et al. Safety and Efficacy of Roux-en-Y Gastric Bypass to Treat Type 2 Diabetes Mellitus in Non-severely Obese Patients. Obes Surg 2011; 21: 1330-6. [ Links ]
15. Fried M, Ribaric G, Buchwald JN et al. Metabolic Surgery for the Treatment of Type 2 Diabetes in Patients with BMI < 35 kg/mt2: An Integrative Review of Early Studies. Obes Surg 2010; 20: 776-790. [ Links ]
16. American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care 2009; 32 (1): S62-6. [ Links ]
17. Leyba JL, Aulestia SN, Llopis SN. Laparoscopic Roux-en-Y gastric bypass versus laparoscopic sleeve gastrectomy for the treatment of morbid obesity. A prospective study of 117 patients. Obes Surg 2011; 21: 212-6. [ Links ]
18. Navarrete SA, Leyba JL, Llopis SN. Laparoscopic sleeve gastrectomy with duodenojejunal bypass for the treatment of type 2 diabetes in non-obese patients: technique and preliminary results. Obes Surg 2011; 21 (5): 663-7. [ Links ]
19. Rubio MA. Criterios de Evaluación a largo plazo. En Guía práctica de la cirugía de la obesidad: una visión multidisciplinaria. Grupo de trabajo en cirugía de la obesidad: Bretón Lesmes I et al. Novartis Medical Nutrition. [ Links ]
20. Huang Ch, Shabbir A, Lo CH et al. Laparoscopic Roux-en-Y Gastric Bypass for the Treatment of Type II Diabetes Mellitus in Chinese Patients with Body Mass Index of 25-35. Obes Surg 2011; 21: 1344-9. [ Links ]
21. Lee WJ, Wang W, Lee YC et al. Effect of laparoscopic mini-gastric bypass for type 2 diabetes mellitus: comparison of BMI > 35 and < 35 kg/m2. J Gastrointest Surg 2008; 12: 945-52. [ Links ]
22. Lee WJ, Wang W. Bariatric surgery: Asia-pacific perspective. Obes Surg 2005; 15: 751-757. [ Links ]
23. Wickremesekera K, Miller G, Naotunne TD et al. Loss of insulin resistance after Roux-en-Y gastric bypass surgery: a time course study. Obes Surg 2005; 15 (4): 474-81. [ Links ]
24. Hayes M, Foo J, Besic V et al. Is Intestinal Gluconeogenesis a Key Factor in the Early Changes in Glucose Homeostasis following Gastric Bypass. Obes Surg 2011; 21: 759-762. [ Links ]
25. Hayes M, Hunt L, Foo J et al. A model for predicting the resolution of Type 2 Diabetes in Severely Obese Subjects Following Roux-en-Y gastric Bypass Surgery. Obes Surg 2011; 21: 910-916. [ Links ]
26. Orci L, Chilcott M, Huber O. Short versus long Roux-en-Y gastric Bypass Surgery for the Treatment of Morbid and Super Obesity a Systematic Review of the Literature. Obes Surg 2011; 21: 797-801. [ Links ]
27. Ocon J, García P, Benito S et al. Efecto del Bypass Gástrico en el Síndrome Metabólico y en el Riesgo Cardiovascular. Nutr Hosp 2010; 25 (1): 67-71. [ Links ]
28. García Caballero M. Cirugía de la diabetes mellitus tipo 2: el gran descubrimiento de la cirugía bariátrica. Nutr Hosp 2010; 25 (5): 693-694. [ Links ]
29. Kasama K, Tagaya N, Kanehira E et al. Laparoscopic sleeve gastrectomy with duodenojejunal bypass: technique and preliminary results. Obes Surg 2009; 19: 1341-5. [ Links ]
30. Praveen Raj P, Kumaravel R, Chandramaliteeswaran C et al. Is Laparoscopic Duodenojejunal Bypass with Sleeve an Effective Alternative to Roux en Y gastric Bypass in Morbidly Obese Patients: Preliminary Results of a Randomized Trial. Obes Surg 2011; en prensa. [ Links ]
31. Sovik T, Taha O, Aasheim ET. Randomized Clinical Trial of laparoscopic gastric bypass versus laparoscopic duodenal switch for superobesity. Br J Surg 2010; 97: 160-166. [ Links ]
32. Baltasar A, Bou R, Miro J et al. Laparoscopic biliopancreatic diversion withduodenal switch: technique and initial experience. Obes Surg 2002; 12: 245-248. [ Links ]
33. Scopinaro N, Papadia F, Marinari G, et al. Long-term control of type 2 diabetes mellitus and the other major components of the metabolic syndrome after biliopancreatic diversion in patients with BMI < 35 kg/m2. Obes Surg 2007; 17 (2): 185-92. [ Links ]
34. Herron D, Tong W. Role of surgery in management of type II diabetes. Mount Sinai Med J 2009; 76: 281-93. [ Links ]
35. Dixon J. Obesity and diabetes: the impact of bariatric surgery on type-2 diabetes. World J Surg 2009; 33 (10): 2014-21. [ Links ]
36. Cummings D, Overduin J, Foster-Schubert KE, et al. Role of the bypassed proximal intestine in the anti-diabetic effects of bariatric surgery. Surg Obes Relat Dis 2007; 3 (2): 109-15. [ Links ]
37. Troy S, Soty M, Ribeiro L et al. Intestinal gluconeogenesis is a key factor for early metabolic changes after gastric bypass but not after gastric lap-band in mice. Cell Metab 2008; 8 (3): 201-11. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Salvador Navarrete Aulestia
Clínica Santa Sofia, piso 3, consultorio 330
Urb. Santa Sofía, El Cafetal, Caracas 1061, Venezuela
E-mail: navarretesalvador@yahoo.com
Recibido: 15-III-2012
Aceptado: 27-III-2012