Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.34 no.6 Madrid nov./dic. 2017
https://dx.doi.org/10.20960/nh.1207
ARTÍCULO ESPECIAL
Simulador gastrointestinal dinámico (simgi®): una herramienta potencialmente útil en nutrición clínica
The dynamic gastrointestinal simulator (simgi®): a useful tool for clinical nutrition
Alba Tamargo, Irene Gil-Sánchez, Beatriz Miralles, Diana Martín, Mónica Rodríguez García-Risco, Tiziana Fornari, Begoña Bartolomé, M. Victoria Moreno-Arribas y Carolina Cueva
Instituto de Investigación en Ciencias de la Alimentación (CIAL), CSIC-UAM, CEI UAM+CSIC. Madrid
Financiación: este trabajo ha sido realizado gracias a la financiación del MINECO (proyecto AGL2015-64522-C2-R) y la Comunidad de Madrid (Programa ALIBIRD-CM S2013/ABI-2728-CM). Alba Tamargo es beneficiaria de un contrato en el Programa de Garantía Juvenil-CSIC financiado gracias al Fondo Social Europeo. Irene Gil Sánchez es beneficiaria de una beca FPU del MECD (FPU14/05760).
Agradecimientos: los autores agradecen a Roberto Nieto (Programa Garantía Juvenil-CSIC) su asistencia técnica con el simgi®.
Dirección para correspondencia
RESUMEN
Dentro de la microbiota humana, el tracto gastrointestinal alberga el ecosistema más complejo y abundante del cuerpo humano, siendo el colon donde se encuentra la concentración más alta de microorganismos (1012 cél/g). La microbiota intestinal desempeña funciones metabólicas, tróficas y de protección que son de gran importancia para el hospedador. Durante las últimas décadas, son numerosos los estudios que han tratado de aportar evidencias científicas acerca de los factores que, a través de cambios en la composición de la microbiota intestinal, influyen en la salud humana. Sin embargo, esta aproximación está cambiando, y son cada vez más los expertos que apuestan por evaluar cambios a nivel de funcionalidad de la microbiota. Si aplicamos este enfoque dual al papel desempeñado por la dieta, resulta obvia la necesidad de disponer de modelos dinámicos de simulación gastrointestinal, como es el simgi®, que permitan evaluar las transformaciones que sufren los alimentos y/o ingredientes alimentarios durante el tránsito por el tracto gastrointestinal, así como para determinar los posibles cambios en la composición y funcionalidad de la microbiota intestinal derivados de la ingesta de alimentos. Los estudios llevados a cabo hasta el momento con el simgi® constatan sus potenciales aplicaciones en el área de los alimentos como paso previo a su aplicación en nutrición clínica, para prevenir y/o tratar enfermedades asociadas a disbiosis intestinal, así como trastornos metabólicos. Asimismo, esta revisión recoge posibles perspectivas de utilización del simgi® en la investigación clínica relativa a enfermedades vinculadas con disfunciones de la microbiota intestinal.
Palabras clave: simgi®. Microbiota intestinal. Nutrición. Salud.
ABSTRACT
The human gastrointestinal tract harbours the most complex and abundant community of the human body, the colon being where the highest microbial concentration is found (1012 cell/g). The intestinal microbiota exerts metabolic, trophic and protective functions which are important in the maintenance of the host health. Over recent decades, numerous studies have attempted to provide scientific evidence about the environmental factors that can impact on human health through the modulation of the intestinal microbiota composition. However, this approach is changing, and a new focus on assessing changes at functional level is being developed. If we apply this dual approach to the role played by the diet, it is obvious the need of dynamic gastrointestinal simulation models such as simgi®, that allow to evaluate the transformations undergone by food and/or food ingredients during their transit through the gastrointestinal tract, as well as to determine potential changes in the composition and functionality of the intestinal microbiota after food ingestion. So far the studies using the simgi® have confirmed its potential applications in the area of food as a prior step to its application in clinical nutrition to prevent and/or treat diseases associated with intestinal dysbiosis and metabolic disorders. Likewise, this review includes feasible perspectives of the use of simgi® in clinical research concerning to diseases related to the intestinal microbiota.
Key words: simgi®. Intestinal microbiota. Nutrition. Health.
INTRODUCCIÓN
En los últimos años se han llevado a cabo diversos proyectos de investigación multidisciplinares (Proyecto MetaHit, Proyecto del Microbioma Humano y Proyecto MyNewGut) que, junto al avance de las técnicas -ómicas, han permitido un gran avance en el conocimiento de la microbiota humana y su composición genética, es decir, el microbioma humano. En el caso particular de la microbiota intestinal, se ha visto que puede clasificarse en 3 grupos o enterotipos, en los que predominan Bacteroides, Prevotella y Ruminococcus, y cuya distribución a su vez se ve influenciada por la diversidad de genes de la microbiota: low gene count o LGC (bajo número de genes) vs. high gene count o HGC (elevado número de genes). La mayoría de los casos de LGC presentan un enterotipo 1, dominado por bacterias del género Bacteroides, mientras que un porcentaje elevado de individuos HGC pertenecen al enterotipo 3 en el que predominan los Ruminococcus. Más específicamente, se ha visto que los individuos HGC presentan una mayor distribución de especies antiinflamatorias tales como Faecalibacterium prausnitzii y Roseburia inulinivorans, mientras que los individuos LGC presentaban niveles más altos de Bacteroides y de Ruminococcus gnavus, bacterias proinflamatorias y asociadas a enfermedad inflamatoria intestinal (EII) (1,2).
En condiciones de homeostasis intestinal, la microbiota intestinal desempeña funciones metabólicas, tróficas y de protección, que resultan claves en la salud del hospedador; sin embargo, existen determinados factores ambientales, como son el estrés, los antibióticos y la dieta, que pueden modificar la composición y/o funcionalidad de la microbiota intestinal. En el caso concreto de la dieta, se ha visto que es uno de los factores más influyentes en la microbiota intestinal humana. Un ejemplo claro de cómo la dieta puede modificar la composición de la microbiota intestinal lo constituye un estudio llevado a cabo por Filippo y cols. (3), en el que se comparó la composición de la microbiota intestinal de niños italianos con una dieta típica occidental, frente a la de niños africanos, con una dieta típica rural de alto contenido en fibra. Los resultados mostraron que en las dietas ricas en fibra predominaban Bacteroidetes (principalmente Prevotella y Xylanibacter), en detrimento de Firmicutes, y tenía lugar un descenso significativo en la cantidad de enterobacterias. De igual forma, un estudio llevado a cabo por Wu y cols. (4) con adultos americanos de la misma área geográfica y similar origen cultural mostró la vinculación existente entre los patrones de la dieta y los denominados enterotipos de la microbiota intestinal. En concreto, se vio que el enterotipo Bacteroides se asociaba positivamente con la ingesta de proteínas y grasas animales, mientras que el enterotipo Prevotella lo hacía con dietas ricas en carbohidratos.
A pesar de los estudios que evidencian el papel de la dieta en la salud humana a través de cambios en la composición de la microbiota intestinal, son cada vez más los expertos que apuestan por evaluar cambios a nivel de funcionalidad (5,6). Un ejemplo claro lo constituye el estudio llevado a cabo por David y cols. (7), en el que se compararon los efectos a corto plazo (5 días) en la composición y actividad metabólica de la microbiota de individuos con una dieta exclusiva de plantas, frente a individuos con una dieta de origen animal. Los resultados mostraron que, el perfil de expresión de los genes microbianos, se agrupaba de acuerdo a la dieta y no tanto a los individuos, lo que pone de manifiesto que la microbiota intestinal se adapta rápidamente a cambios en la dieta. Recientemente, Wu y cols. (8) compararon el metaboloma de individuos vegetarianos frente a individuos omnívoros de una zona urbana occidental. Los autores encontraron que, si bien no había grandes diferencias entre ambos grupos a nivel de composición de la microbiota intestinal, sí existían cambios importantes en el perfil de metabolitos urinarios, especialmente en aquellos derivados del metabolismo microbiano.
Por tanto, la dieta podría constituir una nueva vía terapéutica a través de la nutrición clínica para el tratamiento de aquellas enfermedades asociadas a desequilibrio en la diversidad o función de la microbiota intestinal, término que se conoce con el nombre de disbiosis intestinal. En este punto, resulta obvia la necesidad de disponer de modelos de simulación gastrointestinal, como es el simgi® (SIMulador GastroIntestinal Dinámico), que evalúen las transformaciones que sufren los alimentos y/o ingredientes durante el tránsito por el tracto gastrointestinal, así como los cambios en la composición y/o funcionalidad de la microbiota intestinal, como paso previo a los estudios de intervención en humanos, más costosos y con limitaciones éticas. En la siguiente revisión profundizamos en la importancia clínica de la microbiota intestinal, así como en la aplicabilidad de los modelos de simulación, y en concreto del simgi®, en el ámbito de la nutrición clínica.
IMPORTANCIA CLÍNICA DE LA MICROBIOTA INTESTINAL
Una microbiota sana se caracteriza por una alta diversidad y por su capacidad para resistir la invasión por patógenos (9). Por el contrario, un desequilibrio en la diversidad o función de la comunidad microbiana, término que se conoce con el nombre de disbiosis (Fig. 1), se asocia a enfermedades humanas, incluidas las gastrointestinales (EII), sistémicas (obesidad, diabetes tipo II) y locales (trastornos de la función cerebral). Como se ha mencionado anteriormente, estudios recientes sugieren que la dieta es uno de los factores causantes de los cambios en la ecología intestinal con consecuencias clínicas (11). A continuación, se revisan brevemente las principales enfermedades gastrointestinales, sistémicas y locales asociadas a disbiosis de la microbiota intestinal (Fig. 1), haciendo especial hincapié en la influencia de factores dietéticos.
Enfermedades gastrointestinales
Enfermedad inflamatoria intestinal (EII): una característica típica de pacientes afectados de EII es la reducción de la biodiversidad y funcionalidad de la microbiota intestinal (12). En general se ha visto que tiene lugar una disminución de miembros del filo Firmicutes, una reorganización de las especies de Bacteroides, en concreto una mayor proporción de Bacteroides fragilis (13) y un aumento de miembros del filo proteobacteria (14).
Además, en el caso concreto de pacientes afectados de colitis ulcerativa (CU), se ha visto que tienen niveles reducidos de los géneros Faecalibacterium y Roseburia y un aumento de Ruminococcus y de la familia Enterobacteriaceae, incluida Eschericia coli adherente e invasiva (12). De igual forma, en pacientes con enfermedad de Crohn (EC) se ha observado que presentan una menor abundancia de F. prausnitzii y Bifidobacterium adolescentes y un aumento de Ruminococcus gnavus (15).
Síndrome del intestino irritable (SII): en estos pacientes se han descrito alteraciones en la composición taxonómica (enriquecimiento del filo Firmicutes respecto de Bacteroidetes) (16) y funcional (metabolismo alterado de los hidratos de carbono y proteínas en el intestino) de la microbiota y en las interacciones microbiota-huésped (17).
Enfermedades sistémicas:
Obesidad: en los últimos años, han surgido múltiples publicaciones que plantean el papel de la microbiota intestinal en el desarrollo de esta enfermedad. En un estudio llevado a cabo por Karlsson y cols. (18) con niños obesos se vio que tenían una microbiota rica en miembros de la familia Enterobacteriaceae y una proporción reducida de Bacteroides spp y Bacteroidetes respecto a Firmicutes. Asimismo, estos niños presentaban una disminución de Desulfovibrio y Akkermansia muciniphila, las cuales resultan relevantes para la función de la barrera intestinal. Por otro lado, un estudio metagenómico reciente ha dividido a los individuos obesos, en base a la riqueza de genes, en individuos con bajo número de genes (LGC) e individuos con alto número de genes (HGC). Estos últimos se caracterizan por tener una mayor prevalencia de especies antiinflamatorias como F. prausnitzii así como un mayor potencial para producir ácidos orgánicos, incluyendo el butirato (19). Por su parte, los individuos LGC presentan una mayor abundancia de especies de Bacteroides spp proinflamatorias y de genes implicados en la respuesta al estrés oxidativo. Además, esta riqueza de genes puede ser modificada por la dieta, como ha demostrado un estudio con individuos obesos llevado a cabo por Cotillard y cols. (1). En concreto, estos autores observaron que la restricción de energía aumentaba la diversidad de genes en un 25% en los individuos LGC, si bien los efectos sobre la disminución de peso, la mejora en la sensibilidad a la insulina y la disminución de la inflamación fueron menos eficientes que en individuos HGC. En conjunto, estos resultados evidencian la importancia de las funciones metabólicas de la microbiota en la patogenia de la obesidad, así como de la necesidad de tratamientos personalizados para conseguir resultados eficaces.
Diabetes tipo 2: la microbiota fecal de estos pacientes presenta poblaciones reducidas de Firmicutes, incluyendo el grupo de los clostridios (20). No obstante, todavía son necesarios más estudios que investiguen si dichos cambios son la causa o bien la consecuencia de la enfermedad.
Enfermedades locales: estudios recientes han mostrado que la microbiota intestinal también puede afectar directamente al sistema nervioso enteral (SNE) a través de la liberación de productos de síntesis y metabolitos bacterianos, e indirectamente a través de la inducción a la liberación de mediadores inmunológicos del huésped con impacto en el SNE (21). No obstante, y dada la complejidad del binomio microbiota-cerebro, son necesarios más estudios que aporten evidencias científicas acerca del papel de la microbiota en el desarrollo de enfermedades relacionadas con la función cerebral, especialmente el autismo y la depresión.
MODELOS DE SIMULACIÓN DE LA MICROBIOTA INTESTINAL: CASO ESPECÍFICO DEL simgi®
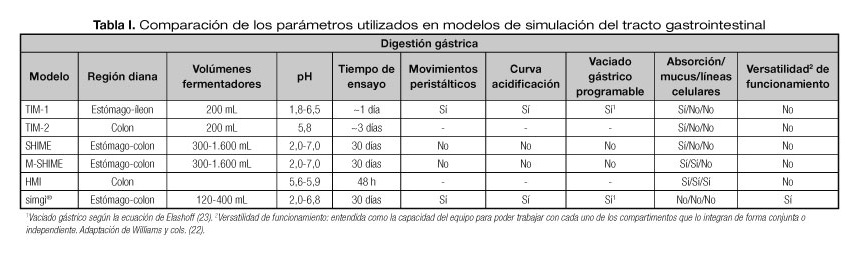
Si tenemos en cuenta que, como se ha mencionado anteriormente, la dieta es uno de los factores más influyentes en la composición y/o funcionalidad de la microbiota intestinal, resulta obvia la necesidad de disponer de modelos de simulación gastrointestinal que permitan estudiar factores dietéticos, como paso previo a los estudios de intervención en humanos, más costosos y con limitaciones éticas. Los modelos de simulación gastrointestinal que incluyen microbiota intestinal humana se emplean habitualmente para evaluar las transformaciones que sufren los alimentos y/o ingredientes alimentarios durante el tránsito por el tracto gastrointestinal, así como para determinar los posibles cambios en la composición y funcionalidad de la microbiota intestinal como consecuencia de la ingesta. Las principales ventajas de estos modelos son que permiten realizar toma de muestras en regiones de difícil acceso (estómago, intestino, colon) y monitorizar de un modo dinámico las distintas variables fisiológicas, i.e. movimientos peristálticos, tiempos de retención, variaciones de pH, composición de los fluidos gastrointestinales, diversidad de la microbiota, metabolismo colónico, etc. No obstante, debido a su enorme complejidad, así como al elevado coste de instalación y puesta a punto, existen muy pocos simuladores de este tipo en el mundo. A nivel europeo, cabe destacar los modelos TIM-1 y TIM-2 (Netherlands Organisation for Applied Scientific Research -TNO-, Holanda), y el modelo SHIME (Simulator of the Human Intestinal Microbial Ecosystem, Universidad de Gante, Bélgica) (22) (Tabla I). A su vez, este último modelo presenta dos adaptaciones, el M-SHIME y el HMI, que permiten simular la mucosa intestinal y la interacción mucosa-hospedador, respectivamente.
Recientemente se ha desarrollado un nuevo modelo, el Simulador Gastrointestinal Dinámico, que responde al acrónimo de simgi®. Esta infraestructura pretende simular el funcionamiento del tracto gastrointestinal humano a través de la evaluación de los procesos de digestión gastrointestinal y fermentación colónica de los alimentos. Se compone de varios compartimentos, que incluyen estómago, intestino delgado, y colon (ascendente, transverso y descendente) gobernados por un autómata, y que pueden operar de forma conjunta o independiente (Fig. 2). El estómago se compone de dos unidades con paredes flexibles y rodeadas por una camisa de metacrilato donde se bombea agua, que permite, por un lado, mantener una temperatura constante y por otro, el mezclado del contenido estomacal por movimientos peristálticos. El sistema permite variar la consigna de control de pH y el tiempo de vaciado al intestino delgado. El intestino delgado es un reactor donde tiene lugar, en condiciones anaerobias y de pH controlado, la mezcla del contenido gástrico con las secreciones intestinales- mediante agitación mecánica regulable. Por último, el colon se compone de tres reactores (colon ascendente, transverso y descendente) que operan en condiciones de anaerobiosis, con agitación mecánica y pH controlado, y donde se aloja una densa microbiota intestinal de origen humano. Además, el simgi® dispone de diferentes puntos de toma de muestras en cada uno de los compartimentos para llevar a cabo los análisis bioquímicos y microbiológicos correspondientes.
Desde su puesta en marcha, son varios los estudios que se han llevado a cabo y que se pueden dividir en dos grupos: a) los enfocados a la optimización y puesta en marcha del sistema y b) los que están dirigidos a simular los procesos de digestión gástrica e intestinal y/o fermentación colónica de alimentos y/o ingredientes alimentarios.
En una primera fase de optimización, se evaluó la estabilización y diferenciación de la microbiota colónica, utilizando para ello los compartimentos correspondientes al intestino delgado y colon. Una vez establecidas las variables de funcionamiento, se llevó a cabo la inoculación de los fermentadores colónicos con microbiota fecal humana. Los resultados de este estudio demostraron que el simgi® permite obtener una microbiota colónica estable y diferenciada tanto en composición como en funcionalidad (24). Alcanzado este objetivo, el siguiente paso fue definir los modos de operación del simgi®, quedando establecidos en 3 (Tabla II), lo que permite una gran versatilidad experimental.
A continuación, se adecuaron al funcionamiento del sistema los parámetros fisiológicos que pueden influir en la microbiota y su actividad metabólica, y se fijaron los tiempos de muestreo en los colectores del intestino delgado y colónicos (25). Paralelamente, se llevó a cabo la optimización de los parámetros de digestión y vaciado gástrico en el compartimento del estómago, empleando para ello proteínas de suero lácteo (26). Los resultados mostraron que el simgi®, a diferencia del modelo de digestión estático, permite, con los parámetros seleccionados, una liberación secuencial de péptidos, más cercana a una situación fisiológica. Recientemente, y con el fin de adecuar los parámetros del sistema completo a matrices alimentarias, se ha llevado a cabo la simulación con un compuesto inerte (complejo Cr-EDTA) y se ha monitorizado su elución tras las etapas de digestión gástrica e intestinal y fermentación colónica mediante la determinación de cromo en los eluidos gastrointestinales por espectrometría de masas con plasma de acoplamiento inductivo (ICP-MS). Así, se ha establecido que el tiempo de residencia mínimo del alimento en el sistema es de 48 h, siendo necesarios 8 días para que el alimento complete su recorrido a lo largo del simgi®. De igual forma, se han podido establecer los tiempos de toma de muestra de los digeridos para conseguir una distribución representativa del alimento entre los distintos compartimentos.
Transcurrida la etapa de optimización, se han llevado a cabo diferentes ensayos de simulación con alimentos y/o ingredientes alimentarios. A continuación, se describen brevemente los resultados más relevantes de estos trabajos. Para el primer ensayo con una matriz alimentaria, se seleccionó vino, debido a su abundancia en polifenoles y a su variada composición fenólica, y tuvo como objetivo evaluar el metabolismo colónico tras la ingesta aguda de un vino tinto (25). Los resultados mostraron que la combinación de polifenoles del vino modula la actividad metabólica de la microbiota intestinal. A su vez, los datos de este estudio se compararon con los de un estudio previo de intervención en humanos con el mismo vino (27). La consistencia entre ambos resultados a nivel metabólico confirmó la idoneidad del simgi® como modelo de simulación.
En relación a los resultados del estudio anterior, se llevó a cabo otro experimento, cuyo objetivo fue evaluar el metabolismo colónico tras la ingesta aguda y crónica de un ingrediente activo, en concreto un extracto de orujo de uva, que combina una importante cantidad de fibra y polifenoles, y que previamente había demostrado reducir la glucosa en un estudio de intervención en humanos (28). Los resultados de la simulación colónica mostraron que, en general, una ingesta continuada de polifenoles activa el metabolismo de la microbiota colónica, a la vez que favorece el crecimiento de algunos grupos bacterianos, considerados beneficiosos, como son los lactobacilos, los cuales podrían ser los responsables, al menos en parte, de los cambios fisiológicos observados en los ensayos in vivo.
Recientemente, y con la idea de ampliar la oferta de aplicaciones del simgi®, se ha llevado a cabo una simulación combinada de una cepa probiótica de interés, con un extracto de uvas tintas, con el doble objetivo de conocer por un lado la implantación de probióticos a nivel intestinal y, por otro, evaluar su impacto en el metabolismo colónico de los polifenoles. Los resultados obtenidos han confirmado la resistencia gástrica y posterior implantación de la cepa probiótica en los fermentadores colónicos, así como su contribución al metabolismo colónico de los polifenoles (resultados no publicados).
Los estudios descritos anteriormente se han llevado a cabo con microbiota colónica de individuos sanos en condiciones de homeostasis intestinal. Sin embargo, la versatilidad y la automatización del sistema también permiten simular situaciones de disbiosis intestinal asociadas a patologías o desequilibrios en la dieta. En este sentido, un estudio reciente ha evaluado el efecto de un ingrediente prebiótico en la reversión del estado de disbiosis asociado a una microbiota colónica procedente de un individuo obeso hacia un estado de normobiosis (29).
PERSPECTIVAS DE LOS SIMULADORES GASTROINTESTINALES DINÁMICOS EN LA INVESTIGACIÓN CLÍNICA
Los estudios llevados a cabo hasta el momento con simuladores gastrointestinales como el simgi® constatan las múltiples aplicaciones de este tipo de equipos en el área de la alimentación, en relación al metabolismo de ingredientes e impacto en la microbiota intestinal, como paso previo a su aplicación en el área clínica para prevenir y/o tratar enfermedades asociadas a disbiosis intestinal.
Entre las estrategias que se llevan a cabo actualmente para tratar los trastornos asociados a desequilibrios en la microbiota intestinal, destacan la ingesta de prebióticos y/o probióticos y los trasplantes fecales. En el caso de los probióticos, un estudio reciente ha demostrado que su ingesta mejora ligeramente la sintomatología del SII, si bien en niños los mejores resultados se obtuvieron con Lactobacillus rhamnosus GG mientras que en adultos fue con bacterias del género Bifidobacterium spp. Por otro lado, los prebióticos también podrían influir en el desarrollo de algunas enfermedades como la obesidad, modificando tanto algunos grupos taxonómicos de la microbiota intestinal como los genes implicados en el transporte de aminoácidos, el metabolismo lipídico y en la conversión y en la producción de energía (30).
Junto a los probióticos y prebióticos, algunos autores también consideran que los polifenoles, denominados conjuntamente como "las P´s para la salud intestinal" podrían ser utilizados como una herramienta útil en la modulación de la composición y/o actividad metabólica de la microbiota intestinal (31). Este efecto viene determinado en gran medida por la bioaccesibilidad de los polifenoles, los cuales en su mayoría (alrededor del 95%) llegan intactos al colon, donde son metabolizados por la microbiota residente en toda una batería de metabolitos biológicamente activos (32). Un hecho relevante que evidencian los estudios más recientes es que la población humana puede estratificarse en función de su capacidad para metabolizar los polifenoles de distintos alimentos, pudiéndose establecer distintos patrones de metabolismo fenólico o "metabotipos" (27,33). El desafío está ahora en relacionar diferentes metabotipos con estados de salud/predisposición a padecer enfermedad y establecer si un determinado metabotipo está mejor preparado para responder a la ingesta de polifenoles. En este sentido, y como se ha descrito en la sección anterior, los resultados obtenidos hasta el momento en el simgi® constituyen una base sólida como paso previo al uso de polifenoles en estudios de intervención en humanos, a la vez que refuerzan la idea de utilizar estos compuestos como una estrategia dietética para el tratamiento de enfermedades asociadas a disbiosis. Recientemente, se ha comprobado que los polifenoles del vino modulan de forma específica la microbiota intestinal de pacientes obesos con síndrome metabólico, incrementando el número de bifidobacterias y Lactobacillus spp (protectores de la barrera intestinal) y de bacterias productoras de butirato (F. prausnitzii y Roseburia spp), y disminuyendo el de los grupos bacterianos productores de lipopolisacárido (Escherichia coli y Enterobacter cloacae) (34). Estos cambios en la microbiota intestinal parecen ser los responsables de la mejora observada en los marcadores del síndrome metabólico.
Un caso particular, y de reciente utilización para revertir procesos de disbiosis, lo constituyen los trasplantes de microbiota fecal, que consisten en transferir heces de donantes sanos, previamente tratadas y homogeneizadas, a una persona enferma con el fin de restaurar la homeostasis intestinal. Actualmente, a nivel clínico, los trasplantes de microbiota fecal han sido aplicados con gran éxito en el tratamiento de Clostridium difficile recurrente, lo que unido a su aparente carencia de efectos secundarios ha llevado a los expertos a plantearse su uso en el tratamiento de enfermedades crónicas como la EII. De hecho, un estudio reciente ha mostrado que la administración semanal a personas afectadas de CU de enemas fecales (procedentes de personas sanas) causa una remisión de la enfermedad (35). También se ha visto que individuos con síndrome metabólico trasplantados con microbiota fecal de individuos sanos delgados mejoraban el perfil de resistencia insulínica a los pocos días de dicho trasplante (36). Las implicaciones clínicas de estos cambios precisan de más estudios, aunque está claro que este abordaje emerge como una nueva vía terapéutica.
Recientemente, y dada la influencia directa de la dieta en la funcionalidad de la microbiota intestinal, se ha propuesto una nueva estrategia consistente en utilizar los metabolitos resultantes del metabolismo microbiano. En esta línea, Richards y cols. (37) han propuesto el empleo de ácidos grasos de cadena corta (AGCC), implicados directamente en la homeostasis de la mucosa intestinal, como una alternativa segura y económica para el tratamiento de las disbiosis asociadas a las dietas occidentales y que causan una disminución de los grupos bacterianos productores de AGCC.
De forma más visual, la tabla III recoge un esquema de posibles perspectivas de utilización de los simuladores gastrointestinales en la investigación clínica relativa a las enfermedades relacionadas con la microbiota intestinal. La versatilidad de estos equipos en relación al modo de alimentación (aguda/crónica), tiempo de operación, tipología de la microbiota inoculada, recogida de muestras, etc., permite llevar a cabo diseños experimentales adecuados que responden al objetivo planteado en cada caso (Tabla III).
En definitiva, y aunque todavía son necesarios más estudios científicos que avalen la relación causa-efecto entre la disbiosis intestinal y determinadas enfermedades, parece evidente que la restauración y el mantenimiento de una microbiota intestinal sana a través de la alimentación emerge como una nueva vía terapéutica. En este marco, el simulador gastrointestinal dinámico (simgi®), un equipo novedoso a la vez que versátil, se perfila como una herramienta potencialmente útil en el área de la nutrición clínica, como paso previo a los estudios de intervención en humanos, más costosos y con limitaciones éticas.
BIBLIOGRAFÍA
1. Cotillard A, Kennedy SP, Kong LC, Prifti E, Pons N, Le Chatelier E, et al. Dietary intervention impact on gut microbial gene richness. Nature 2013;500(7464):585-8.
2. Final Report Summary-METAHIT (Metagenomic of the Human Intestinal Tract); 2012.
3. De Filippo C, Cavalieri D, Di Paola M, Ramazzotti M, Poullet JB, Massart S, et al. Impact of diet in shaping gut microbiota revealed by a comparative study in children from Europe and rural Africa. Proc Natl Acad Sci 2010;107(33):14691-6.
4. Wu GD, Chen J, Hoffmann C, Bittinger K, Chen Y-Y, Keilbaugh SA, et al. Linking long-term dietary patterns with gut microbial enterotypes. Science 2011;334(6052):105-8.
5. Zhernakova A, Kurilshikov A, Bonder MJ, Tigchelaar EF, Schirmer M, Vatanen T, et al. Population-based metagenomics analysis reveals markers for gut microbiome composition and diversity. Science 2016;352(6285):565-9.
6. Graf D, Di Cagno R, Fåk F, Flint HJ, Nyman M, Saarela M, et al. Contribution of diet to the composition of the human gut microbiota. Microb Ecol Health Dis 2015;26:26164.
7. David LA, Maurice CF, Carmody RN, Gootenberg DB, Button JE, Wolfe BE, et al. Diet rapidly and reproducibly alters the human gut microbiome. Nature 2014;505(7484):559-63.
8. Wu GD, Compher C, Chen EZ, Smith SA, Shah RD, Bittinger K, et al. Comparative metabolomics in vegans and omnivores reveal constraints on diet-dependent gut microbiota metabolite production. Gut 2014;65(1):63-72.
9. Taguer M, Maurice CF. The complex interplay of diet, xenobiotics, and microbial metabolism in the gut: Implications for clinical outcomes. Clin Pharmacol Ther 2016;99(6):588-99.
10. Boulangé CL, Neves AL, Chilloux J, Nicholson JK, Dumas M-E. Impact of the gut microbiota on inflammation, obesity, and metabolic disease. Genome Med 2016;8(1):1.
11. Chan YK, Estaki M, Gibson DL. Clinical consequences of diet-induced dysbiosis. Ann Nutr Metab 2013;63(Suppl. 2):28-40.
12. Kang S, Denman SE, Morrison M, Yu Z, Dore J, Leclerc M, et al. Dysbiosis of fecal microbiota in Crohn's disease patients as revealed by a custom phylogenetic microarray. Inflamm Bowel Dis 2010;16(12):2034-42.
13. Swidsinski A, Weber J, Loening-Baucke V, Hale LP, Lochs H. Spatial organization and composition of the mucosal flora in patients with inflammatory bowel disease. J Clin Microbiol 2005;43(7):3380-9.
14. Mukhopadhya I, Hansen R, El-Omar EM, Hold GL. IBD-what role do Proteobacteria play? Nat Rev Gastro Hepat 2012;9(4):219-30.
15. Joossens M, Huys G, Cnockaert M, De Preter V, Verbeke K, Rutgeerts P, et al. Dysbiosis of the faecal microbiota in patients with Crohn's disease and their unaffected relatives. Gut 2011;60(5):631-7.
16. Jeffery IB, Claesson MJ, O'Toole PW, Shanahan F. Categorization of the gut microbiota: enterotypes or gradients? Nat Rev Microbiol 2012;10:591-2.
17. Tojo González R, Suarez Gonzalez A, Rúas Madiedo P, Mancebo Mata A, Pipa Muñiz M, Barreiro Alonso E, et al. Síndrome de Intestino Irritable; papel de la microbiota y probiótico-terapia. Nutr Hosp 2015;31(s01):83-8.
18. Karlsson CL, Önnerfält J, Xu J, Molin G, Ahrné S, Thorngren-Jerneck K. The microbiota of the gut in preschool children with normal and excessive body weight. Obesity 2012;20(11):2257-61.
19. Le Chatelier E, Nielsen T, Qin J, Prifti E, Hildebrand F, Falony G, et al. Richness of human gut microbiome correlates with metabolic markers. Nature 2013;500(7464):541-6.
20. Larsen N, Vogensen FK, van den Berg FW, Nielsen DS, Andreasen AS, Pedersen BK, et al. Gut microbiota in human adults with type 2 diabetes differs from non-diabetic adults. PloS one 2010;5(2):e9085.
21. Mayer EA, Knight R, Mazmanian SK, Cryan JF, Tillisch K. Gut microbes and the brain: paradigm shift in neuroscience. J Neurosci 2014;34(46): 15490-6.
22. Williams C, Walton G, Jiang L, Plummer S, Garaiova I, Gibson GR. Comparative analysis of intestinal tract models. Annu Rev Food Sci Technol 2015;6:329-50.
23. Elashoff JD, Reedy TJ, Meyer JH. Analysis of gastric emptying data. Gastroenterology 1982;83(6):1306-12.
24. Barroso E, Cueva C, Peláez C, Martínez-Cuesta MC, Requena T. Development of human colonic microbiota in the computer-controlled dynamic SIMulator of the GastroIntestinal tract SIMGI. LWT-Food Sci Technol 2015;61(2):283-9.
25. Cueva C, Jiménez-Girón A, Muñoz-González I, Esteban-Fernández A, Gil-Sánchez I, Dueñas M, et al. Application of a new dynamic gastrointestinal simulator (SIMGI) to study the impact of red wine in colonic metabolism. Food Res Int 2015;72:149-59.
26. Miralles B, del Barrio R, Cueva C, Recio I, Amigo L. In vitro dynamic gastric digestion of whey proteins. Comparison with the Infogest-harmonized model. 29th Effost International Conference Proceedings 2015:1853-8.
27. Muñoz-González I, Jiménez-Girón A, Martín-Álvarez PJ, Bartolomé B, Moreno-Arribas MV. Profiling of microbial-derived phenolic metabolites in human feces after moderate red wine intake. J Agr Food Chem 2013;61(39):9470-9.
28. Gil-Sánchez I, Cueva C, Sanz-Buenhombre M, Guadarrama A, Moreno-Arribas MV, Bartolomé B. Dynamic gastrointestinal digestion of grape pomace extracts: Bioaccessible phenolic metabolites and impact on human gut microbiota. J Food Compos Anal 2017. DOI: 10.1016/j.jfca.2017.05.005.
29. Barroso E, Montilla A, Corzo N, Peláez C, Martínez-Cuesta MC, Requena T. Effect of lactulose-derived oligosaccharides on intestinal microbiota during the shift between media with different energy contents. Food Res Int 2016;89:302-8.
30. Everard A, Lazarevic V, Gaïa N, Johansson M, Ståhlman M, Backhed F, et al. Microbiome of prebiotic-treated mice reveals novel targets involved in host response during obesity. ISME J 2014;8(10):2116-30.
31. Marchesi JR, Adams DH, Fava F, Hermes GD, Hirschfield GM, Hold G, et al. The gut microbiota and host health: a new clinical frontier. Gut 2016; 65(2):330-9.
32. Cueva C, Moreno-Arribas MV, Martín-Álvarez PJ, Bills G, Vicente MF, Basilio A, et al. Antimicrobial activity of phenolic acids against commensal, probiotic and pathogenic bacteria. Res Microbiol 2010;161(5):372-82.
33. Tomás-Barberán FA, García-Villalba R, González-Sarrías A, Selma MV, Espín JC. Ellagic acid metabolism by human gut microbiota: Consistent observation of three urolithin phenotypes in intervention trials, independent of food source, age, and health status. J Agri Food Chem 2014;62(28):6535-8.
34. Moreno-Indias I, Sánchez-Alcoholado L, Pérez-Martínez P, Andrés-Lacueva C, Cardona F, Tinahones F, et al. Red wine polyphenols modulate fecal microbiota and reduce markers of the metabolic syndrome in obese patients. Food Funct 2016;7:1775-87.
35. Moayyedi P, Surette MG, Kim PT, Libertucci J, Wolfe M, Onischi C, et al. Fecal microbiota transplantation induces remission in patients with active ulcerative colitis in a randomized controlled trial. Gastroenterology 2015;149(1):102-9.36.
36. Vrieze A, Van Nood E, Holleman F, Salojärvi J, Kootte RS, Bartelsman JFWM, et al. Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with metabolic syndrome. Gastroenterology 2012;143(4):913-6.e7.
37. Richards JL, Yap YA, McLeod KH, Mackay CR, Mariño E. Dietary metabolites and the gut microbiota: an alternative approach to control inflammatory and autoimmune diseases. Clin Transl Immunology 2016;5(5):e82.
 Dirección para correspondencia:
Dirección para correspondencia:
Carolina Cueva Sánchez.
Departamento Biotecnología y Microbiología de Alimentos.
Instituto de Investigación en Ciencias de la Alimentación (CIAL) CSIC-UAM, CEI UAM+CSIC.
C/ Nicolás Cabrera, n.º 9.
28049 Madrid
e-mail: carolina.cueva@csic.es
Recibido: 19/04/2017
Aceptado: 17/08/2017