INTRODUCCIÓN
La cirugía del cruce duodenal (CD) consta de dos operaciones, gastrectomía vertical (GV) más derivación biliopancreática (DBP). Es la técnica más compleja en cirugía bariátrica por obesidad mórbida (OM). El CD combina la restricción de la ingesta de alimentos y la malabsorción en el intestino delgado. Scopinaro comenzó la DBP en 1976 (1).
Hess (2) describe cómo: a) la GV elimina la curvatura mayor gástrica, reduce el volumen gástrico y la ingesta, y permite un vaciado normal; y b) deriva la ingesta post-píloro desde duodeno a íleon, DBP, para causar malabsorción.
Hess (3) recomienda medir todo el intestino delgado, sin tensión, desde Treitz hasta válvula ileocecal y utiliza el 50% de su longitud proximal como asa biliopancreática (ABP), el 10% distal como asa común (AC) y el 40% intermedio como asa alimentaria (AA).
Marceau (4,5) hacía DBP estándar hasta 1991 y cambió al CD y es el primer autor que publica (6) en 1993 la gastrectomía parietal más DBP.
Lagacé (7) informó sobre los primeros buenos resultados del CD en 61 pacientes en 1995 y Marceau comparó en 1998 (8) 252 DBP con gastrectomía distal y 465 CD con una mortalidad operatoria del 1,7%.
Hess (9) y Baltasar (10 11 12 13 14 15 16-17) describen la parte gástrica de la operación como gastrectomía vertical (GV) y creación de un tubo gástrico (TG). Anthone (18) y Almogy (19) lo llamaron gastrectomía longitudinal y Rabkin (20), gastrectomía de la curvatura mayor.
El CD (21 22 23 24 25-26) se estandarizó en los años 90 (Fig. 1). Hess (9) modificó el procedimiento invaginando y suturando la serosa de la GV en los siguientes 188 casos para reducir la incidencia de fugas en la línea de grapas. Ren (27) hizo el primer CDL completo en julio de 1999 y Baltasar (28) realizó el primer CDL en Europa en el año 2000 (29). Paiva (30) en Brasil y Scopinaro (31) en Italia hacen en el año 2000 la primera DBP laparoscópica estándar.
Para medir resultados del peso, se usa el índice de masa corporal (IMC = kg/m2) de Quetelet, pero después de revisar 7.410 pacientes, nuestro matemático desarrolló el concepto de IMC predictivo (32) tomando como control un IMC inicial superior a 25 (IMCI; 25 sería el de un peso ideal) y hace el cálculo no desde el IMCI sino desde el IMCI en exceso de 25. Los porcentajes de pérdida de sobrepeso perdido (PSP) no son iguales en un sujeto con OM grado 2 que en un sujeto con obesidad triple, y de esta forma solo medimos el IMC en exceso de 25. El porcentaje de pérdida de peso en exceso sería entonces del IMC predictivo = IMCI x 0.4 + 11,75. Este concepto ha sido ya utilizado por otros (33) de forma positiva.
TÉCNICA OPERATORIA
Cruce duodenal abierto (CDA) por laparotomía
El paciente está en posición forzada de Trendelenburg. La operación la realizan tres cirujanos a través de una incisión supraumbilical transversa entre ambos márgenes costales (Fig. 2A y B). Ya en el abdomen, se seccionan los ligamentos redondo y falciforme y se extirpan la vesícula biliar y el apéndice.
Se mide todo el intestino empezando por distal, desde la válvula ileocecal, y se marca con un clip el asa común (AC) como 10% del intestino. El asa alimentaria (AA) corresponde al 40% del intestino más proximal y se divide con una grapadora lineal. El 50% más proximal es el asa biliopancreática (ABP) y empieza en el duodeno proximal, D1. Se empalma el AA distal a la unión ABP y AC por una anastomosis yeyuno-ileal (AYI) con sutura absorbible continua monoplano y se cierra el defecto mesentérico con una sutura no reabsorbible.
Se expone el estómago y se introduce una sonda nasogástrica de 12 mm como guía a la curvatura menor. Se devasculariza toda la curvatura mayor gástrica con bisturí ultrasónico desde 3 cm distal al píloro hasta el ángulo de His. Se divide secuencialmente el estómago con grapadoras desde el píloro hasta la unión esofagogástrica y se extirpa incluyendo la curvatura gástrica mayor. En curvatura menor queda el tubo gástrico (TG), que se refuerza con sutura invaginante continua y que incluye el epiplón separado y ambas paredes gástricas, evitando su torsión y fugas.
Se crea un túnel retroduodenal, distal a la arteria gástrica derecha, y se divide duodeno en D1 con grapadora lineal. Una sutura invertida refuerza el muñón duodenal.
El AA proximal pasa retrocólica por la derecha y se realiza una anastomosis duodeno-ileal (ADI) en sutura continua reabsorbible. La operación tiene cuatro líneas de sutura (refuerzo gástrico, ADI, AYR y el muñón duodenal distal). Se colocan dos drenajes, uno al lado del TG y otro en la ADI.
La incisión abdominal se cierra en dos planos con Maxon continuo. Tras perder peso, la longitud de la cicatriz se reduce en un tercio (Fig. 2B) y permite a la abdominoplastia alcanzar el área púbica (Fig. 2C). Iniciamos el CDA el 17 de marzo de 1994 y el tiempo quirúrgico medio fue de 91 minutos.
Cruce duodenal laparoscópico (CDL)
Se realiza también por un equipo de tres cirujanos. Se usan seis puertos. Un trocar óptico de Ethicon # 12 ingresa al abdomen, bajo visión, en el borde lateral del músculo recto derecho, a tres traveses de dedo y por debajo del margen costal, y es el puerto principal de trabajo. Un puerto supraumbilical de 10 mm se usa para la cámara en la línea media (Fig. 3). El resto de cuatro trocares de 5 mm son tipo Ternamian, que no se deslizan. Colocamos dos subcostales situados a derecha e izquierda, uno en el hipocondrio izquierdo y otro en el epigastrio utilizado para retraer el hígado. El resto del procedimiento es como en la técnica abierta.
Las anastomosis son manuales monocapa, se inician con el punto deslizante autobloqueante de Serra-Baltasar (38,39) y finalizan con el nudo Cuschieri (40). Para evitar lesiones serosas, todo el intestino se mide con pinzas marcadas a 5 cm de distancia. Extraemos el estómago sin bolsa protectora. Una sutura Maxon cierra el puerto de 12 ms. Iniciamos el CDL el 5 de septiembre de 2000 (41). El tiempo operatorio promedio fue de 155’ después de los primeros 50 casos.
Al alta, los pacientes recibieron prescripciones con complejo multivitamínico (Centrum Forte), vitamina A 20.000 UI, vitamina D 50.000 UI, carbonato de calcio 1.000 mg y sulfato ferroso 300 mg y vitaminas B1 y B12.
MATERIAL Y MÉTODO
Fueron intervenidos 950 pacientes OM consecutivos (518 CDA y 432 CDL) desde 1994 hasta 2011, después de una evaluación preoperatoria multidisciplinaria completa y consentimiento informado legal; 782 eran mujeres (82,3%) y 168 eran hombres (17,7%). La edad promedio fue de 35 años (24-63). Fueron operados 474 ciudadanos extranjeros (376 de Estados Unidos, seis de Canadá, 71 de Noruega y 23 de Inglaterra) por el mismo personal quirúrgico, en la clínica privada.
El IMCI promedio (kg/m2) era de 49,23 kg/m2 (mujeres 49,26 y hombres 49,07). Rango de obesidad: a) obesidad no grave, grado 2 con comorbilidades (IMCI < 40), 110 pacientes (media 37,66); b) obesos mórbidos (IMCI 40-50), 464 pacientes (media 45,11); c) superobesos (SO) (IMC de 50-60), 272 pacientes (media 54,32); y d) pacientes con obesidad triple (OT) e IMCI > 60, 104 pacientes (media > 66,50) y un paciente con IMCI-100.
Con respecto a las comorbilidades, 115 pacientes sufrían diabetes tipo 2 (DMII); 103, hipertensión; cinco, enfermedades cardiacas; 62, dislipidemias; 19, síndrome de la apnea obstructiva del sueño (SAOS); 16, osteoartritis; y uno, un pseudotumor cerebral.
RESULTADOS
PRINCIPALES COMPLICACIONES INTRAOPERATORIAS
Tres pacientes necesitaron traqueotomía por fallo de intubación oral y desaturación severa, sin incidentes.
En tres pacientes, la sonda gástrica de 12 mm no pasó más allá de cardias y el engrapado del estómago se hizo visualmente.
La mortalidad operatoria a 30 días ocurrió en seis CDA pacientes (1,38%). Las causas fueron: a) fuga en ADI: 1; b) fuga AYR, rabdomiólisis y fracaso multiorgánico: 1; c) embolia pulmonar: 2; d) fuga en el muñón duodenal: 1; y e) fuga en su ángulo de His: 1. Dos pacientes con CDL murieron (0,38%) por émbolos pulmonares. La mortalidad promedio de ambos grupos fue del 0,84%.
MORBILIDAD POSTOPERATORIA
Fugas
Hubo 46 fugas para una tasa de fugas total del 4,84%.
Fugas en su ángulo de His: veintiún casos (2,3% de incidencia). Fueron tratadas con endoprótesis en diez casos, drenaje o laparotomía y derivación en Y-de-Roux en tres casos. Uno de los pacientes murió.
Fuga del muñón duodenal: un paciente sufrió una fuga en el muñón duodenal que se reparó, pero murió de sepsis. Desde entonces, protegemos todo grapado del muñón duodenal con una sutura invaginante y no ha habido más fugas.
Fugas de ADI: veinticuatro casos (2,5% de incidencia) y es la anastomosis más difícil. Diecinueve de ellos sufrieron fugas tempranas, que se trataron exitosamente con drenaje o se volvió a realizar la anastomosis. Cinco casos presentaron fugas tardías (hasta 2-14 años después) y necesitaron una nueva operación y rehacer la anastomosis. En un caso, la fuga se produjo tres años después de la intervención, como una fístula gastropleural, y se trató con gastrectomía total.
Fuga en AYR: a un paciente con divertículo de intestino delgado a 100 cm de la válvula ileocecal se le extirpó y se realizó una AYR abierta en el sitio sin incidentes. Hubo fuga y las pruebas radiológicas de diagnóstico no aclararon la causa. Con diagnóstico tardío, fue reexplorado, sufrió rabdomiólisis y falleció.
Embolia pulmonar
Dos pacientes con BMI-70 y BMI-65 tuvieron embolia a pesar de la terapia profiláctica y murieron. La trombosis venosa profunda en un caso fue tratada con éxito.
Hígado
Trastornos hepáticos: doce pacientes sufrieron alteraciones tempranas en la función hepática, con elevaciones significativas de bilirrubina (hasta 15 y 29) y resueltas con tratamiento médico.
Fallo hepático: dos pacientes sufrieron insuficiencia hepática (0,2%). El primero ocurrió en una paciente seis meses después de la cirugía; se incluyó en lista de trasplante hepático urgente pero murió a la falta de donante. La segunda paciente sufrió insuficiencia hepática tres años después de la cirugía y recibió un trasplante de hígado exitoso más reversión de la DBP. Está sana cuatro años después. Un paciente ha fallecido 13 años tras CDA por alcoholismo.
Desnutrición calórica-proteica (DCP)
Treinta y tres pacientes (3,3%) desarrollaron DCP y 24 requirieron alargamiento del AC. Trece de ellos se hicieron abiertos sin complicaciones. En once casos, el AC se alargó laparoscópicamente y en dos de ellos el intestino delgado resultó lesionado por las pinzas de disección, que perforaron fácilmente por debilidad de la pared (Fig. 4). Ambos casos fueron diagnosticados intraoperatoriamente y reparados, pero murieron más tarde debido a fugas. Se encontraron múltiples hernias mucosas en la débil pared muscular entre los vasos del mesenterio. Este tipo de hernias no han sido informadas previamente. Por lo tanto, recomendamos laparotomía para el alargamiento intestinal.
Fístula pancreática-cutánea (Fig. 5): las dos fístulas y las lesiones de la piel sanaron espontáneamente.
Hipoglucemia: dos pacientes tuvieron episodios recurrentes de hipoglucemia que requirieron reversión de la DBP.
Evisceración: se dio en cuatro casos sin consecuencias después de una reparación adecuada.
Obstrucción intestinal tardía: siete casos (incidencia del 0,73%). Tratamos a dos en nuestra unidad y los otros fueron tratados en otras unidades, con resección del intestino delgado.
Beriberi: tres casos presentaron deficiencia de vitamina B1 con síntomas neurológicos, cambios en la marcha y caída espontánea. Todos fueron corregidos con éxito. Esta grave complicación necesita administración urgente de B1 intravenosa.
Fracturas: fueron debidas a la mala absorción de Ca y requirieron vitamina D25 más Ca. Se presentaron dos casos que son asintomáticos después de la atención adecuada.
Megacolon tóxico: debido a colitis pseudomembranosa 16 años después de la cirugía. La paciente requirió una colectomía subtotal a 22 cm del ano, con ileostomía terminal. Más tarde se unió el íleon al recto.
Varios: neumonía (cuatro casos), seroma (cuatro casos), infección de herida (15 casos), hemorragias digestivas (cinco casos, tres de los cuales requieren laparotomía) y sepsis relacionada con el catéter (tres casos).
MORTALIDAD A LARGO PLAZO
Se dieron una apendicitis aguda no diagnosticada a los dos años y una necrosis intestinal por hernia interna a los tres años. Hubo otras causas de muerte no relacionadas con el CD (cáncer, melanoma, infarto de miocardio, etc.).
RESULTADOS DE PÉRDIDA DE PESO
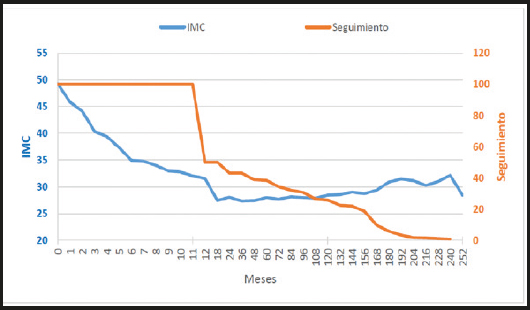
El IMCF se midió en el 60% de 914 pacientes al año y en el 30% a los ocho años. El IMCI medio de 49,3 cayó a un IMCF medio de 30 y el porcentaje de pérdida de IMC (PPIMC) fue del 80% a los 12 meses (Fig. 6).
La figura 6 muestra en azul la caída del promedio del IMC, que bajó alrededor de 30, y en rojo el porcentaje de seguimiento.
La figura 7 muestra, en azul, el IMC esperado de 30 y en rojo, el porcentaje de IMC predictivo dependiente del rango del IMC inicial y que supera el 100% a partir de los 12 meses.
Por lo tanto, el PSP ha sido excelente en la serie y probablemente sea mejor que con cualquier otra operación de obesidad.
Hay que destacar que el CD es tan eficaz en los super/superobesos cuando se mide el %PIMCEsp, como se ve en la figura 8.
CORRECCIÓN DE COMORBILIDADES
Diabetes tipo II
El CD es una operación muy efectiva para tratar la diabetes. El 98% de nuestros pacientes son normoglucémicos, con una hemoglobina glicosilada normal. Dos pacientes no diabéticos sufrieron hipoglucemia grave y hubo que revertir la DBP. La hipertensión se corrigió en el 73% de los casos y la apnea del sueño, en el 100%.
CALIDAD DE VIDA
Utilizamos la clasificación Horia-Ardelt (41) de la escala BAROS para evaluar los cambios en la calidad de vida de los pacientes. Los cambios después de la cirugía incluyeron: autoestima, actividad física, actividad social, actividad laboral y actividad sexual en una escala de -1 a +1. El puntaje promedio fue de 2,03 de un máximo de tres puntos en 348 pacientes, lo que significa una mejora significativa en su calidad de vida.
Los síntomas gastrointestinales se evaluaron de un mínimo de 1 como excelente a un máximo de 5 como muy malo. En los 558 pacientes evaluados, la ingesta de alimentos de todos los tipos fue de 1,4, vómitos 1,3, apetito 1,96, tipo de deposiciones (de pastosas a líquidas) 2,2, frecuencia (de sin problema a intolerable) 1,8, olor a heces 3,35 e hinchazón abdominal 2,26. Por lo tanto, la suma de todas las medidas fue de 12,14, para una calificación total de 5 (excelente) a 35 (mala). El peor efecto secundario fue el mal olor de las heces, con una media de 3,35.
DISCUSIÓN
El CD nunca fue una terapia popular entre los cirujanos, posiblemente por su complejidad. Hess (6) describe cómo después de ver un vídeo nuestro en Seatle-1996, en la reunión de ASBS, modificó el procedimiento con una sutura de la curvatura mayor y solo tuvo una fuga en 188 casos (17).
Por su dificultad, muy pocos cirujanos siguieron haciendo el CD y, de hecho, se creó una subdivisión en la ASBS denominada “The Switchers”, con logo propio. Siguió siendo impopular y tuvimos que reunirnos, durante años, fuera de la sede de los congresos como un grupo aparte formado por 25-30 cirujanos.
Al contrario, “los del cruce” hemos seguido haciendo la intervención y muchos pacientes, incluso extranacionales, supieron de sus ventajas y buscaron esta terapia. No hemos escondido las dificultades de la operación ni, sobre todo, sus complicaciones. Más de 72 cirujanos bariátricos nos visitaron y hemos intervenido en directo en varios congresos nacionales y extranjeros. Nuestro vídeo de CDL fue segundo premio en IFSO 2002 de Sao Paulo (42). Tres pacientes requirieron una traqueotomía de emergencia (43,44).
En el año 2000 usamos endoprótesis rígida no extraíble (45) y luego, endoprótesis extraíbles (46). Nueve pacientes requirieron gastrectomía total (47). En tres pacientes usamos una derivación Y-de-Roux (48,49) en las fugas y esta es aceptada como la más eficaz (50).
Pueden ocurrir trastornos hepáticos (51,52) e incluso fallos con necesidad de trasplante (53-55), pero también en las DG (56), fístulas bronquiales (57) o pancreáticas (58), desnutrición calórica-proteica (59) y necesidad de alargamientos (60) para corregirlas con posibles fugas (61) por defectos herniarios de la pared intestinal.
En la conferencia de consenso de 2004, Buchwald (62) declaró que en OM, idealmente, la cirugía debe considerarse para pacientes con obesidad superior a clase I (IMC 30-34,9) y con condiciones comórbidas asociadas. Debe tener una baja morbilidad y mortalidad, mientras que proporciona un PSP óptimo y sostenido con efectos secundarios mínimos. Ninguna técnica bariátrica es 100% exitosa o duradera en todos los pacientes, ni existe un único procedimiento estándar, y probablemente nunca lo habrá. Además, la cirugía no puede ser la solución para los 1.700 millones de OM que pueblan la tierra.
Las fugas de la GV son causa de importante morbilidad manifestada en las reuniones específicas de GV de Deitel y Gagner (63). Antes de la década de 1990, esta complicación era rara y los cirujanos del CD (los “switchers”) fueron los primeros en comunicarla. La sutura invaginante seroserosa de la línea de grapas con epiplón evita la torsión del TG y las fugas (13).
El CD es un procedimiento largo y difícil que requiere cirujanos expertos y con experiencia. La mortalidad operatoria debería ser < 1% y la morbilidad, < 5%. Nuestra mortalidad del CDL es baja (0,38%). Como los pacientes con CD tienen cuatro líneas de sutura, la detección temprana de fugas es esencial.
Mason (64) llamó la atención sobre la taquicardia como primera señal de advertencia de fugas y ningún paciente debería ser dado de alta con taquicardia.
Duncan (65) ha dado alta precoz en cirugía ambulatoria sin estancia a más de 2.000 pacientes. Nuestra estancia tras CDL es de 2-3 días, instruimos (66) al ingreso a los pacientes para tomar pulso y temperatura de forma digital y nos notifican dichos parámetros cada cuatro horas, durante dos semanas, en una base de datos telemática. Los pacientes con cambio significativo en estos parámetros necesitan una consulta inmediata y urgente.
DeMaria (67) informó que 450 instituciones y 800 cirujanos participaron en el programa 2009 de BSCOE en dos años (2007-2009). A solo el 0,89% de los 57.918 pacientes se les hizo CDL.
English (68) informa en ASMBS-2016 que la obesidad ha aumentado de forma alarmante en las últimas cinco décadas en Estados Unidos, del 13,4% al 36,4% en 2014. Los costos indirectos de la obesidad y el impacto económico general se estiman en 1,42 billones de dólares, el 8,2% del producto interno bruto y más del doble del gasto en defensa. La obesidad es el quinto factor de riesgo más importante de mortalidad en el mundo. En ASMBS-2016 se realizaron 215.666 operaciones en 795 centros acreditados (GV: 58,1%) y aunque se hicieron 1.187 DBP, solo un 0,6% fue CD y el 26%, CDL.
Utilizando datos BOLD de 2007-2010, Nelson (69) identificó 78.951 pacientes sometidos a derivación gástrica (DG) o a CD. De estos pacientes, al 98% se les hizo DG y solo el 2% tenía CD. El CD se asoció con tiempos de operación quirúrgicos más largos, pérdida de sangre y estancias hospitalarias más prolongadas. Las tasas de reintervención temprana fueron más altas en el grupo con CD (3,3% vs. 1,5%). La caída del IMC fue significativamente mayor en los casos de CD en todos los intervalos de seguimiento (p > 0,05). En los SO (IMC > 50) también hubo mayor caída a los dos años, 79% de CD frente a 67% de DG. La mejora de las comorbilidades (diabetes, hipertensión y apnea del sueño) fue superior con CD (todas p < 0,05).
La tasa de reintervención fue del 14%. Las revisiones, incluidas las conversiones, pueden superar en breve el número de procedimientos primarios en bariatría, lo cual sugiere la necesidad de desarrollar mejores algoritmos basados en la evidencia para minimizar el uso de nuevas operaciones. Es evidente que el número de fallos es muy alto y se necesitan operaciones iniciales efectivas.
En 2005, Hess (9) describió 1.150 pacientes con CD e IMCI-50,9. En 15 años hubo ocho reversiones (0,61%) y 37 revisiones (3,7%). La DMII curó en el 98% de los pacientes. Los 19 adolescentes (de 14-18 años) mejoraron, por lo que aboga por CD como la mejor operación en adolescentes. Asimismo, concluyó que el CD es una operación segura y efectiva.
Iannelli (70), en 110 pacientes con IMC > 50, encontró una reducción en la tasa de complicaciones postoperatorias al realizar CD de dos etapas. Al estudiar el procedimiento, solo 39 pacientes (35,5%) requirieron GV y se evitó la DBP en el 74,5% de los pacientes.
Biertho (71) hizo CD en 1.000 pacientes en 2006-2010. La tasa de conversión en el grupo de laparoscopia fue del 2,6%. Hubo una muerte postoperatoria (0,1%) debido a embolia. La estancia hospitalaria media fue más corta con CDL que con CDA. Las complicaciones fueron del 7,5%, sin diferencias significativas.
Biertho (72) trató a 566 pacientes entre 2011-2015 con CDL con IMC-49 y sin mortalidad a los 90 días. La estancia promedio en el hospital fue de 4,5 días. Las complicaciones mayores a los 30 días ocurrieron en el 3,0% de los pacientes y las menores, en el 2,5%. El PSP fue del 81% a los 12 meses, del 88% a los 24 meses y del 83% a los 36 meses. Los pacientes con HbA1C por encima del 6% disminuyeron del 38% al 1,4%. La readmisión fue del 3,5% y solo el 0,5% de los pacientes necesitaron una nueva operación. La tasa de complicaciones a corto y medio plazo del CDL es como en los procedimientos bariátricos mixtos y con excelentes resultados metabólicos.
Biron (73) estudió la calidad de vida de 112 pacientes. El seguimiento fue de 8,8 años y observó mejora de la calidad de vida específica de la enfermedad a corto y largo plazo.
Prachand (74) observó en 152 pacientes con DG y PSP-54%. Y en 198 pacientes con CD y el PSP-68% y así mostró que el CD fue más efectivo.
Para Strain (75), el CD proporciona mejor PSP que la DG en pacientes con obesidad severa. El peso promedio disminuyó un 31,2% después de la DG y un 4,8% tras el CD.
Topart (76,77) realizó 83 CD y 97 DG entre 2002 y 2009, con IMCI-55. Después de tres años de seguimiento, el PSP promedio fue del 63,7% después de la DG y del 84,0% después de CD (p > 0,0001). Los resultados fueron significativamente mejores con CD que con DG.
Våge (78) trató a 182 pacientes consecutivos con CD entre 2001-2008 sin mortalidad a los 30 días. Un paciente necesitó cirugía debido a una fuga, tres pacientes debido a sangrado y uno debido a fugas de bilis. Seis pacientes (3,2%) se sometieron a revisión quirúrgica por DCP, lo que refleja datos similares a los nuestros (3,3%).
Søvik (79) mostró mejores PSP después de CD que con DG en pacientes con OM. El promedio de IMC disminuyó un 31,2% después del DG y un 44,8% después del CD.
Angrisani (80) informa que en 2018 se realizaron 685.874 operaciones bariátricas en todo el mundo, el 92,6% fueron intervenciones primarias, un 7,4% de revisión, un 96% quirúrgicas y el 4% endoluminales. Fueron GV el 53,6%, DG el 30,1%, DGUA (derivaciones gástricas de una anastomosis) el 4,8% y solo un 1,3% fueron CDL
En resumen, los pacientes sometidos a CD constantemente reducen el IMC más que los pacientes con DG. Entonces, ¿por qué hay tan pocos pacientes con CD?
Rabkin (81) informa que el CD no está asociado con deficiencias nutricionales extensas. Los estudios anuales de laboratorio, tras cualquier tipo de operación bariátrica, parecen ser suficientes para identificar tendencias desfavorables. En pacientes seleccionados son necesarios suplementos de hierro y calcio adicionales.
Keshishian (82) realizó una biopsia hepática con aguja preoperatoria en 697 pacientes con CD. Hubo empeoramiento transitorio de AST (13% del valor de referencia, p < 0,02) y ALT (130-160% de los niveles de referencia, p < 0,0001) hasta seis meses después del CD. Asimismo, observó una mejoría progresiva de tres grados en la gravedad de NASH y del 60% en la esteatosis hepática a los tres años tras CD.
DIABETES TIPO II
Buchwald (83) informa que CD y DBP tienen tasas de resolución de diabetes que superan el 90%. En comparación, la tasa de la DG es del 70%, aproximadamente. Tsoli (84) mostró que GV era comparable al DBP en la resolución de la DTII pero menor en la dislipidemia y la presión arterial.
Baltasar (85) trató en 2004 a un paciente con bajo IMC-35 con CDL sin GV con excelentes resultados a los diez años.
Våge (86) piensa que el CD es efectivo en DMII, hipertensión e hiperlipidemia y que la duración de la diabetes y la edad son los predictores preoperatorios más importantes.
Según Eisenberg (87), la hipoglucemia hiperinsulinémica refractaria después de la cirugía es muy rara y su fisiopatología aún no se ha dilucidado por completo. La pancreatectomía parcial se asocia con una morbilidad potencial importante y no debe recomendarse. La reversión de la DBP es la terapia más simple y la mejor operación para dichas hipoglucemias, y así lo hicimos a dos de nuestras pacientes.
En el CD por estadios, ¿qué parte de la operación se debe hacer? ¿La DBP o la GV? La mayoría de los cirujanos recomiendan hacer primero la GV.
Marceau (88) trató a 1.762 pacientes de 2001 a 2009, todos programados para CD. Como primera etapa, trató 48 DBP aisladas sin SG y 53 casos de GV aislada. Los resultados a largo plazo de PSP y resolución de anormalidades metabólicas fueron mejores con DBP aislada que con GV aislada. Los PSP con CD completa fueron superiores a los realizados en dos etapas. La GV y la DBP contribuyen de forma independiente a los resultados metabólicos beneficiosos.
Moustarah (89) trató a 49 pacientes SO con DBP sin GV. El peso inicial fue de 144 kg y el IMCI, de 52,54. La caída en el IMC de 14,5 kg/m2 fue muy significativa (p < 0,001).
La DBP sin GV ha sido raramente utilizada como procedimiento único de pérdida de peso, pero en pacientes cuyas indicaciones clínicas justifican la omisión del GV, la DBP aislada tiene mejores resultados de pérdida de peso. En esta serie, PSP a los dos años se compara favorablemente con otras operaciones bariátricas.
La ventaja es que la DBP sin SG es reversible y la GV puede agregarse en cualquier momento posterior. Creemos que, con estos resultados en mente, deberíamos hacer primero la DBP ya que es un procedimiento totalmente reversible y más fácil que el GV sobre todo en SSO, ya que se realiza en una parte más baja del abdomen. La GV, además, se puede agregar con más facilidad luego si fuese necesaria y en cualquier momento.
No debemos olvidar la extraordinaria participación de cirujanos españoles en desarrollar las técnicas malabsortivas. Larrad y Sánchez desarrollaron una técnica de DBP e hicieron varias publicaciones muy importantes (90,91). Así como Solano y Resa (92), Ballesteros (93) y Hoyuela (94).
La aportación de Sánchez-Pernaute y Torres (95), del Hospital Clínico de Madrid, al hacer una variante del CDL con el CD de una sola anastomosis (CDUA) es muy importante y además se está haciendo popular en todo el mundo.
Un problema mayor del seguimiento del paciente con CD es que otros médicos y/o cirujanos pueden no entender cómo prevenir o tratar sus complicaciones a largo plazo.
El seguimiento de los pacientes con CD es muy importante. Al alta, se proporcionan una explicación técnica detallada de la operación y una extensa hoja explicativa de los análisis de laboratorio necesarios de por vida, de cada una de las posibles complicaciones y de su corrección.
La determinación de albúmina sérica es el dato más importante a largo plazo para detectar DCP. Vigilar PTH y vitamina D25 para detectar malabsorción de calcio y prevenir patología. Los déficits de hierro deben tratarse con Fe intravenoso.
Además de las fugas, la complicación más grave a largo plazo de CD es la DCP. La corrección quirúrgica es simple porque emplea la técnica de anastomosis yeyuno-yeyunal denominada “operación X-en beso” para alargar el AC, preferiblemente por laparotomía.
Los pacientes OM deberían recibir al alta el DVD de su operación, para que, si es necesaria una nueva operación, el cirujano conozca al detalle la técnica original.
Y también conocer que el apoyo de Endocrinología, Enfermería y Nutrición es esencial en todo el proceso.
UN CAMBIO AL CRUCE DUODENAL
Una llamada de atención para cambiar al CD
Halawani (96) afirma que un tercio (34,9%) de los adultos estadounidenses son obesos. En los años 2011-2015, el número de CDL en Estados Unidos fue inferior al 1%. Hay que añadir el CD a la práctica de los Centros de Excelencia en Obesidad (CEO).
El CD da un PSP superior y tiene una tasa más baja de recuperación de peso. Además, es mejor que la DG, conserva el píloro y produce un vaciamiento gástrico más lento. Con ajustes a la longitud del AC y el tamaño del tubo gástrico, cualquier paciente obeso puede ser candidato a CD.
Los pacientes con IMC < 50 pueden ser también candidatos. El CD es una opción viable debido a su flexibilidad. El cirujano puede ajustar el tamaño del TG y alterar el impacto de la restricción. La longitud de AC puede ser variable.
El CD es bueno en pacientes crónicos, que usen antiinflamatorios no esteroideos y esteroides. La tasa de mortalidad temprana en comparación con la GVL (0,28%) es ligeramente más alta (0,43%), aunque todavía se considera un procedimiento complejo de alto riesgo y los resultados deben analizarse con cautela.
El CD es muy versátil y puede ofrecer un manejo integral de la obesidad y sus comorbilidades metabólicas. Con dedicación, capacitación adecuada y una educación integral, el CD se puede implementar en la práctica.
CONCLUSIONES
Las técnicas de CD no son comunes para el manejo de la OM. El CD es la técnica más compleja y su curva de aprendizaje es más larga que en otras operaciones. Para estandarizar la técnica, nos llevó al menos 25 casos en CDA y 50 en CDL. El CD es seguro y el más eficaz en términos de resultados de pérdida de peso a largo plazo.
CONSIDERACIONES ÉTICAS
Todos los procedimientos que involucran participantes humanos se realizaron en los estudios citados en este documento de acuerdo con los estándares éticos de los comités de investigación nacionales e institucionales y con la Declaración de Helsinki y sus enmiendas.
El consentimiento informado se obtuvo de todos los participantes individuales incluidos en los estudios citados.











 texto en
texto en