INTRODUCCIÓN
La nutrición parenteral domiciliaria (NPD) constituye hoy en día el tratamiento de elección para aquellos pacientes con fallo intestinal que dependan de la nutrición y de la fluidoterapia intravenosa para poder mantener un adecuado estado nutricional sin requerir la hospitalización convencional. Esta técnica surgió en la década de los setenta, aunque no se inició en España hasta los años ochenta, y ha permitido aumentar la supervivencia y la calidad de vida de estas personas.
Debido a los avances médico-quirúrgicos y al desarrollo de la hospitalización domiciliaria, la prescripción de la NPD se ha incrementado sustancialmente en la última década y, con ello, también han variado sus indicaciones, así como la prevalencia y complicaciones asociadas. De esta forma, hoy en día son numerosos los pacientes con patología oncológica que reciben NPD, mientras que en los inicios de esta técnica las patologías eran en su mayoría de origen benigno. Debido al progreso de este soporte nutricional, recientes estudios encontraron, además, un mejor pronóstico para aquellos pacientes con NPD frente a los que reciben un trasplante intestinal, especialmente en aquellos con síndrome de intestino corto (1-4), lo que explica que el trasplante intestinal no haya tenido el mismo éxito que el trasplante de órganos sólidos (riñón, corazón e hígado).
El conocimiento de su epidemiología es fundamental como punto de partida a la hora de plantear directrices o guías que estandaricen su uso; no obstante, actualmente no disponemos de un registro nacional que nos proporcione dichos datos. Para suplir esta deficiencia, cada año, el grupo de Nutrición Artificial Domiciliaria y Ambulatoria (NADYA), de la Sociedad Española de Nutrición Clínica y Metabolismo (SENPE), publica un informe anual del registro de pacientes, elaborado con la información comunicada voluntariamente por los profesionales sanitarios. Según sus últimos datos publicados, la prevalencia en España se sitúa en 6,61 pacientes/millón de habitantes para el año 2017; sin embargo, en otros países el uso de la NPD ha evolucionado de forma muy variable y los datos disponibles de prevalencia son muy dispares (6-8). En el caso de Andalucía, la prevalencia es similar a la del resto de España (9).
Este estudio tiene el objetivo de analizar los diferentes datos epidemiológicos y de práctica clínica en NPD mediante una revisión sistemática de la bibliografía disponible.
MATERIAL Y MÉTODOS
CRITERIOS DE SELECCIÓN
Se llevó a cabo una revisión sistemática en concordancia con la guía PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analysis). Los criterios de inclusión de los estudios según PICOS (Población, Intervención, Comparación, Resultados y Diseño del estudio) y los criterios de exclusión para la revisión sistemática se recogen en la tabla I.
FUENTES DE INFORMACIÓN
Se llevó a cabo una búsqueda bibliográfica por lenguaje controlado de la literatura publicada en los diez últimos años (desde enero de 2009 hasta marzo de 2019) en las principales bases de datos: MEDLINE (PubMed) y EMBASE. La última, se ejecutó con fecha 27 de marzo de 2019. La estrategia de búsqueda se detalla en el Anexo I.
Para completar la búsqueda y reducir los posibles sesgos de publicación, se examinó detenidamente el listado bibliográfico de los artículos seleccionados en el paso anterior, para así poder identificar estudios que no fueran detectados en la revisión.
Los autores establecieron de forma consensuada los criterios de inclusión y exclusión a aplicar y, si había alguna discrepancia, se decidió por mayoría.
SELECCIÓN DE ESTUDIOS Y EVALUACIÓN DE LA CALIDAD
En primer lugar, los duplicados fueron eliminados. A continuación, dos revisores (MM y HR) de manera independiente seleccionaron los artículos a partir de la información obtenida del título y del resumen, y procedían a leer el texto completo si fuese necesario.
Para asegurar la reproducibilidad y minimizar el sesgo, un tercer revisor (RS) resolvió cualquier desacuerdo. Posteriormente, se llevó a cabo una lectura crítica de los artículos seleccionados a texto completo.
Para evaluar la calidad de los artículos, se realizó una búsqueda de las herramientas aplicables a estudios observacionales; sin embargo, no se encontró ninguna que se ajustara al diseño de nuestros manuscritos. Por ello, se tuvo en cuenta que este tipo de estudios son susceptibles de verse afectados por diferentes sesgos, aunque todos estaban publicados en revistas científicas de prestigio, por lo que asumimos que cumplen criterios de rigor metodológico.
EXTRACCIÓN DE DATOS Y RESULTADOS
Se realizó un análisis descriptivo de las principales características de los estudios seleccionados. Para ello, se extrajeron distintas variables, que se expusieron en forma de tabla. Las principales características del estudio recogidas fueron: país, años de seguimiento, número de pacientes incluidos, si se trataba de un estudio unicéntrico o multicéntrico y los criterios de inclusión en el estudio. Además, se extrajeron las variables demográficas, entre las que distinguimos edad de los pacientes al inicio de la NPD y sexo, así como variables epidemiológicas, tales como la patología de base (distinguiendo entre maligna o benigna) y el motivo de indicación de NPD. Finalmente, se recogió la duración media de la NPD, el tipo de catéter, el número de catéteres, las complicaciones asociadas a la NPD, la causa del fin, el motivo de exitus en los pacientes fallecidos, la supervivencia, el porcentaje de adaptación intestinal y otras variables estudiadas por los distintos autores, en cuyos resultados no nos hemos centrado por tratarse de aspectos muy concretos de cada estudio.
Es importante mencionar que, a la hora de extraer las variables, estas se recogieron en la forma o unidades más habituales para luego poder realizar una comparación entre los distintos estudios, por lo que aquellas expresadas de manera distinta a la estipulada por los autores se recalcularon o, de no ser posible, se consideraron como “no documentado” .
Para la exposición de resultados, se realizaron dos tablas independientes. La primera contenía los datos obtenidos de los artículos basados en sujetos adultos y los que incluían tanto pacientes adultos como pediátricos, dado que los datos de las dos poblaciones se expresaban de forma conjunta. En la segunda, se recogían los resultados de los artículos que se centraban exclusivamente en población pediátrica. Aquellas variables analizadas en las cohortes con población adulta, pero que no fueron estudiadas en la población pediátrica, se eliminaron de dicha tabla.
RESULTADOS
BÚSQUEDA BIBLIOGRÁFICA
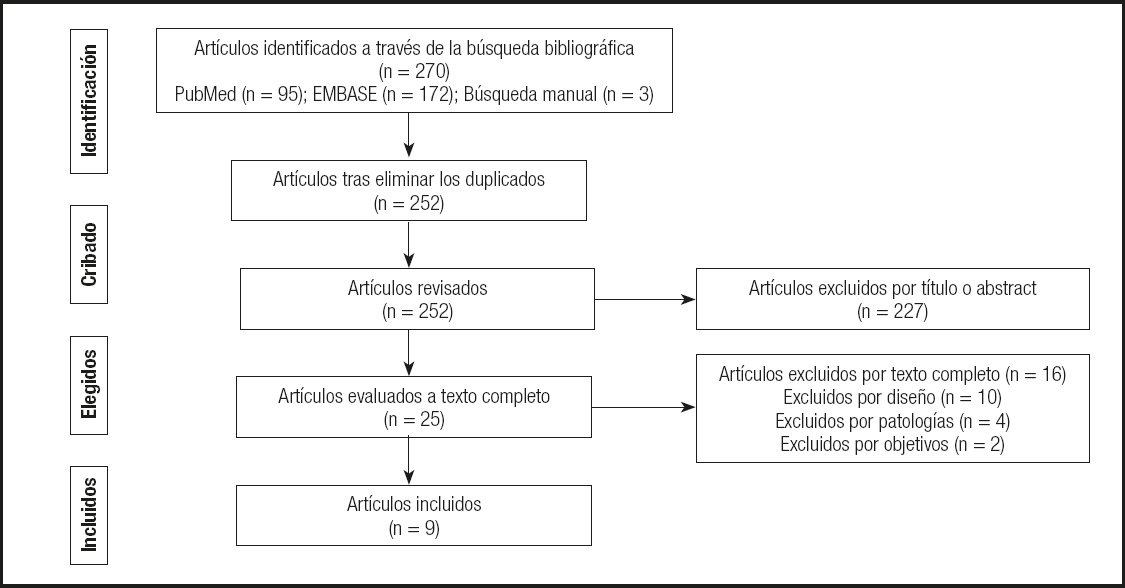
Se identificaron un total de 267 artículos procedentes de las distintas bases de datos consultadas (95 en PubMed y 172 en EMBASE).
Finalmente, 9 artículos fueron los seleccionados por cumplir los criterios de inclusión y ninguno de exclusión. Todos ellos eran estudios descriptivos, de los cuales 8 eran retrospectivos y el restante, prospectivo. La figura 1 expone a través de un diagrama de flujo el proceso de selección llevado a cabo por los autores.
Los principales motivos de exclusión de los estudios tras su lectura a texto completo fueron que presentaran un diseño distinto al establecido, que los objetivos no cumplieran con los fijados y que se centraran en patologías concretas o excluyeran algunas de ellas.
LIMITACIONES Y CONSIDERACIONES PREVIAS
A la hora de expresar sus resultados, cabe mencionar que el estudio llevado a cabo por Spiliotis y cols. (10) consideró como patología de base el síndrome de intestino corto (SIC), mientras que, en otros artículos, se considera una indicación de NPD subyacente a otra enfermedad. Por otra parte, Vafa y cols. (11) no analizan los datos de forma global, sino que en todo momento hacen una separación entre patologías malignas y benignas.
Por otro lado, tanto Higuera y cols. (12) como Dibb y cols. (13) incluyen en sus estudios tanto población adulta como pediátrica, sin hacer distinción en los resultados, por lo que sus resultados se analizaron conjuntamente en este trabajo.
El estudio de Hallum y cols. (14) es el único prospectivo, por lo que la duración máxima está limitada al período de estudio.
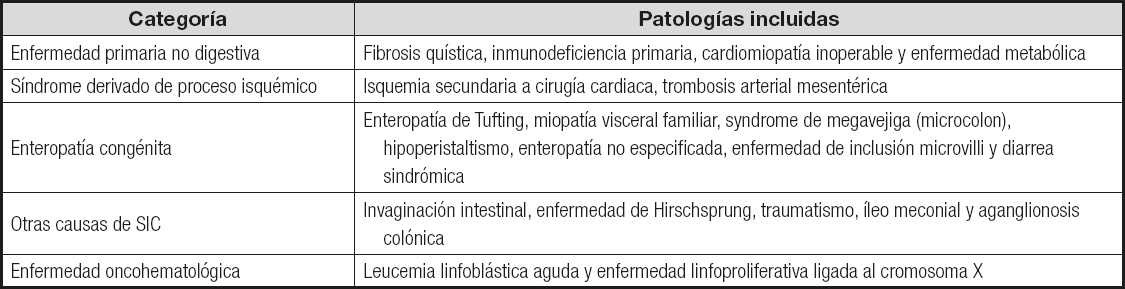
En relación con los tres artículos que incluyen exclusivamente población pediátrica (15-17), en todos ellos se expresan de forma conjunta los diagnósticos y las indicaciones de la NPD, sin hacer distinción clara entre ambos, por lo que se decidió exponer estos datos unificando ambas variables. Además, debido a su elevada heterogeneidad, se agruparon en las categorías recogidas en la tabla II.
Tabla II. Agrupación por categorías de las principales indicaciones y diagnósticos en pacientes pediátricos
Por último, Abi Nader y cols. (15), a la hora de calcular los pacientes que logran la conversión a vía oral y la duración de la terapia, descartan del total aquellos que fallecieron con NPD. Por su parte, Brown y cols. (16) también excluyen de ciertos cálculos tres pacientes por ser un tratamiento paliativo.
ESTUDIOS EN POBLACIÓN ADULTA
En la tabla III se recogen las diferentes variables extraídas de los artículos. Cabe destacar que todos ellos tienen una muestra de pacientes considerable, que oscila entre 91 (12) y 545 (13). Además, todos ellos se desarrollan dentro del continente europeo. La edad de inicio se distribuye en torno a una media de 51,86 ± 3,53 años.
Tabla III. Variables extraídas de los estudios basados en población adulta
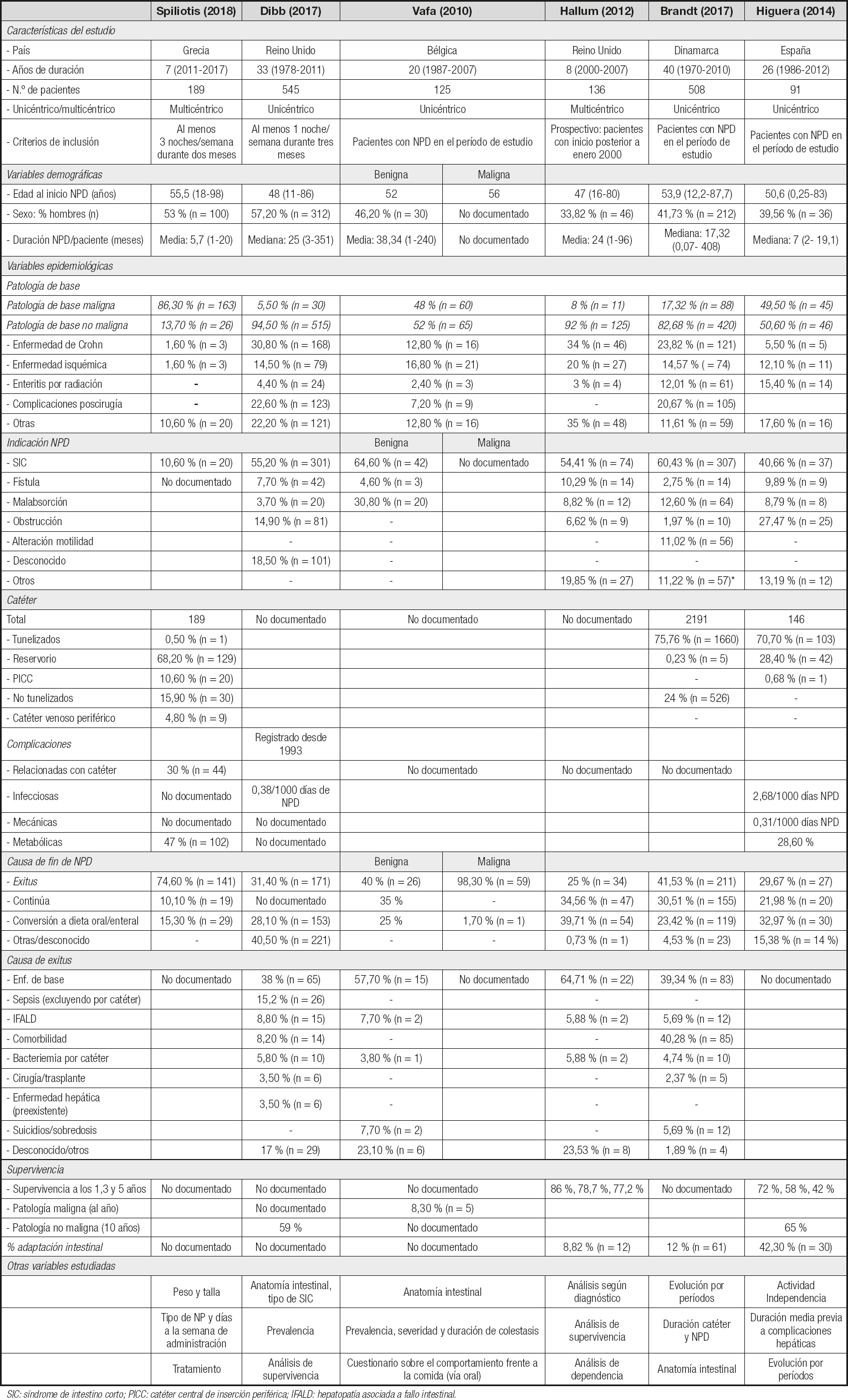
SIC: síndrome de intestino corto; PICC: catéter central de inserción periférica; IFALD: hepatopatía asociada a fallo intestinal.
Se halló una gran diferencia en las patologías de base de los pacientes incluidos en los diferentes estudios: en 5 de los 6 artículos la patología de base no oncológica fue mayoritaria; sin embargo, los porcentajes en los que se presentó variaron entre un 13,70 % y un 94,5 %. En cuanto a las patologías oncológicas, su representación osciló entre un 5,50 % y un 86,36 % de los pacientes incluidos.
En cuanto a las indicaciones de NPD, todas las publicaciones que han recogido al detalle esta variable coinciden en que la indicación más frecuente es el SIC con porcentajes que oscilan entre el 40,66 % (12) y el 60,43 % (18).
Tan solo la mitad de los estudios analiza el tipo de catéter empleado. Examinando los datos, observamos que tanto Higuera y cols. (12) como Brandt y cols. (18) coinciden en el uso mayoritario del catéter tunelizado, con porcentajes que rondan el 70 %, mientras que Spiliotis (10) recoge un mayor porcentaje de reservorios (68,20 %).
Respecto a la causa de fin de la NPD, cabe destacar que el estudio español no muestra una proporción superior de pacientes fallecidos cuando se compara con otros estudios con una mayoría de pacientes no oncológicos. En el estudio griego, sin embargo, la proporción de pacientes que fallecen es considerablemente alta, en línea con la principal patología de base.
Para aquellos artículos que analizan la causa de exitus, el principal motivo es la enfermedad de base y las comorbilidades. Las tasas de exitus asociadas a una infección por catéter y a la enfermedad hepática asociada a fallo intestinal (Intestinal Failure Associated Liver Disease –IFALD–) fueron similares en los distintos estudios en los que se registraron (11,13,14,18).
En el análisis de supervivencia, si comparamos los valores de supervivencia a los 1, 3 y 5 años de los estudios de Hallum y cols. (14) (86 %, 79 % y 77 %) con el de Higuera y cols. (12) (72 %, 58 % y 42 %), encontramos una disparidad considerable, fundamentalmente a los 3 y 5 años. Dos manuscritos (12,13) aportan el porcentaje de supervivencia a los 10 años, ambos centrados exclusivamente en patologías no malignas, con unos valores similares (59 % y 65 %).
Sin embargo, solo el artículo de Vafa y cols. (11) da el porcentaje de supervivencia en pacientes con patología oncológica, y lo calculan al año, presentando una cifra del 8,3 %, muy inferior respecto a las cifras anteriores.
Los datos de adaptación intestinal tampoco se facilitan en todos los estudios y oscilan entre el 8,82 % y el 42,30 %.
ESTUDIOS EN POBLACIÓN PEDIÁTRICA
La bibliografía disponible en población infantil es exigua y heterogénea, lo que dificulta la obtención de conclusiones. No obstante, consideramos relevante la exposición de las variables recogidas (disponibles en la tabla IV). Se trata de muestras que van de 31 a 251 pacientes, con una mayoría de individuos que reciben NPD en los primeros meses de vida. Al igual que los adultos, todos ellos se desarrollan en países europeos.
Tabla IV. Variables extraídas de los estudios basados en población pediátrica
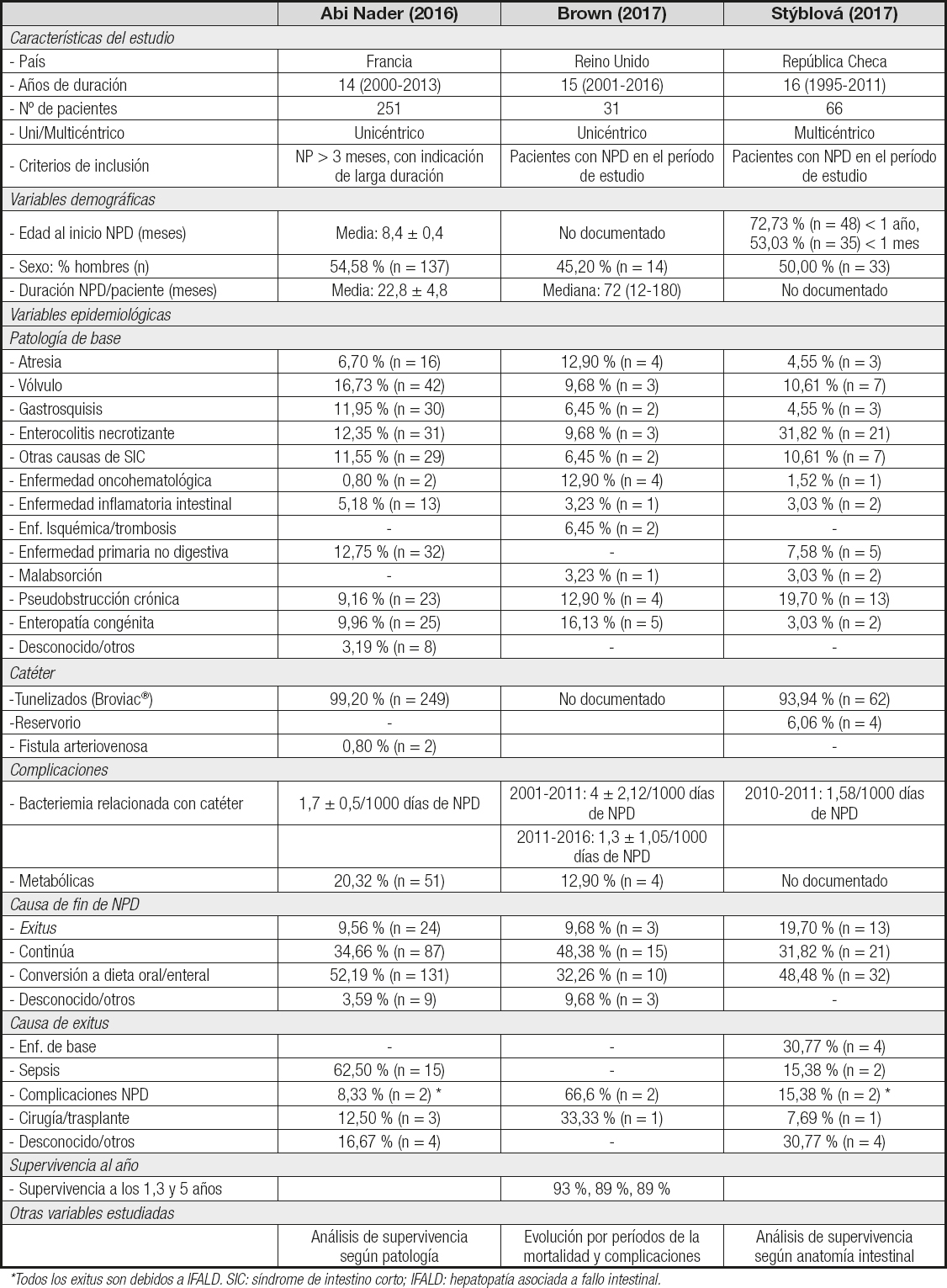
*Todos los exitus son debidos a IFALD.
SIC: síndrome de intestino corto; IFALD: hepatopatía asociada a fallo intestinal.
En cuanto al uso de catéteres existe un empleo generalizado de los dispositivos Broviac®. Las tasas de bacteriemia relacionada con el catéter muestran datos similares entre sí, que van desde 1,3 a 1,7 por cada 1000 días de NPD. Para el estudio de Brown y cols. (16) se seleccionó el dato disponible más reciente (del año 2011 al 2016), pues lo desglosan en dos periodos.
Un detalle a resaltar es que ninguno de los artículos distingue, para aquellos pacientes que fallecen a causa de una sepsis, si esta se debe a una infección relacionada con el catéter o tiene otro origen. Respecto a los pacientes que fallecen por IFALD, van del 8,33 % al 15,38 %.
Una parte destacable de los pacientes logra la conversión a dieta oral, con porcentajes que oscilan entre el 32,26 % y el 52,19 %. Estos datos contrastan con los encontrados en adultos, en los que la conversión a la dieta oral es bastante menos frecuente (15,30-39,71 %).
Cabe destacar, asimismo, las diferencias encontradas en las poblaciones pediátricas y adultas en el análisis de supervivencia. La población adulta sufrió un número más elevado de exitus debido, mayoritariamente, a su enfermedad de base; en los niños, sin embargo, la causa principal de muerte fue diferente para los estudios incluidos. En este sentido, hay que resaltar el elevado número de fallecimientos debido a sepsis (62,5 % de los exitus) en los pacientes estudiados por AbiNabder y cols. (15), sin que haya una correlación clara con el número de episodios de bacteriemia relacionada con catéter, cuyos valores fueron similares al resto de estudios pediátricos.
DISCUSIÓN
La utilización de la NPD en patología oncológica está sometida a una amplia variabilidad geográfica, lo que demuestra una clara falta de consenso a nivel europeo. Diferentes estudios han mostrado un incremento del uso de NPD en pacientes oncológicos en los últimos años; sin embargo, pese a haber incluido solo artículos recientes, parece que algunos países aún se muestran reticentes a realizar esta evolución (5).
Una mayor proporción de pacientes oncológicos y menor de aquellos con enfermedad de Crohn hubiera sido lo esperable de forma generalizada, con base en las sustanciales mejoras en el arsenal terapéutico para tratar ambas patologías; sin embargo, solo la mitad de los estudios mostró esta posibilidad. Así, los dos estudios realizados en el Reino Unido tienen datos similares que también se correlacionan con los de Dinamarca, donde la gran mayoría son pacientes no oncológicos, mientras que en Grecia los porcentajes se invierten. En países como Bélgica o España encontramos que la proporción de pacientes está repartida de forma más equilibrada entre ambos grupos.
En cuanto a los estudios pediátricos, como ya se ha comentado, la heterogeneidad a la hora de expresar las patologías de base e indicaciones, que difiere respecto de la población adulta y aporta una información desagregada en diferentes patologías, dificulta la interpretación y el análisis del pronóstico por patología.
En relación a la duración media de la NPD por paciente, impresiona su relación con la patología de base. Así, para aquellos estudios en los que la patología oncológica es una minoría o se excluye del cálculo, este valor de tiempo se incrementa considerablemente. De este modo, parece interesante la propuesta de Vafa y cols. (11), pues realizan el cálculo en función de la patología de base, aunque se echa en falta el dato correspondiente a enfermedad maligna.
Tanto en adultos como en niños se aprecia un uso extendido de catéteres tunelizados, en línea con las recomendaciones de las guías ESPEN (7,19), con excepción del estudio griego (10), en el que predominan los reservorios. Esto se explica porque la muestra es principalmente de pacientes oncológicos, en la que con frecuencia se emplea este tipo de catéter para la administración de quimioterapia sistémica.
El análisis de supervivencia se realiza de forma dispar por los diferentes estudios, por lo que los datos difícilmente nos permiten realizar comparaciones para obtener conclusiones. La diferencia hallada puede deberse a que los pacientes del estudio de Hallum y cols. (14), en su inmensa mayoría (92 %), presentan una patología de base no oncológica, mientras que en la cohorte de Higuera (12) su proporción es muy inferior (50,6 %). Este mismo razonamiento explicaría las diferencias en los perfiles de supervivencia y conversión a dieta oral en la población pediátrica, pues en esta población los pacientes con enfermedad oncohematológica también constituyen una minoría.
Por todo ello, consideramos fundamental destacar la importancia de la expresión de los resultados de forma homogénea, lo que permite un análisis posterior adecuado. De esta forma, dadas las enormes diferencias entre la supervivencia de patologías oncológicas y no oncológicas, recomendamos que esta variable se presente por categorías en lugar de globalmente, expresando la supervivencia a corto plazo en el caso de las patologías oncológicas y a cinco o diez años en el caso de las patologías no oncológicas.
Las principales fortalezas de nuestro artículo son que no se ha aplicado ninguna limitación en cuanto a la población de estudio, incluyendo tanto a adultos como a niños, con independencia del tiempo que hayan estado en tratamiento con NPD. Tampoco se ha hecho ninguna restricción en cuanto al diseño de los posibles artículos a incluir. Además, se han analizado detenidamente las distintas variables que presentaban en común los estudios incluidos.
Las principales limitaciones del estudio son la baja calidad de los artículos incluidos, ya que todos ellos son estudios observacionales, dado que no se ha podido encontrar en la literatura revisiones sistemáticas o metaanálisis. Además, la búsqueda bibliográfica se ha restringido a los diez últimos años, puesto que, aunque la técnica se ha desarrollado en las últimas décadas, deseábamos obtener resultados lo más actualizados posibles. Finalmente, se ha limitado la duración de los estudios a aquellos que se desarrollaran durante cinco o más años para poder tener un horizonte temporal suficiente.
CONCLUSIONES
La NPD constituye en la actualidad el tratamiento fundamental de aquellos pacientes que presentan fallo intestinal, lo que permite la supervivencia a largo plazo de muchos de ellos. Sin embargo, el acceso a esta prestación no es equitativo.
Sería recomendable establecer directrices de uso en enfermos oncológicos a nivel europeo, como ya existen para la patología benigna, y garantizar así el mejor tratamiento a todos los pacientes, con independencia de su país de origen.
Por otra parte, consideramos fundamental definir una serie de indicadores mínimos, así como la realización de estudios de calidad, que aporten información rigurosa y homogénea para continuar mejorando en el abordaje de esta técnica.