INTRODUCCIÓN
En las últimas décadas se ha avanzado notablemente en la comprensión de los efectos biológicos y moleculares que ejercen los nutrientes sobre la homeostasis del paciente crítico. Esto ha propiciado que la nutrición se convierta en una verdadera "terapia nutricional" que pretende atenuar la respuesta metabólica al estrés, prevenir el daño celular por oxidación y modular favorablemente la respuesta inmune.
El uso de la nutrición parenteral (NP) es frecuente en el paciente crítico posquirúrgico por la necesidad que este tiene de reposo intestinal, por su situación hipercatabólica o por una combinación de ambas cosas. Los lípidos constituyen uno de sus componentes básicos por ser una eficiente fuente de energía y aportar ácidos grasos esenciales; pero además, desde hace años sabemos que ejercen otras funciones importantes, como formar parte de las membranas celulares, las enzimas y los receptores, y ser precursores de mediadores pro y antiinflamatorios (1,2).
Las emulsiones lipídicas (EL) son la forma en que los lípidos se vehiculizan en la NP. Las investigaciones sobre el papel de los ácidos grasos en la respuesta inflamatoria e inmunológica, y sus posibles consecuencias sobre los desenlaces clínicos, han dado como resultado la comercialización de EL con distintos componentes, como el aceite de pescado, rico en ácidos Ω3, o el aceite de oliva, rico en ácido oleico (Ω9).
El ácido oleico posee las ventajas de ser resistente a la peroxidación lipídica y mostrar un efecto neutro sobre la función inmune (3). En los estudios clínicos, estas EL basadas en el aceite de oliva (EBAO) han mostrado efectos beneficiosos en distintos tipos de pacientes, incluidos los críticos (4,5).
El aceite de pescado, por su parte, es fuente de los AG Ω3 eicopentaenoico (EPA) y docosahexaenoico (DHA), los cuales han demostrado que pueden afectar beneficiosamente a la respuesta inflamatoria, a la metabólica y al estrés oxidativo (6). La administración de EL con aceite de pescado disminuye significativamente los marcadores de inflamación y aumenta los marcadores de defensa inmunitaria, lo que en la clínica se traduce, como efecto más descrito, en una disminución de las infecciones nosocomiales y de la estancia hospitalaria (7).
Actualmente existe una fuerte fundamentación teórica a favor del uso de EL con AP en el paciente crítico posquirúrgico. Así lo manifestó un grupo de expertos en la cumbre "Lipids en parenteral nutrition" (2). Sin embargo, la mayoría de los estudios que se incluyen en los metaanálisis comparan el AP con los estándares anteriores (aceite de soja o MCT/LCT). Muy pocos estudios comparan las EBAO con las EL enriquecidas con aceite de pescado, y solo encontramos 2 estudios en pacientes quirúrgicos, aunque no críticos (8,9).
El objetivo de este estudio fue comparar la eficacia y la seguridad de dos EL distintas, utilizadas en la NP de los pacientes críticos posquirúrgicos: una enriquecida con aceite de pescado (SMOFlipid®) frente a otra basada en el aceite de oliva (Clinoleic®), analizando la aparición de infecciones nosocomiales, los parámetros analíticos y las variables evolutivas.
PACIENTES Y MÉTODO
DISEÑO DEL ESTUDIO
Ensayo clínico de fase III, de no inferioridad, unicéntrico, aleatorizado, ciego, controlado, con tratamiento activo y de grupos paralelos. La población estudiada la constituyeron los pacientes mayores de edad intervenidos de cirugía mayor abdominal e ingresados en la Unidad de Cuidados Intensivos del Hospital General Universitario Reina Sofía de Murcia, entre mayo de 2014 y diciembre de 2017, que precisaron NP durante al menos 5 días.
El protocolo del estudio fue evaluado y aprobado por el Comité Ético de Investigaciones Clínicas de nuestro centro, y redactado de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Todos los pacientes incluidos recibieron las explicaciones pertinentes y aportaron un consentimiento informado firmado por ellos mismos o por sus representantes.
El estudio recibió financiación mediante una beca del Instituto de Salud Carlos III (PI 1301551).
Los criterios de exclusión del estudio fueron: NP preoperatoria, obesidad mórbida, insuficiencia renal crónica con creatinina basal > 4 mg/dl o diálisis, hiperlipidemia sin control pese a tratamiento, inmunodeficiencia, pancreatitis aguda grave, enfermedad hepática, neoplasia con metástasis y quimio o radioterapia durante el mes anterior.
Los pacientes que cumplieron los criterios de ingreso se indentificaron con un número según el orden de inclusión y se aleatorizaron en proporción de 1:1 para recibir una u otra EL mediante un método de aleatorización por bloques balanceados. El código de aleatorización fue custodiado por el farmacéutico hasta finalizar la fase de inclusión.
Las formulaciones de NP se individualizaron y solo difirieron en la EL: SMOFlipid®, compuesta por una mezcla de aceite de soja/MCT/aceite de oliva/aceite de pescado en una proporción del 30 %, 30 %, 25 % y 15 %, respectivamente, o Clinoleic®, compuesta por aceite de oliva/aceite de soja en proporción del 80 %/20 %. Las fórmulas individualizadas se ajustaron en su composición a las "Recomendaciones para el soporte nutricional y metabólico especializado del paciente crítico, consenso SEMICYUC-SENPE 2011" (10,11). Solo el preparador de la mezcla en la farmacia conocía el tipo de EL administrado a cada paciente. No se permitió ningún tratamiento concomitante con infusiones continuas de propofol ni otros fármacos vehiculizados en emulsión lipídica.
DESARROLLO DEL PROTOCOLO
Los datos y variables de los pacientes incluidos se recogieron según el siguiente protocolo:
– Al ingreso: consentimiento informado, datos antropométricos, motivo de ingreso, antecedentes, escalas de gravedad, analítica.
– A diario: composición de la NP, aparición de complicaciones.
– Cada semana: analítica.
– Al alta: estancia en la UCI y hospitalaria, días de ventilación mecánica (VM), sonda urinaria y vía central.
– Al mes y a los 6 meses: mortalidad.
EFICACIA Y SEGURIDAD
La eficacia terapéutica de las dos EL se determinó como criterio de valoración principal por la diminución de infecciones nosocomiales. Como criterios secundarios se compararon los parámetros evolutivos (estancias en UCI y hospital, días de VM) y analíticos (marcadores de inflamación: PCR y TNFα).
El criterio de valoración principal de la seguridad fue la mortalidad global (en UCI, en hospital y a los 6 meses). Como criterios secundarios se evaluaron la aparición de disfunción hepática, hipercolesterolemia o hipertrigliceridemia a los 7 y 14 días.
ANÁLISIS ESTADÍSTICO
La información recogida se introdujo en una base de datos generada con el programa estadístico SPSS v.22®. El análisis estadístico se realizó según el principio de intención de tratar.
Se emplearon métodos descriptivos básicos (porcentaje, media y desviación estándar) para el análisis descriptivo. La comparación de variables cualitativas se realizó mediante la prueba del chi cuadrado o el test de Fisher, añadiendo un factor kapa (variable control) para crear un análisis multidimensional. Las medias entre los grupos se compararon empleando el test de la "t" de Student. Los supuestos paramétricos de normalidad y homogeneidad de las varianzas se comprobaron con el test de Kolmogorov-Smirnov y el test de Levene. Para el análisis principal de no inferioridad de la variable principal se aplicaron los test de Farrington-Manning, Miettinen-Nurminen y Gart-Nam, con un nivel de significación de 0,05 y un límite de no inferioridad del 10 %.
RESULTADOS
Durante el periodo de reclutamiento se evaluaron un total de 99 pacientes, de los cuales se rechazaron 23 por cumplir algún criterio de exclusión y 3 más que no aceptaron firmar el consentimiento informado, por lo que llegaron a la fase de aleatorización 73 pacientes: 37 recibieron Clinoleic® y 36 SMOFlipid®.
Las características de los pacientes se muestran en la tabla I. La causa que motivó el ingreso hospitalario con más frecuencia fue el abdomen agudo con un 41 % (n = 30), seguida de la cirugía programada (35,6 %, n = 26). La causa más frecuente de ingreso en la UCI fue el síndrome de respuesta inflamatoria sistémica (SRIS), con un 59 % (n = 43). No existieron diferencias estadísticamente significativas entre ambos grupos para ninguna de estas variables.
Los dos grupos de pacientes recibieron una NP homogénea en cuanto a composición, sin diferencias en cuanto a los días de tratamiento (Tabla II).
Tabla II. Composición y duración de la nutrición parenteral

*: media (DE); †: se contabilizan las U/día de insulina solo en aquellas NP que la llevaban (52 %).
EFICACIA
En nuestro estudio, un total de 37 pacientes presentó algún tipo de infección: 20 (54 %) en el grupo de Clinoleic® y 17 (47,2 %) en el grupo de SMOFlipid®, sin alcanzar la significación estadística (p = 0,559).
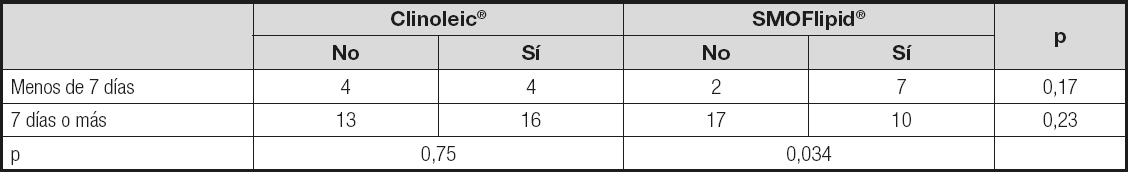
También se estudió si existía relación entre la aparición de infecciones nosocomiales y el haber recibido NP más o menos de 7 días. Al comparar los dos grupos de EL entre sí, no se observaron diferencias significativas; sin embargo, dentro del grupo de pacientes que recibieron SMOFlipid® sí que aparecieron más infecciones en los que habían recibido NP menos de 7 días, con una diferencia estadísticamente significativa (Tabla III).
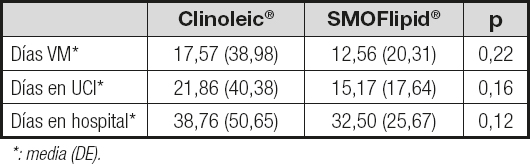
Entre los criterios de evaluación secundaria de la eficacia, los parámetros evolutivos (disminución de los días de VM, disminución de la estancia en UCI y de la estancia hospitalaria) no mostraron diferencias estadísticamente significativas entre ambos grupos para ninguno de las variables comparadas (Tabla IV).
Tras 7 días de tratamiento, en el 44 % de los pacientes habían aumentado los valores de TNFα más de un 50 %, y en el 24 % habían disminuido más del 50 %, no existiendo diferencias estadísticamente significativas entre ambos grupos de tratamiento (p < 0,05).
Tampoco existieron diferencias significativas en las variaciones de la PCR entre los días 1 y 7 de tratamiento, habiendo mostrado un descenso mayor del 50 % el 16 % de los pacientes y un aumento mayor del 50 % el 33 % de los pacientes.
SEGURIDAD
Durante el periodo de seguimiento murieron un total de 28 pacientes (38 %): 14 (37,8 %) en el grupo de Clinoleic® y 14 (38,9 %) en el grupo SMOFlipid® (p = 0,95). De ellos, 16 (30 %) lo hicieron durante el ingreso en la UCI, 11 (15 %) durante su estancia en la planta y solo 1 paciente falleció después del alta hospitalaria. No existieron diferencias estadísticamente significativas entre los dos grupos para ninguna de estas variables.
Los criterios de valoración secundaria de la seguridad fueron las alteraciones de los parámetros analíticos de función hepática y la aparición de hipertrigliceridemia o hipercolesterolemia, medidos todos ellos el día 1, 7 y 14 de NP. En el grupo de Clinoleic®, el 29 % de los pacientes presentó aumento de la GOT, el 34 % de la GPT, el 25,9 % de la LDH, el 42 % de la fosfatasa alcalina y el 25 % de la bilirrubina total; para el grupo de SMOFlipid®, este aumento se produjo en el 20 % (p = 0,41), el 26,6 % (p = 0,51), el 21,4 % (p = 0,92), el 53 % (p =0,68) y el 31 % (p = 0,85), respectivamente.
Tampoco existieron diferencias estadísticamente significativas entre los dos grupos para la aparición de hipertrigliceridemia (16 % con Clinoleic® vs. 10 % con SMOFlipid®, p = 0,87) o hipercolesterolemia (ningún caso de nueva aparición en ninguno de los grupos).
DISCUSIÓN
Los resultados del presente estudio indican que las dos EL comparadas poseen un perfil de eficacia y seguridad similar.
Los estudios que comparan las EBAO con el aceite de pescado son escasos e incluyen pocos pacientes de características heterogéneas (8,9,12,13). Piper y cols., en 2009, compararon SMOFlipid® y Clinoleic® en un grupo de 44 pacientes no críticos, concluyendo que los que recibieron aceite de pescado presentaban menor elevación de enzimas hepáticas (9). En 2014, Deshpande y cols. hicieron lo mismo en un grupo de 30 neonatos, llegando a la conclusión de que el grupo de SMOFlipid® presentaba un menor índice de peroxidación lipídica (13). Otros estudios, como el de Badía-Tahull o el de Gultekin, compararon EBAO frente a EBAO más aceite de pescado. Badía-Tahull y cols. lo hicieron en 27 pacientes quirúrgicos (no críticos), mostrando un menor número de infecciones en los que recibieron la mezcla con aceite de pescado (8). Gultekin y cols. estudiaron 32 pacientes críticos sépticos, concluyendo que los que recibieron aceite de pescado mostraban unos niveles menores de marcadores inflamatorios (proteína C-reactiva y leucotrieno B4) (12). En el estudio más reciente, Demirer y cols. administraron distintas EL (MCT/LCT, EBAO y EBAO + Ω3) a 52 pacientes quirúrgicos no críticos con el único resultado estadísticamente significativo de que las EBAO conseguían mejorar el estado antioxidante de los pacientes (14).
Todos los pacientes de nuestra serie fueron postoperados de cirugía mayor abdominal, programada o urgente, que estuvieron ingresados en la UCI antes de la cirugía o durante el postoperatorio inmediato. En este tipo de pacientes existe evidencia de que un déficit calórico y proteico ejerce una influencia negativa sobre el pronóstico, disminuyendo las posibilidades de poder dar el alta para regresar al domicilio (15).
La causa más frecuente de ingreso en la UCI fue el SRIS; en ese escenario de estrés se produce una respuesta metabólica que lleva al paciente a una situación de riesgo nutricional en la que el soporte especializado se hace imprescindible (16,17). Por otra parte, la cirugía mayor puede en ocasiones inducir un SRIS que puede ser difícil de distinguir de las complicaciones sépticas precoces (18).
Los dos grupos de nuestro estudio fueron homogéneos en cuanto a la duración y la composición de la NP, que se formuló de manera individualizada de acuerdo con las recomendaciones de consenso de la SEMICYUC-SENPE de 2011 (10,11).
El criterio de valoración principal de la eficacia fue el número de infecciones nosocomiales. Se han publicado numerosos metaanálisis que incluyen este objetivo al enfrentar EL enriquecidas con AP con otras (aceite de soja y MCT/LCT, principalmente), pero ninguno de los estudios que comparan EBAO frente a EL enriquecidas con AP ha conseguido demostrar este efecto de forma estadísticamente significativa. En nuestra serie, aunque el grupo de SMOFlipid® presentó un menor número de infecciones, la diferencia tampoco resultó estadísticamente significativa.
Otro aspecto importante fue analizar si la duración de la NP podía tener efecto sobre la aparición de infecciones. En nuestro estudio no se observaron diferencias entre los dos grupos en función de la duración de la NP, mayor o menor de 7 días; sin embargo, dentro del grupo de pacientes que había recibido SMOFlipid®, aparecieron más infecciones en los que había recibido NP menos de 7 días, y esta diferencia sí fue estadísticamente significativa. Este hallazgo nos parece muy interesante porque indicaría que los efectos beneficiosos del AP sobre la inmunidad y el descenso de las infecciones podría ser tiempo-dependiente. Klek y Waitzberg, en una revisión sobre el efecto de los Ω3 en pacientes quirúrgicos, observó que, mientras que la influencia sobre los parámetros inmunológicos y de función hepática ya aparecía con infusiones más cortas, la disminución de las complicaciones y el acortamiento de la estancia hospitalaria precisaban tratamientos mayores de 5 días (19).
La eficacia de las dos EL también se comparó midiendo variables evolutivas y analíticas. Los días de VM, si bien presentaron una tendencia a ser menores en el grupo de SMOFlipid®, no difirieron de manera estadísticamente significativa. Algo parecido ocurrió con las estancias en UCI y hospitalaria, más cortas, aunque sin diferencia estadísticamente significativa, en el grupo de SMOFlipid®.
En nuestro estudio no se encontraron diferencias estadísticamente significativas al comparar las variaciones de los niveles plasmáticos de PCR y TNFα entre los días 1 y 7 entre los dos grupos. Al igual que en otros estudios, nuestros pacientes presentaron un descenso de los niveles de PCR y un ascenso del nivel de TNFα a lo largo de la primera semana (20). Las variaciones de la citoquina proinflamatoria TNFα y de la PCR se han utilizado con frecuencia para valorar la eficacia de las distintas EL y, hasta ahora, los resultados de los metaanálisis que comparan EL ricas en AP con otras EL eran prometedores y apuntaban que el AP podría disminuir el perfil inflamatorio del paciente crítico; sin embargo, al igual que en nuestro estudio, los resultados no fueron concluyentes cuando se compararon EBAO y AP (8,21).
El criterio de valoración principal de la seguridad fue la mortalidad. En nuestro estudio no existieron diferencias estadísticamente significativas en la mortalidad global, en UCI, en planta ni en los primeros 6 meses entre los dos grupos de tratamiento. El único estudio comparable que analizó la mortalidad es el de Badía-Tahull, con el mismo resultado (8).
En cuanto a las alteraciones de la función hepática, al 7º día de tratamiento, el grupo Clinoleic® mostró una tendencia no significativa hacia la elevación de la GOT, la GPT y la LDH. Sin embargo, las alteraciones de la fosfatasa alcalina y la bilirrubina fueron más frecuentes en el grupo SMOFlipid®. Este resultado se asemeja al de Badía-Tahull y cols., quienes también describieron un aumento no significativo de los niveles de GPT y GGT en el grupo con EBAO (8). Las complicaciones hepatobiliares de la NP son multifactoriales. Grau y cols., en un estudio de cohortes con más de 700 pacientes críticos, las relacionaron de forma independiente con la sepsis, el uso precoz de nutrición artificial y la administración de más de 25 kcal/kg de energía (22). Piper y cols. estudiaron la integridad hepatocelular de pacientes críticos quirúrgicos a los que administraron SMOFlipid® frente a Clinoleic®, describiendo un aumento significativo de la GOT, la GPT y la α-glutatión-s-transferasa al cabo de 2 y 5 días de tratamiento con Clinoleic® (9).
La aparición de hipertrigliceridemia tampoco mostró diferencias estadísticamente significativas, aunque fue más frecuente en el grupo Clinoleic®. Del mismo modo, Piper y cols. describieron un menor aumento de las cifras de triglicéridos en los pacientes que recibieron SMOFlipid® frente a los que recibieron Clinoleic® (9). En el estudio de Gultekin, los niveles de triglicéridos disminuyeron después de 6 días de tratamiento con EBAO + AP y aumentaron en el grupo que solo había recibido EBAO, aunque sin una diferencia estadísticamente significativa (12).
En relación al colesterol, ningún paciente presentó cifras de colesterol total dentro del rango patológico en los controles realizados a los 7 y 14 días. Este hallazgo coincide con los resultados del estudio de Gultekin (12).
Hasta el momento de esta revisión no se han publicado estudios que analicen la no inferioridad de SMOFlipid® frente a Clinoleic®. Nuestros resultados deberán extrapolarse con precaución ya que, en la seguridad y la eficacia de una técnica como la administración de la NP, participan muchos y muy distintos elementos que abarcan desde las características del paciente y la indicación, hasta la administración o el cuidado de la vía de acceso, además de otros factores intercurrentes que pueden condicionar la evolución de estos pacientes. Junto a esto, la limitación principal de nuestro estudio la constituye el escaso número de pacientes incluidos a lo largo de un extenso espacio de tiempo, por tratarse de un trabajo unicéntrico.
CONCLUSIONES
A pesar de la amplia literatura científica existente sobre el uso de EL enriquecidas con ácidos grasos Ω3, en la actualidad apenas existen estudios que las comparen con las EBAO.
Según los resultados de nuestro estudio, el uso de las dos emulsiones lipídicas comparadas (SMOFlipid® y Clinoleic®) es eficaz y seguro en los pacientes críticos quirúrgicos, y no existen diferencias estadísticamente significativas en cuanto a la aparición de infecciones nosocomiales, mortalidad u otros parámetros de evolución clínica y analítica. De nuestro estudio se desprende que SMOFlipid® no es inferior a Clinoleic® en términos de eficacia y seguridad terapéuticas.
Los pacientes que recibieron SMOFlipid® durante 7 o más días presentaron un riesgo de desarrollar infecciones nosocomiales menor que el de aquellos otros que lo recibieron menos de 7 días.