INTRODUCCIÓN
La gestión del paciente crónico es uno de los objetivos más importante del sistema sanitario público. En España, el 45,6 % de la población mayor de 16 años sufre al menos un proceso crónico (1). Este tipo de patologías son, hoy por hoy, la causa más importante de mortalidad y de utilización de los servicios sanitarios. Distintas sociedades científicas, han elaborado guías de práctica clínica que contemplan el manejo y seguimiento de pacientes con pluripatologías y comorbilidades (2,3).
La esclerosis lateral amiotrófica (ELA) es una enfermedad neurodegenerativa progresiva que afecta predominantemente a las motoneuronas superior (MNS) e inferior (MNI). De acuerdo con el lugar de inicio, se diferencia entre ELA espinal, que comienza con trastornos motores en las extremidades, y ELA bulbar, con afectación de la musculatura bulbar (4).
Los pacientes con ELA son un grupo de pacientes crónicos complejos debido a sus características (enfermedad rápidamente progresiva, comorbilidades, aspectos cognitivos y funcionales) y a los importantes cuidados sanitarios que precisan (asistencia sanitaria especializada, ventilación asistida, ostomías) (5,6), por lo que deben tratarse en unidades multidisciplinares.
El 16-55 % de los pacientes con ELA presentan al diagnóstico algún signo de desnutrición que puede empeorar el curso de la enfermedad (7). Además, dado su carácter progresivo, la mayoría de los pacientes con ELA bulbar y un porcentaje muy significativo de aquellos con ELA espinal acabarán precisando la colocación de una sonda enteral de alimentación (8,9), siendo la gastrostomía percutánea endoscópica (PEG) la vía de acceso enteral más usada (10).
La manipulación de los fármacos para su administración a través de estas sondas de alimentación conlleva algunos riesgos y puede disminuir su eficacia terapéutica. Al modificarse la forma farmacéutica original, se puede disminuir la efectividad del fármaco (por cambio en el lugar de absorción o favoreciendo su inactivación), alterar la duración de su acción o aumentar su toxicidad. Por otro lado, las formas farmacéuticas administradas pueden obstruir la sonda y requerir la retirada de esta, originando por tanto la imposibilidad de alimentarse adecuadamente (11) y precisando una nueva colocación.
El personal sanitario presenta por lo general múltiples dudas en la manipulación que los medicamentos requieren para ser administrados por esta vía. En la bibliografía se constata que un importante porcentaje del personal de enfermería tritura rutinariamente los medicamentos con cubierta entérica y de liberación prolongada (12,13). Pero en el caso de los cuidadores o familiares en el domicilio, el problema se agrava al no disponer ni de la formación, ni de la información necesarias (14).
Por otro lado, el Institute for Safe Medication Practices (ISMP) también informó de los riesgos de la administración de fármacos a través de sondas de nutrición enteral e incluso publicó unas recomendaciones de administración (15,16).
Además de los aspectos reseñados, hay que considerar también la exposición del paciente o cuidador a los posibles efectos tóxicos de los llamados medicamentos peligrosos (incluidos en la lista del National Institute of Occupational Safety and Health, NIOSH, y adaptada en España por el Instituto Nacional de Seguridad e Higiene en el Trabajo) (17,18), cuando se modifica la forma farmacéutica original. La NIOSH agrupa estos fármacos en una Lista 1 de medicamentos carcinógenos y una Lista 2 integrada por aquellos medicamentos no clasificados como carcinógenos pero que reúnen alguna otra característica de peligrosidad (teratogenia, toxicidad reproductiva, genotoxicidad o toxicidad para órganos a bajas dosis). La última versión de esta lista de medicamentos peligrosos publicada por la NIOSH se encuentra en fase de alegaciones o de aprobación.
Un aspecto muy importante en el manejo de pacientes crónicos complejos es el de fomentar el empoderamiento y la corresponsabilidad desde el inicio del tratamiento, así como garantizar la continuidad asistencial estableciendo mecanismos de comunicación adecuados.
El objetivo principal del presente trabajo es describir y analizar el grado de adecuación de la prescripción de los fármacos administrados por una PEG en pacientes con ELA y NE, según criterios de eficacia (pérdida de la actividad del fármaco, cambios en la duración de su acción), toxicidad, compatibilidad con la NE (posibilidad de obstrucción de la sonda) y riesgo para el manipulador, así como detallar las intervenciones farmacéuticas realizadas para mejorar y garantizar la efectividad y seguridad del tratamiento recibido.
Adicionalmente, se persigue describir el circuito de trabajo del farmacéutico hospitalario integrado con la Unidad de ELA del centro.
MATERIAL Y MÉTODOS
Al ingreso de un paciente con ELA en el hospital para la colocación de una PEG, y tras una interconsulta por parte de la Unidad de ELA, el farmacéutico responsable revisa el tratamiento farmacológico del paciente a nivel ambulatorio y hospitalario, validando su adecuación, efectividad y seguridad, la posibilidad de su administración por PEG (según especialidad farmacéutica, forma farmacéutica y pauta de administración), el riesgo para el manipulador (según lista NIOSH 2020) (17) y la compatibilidad con la NE, según la información contenida en la “Guía de administración segura de fármacos por sondas de alimentación”, elaborada por el Servicio de Farmacia del Hospital, u otras bases de datos relevantes (17,19-24). Para acceder a dichos datos se han seguido los protocolos establecidos en nuestro centro sanitario.
Los cambios de medicación realizados, donde se indica la utilización de otras vías de administración o de formas farmacéuticas líquidas o dispersables alternativas, se comunican al médico mediante un informe que consta en la historia electrónica corporativa del paciente. En los casos en los que no se pueda administrar el tratamiento por la PEG, se propone cambio de medicación según la “Guía para el Intercambio Terapéutico” del hospital (22). También se informa del riesgo 1para el manipulador y de la compatibilidad con la NE.
Al alta, el farmacéutico realiza una entrevista personal con el paciente y el cuidador, informando de las peculiaridades del tratamiento y resolviendo las dudas sobre el mismo (administración, horarios, trámites administrativos, etc.). Además, se facilita material escrito de fácil comprensión con un conjunto de recomendaciones generales de administración de fármacos por sonda (elaborado por el Servicio de Farmacia del hospital) (19), así como una información individualizada para cada paciente según su perfil farmacoterapéutico.
Durante el periodo comprendido desde junio de 2017 hasta diciembre de 2020 se revisaron los perfiles farmacoterapéuticos de los 34 pacientes sobre los que el neurólogo había formulado interconsultas. El 56 % fueron hombres con una mediana de edad de 68 años (rango 44-79). En todos los casos los pacientes eran portadores de una PEG y el tamaño de la sonda utilizada era de 12F. La pauta de administración de la NE fue intermitente cada 4-6 horas y el tipo de dieta utilizada fue en todos los casos polimérica hiperproteica.
RESULTADOS
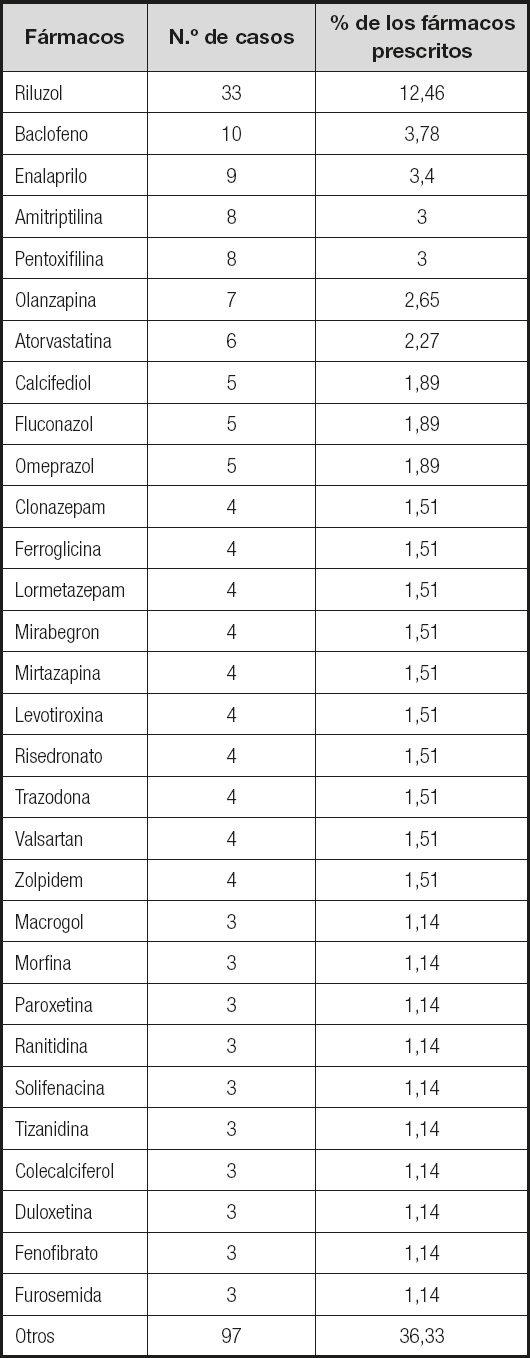
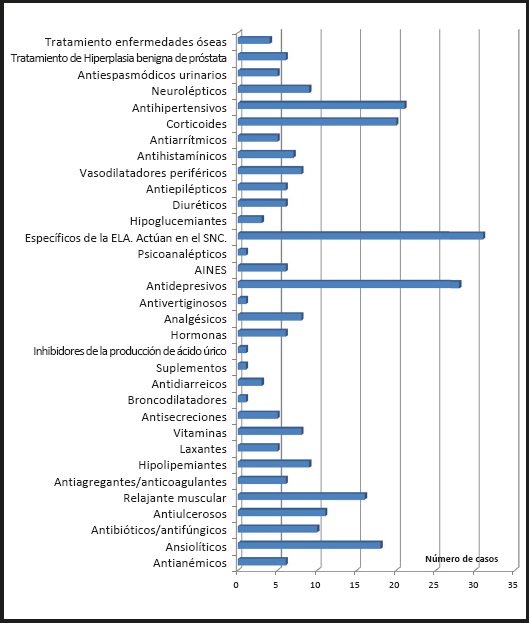
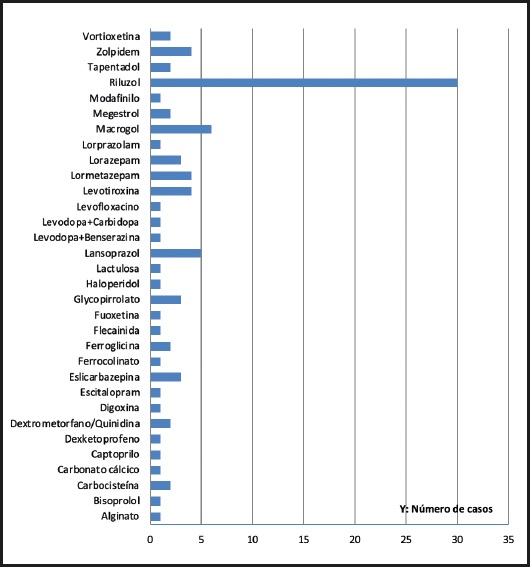
A los 34 pacientes del estudio se les prescribieron en total 307 medicamentos, una mediana de 8 fármacos por paciente (rango, 2-17). Los fármacos más prescritos aparecen en la tabla I, destacando el riluzol y el baclofeno. Los grupos farmacológicos más prescritos fueron el correspondiente al riluzol (10,7 % de los fármacos), afectando al 100 % de los pacientes; antidepresivos (9,1 % de los fármacos), afectando al 66,7 % de los pacientes; antihipertensivos (6,8 %), afectando al 39,4 % de los pacientes, y benzodiacepinas (5,9 %), en el 24,2 % de los pacientes (Fig. 1).
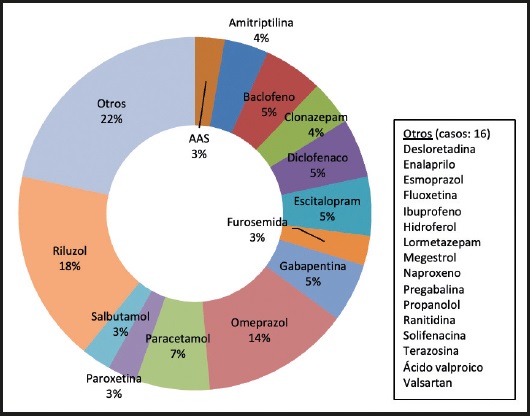
Se pautaron por la PEG un total de 267 fármacos, con una mediana de 7 medicamentos por paciente (rango, 2-15). De los 267 fármacos, 218 fueron formas sólidas (81,7 %), de las que se realizaron modificaciones de la forma farmacéutica en 93 casos (43 %), afectando al 97 % de los pacientes (Fig. 2). En 49 casos (52,7 %) se recomendó cambiar a formas líquidas, en 27 medicamentos (29 %) a formas bucodispersables, en 9 (9,7 %) a gránulos o sobres, en 6 (6,5 %) se cambió de comprimidos de liberación retardada a los correspondientes de liberación inmediata, en 3 (3,2 %) se aconsejó cambio de comprimidos a cápsulas, y en un solo fármaco se propuso cambio a comprimidos efervescentes.
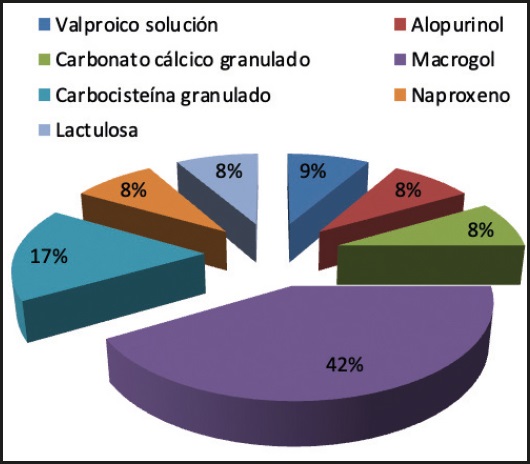
En 12 medicamentos (5,5 %) se indicó el aumento del volumen de dilución del fármaco para su administración, así como la cantidad del agua de lavado de la sonda posterior por riesgo de obstrucción de ésta debido a la naturaleza de la forma farmacéutica utilizada (Fig. 3).
Se aconsejó administrar inmediatamente el fármaco, para evitar la degradación de los principios activos y por tanto la pérdida de eficacia de los mismos, en 62 casos (28,4 %), destacando en estos casos la prescripción de pentoxifilina (13,1 %), calcifediol (8,2 %), lormetazepam (6,6 %), clonazepam (6,6 %) y ebastina (6,6 %).
En el 6,40 % de los fármacos (14 medicamentos) se recomendó su administración junto con la NE debido al potencial gastrolesivo del fármaco (baclofeno 10, diclofenaco 2, dutasterida 2).
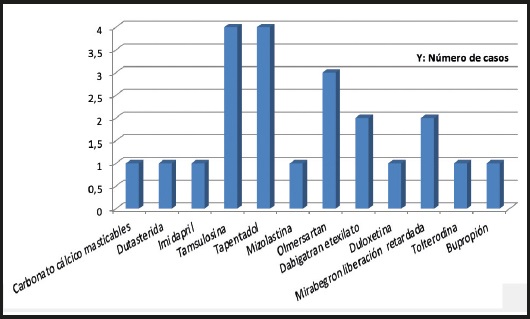
Se propuso el cambio de fármaco al no disponer de forma farmacéutica alternativa disponible que pudiera administrarse por PEG en 22 casos (10 %). En 13 de ellos por ser profármaco o inactivarse con el pH gástrico, en 9 por tratarse de comprimidos de liberación prolongada y no disponer de forma de administración rápida o por existir otras vías de administración alternativas, como es el caso del tapentadol, en el que se aconsejó recurrir a la presentación de parches transdérmicos de fentanilo (Fig. 4).
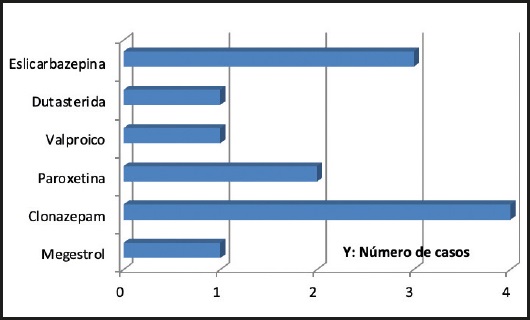
En el 5,4 % de los fármacos se aconsejó la protección del manipulador por tratarse de fármacos incluidos en la Lista 2 de NIOSH 2020 (Fig. 5).
En el 9,5 % (17 casos) de los tratamientos se realizaron recomendaciones especiales relativas a su seguridad (gastrotoxicidad, 7,8 %; protección ocular, 1,7 %) y en un 17,9 % (39 casos) se recomendó monitorizar la eficacia del tratamiento (hipoglucemiante 10,3 %, antihipertensivos 76,9 %, antiagregantes 7,6 %, anticoagulantes 5,2 %).
En el caso de 94 fármacos se aconsejó administrarlos una hora antes o dos horas después de la NE (30,6 % de los fármacos administrados por sonda), afectando al 100 % de los pacientes (Fig. 6). En relación con 79 fármacos se debió a problemas de estabilidad con la NE. En 15 medicamentos, incluyendo lansoprazol (5,6 %), zolpidem (4,5 %) y lormetazepam (4,5 %), se aconsejó su administración separada de la NE con el objetivo de mejorar la absorción de estos y, por tanto, su eficacia.
Durante el seguimiento, ningún paciente sufrió obstrucción de la sonda PEG que motivara un recambio antes de lo programado.
DISCUSIÓN
Un 86 % de los pacientes con ELA presentan problemas de disfagia en el curso de su enfermedad, con pérdidas importantes de peso y, por tanto, algún tipo de desnutrición, por lo que muchos de ellos (53 %) son portadores de sondas enterales de alimentación, lo que dificulta la administración de fármacos y pone en riesgo la eficacia del tratamiento (25,26).
El número de medicamentos prescritos, el número de administraciones diarias, la utilización de la sonda durante un largo periodo de tiempo, así como el uso de la NE, son factores de riesgo que aumentan la probabilidad de aparición de complicaciones mecánicas o problemas de obstrucción de la sonda (27,28).
En nuestro estudio, la presentación del 81,7 % de los fármacos prescritos era sólida, suponiendo una mediana de 7 fármacos sólidos por paciente. Estos pacientes son subsidiarios de sufrir algún tipo de complicación relacionada con la administración de medicamentos por la sonda (27), siendo necesario el cambio a presentaciones líquidas (soluciones, gotas), o dispersables (comprimidos bucodispersables, gránulos), o incluso el cambio de principio activo, en un 43 % de estas, con el objetivo de disminuir el riesgo de obstrucción de la sonda. Estos resultados son superiores a los observados en otros estudios realizados donde la prescripción de medicamentos en forma líquida era minoritaria (29-31).
Como en otros estudios consultados (32), cabe destacar en nuestra serie la gran proporción de pacientes afectados por estas intervenciones (97 %). Estos datos son incluso superiores a otros trabajos publicados, donde al 43 % de los pacientes se les manipuló o trituró la medicación oral para administrarla por sonda de manera inadecuada (29). Esto pudo deberse a que la gran mayoría de nuestros pacientes llevaban tratamiento con riluzol y al elevado número de fármacos prescritos por paciente. Todos estos cambios evitaron la necesidad de recambio precoz de sonda por obstrucción, lo que redunda en una reducción de los desplazamientos al hospital y una menor carga asistencial en los servicios de endoscopias.
Entre los fármacos a los que se cambió la forma farmacéutica para facilitar su administración destacaron el omeprazol, riluzol, y paracetamol. Coincidiendo con otros estudios consultados, el omeprazol y el paracetamol fueron los medicamentos que más frecuentemente se administraron (27,30,31). Aunque el omeprazol puede administrarse por sonda, en nuestros pacientes se prefirió utilizar otro fármaco del mismo grupo farmacoterapéutico, como es el lansoprazol bucodispersable, de más fácil administración, como también aparece recogido en otras series (27).
Las recomendaciones para la administración de fármacos por sonda aconsejan el cambio de la forma farmacéutica sólida a la líquida siempre que exista una presentación comercializada correspondiente (33,34). En el caso del riluzol, aunque los comprimidos se pueden triturar, se prefirió el cambio a forma líquida para evitar la obstrucción de la sonda. Por otro lado, en los tratamientos con escitalopram o diclofenaco se aconsejaron comprimidos bucodispersables, mientras que en el caso del paracetamol y el baclofeno, estos se cambiaron a formas líquidas.
Como en otros estudios, la forma farmacéutica de las cápsulas fue poco prescrita, a pesar de ser más fácil su administración por sonda. Por ese motivo, en algunos fármacos sin formas líquidas comercializadas se prefirió el uso de capsulas (27).
Conforme avanzaba el estudio, algunos de los fármacos que inicialmente se pautaban en forma sólida, como resultado de la información dada al facultativo en relación con pacientes previos se prescribieron en forma líquida o bucodispersable, como es el caso de lansoprazol, riluzol, paracetamol, etc., con el fin de facilitar su administración, lo que demuestra la sensibilización del personal facultativo hacia este problema. El uso de estas formulaciones desde la primera prescripción, cuando están disponibles, además de disminuir el riesgo futuro de atragantamiento en los pacientes con disfagia puede facilitar la posterior adherencia terapéutica, al disminuir el número de cambios de tratamiento necesarios al colocar la PEG.
El grupo farmacológico más prescrito fue el relacionado con el sistema nervioso central, algo lógico considerando que se dispone de un tratamiento modificador del curso de la enfermedad (riluzol) y que gran parte de los síntomas presentes en esta patología (como la espasticidad, la sialorrea, el insomnio, los problemas del sueño, la fatiga, la ansiedad o la depresión) se tratan con fármacos que actúan en el sistema nervioso central (8).
Todos los pacientes, un porcentaje superior al recogido en la bibliografía (35), presentaban alguna incompatibilidad del tratamiento con la nutrición enteral, ya que a la mayoría de los ellos se les prescribió riluzol. Las guías de administración de fármacos por sonda consultadas (36) aconsejan su administración separada de la nutrición enteral. También destacaron tratamientos con macrogol (gran riesgo de interacción y obstrucción de la sonda) y tiroxina (incompatible con fórmulas enterales con fibra y soja). En un 14,89 % de los casos en que se administraron separados de la NE, se aconsejó administrarlos una hora antes de la nutrición enteral para facilitar su absorción, tal y como indicaba la ficha técnica, y mejorar así su eficacia.
La protección del manipulador fue otro aspecto a considerar. Aunque fue pequeño el porcentaje de actuaciones con medicamentos peligrosos, no hay que olvidar la importancia de informar al paciente y, especialmente, a los cuidadores acerca de los riesgos ligados con la manipulación de este tipo de medicamentos, ya que se ven expuestos reiteradamente a ellos. En nuestro estudio se trató de medicamentos pertenecientes a la clase 2 de NIOSH (clonazepam, paroxetina, valproico, eslicarbazepina, megestrol). En otros trabajos consultados (37), este tipo de medicamentos supuso el 11,6 % de las intervenciones, la mayoría perteneciente al grupo 1 de la NIOSH. Cabe destacar la información dada a un pequeño porcentaje de pacientes referentes a la posible toxicidad ocular al triturar los comprimidos de solifenacina (1,7 %), en los que se aconsejó realizar la operación en una bolsa de plástico.
Tal y como aconseja la bibliografía consultada (27), en los medicamentos que no podían administrase por la sonda y no existía forma farmacéutica alternativa de administración (10 %), fue necesario considerar otra vía posible de administración o incluso el cambio a otro fármaco con efecto farmacológico semejante que pudiese administrarse por la sonda.
En un 46,3 % de los fármacos se realizaron recomendaciones relativas a la eficacia del tratamiento, la administración inmediata o la monitorización del efecto terapéutico (como, por ejemplo, en el caso de anticoagulantes, antihipertensivos e hipoglucemiantes), y en un 14,7 % estuvieron relacionadas con la seguridad del paciente (gastrolesividad, toxicidad ocular, obstrucción de sonda), ya que estos aspectos, como se ha observado en la bibliografía consultada, pueden influir en el fracaso terapéutico o en la falta de adherencia al tratamiento (38).
CONCLUSIONES
Los pacientes con ELA y con sondas de alimentación, en concreto con PEG, presentan un riesgo elevado de presentar problemas de seguridad y de pérdida de efectividad del tratamiento relacionados con la manipulación de la forma farmacéutica original y las interacciones con la nutrición enteral.
La formación e información al paciente y al cuidador es una estrategia que puede ayudar a incrementar la efectividad y seguridad del tratamiento, especialmente en este tipo de pacientes ya que, debido a sus características, tienen que manipularse para poder administrarlos por sondas. El trabajo coordinado de los distintos miembros del equipo asistencial ayuda a resolver estos problemas, aumentando la calidad de la atención sanitaria.