INTRODUCCIÓN
La diabetes mellitus (DM) es una enfermedad crónica con una prevalencia que oscila entre el 4,0 % y 6,0 % de los adultos en todo el mundo (1). Las guías de la American Diabetes Association (ADA) 2022 establecen unas recomendaciones de alimentación saludable, siguiendo un patrón de dieta mediterránea. De forma concreta, recomiendan una dieta rica en ácidos grasos monoinsaturados a partir del aceite de oliva, ácidos grasos poliinsaturados (omega-3) y fibra y controlada en sodio. Respecto a la carga y al índice glucémico, las guías de la ADA sugieren su individualización según la situación clínica del paciente (2).
La desnutrición relacionada con la enfermedad (DRE) en la diabetes es una complicación que muchas veces pasa desapercibida. El estudio VIDA, realizado en pacientes ancianos diabéticos hospitalizados, puso de manifiesto que la prevalencia de malnutrición es superior a la de pacientes no diabéticos: alcanza unas tasas de malnutrición del 21,2 % y de riesgo de malnutrición del 39,1 % (3,4). La DRM en el paciente diabético supone un incremento de la mortalidad (5).
El tratamiento nutricional del paciente desnutrido tiene como base el consejo dietético, incidiendo en el fortalecimiento de la ingesta dietética, especialmente energética y proteica, y su combinación con la pauta de suplementos nutricionales orales (SNO) o el uso de nutrición enteral por sonda cuando las circunstancias clínicas impiden alcanzar los requerimientos nutricionales por vía oral. De forma concreta, los SNO se reconocen cada vez más como parte integral de la estrategia global de tratamiento de la desnutrición de los pacientes, tanto a nivel hospitalario como comunitario (6). Diferentes estudios han demostrado que el uso de los SNO resulta eficaz para incrementar la ingesta nutricional, mejorar la evolución clínica del paciente y ser coste-eficaces (6).
Los pacientes diabéticos desnutridos pueden beneficiarse de SNO específicos que favorezcan su control glucémico y metabólico. Para ello, suelen formularse siguiendo las recomendaciones generales de las guías ADA y de los diferentes estudios desarrollados en este grupo de pacientes (7-14). En su mayoría, las fórmulas específicas para diabetes (FED) presentan un mayor porcentaje de grasa (en torno al 40 %), con un elevado componente de ácidos grasos monoinsaturados (> 20 %, VCT); un moderado aporte de hidratos de carbono (en torno al 40 %) a partir de polisacáridos (almidón resistente), oligosacáridos de bajo índice glucémico (dextrinas), fructosa e isomaltulosa (isómero de la glucosa); un porcentaje de proteínas del 15-20 % a partir de proteína láctea (lactosuero, caseinato) o proteína vegetal, y fibra, habitualmente a partir de una mezcla soluble e insoluble o solo soluble (15). Teniendo en cuenta que los pacientes diabéticos suelen presentar frecuentemente alteraciones del gusto (16), las FED suelen presentar una composición que favorece simultáneamente su palatabilidad y el control glucémico y metabólico.
El objetivo principal del estudio fue comparar la aceptación sensorial de un suplemento nutricional líquido específico para diabetes con la de un suplemento nutricional oral estándar en pacientes en riesgo de desnutrición con diabetes mellitus tipo 2 (DM2).
MATERIAL Y MÉTODOS
Ensayo clínico, aleatorizado, doble ciego, cruzado, multicéntrico y controlado realizado desde marzo de 2019 hasta abril de 2022. El estudio se registró en ClinicalTrials.gov con el identificador NCT05423938.
PACIENTES
Se reclutaron pacientes adultos con diagnóstico de DM2 (confirmado por el uso de hipoglucemiantes orales durante al menos dos meses) en riesgo de desnutrición o desnutridos (diagnosticados con valoración global subjetiva [VGS]). Se excluyeron pacientes con DM1, DM2 en tratamiento con insulina y DM secundaria a esteroides, pacientes en tratamiento con inhibidores de la alfaglucosidasa, IMC > 35 kg/m2, neoplasia maligna, enfermedad renal crónica avanzada (filtrado glomerular < 30 ml/min), hepatopatía y gastroparesia graves, enfermedad infectocontagiosa crónica (tuberculosis activa, hepatitis B o C o VIH), embarazadas o lactantes o que presentasen una alergia o intolerancia a alguno de los ingredientes de las fórmulas.
MÉTODO
En la visita inicial, el paciente fue valorado nutricionalmente. Se realizó un diagnóstico nutricional con VGS. Tras la aleatorización del orden de ingesta de los suplementos a estudio, el paciente se tomó el primer suplemento nutricional oral (SNO) de 200 ml en presencia del investigador. Tras su ingesta completa, se realizó una valoración sensorial en la que se evaluó el olor, el sabor y la textura percibida, que se puntuaron en una escala del 1 al 4. Las respuestas se clasificaron de forma cualitativa en: muy malo, malo, regular, bueno o muy bueno. En el día 8 se realizó la segunda visita, en la que se repitió el mismo procedimiento que en la visita inicial, pero el SNO que se tomó el paciente fue la segunda fórmula a estudio.
FÓRMULAS A ESTUDIO
– FED (Bi1 DIACARE® hp/hc, Adventia Pharma). Suplemento nutricional oral (SNO) específico para diabetes, polimérico, hipercalórico e hiperproteico, con fibra.
– FE (Bi1 CONTROL®, Adventia Pharma): SNO estándar, polimérico, hipercalórico e hiperproteico, sin fibra.
La información nutricional de las fórmulas nutricionales se detalla en la tabla I. Los SNO se presentaron en un envase Tetra Pak® de 200 ml en blanco exactamente iguales para ambas fórmulas. Cada envase se etiquetó con un código numérico como única diferenciación entre ambos productos para que el paciente recibiese el suplemento experimental (FED) o el control (FE).
Tabla I. Composición de macronutrientes e ingredientes de las fórmulas por 100 ml.

AGS: ácidos grasos saturados; AGM: ácidos grasos monoinsaturados: AGP: ácidos grasos poliinsaturados; AOVE: aceite de oliva virgen extra; FED: fórmula específica para diabetes; FE: fórmula estándar; VCT %: porcentaje respecto al valor calórico total. A: Bi1 diacare hp-hc®, Adventia Pharma S. L., España; B: Bi1 control hp-hc®, Adventia Pharma S. L., España.
ALEATORIZACIÓN
El procedimiento de aleatorización lo realizó el responsable del análisis estadístico del estudio a través de una tabla numérica. Cada paciente recibió un número de participante que le hizo comenzar el estudio por un producto u otro de forma cruzada (experimental [FED]; control [FE]).
ASPECTOS ÉTICOS
El estudio se llevó a cabo en consonancia con la declaración de Helsinki. El protocolo del estudio, la hoja de información del paciente y el consentimiento informado fueron aprobados por el Comité de Ética de Investigación Provincial de Málaga con fecha 21/2/2019 y código JGA-DIACARE-2018-01.
A todos los pacientes se les informó de las condiciones de participación y accedieron a participar tras firmar el consentimiento informado.
ANÁLISIS ESTADÍSTICO
Se empleó la prueba de t de Student para variables continuas y la prueba de χ2 para variables categóricas. Las diferencias entre grupos para las variables continuas se resumen mediante el intervalo de confianza del 95 % de la diferencia de medias y la desviación estándar. Se consideró estadísticamente significativa una p < 0,05.
RESULTADOS
PARÁMETROS DEMOGRÁFICOS Y DE EVOLUCIÓN DE LA DM TIPO 2
Se incluyeron 29 pacientes en el estudio, de los que el 51 % fueron mujeres. La edad media fue de 68,84 años (DE 11,37). El índice de complejidad de Charlson fue de 4,14 (DE 1,57). Los participantes presentaron un tiempo de evolución de su diabetes mellitus tipo 2 de 8,66 años (DE 6,89), una HbA1c de 6,29 (DE 1,12) % y el tratamiento recibido mayoritariamente fue la metformina (93,1 %), combinado, en algunos casos, con análogos del GLP1 e IDPP-IV.
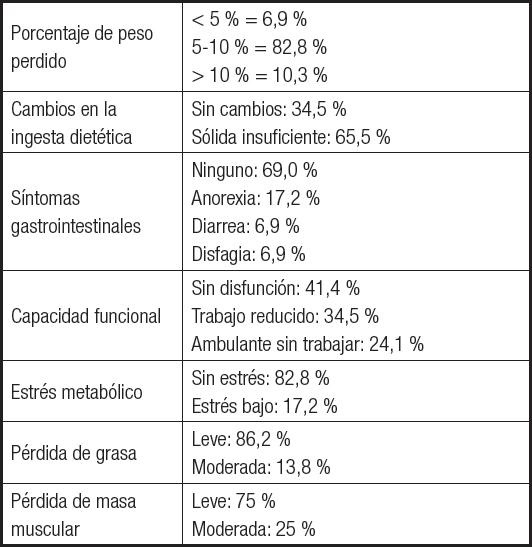
Respecto al estado nutricional, el 86,2 % presentó riesgo de desnutrición (VGS = B) y el 13,8 %, una desnutrición grave (VGS = C). Los resultados se detallan en la tabla II. El porcentaje de peso perdido fue del 8,66 % (DE 5,76), con un IMC de 24,88 kg/m2 (DE 4,52).
Respecto a la valoración sensorial cuantitativa, se observó una mejor valoración de la FED respecto a la FE (Fig. 1), aunque no se alcanzaron diferencias estadísticamente significativas: olor, 0,04 (IC 95 %), de -0,49 a 0,56 (p = 0,092); sabor, 0,14 (IC 95 %), de -0,35 a 0,63 (p = 0,561); textura, 0,14 (IC 95 %), de -0,43 a 0,72 (p = 0,619), ni cuando se agruparon las valoraciones en un sumatorio 0,39 (IC 95 %), de -1,35 a 2,13 (p = 0,653). No se encontraron diferencias estadísticamente significativas cuando se analizaron por orden de aleatorización, sexo, grado de desnutrición, mayor o menor grado de complejidad, mayor o menor tiempo de evolución de la diabetes ni por ser más o menos mayores.

Figura 1. Valoración sensorial cuantitativa de los suplementos a estudio. FED: fórmula específica para diabetes; FE: fórmula estándar.
Respecto a la valoración sensorial cualitativa, se observó una mejor valoración de la FED respecto a la FE (Fig. 2), aunque no se alcanzaron diferencias estadísticamente significativas ni en la percepción del olor (p = 0,986), del sabor (p = 0,755) o de la textura (p = 0,789). No se encontraron diferencias estadísticamente significativas cuando se analizaron por orden de aleatorización, sexo, grado de desnutrición, mayor o menor grado de complejidad, mayor o menor tiempo de evolución de la diabetes ni por ser más o menos mayores.
DISCUSIÓN
La fórmula específica para diabetes con aceite de oliva virgen extra, diseñada específicamente para cubrir las necesidades concretas del paciente diabético, ha demostrado que consigue una aceptación sensorial tan adecuada como una fórmula estándar.
Los pacientes del estudio presentaron una edad avanzada, un largo tiempo de evolución de la diabetes tipo 2 y un índice de comorbilidad elevado. Se conoce que, a mayor edad, los individuos requieren una mayor concentración de ingredientes para percibir los diferentes sabores, especialmente dulces y salados (17). La disminución en la capacidad gustativa es muy común en ancianos y puede condicionar su estado nutricional y su evolución clínica. La pérdida del sentido del gusto resulta una situación multifactorial en la que se incluyen cambios fisiológicos como la disfunción de los receptores celulares del gusto, un inadecuado mantenimiento de la higiene y de la salud bucal, así como una disminución de la función olfativa. Aunque no existe un consenso general sobre la idea de una alteración de la percepción quimicosensorial asociada a la edad avanzada per se, está comúnmente aceptado que son los diferentes eventos asociados a la edad, un mal estado general de salud, la polimedicación y la pluripatología los que pueden condicionar esta disminución en la percepción del gusto (18).
A su vez, se ha demostrado que la diabetes mellitus tipo 2 puede disminuir la percepción de los sabores. En el estudio de Catamo et al., en el que realizaron una comparación en la percepción de los diferentes sabores entre individuos sanos y diabéticos, determinaron que los diabéticos presentaron una menor sensibilidad debido al impacto de los episodios de hiperglucemia (19). Esta disminución en la percepción del gusto puede condicionar una menor ingesta de alimentos de forma general y que requieran que los alimentos, y de forma concreta los SNO, presenten una saborización dulce más marcada.
Aunque en nuestro estudio no se hayan encontrado diferencias por el estadio de la desnutrición, se sabe que esta va a determinar el desarrollo de disgeusia y de otras formas de alteraciones en el sentido del gusto (20). Se sabe que las deficiencias nutricionales, tanto de origen primario como secundario, pueden desencadenar alteraciones en la percepción del gusto o exacerbar los efectos inducidos por el envejecimiento. En particular, el zinc desempeña un papel importante en varias vías metabólicas esenciales y es un componente de una gran variedad de metaloenzimas que intervienen en la transducción del gusto, como la anhidrasa carbónica IV. Se ha identificado la deficiencia de zinc como un factor causante de los trastornos del gusto que pueden provocar cambios en el apetito (21).
Nuestro estudio resulta el primero que plantea la aceptación sensorial de una fórmula diabética respecto a una estándar en pacientes con DM2 en riesgo de desnutrición. Existen otros estudios en los que se ha evaluado la aceptación de FED en pacientes diabéticos, pero, como en el estudio de Grau et al., se evalúa la aceptación entre varias dietas para conocer las preferencias del consumidor final (22).
Como fortalezas del estudio, cabe destacar que es el primero en el que se evalúa la aceptación sensorial de un suplemento nutricional específico para diabetes con AOVE, EPA y DHA sin azúcares añadidos. El AOVE es un alimento con marcadas características organolépticas determinadas, fundamentalmente, por sus componentes minoritarios (1-3 % del total) a partir de compuestos fenólicos como el hidroxitirosol y sus derivados (oleuropeina y tirosol), tocoferoles y otros compuestos como hidrocarburos (escualeno) o pigmentos como la provitamina A (23). Otros ingredientes de la fórmula FED que pudieron marcar la saborización del producto fueron el EPA y el DHA. Estos dos ácidos grasos provienen del aceite de pescado, cuyas características sensoriales están condicionadas con un olor y un sabor muy marcados por el componente oleoso de esta y por la elevada sensibilidad a su enranciamiento en presencia de oxígeno debida a la configuración espacial de los ácidos grasos omega-3 y a sus insaturaciones (24). Es necesario destacar que el proceso industrial de formulación y de fabricación de un SNO requiere de un trabajo de neutralización de olores y de sabores y posterior saborización y aromatización que favorezcan una adecuada aceptación por parte del paciente. Dentro de los saborizantes empleados, la sacarosa es uno de los ingredientes más habituales, ya que no solo mejora la saborización del SNO, sino que contribuye a obtener un mejor color (reacción de Maillard) y una mejor textura (25).
Respecto a las limitaciones, cabe destacar que solo se recogieron tres variables de la valoración sensorial (olor, sabor y textura). Esta decisión se tomó teniendo en cuenta el perfil del paciente al que estaba dirigida (edad avanzada y sin entrenamiento en el campo de las catas de alimentos) para que pudiese participar de forma sencilla. Respecto al tamaño muestral, de 29 pacientes, ha sido superior al realizado en otros estudios por otros autores y, además, resulta compensatorio al haberse planteado como ensayo clínico cruzado. Cabría destacar que el tiempo prolongado que ha supuesto el reclutamiento de pacientes se ha debido a la parálisis que se produjo por la pandemia COVID durante el año 2020 y primera parte del 2021 y por la falta de concienciación en la detección de desnutrición en la atención ambulatoria del paciente con diabetes tipo 2 por parte del personal sanitario.
CONCLUSIONES
El suplemento nutricional específico para el paciente con diabetes formulado con aceite de oliva virgen extra, EPA y DHA, una mezcla específica en hidratos de carbono, fibra soluble e insoluble, presentó una adecuada aceptación sensorial del paciente desnutrido con diabetes mellitus tipo 2.